索非布韦合成路线
药物Dasabuvir(达萨布韦)合成检索总结报告
药物Dasabuvir(达萨布韦)合成检索总结报告
一、Dasabuvir(达萨布韦)简介
Dasabuvir(达萨布韦)于2014年12月19日在美国上市。
Dasabuvir (达萨布韦)是HCV NS5B RNA-依赖RNA聚合酶抑制剂,适用于基因1型慢性丙肝感染。
Dasabuvir(达萨布韦)不良反应有:疲劳、瘙痒、感觉虚弱或缺乏能量、恶心及失眠。
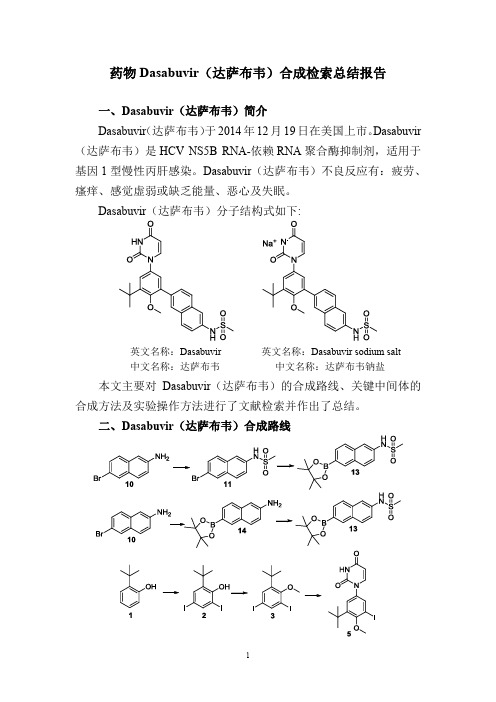
Dasabuvir(达萨布韦)分子结构式如下:
英文名称:Dasabuvir 英文名称:Dasabuvir sodium salt
中文名称:达萨布韦中文名称:达萨布韦钠盐本文主要对Dasabuvir(达萨布韦)的合成路线、关键中间体的合成方法及实验操作方法进行了文献检索并作出了总结。
二、Dasabuvir(达萨布韦)合成路线
三、Dasabuvir(达萨布韦)合成检索总结报告(一) Dasabuvir(达萨布韦)中间体2的合成
(二) Dasabuvir(达萨布韦)中间体3的合成
(三) Dasabuvir(达萨布韦)中间体5的合成方法一。
依非韦伦合成路线

依非韦伦合成路线依非韦伦合成路线是一种常用的有机化学合成方法,它以依非韦伦(E-Phenylvinylphosphonate)作为起始原料,通过一系列化学反应合成目标化合物。
本文将详细介绍依非韦伦合成路线的具体步骤和反应机理。
一、依非韦伦的合成方法依非韦伦是通过苯乙炔和三苯基膦酸反应得到的。
首先,在乙醇溶剂中加入氢氧化钠,使其溶解后形成溶液。
然后,将苯乙炔逐渐滴加到溶液中,同时控制反应温度在0°C以下。
反应完成后,将产物经过适当的萃取和纯化步骤,即可得到纯度较高的依非韦伦。
二、依非韦伦的反应合成路线1. 反应1:依非韦伦和卤代烃的偶联反应在反应容器中,将依非韦伦和卤代烃加入,并加入适量的碱性催化剂。
反应过程中,卤代烃与依非韦伦发生偶联反应,生成相应的取代产物。
该反应通常在惰性气氛下进行,并控制反应温度和时间,以提高产率和选择性。
2. 反应2:依非韦伦的加成反应依非韦伦可以通过与亲电试剂的加成反应来引入不同的官能团。
常用的亲电试剂包括酸、醛、酮等。
在反应中,依非韦伦与亲电试剂发生加成反应,生成新的化合物。
这个反应可以在不同的溶剂和温度条件下进行,以控制产物的选择性和收率。
3. 反应3:依非韦伦的还原反应依非韦伦可以通过还原反应来获得醇类化合物。
常用的还原剂包括金属氢化物、过渡金属催化剂等。
在反应中,依非韦伦与还原剂反应,断裂C=C键,生成醇类产物。
该反应通常在惰性气氛下进行,以避免产物的氧化和水解。
4. 反应4:依非韦伦的羰基化反应依非韦伦可以通过与酸酐或酰氯等羰基化试剂反应引入酯或酰基官能团。
在反应中,依非韦伦与羰基化试剂反应,生成相应的酯或酰基化合物。
该反应通常在惰性气氛下进行,并加入适量的催化剂,以提高反应的速率和产率。
依非韦伦合成路线具有以下优势:1. 反应步骤简单,操作方便,适用于大规模生产;2. 反应条件温和,适用于不同类型的有机化合物;3. 可以通过调整反应条件和反应物的选择,实现多样性化合物的合成。
药物合成反应—重点药物的合成路线

西咪替丁合成
OO
O SOCl2
OH O
O Cl
HCONH2/H2O
O
N
O
KBH4/AlCl3
THF
N
N H
N H
N
S
N H
HH NN
NN
CH3NH2 EtOH,H2O
N
S
N H
H NS
NN
(CH3S)2C=N-CN NaOH,EtOH
NH2
OH HS
N
S
HCl
. HCl
N
H
NH2
奥美拉唑合成
N HO
O
ON
O
NS
O
N H
SOCl2
m-Cl-C6H4-COOOH
N Cl
O
N
SH
N H
NaOCH3/MeOH
O
O
N NS
O
N H
阿司匹林合成
O
OH + OH
OO O
H2SO4 70~75℃
O OH
O O
布洛芬合成
CH2=CHCH3 Na-C
CH3COCl AlCl3
O
ClCH2COOC2H5 CH3CH2ONa
地西泮合成
N
Cl
O (CH3)2SO4 CH3C6H5 Cl
N+
_ O . CH3SO4
Fe, HCl
C2H5OH Cl
NH O
ClCH2COCl Cl C6H12
O N
O Cl (CH2)6N4 . HCl Cl CH3OH
O N
N
N
N N
RX
N
司美替尼的合成工艺改进

司美替尼的合成工艺改进司美替尼(Simeprevir)是一种口服抗病毒药物,用于治疗慢性丙型肝炎(HCV)。
该药物是一种直接作用于病毒的蛋白酶抑制剂,可以抑制HCV复制的能力。
目前,我国已批准司美替尼上市,并成为慢性丙型肝炎治疗中的重要药物之一。
在司美替尼的生产中,合成工艺是关键环节,合理的设计和改进可以有效提高其生产效率和产品质量。
本文将对当前司美替尼合成工艺的优化方案进行讨论。
一、司美替尼的合成工艺1. 司美替尼的化学结构司美替尼的化学名称为(2R, 3aS, 7aR)-N-[(1S)-3-甲氧基-1-(2-甲基丙基)-2-氧代丙基]-2-(2-吡啶基)-2,3,3a,4,5,6,7,7a-八氢-1H-吡唑并[3,4:5,6]哌啶-1-酰胺。
其化学结构如下图所示:2. 司美替尼的合成路径本文将重点探讨的是司美替尼的第一步反应。
其后续步骤主要采用保护反应、缩合反应、氧化反应以及消除反应等常见化学反应,不在此赘述。
司美替尼的合成路径如下:其中第一步是将一分子的溴取代苯甲酰胺和二分子的马来酸二乙酯在氢氧化钠催化下进行缩合反应,生成六元环中间体。
由于该反应条件控制较为困难,反应产率较低,因此需要对合成路线进行改进。
二、司美替尼合成工艺改进方案1. 缩短反应时间该缩合反应中需要控制反应温度和时间,提高反应产率。
通过改进反应条件,缩短反应时间,并增加反应物的加入量等措施,可以有效提高反应产率。
2. 反应中添加助剂在反应中添加助剂,例如有机锡化合物、有机锡碱等可改善反应条件,促进反应的进行,提高反应产率。
需要注意的是,这些添加剂有毒性和污染性,需要采取必要的安全和环保措施。
3. 采用微波加热微波辐射可以使反应物分子内部振动,产生摩擦加热,从而提高反应物的反应速度。
采用微波辐射技术可以缩短反应时间,提高反应产率。
但需要注意的是,微波辐射对反应体系温度分布不均匀,容易导致产物不纯,需要谨慎控制反应条件。
4. 采用新型催化剂研究表明,某些新型催化剂,如MIL-101、MOF-177等,可在反应体系中起到协同催化的作用,提高反应的效率。
新药Fisogatinib(非索替尼)合成检索总结报告

新药Fisogatinib(非索替尼)合成检索总结报告一、Fisogatinib(非索替尼)简介Fisogatinib(非索替尼)是由Blueprint Medicines开发的一款在研的强效、高选择性成纤维细胞生长因子受体-4(FGFR4)抑制剂,用于治疗FGFR4驱动的晚期或转移性肝细胞癌HCC。
Fisogatinib(非索替尼)具有成为首个分子水平生物标记物驱动的HCC靶向药物的潜力。
Fisogatinib(非索替尼)分子结构式如下:英文名称:Fisogatinib中文名称:非索替尼本文主要对Fisogatinib(非索替尼)的合成路线、关键中间体的合成方法及实验操作方法进行了文献检索并作出了总结。
二、Fisogatinib(非索替尼)合成路线三、Fisogatinib (非索替尼)合成检索总结报告(一)Fisogatinib (非索替尼)中间体3的合成合成方法实验步骤参考文献操作方法一1(5.00g,20.5mmol)and 2(3.73g,20.5mmol)were dissolved in tetrahydrofuran (30ml),added with a solution of cesium carbonate (20.00g,61.5mmol)in water (30ml),and added with a catalytic amount of Pd(PPh 3)Cl 2.Theresulting mixture was heated to reflux for 4h under nitrogen atmosphere.The reaction solution was concentrated to dryness and extracted with ethyl acetate.The organic phase was washed once with saturated sodium chloride,dried over anhydrous sodium sulfate,and concentrated under reduced pressure.The resulting crude product was subjected tocolumn chromatography (200-300mesh silica gel,petroleum ether/ethyl acetate=10/1)to obtain intermediate 3(3.80g,yield of 62%)as a pale yellow solid.US2019/209564;(2019);(A1)English;CN110386921;(2019);(A).操作方法二A mixture of 6-bromo-2-chloroquinazoline (1)(5.0g,20.5mmol),3,5-dimethoxyphenylboronic acid (2)(3.7g,20.5mmol),Cs 2CO 3(20.0g,61.5mmol)and Pd(PPh 3)2Cl 2(1.4g,2.1mmol)in THF (50mL),dioxane (50mL)and water (10mL)was degassed with N 2three times,and stirred at 80°C for 3hours.An aliquot of the reaction mixture was analyzed by both TLC and LCMS,which indicated that the reaction had proceeded to completion.The mixture was cooled to room temperature,and extracted with EtOAc (3×200mL).The combined organic layers were washed with water and brine,dried over sodium sulfate,filtered and concentrated.The residue was purified by silica gel chromatography (petroleum ether/EtOAc =8:1)to obtain 2-chloro-6-(3,5-dimethoxyphenyl)quinazoline (3)as a light yellow solid (2.4g,38%).WO2014/11900;(2014);(A2)English;US2015/197519;(2015);(A1)English;US2017/9695165;(2017);(B2)English(二)Fisogatinib(非索替尼)中间体4的合成合成方法实验步骤参考文献操作方法一To a solution of2-chloro-6-(3,5-dimethoxyphenyl)quinazoline(3)(2.7g,8.9mmol)indry THF(80mL)wasadded dropwise sulfuryl chloride(3.0g,22.3mmol)at-20°C,and the reactionmixture was stirred for an additionalhour.An aliquot of the reaction mixture was analyzed byboth TLC and LCMS,which indicated that the reaction hadproceeded to completion.The reaction mixture wasquenched with water(1mL),and the solvents were removedunder reduced pressure.The precipitate was washed withCH3CN and dried to obtain2-chloro-6-(2,6-dichloro-3,5-dimethoxyphenyl)quinazoline(4)(2.6g,79%)as a whitesolid.WO2014/11900;(2014);(A2)English;US2015/197519;(2015);(A1)English;US2017/9695165;(2017);(B2)English操作方法二3(3.80g,12.6mmol)was dissolved in tetrahydrofuran(100ml),under nitrogen cooled to-20~30o C,was addeddropwise sulfuryl chloride(5.11g,37.9mmol),the resultingmixture at the same temperature reaction for2hours.Thereaction mixture was slowly raised to ambient temperature,was added acetonitrile(100ml),stirred for10minutes,theresulting solid was collected by filtration.Drying,to giveintermediate4(2.80g,60%yield)as a pale yellow solid.US2019/209564;(2019);(A1)English;CN110386921;(2019);(A).(三)Fisogatinib(非索替尼)中间体6的合成合成方法实验步骤参考文献操作方法一(3R,4R)-3-(((S)-1-phenylethyl)amino)tetrahydro-2H-pyran-4-ol5(2.0g,9.04mmol)was taken up in methanol(10ml)followed by addition of Et3N(1.260ml,9.04mmol)andBOC-anhydride(2.308ml,9.94mmol).The reaction mixturewas stirred at room temperature overnight.The solvents werethen removed in vacuo and the residue was taken up in DCM(10ml)and hexane(20ml)and heated to80°C.until thesolvent level was reduced by half.The reaction mixture wasremoved from heat and cooled to room temperature whilestirring.5ml of ether was then added and the reaction wasstirred at room temperature for2hours.The reaction mixtureUS2015/119405;(2015);(A1)English。
索非布韦片调研报告

索非布韦片调研报告一、背景介绍索非布韦片(Sofosbuvir)是一种广泛应用于丙型肝炎(HCV)治疗的药物。
2013年,索非布韦片首次获得美国食品药品监督管理局(FDA)的批准,并在随后的几年内获得了全球多个国家的注册和上市。
由于索非布韦片的独特药物机制和良好的疗效,它被普遍认为是丙型肝炎患者的重要治疗选择之一。
本篇报告将对索非布韦片的市场调研情况进行介绍和分析。
二、市场概述丙型肝炎是一种由丙型肝炎病毒(HCV)引起的慢性病毒性肝炎,全球范围内估计有约7100万人感染HCV。
丙型肝炎的传播途径多样,其中包括使用污染的注射器、与HCV感染者共用注射器和性传播等。
长期慢性丙型肝炎感染可能导致肝硬化和肝癌等严重后果。
索非布韦片作为一种直接作用于HCV的新型药物,具有独特的药理特点,能够显著地降低HCV的繁殖和复制。
临床研究表明,索非布韦片能够使丙型肝炎患者的病毒载量迅速下降,并且能够显著提高患者的临床转归。
这使得索非布韦片成为了丙型肝炎患者治疗的重要选择药物。
三、市场调研结果1. 索非布韦片的市场规模根据市场调研数据显示,截至目前,全球索非布韦片市场规模已经达到了XX亿美元,并且还在以每年XX%的速度增长。
其中,美国、欧洲和亚太地区是索非布韦片市场的主要消费地区。
2. 竞争情况目前,全球索非布韦片市场上竞争激烈。
在丙型肝炎药物市场中,索非布韦片与其他直接作用于HCV的药物竞争日趋激烈。
另外,一些国际知名制药企业也纷纷加入到索非布韦片市场,并推出了自己的产品。
3. 市场趋势和前景随着全球丙型肝炎患者数量的不断增加以及治疗技术的不断进步,索非布韦片市场有望继续保持强劲的增长势头。
同时,随着索非布韦片的技术进步和临床验证,患者对于索非布韦片的需求也将不断增加。
四、市场挑战虽然索非布韦片在临床治疗中显示出了良好的疗效和安全性,但该药物的高价格成为了制约其市场推广和普及的主要挑战之一。
另外,由于历史原因,一些地区仍存在对索非布韦片的需求无法满足的情况。
sotorasib 合成路线

sotorasib 合成路线
摘要:
1.Sotorasib 的简介
2.Sotorasib 的合成路线
3.合成路线的优化
4.总结
正文:
【1】Sotorasib 的简介
Sotorasib(索托拉西布)是一种新型抗癌药物,主要用于治疗非小细胞肺癌。
它的研发和应用在医学领域引起了广泛关注,因为它针对特定基因突变,具有很好的靶向作用,从而在提高治疗效果的同时减少副作用。
【2】Sotorasib 的合成路线
Sotorasib 的合成路线分为以下几个步骤:
步骤一:通过酰胺化反应合成喹啉酮衍生物
步骤二:通过环氧化反应引入氧原子
步骤三:进行亲核取代反应,引入胺基
步骤四:最后通过芳香族取代反应引入甲氧基
【3】合成路线的优化
在Sotorasib 的合成过程中,科学家们通过不断优化反应条件、试剂和操作方法,提高了产率和纯度,缩短了合成周期。
例如,采用微波辅助技术可以加快反应速率,提高产率;选择高选择性的试剂和催化剂可以减少副反应,提
高目标产物的纯度。
【4】总结
Sotorasib 作为一种新型抗癌药物,其合成路线的研究和优化为临床应用提供了重要支持。
通过持续改进合成方法,科学家们旨在为患者提供更有效、更安全的治疗选择。
药物remdesivir(伦地西韦、瑞德西韦)合成检索总结报告

药物remdesivir(伦地西韦、瑞德西韦)合成检索总结报告
一、remdesivir(伦地西韦、瑞德西韦)简介
瑞德西韦也叫伦地西韦,英文名称为remdesivir,它是一种抗病毒药物,已经用于抗埃博拉病毒和其他疾病。
瑞德西韦(伦地西韦/remdesivir)分子结构式如下:
CAS:1809249-37-3
二、remdesivir(伦地西韦、瑞德西韦)合成路线
(一)remdesivir(伦地西韦、瑞德西韦)合成路线一
合成路线设计一
(二)remdesivir(伦地西韦、瑞德西韦)合成路线二
合成路线设计二
三、remdesivir (伦地西韦、瑞德西韦)合成检索总结报告
(一)remdesivir (伦地西韦、瑞德西韦)合成路线一检索总结
1、remdesivir (伦地西韦、瑞德西韦)中间体2的合成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
合成索菲布韦可行性研究报告
一、 基本信息:
化学结构
式:
通用名: 索非布韦、索菲布韦、索氟布韦
中文化学名: N-[[P(S),2'R]-2'-脱氧-2'-氟-2'-甲基-P-苯基-5'-尿苷
酰基]-L-丙氨酸异丙酯
英文化学
名:
GS-7977
CAS登记
号:
分子式: C22H29FN3O9P
分子量:
适用症: 索非布韦是一种丙型肝炎病毒(HCV) 核苷酸类似物NS5B聚合酶抑制剂, 适用于作为联合抗病毒治疗方
案中的组合成分治疗慢性丙肝(CHC) 感染
制剂及规
格:
400mg片剂
二、 商品信息
质量标准
医药级
含量 ≥%;单杂≤%,总杂≤%
外观性状 白色结晶性粉末
包装规格 铝箔袋
储存 低温,遮光密闭保存
国外上市情况
索氟布韦,英文名Sofosbuvir,商品名Sovaldi是吉利德公司开发用于治
疗慢性丙肝的新药,于2013年12月6日经美国食品药品监督管理局(FDA)批准
在美国上市,2014年1月16日经欧洲药品管理局(EMEA)批准在欧盟各国上市。
该药还未在中国上市,只能去国外医院获得。
国内上市情况:暂无
三、工艺概述
1)合成路线选择:
从索非布韦的结构式可以看出由两个片段对接而成,片段B磷脂片段
合成较为容易,片段A的合成较为复杂,相对应的中间体也较多,是合成
该反应控制收率和成本的关键中间体。国内为类新药,目前主流合成路线
如下图,国内暂无相关报道专利。
2)合成路线图/反应方程式
路线一:
路线二:
3)工艺路线描述
路线一:
合成索非布韦的路线是有片段A和片段B对接而成,片段A的合成是由起始
原料(R) -2, 2-二甲基-1 ,3-二氧戊环-4-甲醛(A-00),经过witting反应,高
锰酸钾氧化双键,酯化,氧化,还原,氯代,亲核取代等多步反应得到片段A;
片段B是由以 L-丙氨酸异丙酯盐酸盐为原料 经磷酰化、酯化后再与片段B反应
制得索非布韦。总步骤约11步。该路线和起始原料等的选择也是目前国内外研
发的主流路线,不排除企业创新设计其他中间体情况,路线中的11步均有相关
文献报道,故不存在风险问题,路线不通等情况,在实验当中将根据实验结果可
能进行适当改变,从成本,质量,收率等角度进行适当完善适合自己公司的工艺
路线资料。
路线二:
路线二与路线一差别不大,片段B的合成略有差别,使用的辅料不同,导致
中间体不同,根据实际合成路线选择不同的片段B路线合成。
4)实验方案。(略)
四、 相关中间体产品信息情况
产品名称 CAS 结构式
索非布韦
片段A 863329-66-2
片段B
B-00 39613-92-8
B-01 261909-49-3
A-00 22323-80-4
A-04 879551-04-9
A-06 817204-32-3
A-07 817204-32-3
四.产品开发时间与资金。
从起始物到制备出索非
布韦共11步反应,合成路线长,技术难度较大,需要研发人员有较强的专业知
识并且考虑到其它不稳定因素的影响,预计打通工艺路线制备出合格的索非布韦
需要时间约4~6月,尤其是合成片段A,但起始原料和片段A和片段B等有关中
间体市场上均有销售,可以减轻研发人员的开发精力等,鉴于市场上索非布韦的
及中间体价格较贵,预计开发成本较高。
精心搜集整理,只为你的需要
