《中国药典》2015年版一部增修订内容解析
《中国药典》2015年版中药材增修订内容
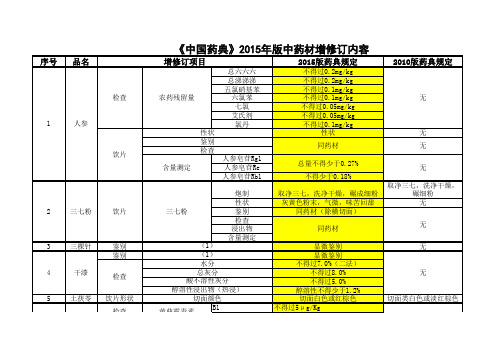
火麻仁 功劳木 甘松 含量测定 含量测定
37
甘草
饮片
B1 不得过5μ g/Kg G2、G1、B2、B1 总量不得过10μ g/Kg 鉴别 同药材 总灰分 总灰分不得过10.0% 检查 重金属及有害元素 同药材 黄曲霉毒素 游离胆红素 高效液相色谱法 胆红素 高效液相色谱法 二氧化硫残留量 不得过400mg/Kg (1) 显微鉴别 金丝桃苷 总量不得少于0.38% 异槲皮苷 (2) 鉴别(2) 丹参酮ⅡA 总量不得少于0.25% 隐丹参酮 丹参酮I 丹酚酸B 不得少于3.0% 来源 果实 功劳木对照提取物 总量不得少于1.5% 盐酸小檗碱 无 盐酸巴马汀 甘松新酮 不得少于0.10% 性状 性状 鉴别 同药材(除横切面) 总灰分 不得过7.0% 检查 水分 同药材 重金属及有害元素
取净大黄片,照炒炭法 炒至表面焦黑色,内部 焦褐色
10 11 12
山银花 山楂 千金子
13
川木香 饮片
煨川木香
无
14 15 16 17 18 19 20 21
川贝母 川芎 广金钱草 女贞子 马兜铃 天仙子 天冬 天花粉
鉴别 性状 饮片 鉴别 鉴别 鉴别 鉴别 检查 饮片 检查 饮片
(2) (3) 表面颜色 表面颜色 (1) (1) (1) (1) 二氧化硫残留量 二氧化硫残留量 二氧化硫残留量 二氧化硫残留量 (1)
鉴别
检查 26 五加皮 浸出物
饮片
27
太子参
性状 含量测定
无
检查 28 水蛭
重金属及有害元素
砷 汞 铜
不得过5mg/Kg 不得过1mg/Kg
无
黄曲霉毒素 饮片(烫水 蛭) 29 30 31 32 牛黄 牛膝 升麻 月季花 检查 含量测定 检查 鉴别 含量测定 鉴别 33 丹参 含量测定
浅谈2015年版中国药典的重点变更-PDF (简)

2015 年版药典收载品种总数约为 5515 个,増幅达到 26.2%。
2010 版药
2015 年版药典
类别
典收载 总收载品种 新增品种 修订品种
中药
2165
化药
2139
药用辅料
132
生物制品
品种 通则、总论
131 10
小计
4567
通则(附录)
---
指导原则
---
2627 2617 约 271 145 14 约 5515 321 31
约 462 约 500
139 14 4 约 1201 29 15
约 400 149 132 62 8
约 751 145 8
不收载 品种
2 5 --6 --13 -----
4. 2015 年版药典的部份增加及修订的项目: 附录是药典的重要部份,药典的灵魂和水平均集中反映在附录中。本版是将三部 药典的附录合一,加强共性的系统化、完善化及规范化,新版 <中国药典> 的附 录调整为凡例、通则与方法、指导原则、药用辅料等单独成卷,为第四部。把以 往各部药典附录里相同的方法之间的归纳统一作为本版药典的工作重点,同时, 亦解决长期以来各部药典之间相同方法/通则要求不统一的问题。再且,附录对 药典以外的其他国家标准具同等法律效力。
4.6 二氧化硫残留的限制 通则里说明,除另有规定外,中药材及饮片(矿物类除外)的二氧化硫残留量不得 超过 150mg/kg (ppm)。
正文品种说明山药、牛膝、粉葛、天冬、天麻、天花粉、白及、白芍、白朮、党 参 10 味药材及其饮片二氧化硫残留量不得超过 400mg/kg(ppm)。
新版药典锐意加强科学监管,防止中药材加工过程中滥用或过度使用硫磺熏蒸,
《中华人民共和国药典(2015年版)》中中药部分的增、修订情况简介

《中华人民共和国药典(2015年版)》中中药部分的增、修订情况简介作者:陈佳钱琛陈桂良来源:《上海医药》2016年第07期摘要本文简要介绍《中华人民共和国药典(2015年版)》中中药部分的增、修订情况及技术特点。
本版药典不仅中药收载品种数大幅增加,而且进一步加强了多药味(成分)的检测、活性成分的控制和杂质(有害物质)的检查,更注重现代分析技术的应用,包括广泛应用了指纹(特征)图谱技术,对提高中药的安全性及其质量整体控制水平具有重要作用。
关键词《中华人民共和国药典(2015年版)》中药药品标准中图分类号:R921.2 文献标识码:C 文章编号:1006-1533(2016)07-0003-02A brief introduction to quality standards of traditional Chinese medicines in the Pharmacopoeia of the People’s Republic of China (2015 version)CHEN jia*, QIAN Chen, CHEN Guiliang* *(Division of Quality Assurance, Shanghai Institute for Food and Drug Control, shanghai 201203, China)ABSTRACT The main changes and the technical characteristics related to the quality standards of traditional Chinese medicines (TCM)in the Pharmacopoeia of the People’s Republic of China (2015 version) was briefly introduced. Not only was the content related to the collection of TCM substantially increased but also the detection of multi-composition, the control of active ingredients and the examination of harmful impurity (or substances) were strengthened, and furthermore,the application of modern analysis technology including the wide use of feature/fingerprint technology was more focused on in this new pharmacopoeia. We believe that these will play an important role in improving the safety of TCM and strengthening their quality control.KEY WORDS Pharmacopoeia of the People’s Republic of China (2015 version); traditional Chinese medicines; drug standards《中华人民共和国药典(2015年版)》(以下简称为“2015年版《中国药典》”)已自2015年12月1日起正式实施。
2015版中国药典第一部 中药质量标准全面提升

2015版中国药典第一部中药质量标准全面提升《中国药典》一部主要收载中药材、饮片、提取物和中成药的质量标准,也就是大家常说的中药标准。
日前正式发行的《中国药典》2015年版一部目录中共收载药材和饮片618个(不含收载在品种下的饮片标准)、植物油脂和提取物47个、成方制剂和单味制剂1493个。
较2010年版药典,2015年版药典的中药标准在安全性、有效性等方面均有所提升。
正如国家药典委员会秘书长张伟所说的那样:“药典是引领产业结构调整和产品质量升级的‘导航仪’。
”由于中药多数来源于天然物质,不仅所含成分非常复杂,而且受气候、生态环境、栽培(生产)技术等因素影响很大。
中药质量标准是随着中药所含成分的不断阐明、对中药安全性认识的不断提升,以及中药市场出现的新问题和现代分析方法的不断出现而不断提高的,因此每版药典一部的标准水平都有较大程度的提升。
据介绍,每一版药典在开始工作前,都需要成立新一届药典委员会,规划新版药典工作,并形成编制大纲。
中药的安全性、有效性和质量可控性是《中国药典》2015年版编制大纲的“规定动作”。
安全性:变单一指标为“组合拳”近年来,随着药品监管理念的不断成熟,加强对中药中有害物质的控制成为国家药品标准工作满足药品监管需求,保障公众用药安全的重要任务。
在国家食品药品监管总局统一部署下,国家药典委员会在《中国药典》2015年版编制工作中,组织有关单位和专家,通过科学研究,参照国际发达国家地区的限度标准,并结合我国中药发展现阶段的实际情况,突出风险控制重点,按照“成熟一个,修订一个,公示一个”的原则,将研究成果应用于《中国药典》制定和修订中。
《中国药典》2015年版在2010年版的基础上,重点加强和完善了安全性控制技术的应用,主要涵盖八个方面:二氧化硫残留、重金属及有害元素、农药残留、真菌毒素(黄曲霉毒素)、色素、内源性有害物质、微生物、致病菌控制。
“新版药典在凡例、通则以及品种的标准中分别增加了对中药安全性检查的总体要求、技术指导则、检测方法和具体品种限度规定,改变了过去单纯强调设置检测项目和指标的做法。
15版药典变化解析

2015版《药典》中药材标准的变化情况新药典变化概述:1.药典一部收载药材和饮片、植物油脂和提取物、成方制剂和单味制剂等,品种共计2598种,其中新增440种,修订517种,不收载7种。
2.重新建立规范的编码体系,并首次将通则、药用辅料单独作为《中国药典》四部。
3.完善了“药材和饮片检定通则”“炮制通则”和“药用辅料通则”。
4.制定了中药材及饮片中二氧化硫残留量限度标准,建立和完善重金属及有害元素、黄曲霉毒素、农药残留量等物质的检测限度标准。
5.中药材增加专属性的显微鉴别检查、特征氨基酸含量测定等。
6.不再新增处方中含羚羊角、豹骨、龙骨、龙齿等濒危物种和化石的中成药品种。
新药典增减药材情况:删除:紫河车新药典“来源”修订情况:新药典“性状”修订情况新药典“显微鉴别”增加品种三颗针、干漆、山楂、广金钱草、女贞子、马兜铃、天仙子、升麻、生姜、瓜子金、瓜蒌皮、老鹳草、西青果、红大戟、花椒、花蕊石、杜仲叶、豆蔻、牡蛎、余甘子、沙苑子、诃子、补骨脂、苦杏仁、苦楝皮、虎杖、知母、使君子、金果榄、金银花、鱼腥草、卷柏、油松节、韭菜子、骨碎补、钩藤、胖大海、夏枯草、浮萍、预知子、菊花、野木瓜、款冬花、棕榈、紫苏叶、紫苏梗、锁阳、蓝布正、槐角、锦灯笼、豨莶草、暴马子皮、薤白、瞿麦、翻白草新药典“检查”修订情况二氧化硫残留量通则规定,除另有规定外,中药材及饮片(矿物类除外)的二氧化硫残留量不得超过150mg/kg。
正文规定,山药、天冬、天花粉、天麻、牛膝、白及、白术、白芍、党参、粉葛10味中药及其饮片的二氧化硫残留量不得超过400mg/kg。
农药残留量注:•总六六六(α-BHC、β-BHC、γ-BHC、δ-BHC之和)不得过0.2mg/kg;•总滴滴涕(pp’-DDE、pp’-DDD、op’-DDT、pp’-DDT之和)不得过0.2mg/kg;•五氯硝基苯不得过0.1mg/kg;•六氯苯不得过0.1mg/kg;•七氯(七氯、环氧七氯之和)不得过0.05mg/kg;•艾氏剂不得过0.05mg/kg;•氯丹(顺式氯丹、反式氯丹、氧化氯丹之和)不得过0.1mg/kg。
《中国药典》2015年版中药材增修订内容

取净大黄片,照炒炭法 炒至表面焦黑色,内部 焦褐色
10 11 12
山银花 山楂 千金子
13
川木香 饮片
煨川木香
无
14 15 16 17 18 19 20 21
川贝母 川芎 广金钱草 女贞子 马兜铃 天仙子 天冬 天花粉
鉴别 性状 饮片 鉴别 鉴别 鉴别 鉴别 检查 饮片 检查 饮片
(2) (3) 表面颜色 表面颜色 (1) (1) (1) (1) 二氧化硫残留量 二氧化硫残留量 二氧化硫残留量 二氧化硫残留量 (1)
鉴别 22 天竺黄
(2) (3)
检查 性状 鉴别 检查 23 天麻 浸出物 含量测定 饮片
体积比 表面颜色 (3) 二氧化硫残留量 醇溶性浸出物 天麻素 对羟基苯甲醇 性状
贝母素乙及贝母辛 无 表面黄褐色 外表皮黄褐色 无 无 无 无 无 无 无 无 (1)溶媒为盐酸与硝酸 (1)溶媒为醋酸2滴,显色剂一滴 的等混合液,显色剂无 变化 (2)显色反应 (2)显示反应 增加天竺黄为对照药材的薄层色谱 无 鉴别 体积比:中粉10g。轻轻 中粉10g,轻轻装入量筒,体积比 装入量筒,体积比不得 不得少于24ml 少于35ml 黄白色至黄棕色 黄白色至淡黄棕色 增加对羟基苯甲醇为对照品的薄层 无 色谱鉴别 不得过400mg/Kg 无 不得少于10%,溶媒为乙 不得少于15.0%,溶媒为稀乙醇 醇 不得少于0.20% 总量不得少于0.25% 无 淡黄色至黄棕色 淡黄色至淡黄棕色
《中国药典》2015年版中药材增修订内容
序号 品名 增修订项目
总六六六 总涕涕涕 五氯硝基苯 六氯苯 七氯 艾氏剂 氯丹 性状 鉴别 检查 含量测定 人参皂苷Rg1 人参皂苷Re 人参皂苷Rb1 炮制 性状 鉴别 检查 浸出物 含量测定
2015版《中国药典》修订情况简介介绍
药品标准形成机制待探索
• 一是要继续推进国家药品标准提高行动计 划的实施,重点抓好列入国家基本药物和 医疗保险目录品种、注射剂、疫苗等高风 险品种以及中药和民族药等产品的标准提 高工作;
• 二是要加快推进国家药品标准形成机制改 革的进程,形成“有进有出、有增有减”的新 格局;
• 三是要加快建立国家药品标准信息化平台 并将其纳入国家总局建设计划,统一规范
七步提升了对药品质量 控制的要求,完善了药典标准的技术规定, 使药典标准更加系统化、规范化。
七大变化
• 三是健全了药品标准体系。特别是药用辅 料品种增加至260个,新增相关指导原则; 在归纳、验证和规范的基础上实现了《中 国药典》各部共性检测方法的协调统一。
未来药品标准的发展
• 社会共举 标准化工作属于社会公益事业, 应当更多地调动地方乃至全社会的力量(包 括资金、技术和人员)支持和参与药品标准 制定。充分发挥药品检验机构、高等院校 和科研院所的作用,深入开展前瞻性、全 局性和关键性课题研究及分析技术攻关, 加强药品标准化战略研究和技术咨询服务。 充分利用媒体广泛介绍药品标准化知识, 宣传工作进展及成果。
未来药品标准的发展
• 市场导向 市场导向就是要利用市场的作用, 提高药品标准的市场适应性。要充分体现 药品标准从市场中来,到市场中去,还药 品标准在市场经济环境中自愿性的属性。 明确药品标准的制定和应用应是一种市场 行为,也是应用者的自愿行为,而不是政 府的行政性行为。在市场经济的条件下, 要使药品标准体系建设有利于促进市场经 济发展,有利于建立统一的市场秩序。通 过药品标准化战略的实施,从标准化角度
药品标准形成机制待探索
• 第三,企业提高药品标准的能力和内在动 力不足。
• 第四,我国未建立起统一、动态、高效的 药品标准信息平台,因此难以准确统计我 国药品标准数量,致使标准总体底数不清; 难以对现有药品标准进行比较分析,致使 标准整体水平不明;难以查询最新标准,致 使执行容易出错。
2015版药典一部凡例变化总结
• 总则七 • 10版:《中国药典》英文缩写为Ch.P. • 15版:《中国药典》英文缩写为ChP
• 正文八 • 10版:品种项下收载的内容统称为正文,正文 系根据药物自身的理化与生物学特性,按照批 准的来源、处方、制法和运输、贮藏等条件所 制定的、用以检测药品质量是否达到用药要求 并衡量其质量是否稳定均一的技术规定 。 • 15版:《药物自身的理化 与生物学特性,按照批 准的来源、处方、制 法和运输、贮藏等条件所 制定的、用以检测 药品质量是否达到用药要求并衡量其质量是否 稳定均一的技术规定 。
• 总则 二 • 10版:国家药品标准由凡例与正文及其 引用的附录共同构成。本部药典收载的 凡例、附录对药典以外的其他中药国家 标准具有同等效力。 • 15版:国家药品标准由凡例与正文及其 引用的通则共同构成。药典收载的凡例、 通则对未载入本部药典但经国家药品监 督管理部门颁布的其他中药标准具有同 等效力。
• 检验方法与限度 • 10版:无 • 15版:新增“采用本版药典收载的方法, 应对方法的适用性进行确认”
谢谢大家!
总则三 10版:凡例是为正确使用《中国药典》 进行药品质量检定的基本原则 ,是对 《中国药典》正文、附录及与 质量检定 有关的共性问题的统一规定。 15版:凡例是正确使用《中国药典》进 行药品质量检定的基本原则 ,是对《中 国药典》正文、通则及与质量检定有关 的共性问题的统一规定。
• 总则四 • 10版:凡例和附录中采用“ 除另有规定 外” 这一用语,表示存在与凡例或附录 有关规定不一致的情况时,则在正文中 另作规定,并按此规定执行。 • 15版:凡例和通则中采用 “ 除另有规 定外” 这一用语 表示存在与凡例或通则 有关规定不一致的情况时,则在正文中 另作规定,并按此规定执行。
2015版药典增修订内容简介
2016年3月24日
了解新版药典变化的目的
了解新版药典增修订情况的变化,更好地理解药
典、更好地执行药典。 了解药品国家标准制修订理念的变化,把握今后 药品标准制修订的方向,提高标准控制水平,促 进产品质量的提升。
《中国药典》2015年版概况
《中国药典》2015年版,共分为四部。
5
《中国药典》2015年版概况
药典四部收载通则和药用辅料 通则(附录),共317个(其中新增43个、修 订67个)。包括制剂通则共38个,检测方法 240个,指导原则30个,标准物质、标准品9 个。 药用辅料270个(其中新增137个、修订97个、 不收载2个)。
《中国药典》2015年版特点 -1
建立了药典标准体例 凡例为统领规定 通则和总论为同类药品基本准则 各论为具体品种基本要求 药品标准体系更加健全,首次将“国家药品标准物质 制备”、“药包材” 以及“药用玻璃容器”等指导原 则纳入药典。
《中国药典》2015年版特点-3
对凡例、通则、总论进行了全面修订,整体上提 升了对药品质量控制的要求。 药典凡例、通则、总论对药典收载以外的药品 具有同样的约束力。 对整合后的通则重新建立了通则编码体系(与 中国药典2010年版附录有编码对照表)
收载品种有较大幅度的增加(新增1082个), 增幅达到23.7%。 扩大收载品种范围,覆盖了国家基本药物目 录品种的90%以上。 对于部分标准不完善、多年无生产、临床不 良反应多的药品,加大调整力度,2010年版 收载而本版药典未收载的品种共计43种。
《中国药典》2015年版特点-2
药品标准更加系统化、全面化、规范化
2015版药典
三、《中国药典》2015年版制剂通则检查方法增修订概况
v 单剂量包装 系指按规定一次服用的包装剂量。凡例中还规定:“各品种[用法与用量] 项下规定服用范围者,不超过一次服用量最高剂量包装者也按单剂量包装 检查”
例如:一次服用量为:6-9g 规格1:每袋装9g——为单剂量包装,检查装量差异 规格2:每袋装12g——为多剂量包装,检查装量 v 重量差异检查边缘数据判断:遇有超出允许粒重范围并处于边缘者,应现
4
一、《中国药典》2015年版附录(总论)制修订概况
有关附录的规划指标
v 调整为风凡例、通则与方法、指导原则、药用辅料等单独成卷 v 开展附录整合工作
附录部分立足规范统、着重完善提高 重点:将原各部附录相同方法之间的规范统一,以解决长期以来各部之间相同方 法要求不统一的问题 v 重点抓好药典附录科研起草工作 扩大收载与修订完善制剂通则及与质量相关的检测项目 加强对药品标准检测方法、检测环境和检测条件的研究 增加新的成熟可靠的方法和修订落后的通用检测方法 进一步补充和完善主要检测方法应指导原则 增订药品生产、流通、储运等各环节的技术指导原则,全面控制药品质量 重视引导、推广国产检验仪器的发展和应5 用
与平均粒重相比较,计算出该粒得差异的百分率,再根据差异限度作为判 定。
31
1
17
二部药典
149条
2 三部药典
149条
8
一、《中国药典》2015年版附录(总论)制修订概况
序号 类别
0100 制剂通则 0200 药材及饮片相关通则 0300 药用辅料相关通则 0400 一般鉴别试验 0500 光谱法与波谱法 0600 色谱法 0700 理化性质 0800 含量测定
0900 限量检查
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
七 、《中国药典》的英 名称为 Pharmacopoeia of The People’s Republic of China ;英 简称为Chinese Pharmacopoeia ; 英 缩写为 ChP 。
凡例
正文 八 、《中国药典》各品种项下收载的内容统 称为标准正文 ,正文系根据药物自身的理 化与生物学特性,按照批准的来源 、处方、 制法和贮藏 、运输等 条件所制定的、用以 检测药品质量是否达到 用药要求并衡量其 质量是否稳 定均一的技术规定。
凡例
十三、正文分为药材和饮片、植物油脂和 提取物、成方制剂和单味制剂三部分 。 饮片系指药材经过炮制后可直接 用于中医 临床或 制剂生产使 用的处方药品。 饮片除需要单列者外 ,一般并列于药材的 正 文中,先列药材的项 目,后列 饮片的项 目,中 间 用 “饮片” 分开 ,与药材相同 的 内容只列出 项 目名称,其要求用 “同 药材”
凡例
项目与要求 十五 、单列饮片的标准,来源项一般描述为 “本 品为X X 的加工炮制品”,并增加〔制法 〕项 , 收载相应的炮制工艺 ,其余同药材和饮片标准。 十 六 、药材和饮片的质量标准,一般按干品制定, 需用鲜品的,另制定鲜品的质量控制指标,并规 定鲜品的用法与用量。 十七 、药材原植(动 )物的科名、植(动 )物 名、拉丁学名、药用部位(矿物药注明类 、族 、 矿石 名或岩石名、主要成分)及采收季节和产地加 工等,均属药材的来源范畴 。
《中国药典》2015 年版一部增修订内容
内容提要
一、一部凡例 二、一部增修订内容 三、方法确认
凡例
总则 一 、《中华人民共和国药典》简称《中国 药典》,依据《中华人民共和国药品管理 法》组织制定和颁布实施。 《中国药典》一经颁布实施,其同品种的上 版标准或其原国家标准即同时停止使 用。
凡例
名称及编排 十一、药材和饮片名称包括中文名、汉语拼音及 拉丁名,其中药材和饮片拉丁名排序为属 名或属 名+种加词在先,药用部位在后;植物油脂和提取 物、成方制剂和单味制剂名称不设拉丁名。 十二、正中未列饮片和炮制项的,其名称与药材 名相同 ,该正文同为药材和饮片标准;正文中饮 片炮制项为净制、切制的,其饮片名称或相关项 目亦与药材相同 。
凡例
九、正文项下根据品种和剂型不同,按顺 序可分别列有:( 1 ) 品名;(2)来源;(3) 处方;(4)制法 ; ( 5 )性状 ;(6)鉴别 ; (7 ) 检查 ;(8 )浸出物;(9 )特 征图 谱或指 纹图谱 ;(1 0 )含量测定; (1 1 )炮 制;(12)性味与归经;(1 3 )功能 与主治 ;(1 4)用法与用量;(1 5 )注 意 ;(1 6 )规 格 ; (1 7 )贮藏 ;(18) 制剂 ;(1 9 )附注等。
凡例
通 则 十、通则主要收载制剂通则、通用检测方 法和指导原则。制剂通则系按照药物剂型 分类 , 针对剂型特点所规定的基本技术要 求;通用检测方法系各正文品种进行相 同 检查项目的检测时 所应采 用的统一的设备 、 程序 、方法及限度等;指导原则系为执行 药典、考 察药品质量、起草与复核药品标 准等所制定的指导性规定。
凡例
表 述 ;不同于药材的内容逐 项列出,并规 定相应的指标。上述编排系为减少正文篇 幅 ,药材和饮片仍应作为两个独立的品种。 植物油脂和提取物系指从植、动物中制得 的 挥发油、油脂、有效部位和有效成分 。 其中,提取物包括 以水或醇为溶剂经提取 制成的流浸膏 、浸膏或干浸膏 、含有一类 或数类有效 成分的有效部位和含量达到 9 0 % 以上的单一有效成分 。
凡例
四、凡例和通则中采用 “除另有规定外” 这一用语 ,表示存在与凡例或通则有关规 定不一致的 情况时 ,则在正文中另作规定, 并按此规定执行。 五 、正文中引 用的药品系指本版药典收载 的品种,其质量应符合相应的规定。 符合《药品 生产质量管理规范》 (Good Manufacturing Practices, G M P ) 的产品 而言 。任何 违 反G M P 或有 未经批准添 加物质所生产的药品,即 使 符 合《中国药 典》或 按 照 《中国药典》没有检出其添加 物质或相关杂质,亦不能认为其符合规定。
凡例
《中国药典》由一部、二部、三部、四部及 其增补本组成。 一部收载中药,二部收载化学药品,三部收 载生物制品,四部收载通则和药用辅料。 除特别注明版次外,《中国药典》均指现 行版《中国药典》。 本部为《中国药典》一部。
凡例
总则 二、国家药品标准由 凡例与正 文及其引 用 的通则共同构成。药典收载的 凡例与通则 对未载入本版药典但经国务院药品监督管 理部门颁布的其他中药标准具同等效力。 三、凡例是正确使用《中国药典》进行药 品质量检定的基本原则,是对《中国药典》 正文、通则及与质量检定有关的共性问题 的统一规定。
凡例
药材原植物的科名、拉丁学名的主要参照 依据为《Flora of China 》和《中国高等植 物》等。 药用部位一般 系指已除去非药用部分的商 品药材。采收 (采挖等)和产地加工系对药 用部位而言 。
凡例
十八 、药材产地加工及炮制规定的干燥 方 法如下:① 烘 干 、晒 干 、阴干均可的, 用 “干燥”;②不宜用较高温度烘干的, 则 用 “晒干” 或 “低温干燥 ” (一般 不 超 过 60℃);③烘 干 、晒 干 均 不适 宜 的,用 “阴干”或 “晾干”;④ 少数药 材需要短时 间干燥 ,则 用 “暴晒 ”或 “及时干燥 ”。
凡例
十四、正文的三个部分分别按中文名笔画 顺序排列 ,同笔画数的字按起笔笔形一 丨 丿 、﹁ 的顺序排列;单列的饮片排在相应 药材的后面 ;制剂中同一正文项下 凡因规 格不同而致内容不同需单列者 ,在其名称 后加括号注明 ;附录(包括制剂通则、通 用检测方法和指导原则)按分类编码。索 引分别按中文索引、汉语拼音索引 、拉丁 名索引和拉丁学名索引顺序排列。
