2012年高考理综化学总复习资料(49)—— 有机化合物官能团的性质
有机化学之官能团性质总结

硝酸酯 硝基化合物
RONO2 R—NO2
酯基
硝酸酯基 —ONO2 硝基—NO2
HCOOCH3 (Mr:60)
1.发生水解反应生成羧酸和醇 酯基中的碳氧单键易断裂
2.也可发生醇解反应生成新酯和新醇
不稳定 一硝基化合物较稳定
易爆炸
一般不易被氧化剂氧化,但多硝基化合物 易爆炸
氨基酸
氨基—NH2 RCH(NH2)COOH 羧基—COOH
分层
色沉淀 出现银镜 色沉淀
呈现 呈现蓝 使石蕊或甲 放出无色 紫色 色 基橙变红 无味气体
溴苯、氯苯归为卤代烃,不过水解是酚,不是醇啊。 硝基能被还原为氨基(铁粉还原)
类 概念
型
分子里某 取 些原子或 代 原子团被 反 其它原子 应 或原子团
所代替
举例(化学方程式) 卤代反应
CH4 + Cl2
CH3Cl + HCl 硝化反应
β-碳上有氢原子才能发生 3.脱水反应:存在浓 H2SO4
消去反应。
140℃分子间脱水成醚
α-碳上有氢原子才能被催 170℃分子内脱水生成烯
化氧化,伯醇氧化为醛, 4.催化氧化为醛或酮
5.去掉氢,发生酯化反应 仲醇氧化为酮,叔醇不能 6.能被重铬酸钾酸性溶液氧化,由橙红色
被催化氧化。
变为绿色
C2H5O C2H5 (Mr:74)
CH3CH=CH2 + NaBr
不饱和 (含双键 或三键) 的化合物
分子中加 氧
氧或去氢 化
以及跟强 反
氧化剂发 应
生的反应
有机物分 还
子中加氢 原
原子或失 反
去氧原子 应
的反应
+ H2O 裂化(深度裂化也叫裂解)
有机物官能团与性质复习
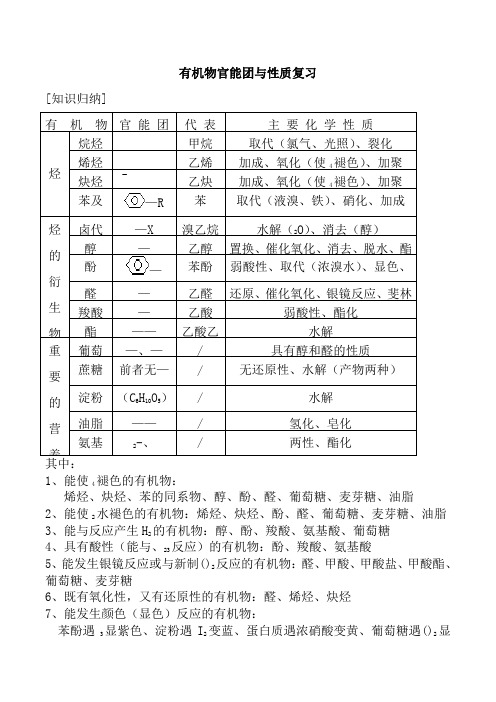
有机物官能团与性质复习[知识归纳]有机物官能团代表主要化学性质烃烷烃甲烷取代(氯气、光照)、裂化烯烃乙烯加成、氧化(使4褪色)、加聚炔烃乙炔加成、氧化(使4褪色)、加聚苯及—R苯取代(液溴、铁)、硝化、加成烃的衍生物卤代—X 溴乙烷水解(2O)、消去(醇)醇—乙醇置换、催化氧化、消去、脱水、酯酚—苯酚弱酸性、取代(浓溴水)、显色、醛—乙醛还原、催化氧化、银镜反应、斐林羧酸—乙酸弱酸性、酯化酯——乙酸乙水解重要的营养葡萄—、—/ 具有醇和醛的性质蔗糖前者无—/ 无还原性、水解(产物两种)淀粉(C6H10O5)/ 水解油脂——/ 氢化、皂化氨基2-、/ 两性、酯化其中:1、能使4褪色的有机物:烯烃、炔烃、苯的同系物、醇、酚、醛、葡萄糖、麦芽糖、油脂2、能使2水褪色的有机物:烯烃、炔烃、酚、醛、葡萄糖、麦芽糖、油脂3、能与反应产生H2的有机物:醇、酚、羧酸、氨基酸、葡萄糖4、具有酸性(能与、23反应)的有机物:酚、羧酸、氨基酸5、能发生银镜反应或与新制()2反应的有机物:醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖6、既有氧化性,又有还原性的有机物:醛、烯烃、炔烃7、能发生颜色(显色)反应的有机物:苯酚遇3显紫色、淀粉遇I2变蓝、蛋白质遇浓硝酸变黄、葡萄糖遇()2显绛蓝[有机物间的相互转化关系]图1:图2:[有机合成的常规方法]1.引入官能团:①引入的方法:烯、炔的加成,烷、苯及其同系物的取代②引入的方法:烯加水,醛、酮加氢,醛的氧化、酯的水解、卤代烃的水解、糖分解为乙醇和2③引入的方法:醇、卤代烃的消去,炔的不完全加成,*醇氧化引入 2.消除官能团①消除双键方法:加成反应 ②消除羟基方法:消去、氧化、酯化 ③消除醛基方法:还原和氧化 3.有机反应类型常见的有机反应类型有取代(包括酯化、水解)、加成、加聚、消去、氧化、还原等。
能够发生各种反应类型的常见物质如下:①烷烃、芳香烃与X 2的反应(1)取代反应 ②羧酸与醇的酯化反应③酯的水解反应 ①不饱和烃与H 2、X 2、(2)加成反应 的反应②醛与H 2的反应(3)加聚反应:烯烃、炔烃在一定条件下的聚合反应。
高中化学常见官能团的性质总结

高中化学常见官能团的性质总结常见官能团的性质一、中学有机化合物分类及常见官能团名称和主要性质在有机化学中,官能团是指有机分子中带有特殊化学性质的原子团。
常见的官能团有羟基、醛基、羰基、羧基、酯基、酰基等。
烷烃中的烷基,芳香烃中的苯基都不是官能团。
二、有机官能团的化学性质与有机基本反应1.氧化反应1)燃烧。
凡是含碳氢的有机化合物燃烧都生成二氧化碳和水。
烃和含氧衍生物的燃烧通式分别为CnH2n+2 +(3n+1)/2O2 → nCO2 + (n+1)H2O和CnH2nOn + (n+1/2)O2 → nCO2 + (n+1)H2O。
2)被酸性高锰酸钾氧化。
能使酸性高锰酸钾褪色的有机物有不饱和烃、不饱和烃的衍生物(含碳碳双键、碳碳三键)、苯的同系物(苯基上的烃基易被氧化)、含醛基的有机物(如醛、甲酸、甲酸酯、甲酸盐、葡萄糖)和石油产品(裂解气、裂化气)。
3)羟基的催化氧化。
某些含羟基的有机物在催化剂的作用下,能被氧气氧化成醛或酮。
当与羟基相连的碳原子上有两个氢原子时,羟基能被氧化成醛基,如2CH3CH2OH + O2 →2CH3CHO + 2H2O。
当与羟基相连的碳原子上有一个氢原子时,羟基能被氧化成羰基(碳氧双键)。
当与羟基相连的碳原子上没有氢原子时,羟基不能被氧化。
4)醛基的氧化。
有机物中的醛基,不仅可以被氧气氧化成羧基,而且还能被两种弱氧化剂(银氨离子和铜离子)氧化成羧基,如2CH3CHO + O2 → 2CH3COOH和CH3CHO +2[Ag(NH3)2]+ + 2OH- → CH3COO- + NH4+ + 2Ag↓ + 3NH3 +H2O和CH3CHO + 2Cu(OH)2 → CH3COOH + Cu2O↓ + 2H2O。
2.取代反应有机物分子中的某些原子或原子团被其他原子或原子团所代替的反应叫做取代反应。
中学常见的取代反应有:1)烷烃与卤素单质在光照下的取代,如CH4 + Cl2 →CH3Cl + HCl。
高中化学(有机官能团化学性质小结表)

高中化学(有机官能团化学性质小结表)
官能团 | 化学性质
---|---
烷基 | 烷基具有亲电性和碱性,能发生置换反应、氧化反应等卤代烷基 | 可发生亲核取代反应和消去反应等
羟基 | 具有醇的性质,可发生酯化反应、醚化反应、酸催化裂解等反应
氨基 | 具有胺的性质,可发生酰化反应、还原反应、烧碱螯合反应等
羧基 | 具有酸的性质,可发生酯化反应、缩合反应、酸催化裂解等
酰基 | 具有酰化的性质,能发生酰化反应、烯醇化反应等
酰胺基 | 具有酰胺的性质,可发生烷化反应、加成反应等
酮基 | 具有酮的性质,可发生加成反应、酯化反应等
醛基 | 具有醛的性质,可发生加成反应、酯化反应等
环氧基 | 具有环氧的性质,可发生开环反应、环氧化反应等苯环 | 具有芳香性,可发生亲电取代反应、电子取代反应等醚基 | 具有醚的性质,可发生加成反应、酯化反应等
烯酮基 | 具有烯酮的性质,可发生加成反应等
烷基硫基 | 具有硫化学的性质,可发生醇化、氧化反应等。
高二化学有机化合物的官能团与性质

高二化学有机化合物的官能团与性质有机化合物是由碳和氢元素以及其他一些元素(如氧、氮、卤素等)组成的化合物。
有机化合物的性质与它们分子中存在的官能团密切相关。
一、醇官能团醇官能团是由羟基(-OH)组成的官能团。
根据羟基的位置,醇可分为一次醇、二次醇和三次醇。
醇具有多种性质。
首先,醇具有醇独特的水解性质。
醇可以和水发生反应,产生相应的羟基离子。
其次,醇能够参与酸碱中和反应。
醇中的羟基会和酸反应生成醚,与碱反应生成盐。
此外,一些醇还具有氧化性。
二、酮官能团酮官能团是由羰基(C=O)组成的官能团。
它是一类特殊的羰基化合物,其中碳原子被两个有机基团取代。
酮的性质主要取决于有机基团的不同。
首先,酮官能团使分子具有极性,有一定的溶解性。
其次,酮官能团的碳原子上的亲电性较高,容易被亲核试剂攻击。
酮化合物在一定条件下可以与亲核试剂发生加成反应,形成新的化合物。
三、醛官能团醛官能团是由羰基(C=O)组成的官能团。
它是一类含有羰基的有机化合物,其中羰基连接一个碳原子和一个氢原子。
醛的性质与它们的结构密切相关。
首先,醛具有较强的还原性。
醛能够被氧化剂氧化,生成相应的酸。
其次,由于羰基的极性,醛具有一定的溶解性,能够在水中形成氢键。
最后,醛还具有亲核试剂与它们发生加成反应的能力。
四、酸官能团酸官能团是由羧基(-COOH)组成的官能团。
羧基是一个碳氧双键和一个羟基的组合。
酸官能团赋予有机化合物酸性。
首先,酸官能团的碳氧双键中的羰基具有极性,使得有机酸具有一定的溶解性。
其次,酸官能团中的羧基可以与碱发生中和反应,生成盐和水。
酸的酸性还与羧基的结构和它所连接的有机基团有关。
总之,有机化合物的官能团与性质密不可分。
醇、酮、醛和酸是有机化合物中常见的官能团,它们赋予了分子不同的性质和化学反应能力。
了解有机化合物中官能团的性质对于理解有机化学的基本原理和化学反应机制非常重要。
有机化学基础知识点整理官能团与官能团的化学性质

有机化学基础知识点整理官能团与官能团的化学性质有机化学基础知识点整理官能团与官能团的化学性质在有机化学中,官能团是指一类具有特定化学性质和在化学反应中发挥特殊作用的原子团或者官能基。
官能团的不同组合和排列方式,决定了有机化合物的性质和反应特性。
本文将整理有机化学中常见的官能团及其化学性质,以帮助读者更好地理解这些基础知识点。
1. 烃类官能团烃是一类仅由碳和氢组成的有机化合物,在官能团的角度来看,烃类官能团可以简单归纳为烷基、烯基和炔基三大类。
烷基是由碳链通过单键相连而形成的官能团,其化学性质相对稳定,难以发生反应。
烯基是指含有碳碳双键的官能团,烯烃的化学性质活泼,容易进行加成反应、氢化反应等。
炔基是指含有碳碳三键的官能团,炔烃的化学性质更为活泼,容易进行加成反应、氢化反应以及与酸、卤素等发生反应。
2. 羟基官能团羟基(-OH)是一类常见的官能团,它的存在使得有机化合物具有醇的特性。
羟基的化学性质主要体现在它的亲电性和亲核性反应中。
例如,醇可以通过酸催化而脱水生成烯丙醇,也可以与酸酐反应生成酯。
此外,醇还具有亲核取代反应、氧化反应和还原反应等性质。
3. 羰基官能团羰基(C=O)是一类重要的官能团,它存在于酮、醛、羧酸和酰氯等化合物中。
羰基的化学性质使得它具备了众多反应途径,如加成反应、还原反应、亲核取代反应以及酸催化等。
酮和醛是羰基官能团的两个典型例子,它们的反应性与取代基的情况、反应条件等因素有关。
4. 羧基官能团羧基(-COOH)是一类含有羧基的官能团,羧基的化学性质主要表现为其酸性。
羧基的酸性主要由羧基内的氧原子吸引共有的电子对而形成,从而使得羧基离子化生成羧酸。
羧酸的酸性与其结构、溶液浓度和环境条件有关。
此外,羧酸还可以发生酯化反应、酰化反应以及酰氯化等反应。
5. 氨基官能团氨基(-NH2)是一类含有氨基的官能团,氨基的化学性质主要表现为其亲电性和亲核性。
氨基可以通过与酸酐反应生成酰胺、与酰卤发生亲核取代反应等。
高考化学专题复习—官能团和有机物的性质
高考化学专题复习—官能团和有机物的性质1、关于化合物2-苯基丙烯(),下列说法正确的是()A.不能使稀高锰酸钾溶液褪色B.可以发生加成聚合反应C.分子中所有原子共平面D.易溶于水及甲苯2、某有机物的结构如图所示,下列关于该有机物的描述不正确的是①所有碳原子可能共面;①能使酸性KMnO4溶液和溴水褪色,且原理相同;①1mol该有机物分别与足量Na或NaHCO3反应,产生气体在相同条件下体积不相等;①能发生酯化反应;①能发生加聚反应;①1mol该有机物完全燃烧生成CO2和H2O消耗O2的体积为280 L(标准状况)A.①①B.①①C.①①D.①①3、有关下图所示化合物的说法不正确的是A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应B.1mol该化合物最多可以与3mol NaOH反应C.既可以催化加氢,又可以使酸性KMnO4溶液褪色D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体4、下列有关有机物的说法正确的是()A.乙烯、氯乙烯、聚乙烯均可以使酸性高锰酸钾溶液褪色B.1 mol苹果酸[HOOCCH(OH)CH2COOH]可与3 mol NaHCO3发生反应C. 酸性条件下,C2H5CO18OC2H5的水解产物是C2H5CO18OH和C2H5OHD.乙酸和油脂都能与氢氧化钠溶液反应5、有机物A的结构如图所示,下列说法中正确的是()A.有机物A易溶于水B.有机物A在铜的催化下与O2反应生成醛C.1 mol A最多能与4 mol H2发生加成反应D.在酸性条件下,有机物A水解形成一种有机物6、某种可用于治疗心脏病的药物X的结构简式为,下列有关X的说法错误的是()A.X可能有香味,是乙酸乙酯的同系物B.X不溶于水,密度可能比水的小C.遇碱溶液或酸溶液均易变质D.与X互为同分异构体7、屠呦呦率领团队先后经历了用水、乙醇、乙醚提取青蒿素的过程,最终确认只有采用低温、乙醚冷浸等方法才能成功提取青蒿素。
高考一轮复习化学课件:官能团的性质与有机反应类型归纳总结
官能团保护和去保护策略
官能团保护
在合成过程中,为了避免某些官能团发生不必要的反应, 需要采取保护措施,如酯化保护羟基、乙酰化保护氨基等 。
官能团去保护
在合成完成后,需要去除保护基团以恢复官能团的原有性 质,如水解去除酯基保护、酸解去除乙酰基保护等。
保护与去保护的选择
根据具体反应条件和目标分子结构,选择合适的保护和去 保护策略。
。
03
利用特征反应
针对某些具有特征反应的官能团,如酚羟基的氧化、醛基的银镜反应等
,进行快速识别。
利用官能团转化关系进行合成设计
官能团之间的转化
了解不同官能团之间的转化条件和反应机理,如 酯化反应、还原反应等。
逆推法
从目标分子出发,逆向分析合成路线,逐步确定 所需官能和反应条件。
合成路线优化
考虑原料来源、反应条件、产率等因素,选择最 优合成路线。
金属催化反应
炔烃在金属催化剂(如林德拉催化剂)作用下,可发生顺式或反式 加氢反应,生成相应的烯烃或烷烃。
亲核加成
炔烃可与含有活泼氢的化合物(如水、醇、胺等)发生亲核加成反 应。
烯烃和炔烃聚合反应
自由基聚合
在引发剂作用下,烯烃和炔烃可发生自由基聚合反应,生成高分子 化合物。
离子聚合
在特定条件下,烯烃和炔烃也可发生离子聚合反应。
化学性质
羧基具有酸性,可以电离出氢离子,与碱发生中和反应。此外,羧基还可以与 醇发生酯化反应,生成酯和水。
羧酸与碱中和反应
中和反应
羧酸与碱发生中和反应,生成羧酸盐和水。例如,乙酸与氢氧化钠反应生成乙酸 钠和水。
方程式表示
R-COOH + NaOH → R-COONa + H2O(R代表烃基)
高考化学有机重点——官能团知识汇总
高考化学有机重点——官能团知识汇总有机化学中,官能团是同学们很头痛一个地方,不管是同分异构体的书写还是有机物的性质都离不开它。
那么今天就给大家好好的汇总一下有关高中化学有机官能团的知识。
同学们在后面的学习中也要学会利用汇总的方法去记忆,这样才能将学习的知识融会贯通!有机物官能团与性质其中:1、能使KMnO4褪色的有机物:烯烃、炔烃、苯的同系物、醇、酚、醛、葡萄糖、麦芽糖、油脂2、能使Br2水褪色的有机物:烯烃、炔烃、酚、醛、葡萄糖、麦芽糖、油脂3、能与Na反应产生H2的有机物:醇、酚、羧酸、氨基酸、葡萄糖4、具有酸性(能与NaOH、Na2CO3反应)的有机物:酚、羧酸、氨基酸5、能发生银镜反应或与新制Cu(OH)2反应的有机物:醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖6、既有氧化性,又有还原性的有机物:醛、烯烃、炔烃7、能发生颜色(显色)反应的有机物:苯酚遇FeCl3显紫色、淀粉遇I2变蓝、蛋白质遇浓硝酸变黄、葡萄糖遇Cu(OH)2显绛蓝有机物间的相互转化关系有机合成的常规方法1.引入官能团:①引入-X的方法:烯、炔的加成,烷、苯及其同系物的取代②引入-OH的方法:烯加水,醛、酮加氢,醛的氧化、酯的水解、卤代烃的水解、糖分解为乙醇和CO2③引入C=C的方法:醇、卤代烃的消去,炔的不完全加成,*醇氧化引入C=O2.消除官能团①消除双键方法:加成反应②消除羟基方法:消去、氧化、酯化③消除醛基方法:还原和氧化3.有机反应类型常见的有机反应类型有取代(包括酯化、水解)、加成、加聚、消去、氧化、还原等。
能够发生各种反应类型的常见物质如下:(1)取代反应:①烷烃、芳香烃与X2的反应②羧酸与醇的酯化反应③酯的水解反应(2)加成分应:①不饱和烃与H2、X2、HX的反应②醛与H2的反应(3)加聚反应:烯烃、炔烃在一定条件下的聚合反应。
(4)消去反应:某些醇在浓H2SO4作用下分子内脱水生成烯烃的反应。
有机物与H2的加成反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2012年高考理综化学总复习资料(49)——有机化合物官能团的性质
班别:____________学号:____________姓名:____________
【练习1】
1.克矽平是一种治疗矽肺病的药物,其合成路线如下(反应均在一定条件下进行):
(1)化合物Ⅰ的某些性质类似苯。
例如,化合物Ⅰ可以一定条件下与氢气发生加
成反应生成右图所示结构,其反应方程式为:
(2)如果化合物Ⅰ可以和Cl 2在光照的条件下发生取代反应,则其反应方程式为:
(3)化合物Ⅱ生成化合物Ⅲ的反应方程式为(不要求标出反应条件)
化合物Ⅲ也可以转化生成化合物Ⅱ,则该反应方程式为(不要求标出反应条件)
(4)化合物Ⅲ生成化合物Ⅳ的反应方程式为(不要求标出反应条件)
(5)下列关于化合物Ⅱ和化合物Ⅲ的化学性质,说法正确的是 (填字母)
A 化合物Ⅱ可以与CH 3COOH 发生酯化反应
B 化合物Ⅱ不可以与金属钠生成氢气
C 化合物Ⅲ可以使溴的四氯化碳溶液褪色
D 化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
— O Ⅰ Ⅱ Ⅲ Ⅳ 克矽平
3
笔记:烷烃、烯烃、苯与甲苯的性质及反应特点
【拓展1】CH2=CHCH3和Cl2在500℃的条件下发生取代反应,则其反应方程式为:
【练习2】
1.在一定条件下可以发生如下反应:
(1)下列关于化合物I、Ⅱ和Ⅲ的说法中,正确的是(填字母)。
A.化合物I可以发生氧化反应
B.化合物I与金属钠反应不生成氢气
C.化合物Ⅱ可以发生水解反应
D.化合物Ⅲ不可以使溴的四氯化碳溶液褪色
E.化合物Ⅲ属于烯烃类化合物
(2)写出由化合物I合成化合物Ⅱ的反应方程式(不要求标出反应条件)。
(3)按要求书写化学反应方程式:
①写出化合物I发生催化氧化的反应方程式:。
②写出化合物I发生消去反应的方程式:。
③分别写出化合物Ⅱ酸性、碱性水解的方程式:。
④化合物Ⅲ使溴的四氯化碳溶液褪色的方程式:。
笔记:醇、酯的性质及反应中断键、成键的情况
【练习3】
3、已知苯甲醇有以下变化过程:
(1)苯甲醇的结构简式为。
苯甲醇可由C6H5CH2Cl在NaOH水溶液中发生取代反应而得,反应方程式为。
(2)化合物Ⅰ的结构简式为。
写出化合物Ⅰ转化成化合物Ⅱ的反应方程式:。
(标出具体反应条件) 4、在一定条件下可以发生以下反应:
(1)由通过消去反应
....制备I的化学方程式为(注明反应条件)_________ ___ _。
(2)化合II与过量C2H5OH在酸催化下发生酯化反应
....,生成的有机物的结构简式为
________ ____________。
笔记:醛、卤代烃的性质及反应特点
【拓展2】若要用CH2=CHCH3来合成CH2=CHCH2OH,你可以设计反应来完成吗?方程式为:_________ ___ _
_________ ___ _。
【课后练习】
1.(2009广州一模25)一种高分子化合物(Ⅵ)是目前市场上流行的墙面涂料之一,其合成路线如下(反应均在一定条件下进行):
回答下列问题:
(1)目前工业上生产乙烯主要是以_________为原料通过__________反应来实现。
(2)化合物Ⅲ生成化合物Ⅳ的副产物为_____________________。
(提示:该反应的逆反应原子利用率为100%)
(3)写出合成路线中从化合物Ⅳ到化合物Ⅵ的两步反应方程式:(不要求标出反应条件)
______________________________________________________________________;
______________________________________________________________________。
(4)下列关于化合物Ⅲ、Ⅳ和Ⅴ的说法中,正确的是(填字母)。
A.化合物Ⅲ可以发生氧化反应B.化合物Ⅲ不可以
...与NaOH 溶液反应C.化合物Ⅳ能与氢气发生加成反应
D.化合物Ⅲ、Ⅳ和Ⅴ均可与金属钠反应生成氢气
E.化合物Ⅳ和Ⅴ均可以使溴的四氯化碳溶液褪色F.化合物Ⅴ可以发生水解反应。
