有机化学 第八章 卤代烃.
合集下载
有机化学第8章卤代烃

在SN2反应中
进攻试剂是从离去基团的背面进攻碳原子的。 进攻试剂是从离去基团的背面进攻碳原子的。 当Nu与碳原子接近时,C-Nu之间的化学键逐渐形成,而C-X之间的 Nu与碳原子接近时,C Nu之间的化学键逐渐形成,而C 化学键逐渐变弱,三者基本在同一直线上,形成了反应的过渡态,中心 碳由sp 转化为sp 碳由sp3转化为sp2杂化状态, Nu继续接近碳原子并与碳原子完全键合,离去基团完全离去,由过渡状 Nu继续接近碳原子并与碳原子完全键合,离去基团完全离去,由过渡状 态变为产物。
1)被羟基取代 加热 R-X + KOH(NaOH,水溶液) KOH(NaOH,水溶液) 2)被烷氧基取代 R-X + R`ONa R-O-R` +NaX R此反应也称为Wiliamson合成反应 合成反应。 此反应也称为Wiliamson合成反应。 3)被NH3取代 R-X + NH3 R-NH2(胺) + HX 胺是有机碱,它与反应生成的HX成盐 成盐, 胺是有机碱,它与反应生成的HX成盐,RNH3+XR-OH + KX
查依采夫规律
一般叔卤代烷最易消去,而伯卤代烷最难。 一般叔卤代烷最易消去,而伯卤代烷最难。仲或叔卤代烷 氢可以消去,因而产物不同。 有几个β氢可以消去,因而产物不同。 1875年俄国化学家查依采夫根据大量事实指出 年俄国化学家查依采夫根据大量事实指出: 1875年俄国化学家查依采夫根据大量事实指出:在β-消 去反应中主要产物是双键碳原子上烃基最多的烯烃, 去反应中主要产物是双键碳原子上烃基最多的烯烃,即得 到最稳定的烯烃。-- 。--查依采夫规律 到最稳定的烯烃。--查依采夫规律
溴甲烷在NaOH溶液中反应生成甲醇,反应时OH 溴甲烷在NaOH溶液中反应生成甲醇,反应时OH-从背面接近中 心碳原子,必须克服三个氢原子的阻力,同时三个C 心碳原子,必须克服三个氢原子的阻力,同时三个C-H键的偏 转使键角发生变化,因而体系的能量升高。达到过渡状态时,能 量也达到最高点。随着溴离子的进一步离去和C 量也达到最高点。随着溴离子的进一步离去和C-O键的进一步 形成,体系的能量逐渐降低,最后形成产物。
《有机化学》第三版 第8章

allyl bromide
有些多卤代烷有其特别的名称,常用俗名或商品名或根据来源命名,例如 CHCl3 称为 氯仿(chloroform) ,CHBr3 称为溴仿(bromoform) ,CHI3 称为碘仿(iodoform) ,CCl4 称为
2
四氯化碳(carbon tetrachloride) 。 2.系统命名法 卤代烃可以看作是烃的衍生物,把卤原子作为取代基,烃作为母体。命名的基本原则与 烃的命名规则相同。对于不饱和卤代烃,编号时,应尽可能使不饱和键的位次最小。双键有 立体构型则还要标出其构型。英文命名时,卤原子用词头 fluoro-、chloro-、bromo-、iodo-表示。 例如:
图 8-3 溴乙烷的 1H-NMR 谱
6
图 8-4 异丙基溴的 1H-NMR 谱 8.3 卤代烃的制备
目前从自然界中发现的天然卤代烃数目很少, 绝大多数卤代烃是通过合成方法得到的。 由于 卤代烃化学性质活泼, 通过化学反应可把卤代烃转化为多种含重要官能团的化合物, 卤代烃 的制备显得非常重要。 8.3.1 饱和碳原子上氢原子的卤代 在光照或高温条件下,烷烃与卤素发生自由基取代反应生成卤代烷(见 4.1 节) ,但烷烃 中几种不同的氢的反应活性相差不大,卤素的反应活性又高(如氯气)的情况下,常常得到 混合物,而且得到的混合产物很难通过化学方法分离,所以一般情况下,通过烷烃的自由基 卤代反应制备卤代烃的意义不大。 但这种自由基取代反应通常用来制备烯丙型和苄基型卤代 烃。工业上,可以通过调节烷烃与卤素的摩尔比和反应条件,来制备一氯甲烷和四氯化碳。 下面这些烃的自由基卤代反应具有较高的选择性,可用于制备卤代烃。
通常把卤素连在双键 α 碳原子上的卤代烃称为烯丙型卤代烃, 卤素直接连在双键碳原子 上的称为乙烯型卤代烃,卤素连在苯环 α-碳原子上的称为苄基型卤代烃,卤素直接连在苯 环上的称为苯基型卤代烃。
有机化学课后习题答案-南开大学版-8卤代烃

(4) O2N Br
NH2
(5)
C=C
3.按与 NaI-丙酮反应的活性顺序排列下面化合物。 (5)>(4)>(1)>(2)>(3)>(6) 4. 按与 AgNO3-酒精(SN1)反应活性顺序排列下列化合物。 (2)>(1)>(4)>(3)>(6)>(5) 5. 比较下列每对反应的速度。 (1)~(6): 全都是 b>a。 6.完成下列转化:
Cl2/H2O Cl2 hv
CH3CHCH2Cl CH2CH=CH2 Cl
Cl2/H2O
b: CH3CH2CH2Cl NaOH/C2H5OH CH3CH=CH2
CH2CH CH2 Cl OH Cl
(3)
OH
PBr3
Br
(CH3)2CuLi
CH3
1
(4)
BrCH3MgI源自CH3Mg 乙醚 Na D2O
CH3CH2 O CH2 Cl
CH3 Cl H CH3 H H B CH3
CH3CH2 O CH2+
CH3CH2O=CH2
+
H 14. H
CH3
Cl H
CH3 H
C=C
H CH3
Cl H
CH3
CH3 H
Cl H
CH3
CH3 H B
H CH3
C=C
H CH3
H
H
CH3 H
CH3
Cl H
CH3 H B
CH3
CHCH2CH3 苄卤代烃 CH2CHCH3 仲卤代烃
1-苯基-1-氯丙烷
1-苯基-2-氯丙烷
CH2CH2CH2Cl
Cl 伯卤代烃
有机化学-第八章

试剂的亲核性大小主要是由两个因素决定的。一个是试剂 的碱性(给电子性),一个是试剂的极化度(变形性)。 这两个因素对试剂的亲核性的影响通常是一致的;但也有 不一致的情况,这时往往是后者起主导作用,有时还与溶 剂性质有关。
8.2 卤代烷的亲核取代反应
1.同一周期的原子作为亲核中心时,试剂的亲核性与碱性 有相同的强弱次序:
的生成。因此,烷基碳正离子越稳定,越易形成,生成时 的活化能越低,反应速率也越快,由于烷基正离子稳定性 的顺序是:
(CH3)3C+ > (CH3)2CH+ > CH3CH2+ > CH3+ 所以,在 SN1 反应中,卤代烷的活性顺序为:
R3CX > R2CHX > RCH2X > CH3X 即 (3° > 2° > 1° > CH3X)
例如, I- 在下面各溴代烷的丙酮溶液中于25℃发生 SN2 反应时的相对反应速率为:
8.2 卤代烷的亲核取代反应
如果在卤代烷的 β- 碳原子上连有支链烷基时,对 SN2 反应的速率也有明显的影响,即卤代烷中心碳( α- 碳)
原子上连接的烷基体积越大,其空间位阻越大,不利于亲
核试剂的攻击。例如,在 C2H5OH 溶剂中 C2H5ONa 与下面 各溴代烷于55℃发生 SN2 反应的相对反应速率为:
C-Cl > C-Br > C-I
根据卤原子变形性的大小可知不同的碳卤键的可极化度的 大小次序与其极性大小次序相反。
8.1 卤代烃的分类及结构
由于卤原子的电负性大于饱和碳原子的电负性, 使饱和卤代烃的碳卤键的成键电子偏向卤原子一 方,而碳原子 具有缺电子的特征,即:
8.1 卤代烃的分类及结构
8.2 卤代烷的亲核取代反应
1.同一周期的原子作为亲核中心时,试剂的亲核性与碱性 有相同的强弱次序:
的生成。因此,烷基碳正离子越稳定,越易形成,生成时 的活化能越低,反应速率也越快,由于烷基正离子稳定性 的顺序是:
(CH3)3C+ > (CH3)2CH+ > CH3CH2+ > CH3+ 所以,在 SN1 反应中,卤代烷的活性顺序为:
R3CX > R2CHX > RCH2X > CH3X 即 (3° > 2° > 1° > CH3X)
例如, I- 在下面各溴代烷的丙酮溶液中于25℃发生 SN2 反应时的相对反应速率为:
8.2 卤代烷的亲核取代反应
如果在卤代烷的 β- 碳原子上连有支链烷基时,对 SN2 反应的速率也有明显的影响,即卤代烷中心碳( α- 碳)
原子上连接的烷基体积越大,其空间位阻越大,不利于亲
核试剂的攻击。例如,在 C2H5OH 溶剂中 C2H5ONa 与下面 各溴代烷于55℃发生 SN2 反应的相对反应速率为:
C-Cl > C-Br > C-I
根据卤原子变形性的大小可知不同的碳卤键的可极化度的 大小次序与其极性大小次序相反。
8.1 卤代烃的分类及结构
由于卤原子的电负性大于饱和碳原子的电负性, 使饱和卤代烃的碳卤键的成键电子偏向卤原子一 方,而碳原子 具有缺电子的特征,即:
8.1 卤代烃的分类及结构
有机化学-第8章:卤代烷

Zn + HCl
CH3(CH2)14CH2I
CH3(CH2)14CH3
RX HI RI HI
-HX
RH + I2
卤代烷的还原
2 中性还原剂
催化氢化
RX (or ArX) H2 / Pd*
RH (orArH) * PdC, Ni, Pt
O
OH
CH2CCH3
CH2CHCH3
O2N
C=N H2 / Pd C H2N
H Br H
CH2 = CHCH2CH3+ CH3CH=CHCH3
19%
81%
CH3 CH3CHCHCH2
H Br H
叔卤代烷
C2H5ONa, C2H5OH
CH3
CH3 CH= C(CH3)2+ CH3CH2C=CH2
71%
29%
消除反应 ( E )
Saytzeff(查依采夫)规律
(1875年俄国化学家Saytzeff总结了当时已知的大量实验事实, 得出以下经验结论.)
(3) ( 4S )-4-甲基-5-乙基-1-溴庚烷 CH3 H
CH3CH2CH C CH2CH2CH2Br C2H5
(2) ( 2S,3S )-2-氯-3-溴丁烷
H Br Cl H CH3 C C CH3
4. (1R,3R)-1,3-二溴环己烷
Br H
H Br
卤代烷的普通命名法
CH3CH2CH2CH2Cl
H2 H1
慢
Br
-
HO
C
-
Br
快
HO
H1 C H2
Br-
H3
定义:
H3ห้องสมุดไป่ตู้
华中科技大学有机化学第八章 卤代烃
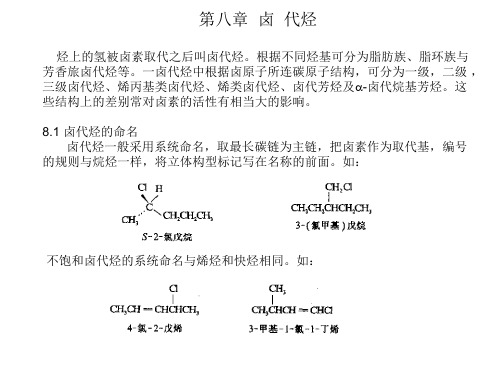
(3) SN1与SN2反应影响因素的比较 它们都属取代反应,但历程不同,因此影响反应速度的因素也各异。 扼要归纳于下表。
如何判断亲核取代反应按SN1还是SN2历程进行,由卤代烃的烃基 部分决定。烃基为伯基或者甲基一般按SN2历程,为叔丁基按SN1历 程,为仲基,烯丙基或者苄基可以是SN1或者SN2。
由实验得知该反应的反应速度与卤代烷和碘负离子的乘积成正比:
同时产物的构型发生转换,即由R转换成S。而叔丁基溴与乙醇加热回流得 到乙基叔丁基醚的反应速度,与乙醇浓度无关,只与叔丁基溴浓度有关。
旅光性的R-2-溴辛烷与水反应得到外消旋的dl-2-辛醇。 从上述实验结果看出,它们用于两种不同的反应过程。推断其历程如下:
这种起始于亲核试剂的进攻而发生的取代反应.称为亲核取代反应, 常用SN来表示(S代表取代反应,N代表亲核试剂进攻)。 亲核取代反应种类很多,在合成上很有用,一些常见的取代反应类 型与取代反应产物的种类如下表。
(1)取代反应历程 SN2与SN1取代反应。反应历程一般是通过测定反应速度与反应物浓度的关 系,以及分析产物构型来推断的。卤代烷与碘化钠在丙酮溶液中的取代反应 是这类反应的典型例子:
从AgX沉淀的速度可以判断此反应的速度,而卤代烷进行SN1与E1反应的 速率为:
NaI-丙酮溶液与卤代烷的反应是按SN2历程进行的, 因此卤代烷的活性次序为:
在卤代烷中加NaI丙酮溶液, 在室温,立即有沉淀产生的为一级溴代烷, 苯甲基卤,烯丙基卤;在50℃,放置3min,有沉淀的为一级氯代烷、二级溴 代烷;50℃,放置长时间出现沉淀的为三级卤代烷、氯代环己烷等。所以, NaI-丙酮与AgNO3-乙醇溶液的测试是很方便的鉴定卤代烷结构的方法。
反应温度升高不利于取代反应。如
天津工业大学有机化学 卤代烃

卤代芳烃: Cl 氯苯
CH2Br 苄基溴
C 按卤素所连的碳原子的类型:
R
RCH2 X
R R
CH X
CX R
R
伯卤代烷(1°) 仲卤代烷(2°) 叔卤代烷(3°)
CH3 CH3CCH2Br
CH3
2,2–二甲基– 1–溴丙烷
CH3
CH3CHCH2CH3 CH3CCH2CH2CH3
Br 2–溴丁烷
Br 2–甲 基–2– 溴戊烷
用途:制备复杂结构的烷烃
, Ph ; X=I, Br, Cl
CH3(CH2)3CH2Br (CH3CH2CH-)2CuLi
CH3
CH3CH2CHCH2CH2CH2CH2CH3 CH3 3- 甲基辛烷 84%
OH R OH
醇
R'OH R OR'
醚
SH R SH
硫醇
R'S
(-X-)
RX
CN
(R = Me, 1°, 2°) O (X = Cl, Br或I) R'CO
CH3(CH2)10CH2OH
SOCl2 回流 7h
CH3(CH2)10CH2Cl
4 卤原子交换
H3C
CH3CΒιβλιοθήκη Cl+NaI
ZnCl2, CS2 室温
H3C
CH2CH3
CH3 C I + NaCl CH2CH3 (96%)
5 偕(连)二卤代烷部分脱卤化氢
CH2 CH CH2
+
NaOH
H2O △
Br Br Br
反应活性: R X : RI > RBr > RCl > RF 1° > 2° > 3°
有机化学第八章卤代烃

该反应是法国有机化学家Grignard(格利雅)于1901年在他的博士论 文研究中首次发现的。为纪念这位化学家对化学事业的贡献,人们 将烷基卤化镁称为Grignard试剂,而把有Grignard试剂参与的反 应,称为Grignard反应。
第15页/共52页
制备Grignard试剂所用的溶剂:乙醚、四氢呋喃(THF)、其 它醚(如:丁醚)、苯等。Grignard试剂在醚中有很好的溶解度, 醚作为Lewis碱,与Grignard试剂中的Lewis酸中心镁原子形 成稳定的络合物。乙醚的作用既是溶剂,又是稳定化剂。
吡啶 回流
R-CL + SO2 + HCl
第7页/共52页
三、卤代烷的互换
§ 8—3 卤 代 烷的性质
一、物理性质 (略) 二、化学性质
卤代烃的化学性质活泼,且主要发生在C—X 键上。 ① 分子中C—X 键为极性共价键,碳带部分正电荷,易受带负电荷 或孤电子对的试剂的进攻。
第8页/共52页
卤代烷:
4、与醇钠(RONa)反应
R-X + R'ONa
R-O R' + NaX 醚
R-X一般为1°RX,(仲、叔卤代烷与醇钠反应时,主要发生消除反应
生成烯烃)。该法是合成不对称醚的常用方法,称为 Williamson (威廉逊)合成
法。该法也常用于合成硫醚或芳醚。
5、与AgNO3—醇溶液反应
醇 R-X + AgNO3
按卤素所连的碳原子的类型
R-CH2-X
伯卤代烃 一级卤代烃(1°)
R2CH-X
仲卤代烃 二级卤代烃(2°)
R3C-X
叔卤代烃 三级卤代烃( 3°)
二、命名
1、简单的卤代烃用普通命名或俗名,(称为卤代某烃或某基卤)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C H 2B r
10
O + O N-Br
CCl4 沸腾,80%
Br +
O N-H O
N-溴代丁二酰亚胺(NBS)
3)芳烃的卤化
CH3 CH3
+
CH3 X
+
X2
Fe
X
2018/10/8 11
2、 由醇制备
醇分子的羟基被卤原子取代而得到相应的卤代烃,这是 制备卤代烃的最常用方法,实验室和工业上都可采用。
2018/10/8 9
1、 烃类的卤代反应
1)烷烃和环烷烃的卤化
在光照和加热的条件下,烷烃和环烷烃可以直接 和卤素作用,产物为一元和多元卤代物的混合物。
2)-H的卤化
CH3CH CH2
Cl2 NBS
CH2CH CH2 Cl CH2CH CH2 Br
C l2
CH3 NBS
2018/10/8
C H 2C l
R OH + HCl
RCl + H2O
除卤化氢外,其它常用的卤化试剂有卤化磷和氯化亚砜等。
R OH + PCl5 R OH + SOCl2
RCl + POCl3 + HCl RCl + SO2 + HCl
2018/10/8
12
3、 不饱和烃的加成
不饱和烃与卤化氢或卤素加成得到卤代烃,这 也是制备卤代烃的常用方法,可用于制备一卤代物 和多卤代物。
2018/10/8 18
水解反应与R结构有关
Cl
NaOH, H2O 。 300 C, 20MPa
OH
2018/10/8
19
(2) 与氰化钠作用
在NaCN的醇溶液中进行,得腈。
´ ¼
RX + Na CN
+
-
RCN + Na+XH2O
RCOOH
该反应是增长碳链的方法之一。(增加一个C)
Cl CH2Cl
X CH2X
2018/10/8
卤代烯烃
乙烯式 烯丙式 孤立式
卤代芳烃
乙烯式
烯丙式
3
二、 按卤素所连的碳原子的类型,分为:
R-CH2-X
伯卤代烃 一级卤代烃 (1° )
(CH3)2CHCH2Cl
R2CH-X
仲卤代烃 二级卤代烃 (2° )
CH3CH2CHClCH3
R3C-X
叔卤代烃
三级卤代烃 (3° )
三氯甲烷(氯仿) 正丙基氯 异丙基氯 叔丁基溴
CH2 =CH-CH2Br CH2Cl
烯丙基溴 氯化苄 (苄基氯)
2018/10/8
5
二、系统命名:(把卤素作为取代基,烃为母体) ①主链:连有卤原子并且支链最多的最长碳链;
②主链编号:最低序列原则、基团次序规则、较优基 团编号大;
③列出顺序:较优基团后列出.
∨
俗名或商品名
CHCl 3
2018/10/8
Cl CCl 2F2 Cl Cl
Cl Cl Cl
8
CHI 3
氯仿
碘仿
氟利昂
六六六
8.2
卤代烃的制法 ( P226)
卤代烃主要制法有两类: 一、直接在烃类分子中引入卤原子, 二、将分子中其它官能团取代成为卤原子。
1、 烃类的卤代反应 2、 从醇制备 3 、从不饱和烃制备 4 、卤原子交换
第八章
卤代烃 ( P210)
烃分子中的氢原子被卤素取代的衍生物。 天然存在的卤代烃种类不多,大多数卤代烃 属于合成产物。 卤代烃一般用RX表示(X=F,Cl,Br,I),卤原子 是卤代烃的官能团。 卤代烃容易发生碳卤键异裂、卤素被取代的反 应,因此在有机合成中起桥梁作用。
2018/10/8
1
卤代烃用途广泛:可以作为灭火剂、制冷剂、气雾 剂、干洗剂、溶剂等。某些卤代烷如氟氯碳化合物(氟 利昂)也是大气污染的主要来源之一, 能导致臭氧层的 破坏,增加地表面的紫外线辐射强度。
2018/10/8
16
8.3.1 亲核取代反应(SN)
Nu : + R
亲核试剂
-
d+ CH2
d X
R
CH2
Nu
+X:
-
底物
产物
离去基团
亲核取代反应: 由亲核试剂进攻而引起的取代 反应。 常见亲核试剂:H2O , NH3 , OH-, RO-, CN,AgNO3等
2018/10/8 17
(1) 水 解
X RC CH HX RC X
2018/10/8
CH2
HX
RC X
CH3
13
4 、卤原子交换
氯代烷或溴代烷与NaI 或KI在无水丙酮中共热,生成 碘代物,该反应只适用于碘烷。
RCl + NaI 丙酮 RI + NaCl
(可制伯碘烷)
例:
RCH=CH2 + HBr
过氧化物
RCH2CH2Br
NaI/丙酮
在H2O或H2O/OH-中进行,得醇。
RX + H2O
É Ä ¿ æ · ´ Ó ¦
ROH + HX £
H2O
OH-
H2O + X
-
例:
C2H5Cl + NaOH
C2H5OH + NaCl
Байду номын сангаас
反应活性:RI>RBr>RCl>RF(难) 加碱的原因:① 亲核性:OH->H2O; ② OH-可中和反应生成的HX。
卤代烯烃命名时,以烯烃为母体,以双键位次最小编号。
∨
×
(Z)-3,5-二甲基-4-乙基-1-氯-3-己烯
2018/10/8 7
卤原子连在环的侧链时:环和卤原子为取代基, 侧链烃为母 体。
CHCH2CHCH3
1CH3 2 3 4 5
2-环己基-4-碘戊烷
I
CH3 CH CH2CH2Cl
3-苯基-1-氯丁烷 2-苯基-4-氯丁烷
说明:目前明令禁止的是 氯氟烃类产品,对于氢氯氟 烃类产品和氢氟烃类制冷剂, 还要有相当长的一段使用时 间。
氯氟烃
2018/10/8 2
8.1 卤代烃的分类和命名( P210)
8.1.1 卤代烃的分类
一、按分子中卤原子所连烃基类型,分为:
卤代烷烃 R-CH2 -X R-CH=CH-X R-CH=CH-CH2-X R-CH=CH(CH2)n-X n≥2
RCH2CH2I
2018/10/8
14
8.3
卤代烷的化学性质 ( P213)
卤代烃的化学反应主要发生在官能团卤原子以 及受卤原子影响而比较活泼的β-氢原子上。
R
CH H
d+ CH 2
X
亲核取代反应
β-消除反应
d
-
2018/10/8
15
已学历程复习
• 自由基取代反应——烷烃饱和氢氯代; • 自由基加成反应——烯烃与溴化氢的加成过氧化物效应; • 亲电加成反应——烯烃的加成; • 亲电取代反应——芳环的取代反应。
(CH3)3 CCI
三、按分子中所含卤原子的数目,分为:
一元卤代烃 多元卤代烃
CH3CH2Br
ClCH2CH2Cl
CH2Br2
CCl4
2018/10/8
4
8.1.2 卤代烃的命名
一、 普通命名法 “某烃基卤”或“卤(代)某烷”
CHCl3 CH3CH2CH2Cl (CH3) 2CHCl
3CBr (CH3)
