金属极化曲线的测定实验报告
极化曲线测试实验

极化曲线的测试与分析一.实验目的:掌握测定金属极化曲线的方法;二.实验装置及实验材料1.电化学测量系统(PS-268A 型) 1 台2.计算机 1 台3.三电极系统(研究电极:试样;参比电极:甘汞;辅助电极;铂) 1 套4. 低碳钢电化学试样 1 个5. 碳钢挂片试样 4 个6. 过饱和KCl 、蒸馏水、丙酮、脱脂棉、砂纸等若干7. 量尺、分析天平、量杯、烧杯、毛刷等。
三.实验原理1、电化学腐蚀原理金属腐蚀按腐蚀机理可分为化学腐蚀,电化学腐蚀两类。
电化学腐蚀是指金属表面与电解质溶液发生电化学反应而引起的破坏。
其特点是反应过程中金属构成电极,整个系统有阳极失去电子和阴极获得电子及电子流动的产生。
电化学腐蚀服从电化学动力学的基本规律。
当金属浸入电解质溶液时,由于水分子极性的静电作用,或由于金属电子的吸附作用。
在两相界面的两侧将形成由电子层与正离子层组成的双电层。
由于双电层的存在而产生的电位差称为金属―溶液体系的电极电位。
不同的金属在不同的溶液体系中有不同的电极电位。
至今还没有可靠的方法可以测定金属电极电位的绝对值,但可以求其相对值。
通常是指定某一电位稳定的电极为基准电极也叫参比电极或参考电极,人为规定其电位值;再把它与被研究电极组成原电池;测定出原电池的电动势,则被研究电极的电极电位就被测出。
通常采用的参比电极是标准氢电极,但在实际工作中常常采用更方便、更结实的参比电极,如甘汞电极,银-氯化银电极等。
实际上,金属大多是含有杂质的或者以合金的形态存在。
因此,金属浸入电解质溶液后,其界面不是存在单一电极而是存在着几个电极,测得的电位也是其混合值,金属与电解质溶液接触一定时间后, 达到的稳定电位值称为 该金属在该电解质溶液中的腐蚀电位或自然腐蚀电位, 又叫开路电位或混合电 位。
腐蚀电位决定于金属材料的成分,金相组织结构,表面状态以及电解质溶 液的成分,浓度,温度和 PH 值等。
腐蚀电位的大小与金属腐蚀速度之间没有简单的对应关系, 但其可以大致 指出金属的耐腐蚀性。
实验八恒电流法测定金属阴极极化曲线
序号
I
dI
Φ
dΦ
现象
3.测自腐蚀电位
(1)预热 15 分钟
(2)“断”“ 恒电位”“ 电流”“ 参比”此时,电位显示为自腐蚀电位,但符号相反 。
加阴极电流
“恒电流”“ 参比”“ 通”“ 电流”(给定电流-50μA)2 min,重测自腐蚀电位 Φa 。
4.极化曲线测量
自腐蚀电位为原始,电流程 2 mA
“恒电流”、“给定”、“通”,I1=-10μA (表显示) dI=1μA “参比” 、“通”读数,逐点测定。 注意:电流表上“-”为阴极极化数据
实验八恒电流测定金属阴极极化曲线
一、实验目的: 1. 掌握恒电流法测定阴极极化曲线的基本原理和方法; 2. 运用极化曲线初步判定实施阴极保护的可能性; 二、基本原理:
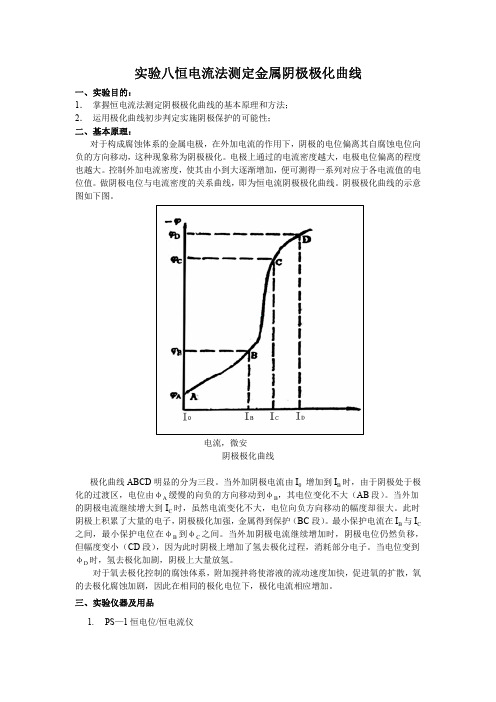
对于构成腐蚀体系的金属电极,在外加电流的作用下,阴极的电位偏离其自腐蚀电位向 负的方向移动,这种现象称为阴极极化。电极上通过的电流密度越大,电极电位偏离的程度 也越大。控制外加电流密度,使其由小到大逐渐增加,便可测得一系列对应于各电流值的电 位值。做阴极电位与电流密度的关系曲线,即为恒电流阴极极化曲线。阴极极化曲线的示意 图如下图。
2. 饱和甘汞电极,铂电极,金属试件(碳钢) 3. 盐桥(饱和氯化钾溶液) 4. 试剂瓶 2 个 (一个放饱和 KCl,一个放 3% NaCl) 5. 铁夹 6. 1200#金相砂纸 无水乙醇棉球 四、实验步骤 1.将以打磨的试件用 1200#金相砂纸打磨,无水乙醇清洗,脱脂,测面积 1 cm2。 2.按下面接线
实验一极化曲线的测定

实验一极化曲线的测定一、实验目的1.掌握用“三电极”法测定不同金属的极化曲线。
2.了解极化曲线的意义和应用。
3.讨论极化曲线在金属腐蚀与防护中的应用。
二、实验概述为了探索电极过程的机理及影响电极过程的各种因素,必须对电极过程进行研究,而在该研究过程中极化曲线的测定乂是重要的方法之一。
在研究可逆电池的电动势和电池反应时电极上儿乎没有电流通过,每个电极或电池反应都是在无限接近平衡下进行的,因此每个电极反应是可逆的。
当有电流通过电池时,则电极的平衡状态被破坏,此时电极反应处于不可逆状态,随着电极上电流密度的增加,电极反应的不可逆程度也随之增大。
在有电流通过电极时,III于电极反应的不可逆而使电极电位偏离平衡值的现象称作电极的极化。
根据实验测出的数据来描述电流密度与电极电位之间关系的曲线称作极化曲线,如图1所示。
A E F图一金属的极化曲线金属的阳极过程是指金属作为阳极,在一定的外电势下发生的阳极溶解过程, 如下式所示:n+~M?M+ne此过程只有电极电位大于其热力学电位时才能发生。
阳极的溶解速度随着电极电位变正而逐渐增大。
这是正常的阳极溶解,但当阳极电位正到某一数值时,其溶解速度达到最大值。
此后阳极溶解速度随着电位变正,反而大幅度的降低,这种现象称为金属的钝化现象。
从A点到B点的电位范围称为金属活性溶解区。
此区域内的AB线段是金属的正常溶解。
A点称为金属的自然腐蚀电位。
从B点到E点称为钝化过渡区。
BE线是山活化态到钝化态的转变过程,B点所对应的电位称为致钝电位,其对应的电流密度I称为致钝电流密度。
从E点到F点的电位范围称为钝化区。
在此区域内由于金属表面状态发生了变化,使金属的溶解速度降低到最小值,与之对应的电流密度很小,基本上不随电位的变化而变化。
此时的电流密度称为维持钝化的电流密度,其数值儿乎与电位变化无关。
FC段的电位范围称为过钝化区,在此区域,阳极电流密度乂重新随电位增大而增大,金属的溶解速度乂开始增大。
实验二 铁的极化曲线的测定

实验二铁的极化曲线的测定实验二铁的极化曲线的测定一、实验目的1、掌握恒电位法测定电极极化曲线的原理和实验技术。
通过测定Fe在H2SO4、HCl溶液中的阴极极化、阳极极化曲线,求得Fe的自腐蚀电位,自腐蚀电流和钝化电势、钝化电流等参数。
2、了解Cl-离子,缓蚀剂等因素对铁电极极化的影响。
3、讨论极化曲线在金属腐蚀与防护中的应用。
二、实验原理1、铁的极化曲线:金属的电化学腐蚀是金属与介质接触时发生的自溶解过程。
例如Fe →Fe2++2e (1)2H++2e →H2(2) Fe将不断被溶解,同时产生H2。
Fe电极和H2电极及H2SO4溶液构成了腐蚀原电池,其腐蚀反应为:Fe+2H+→ Fe2++H2(3)这就是Fe在酸性溶液中腐蚀的原因。
当电极不与外电路接通时,其净电流为零。
即I corr=I Fe=-I H≠0。
图1中ra为阴极极化曲线。
当对电极进行阴极极化,即加比Ecorr更负的电势,反应(1) 被抑制,反应(2)加速,电化学过程以H2析出为主,这种效应称为“阴极保护”。
塔菲尔(Tafel)半对数关系,即:图1中ab为阳极极化曲线。
当对电极进行阳极极化时,即加比Ecorr更正的电势,则反应(2) 被抑制,反应(1) 加速,电化学过程以Fe溶解为主。
符合公式:2、铁的钝化曲线:abc段是Fe的正常溶解,生成Fe2+,称为活化区。
cd段称为活化钝化过渡区。
de段的电流称为维钝电流,此段电极处于比较稳定的钝化区, Fe2+离子与溶液中的离子形成FeSO4沉淀层,阻滞了阳极反应,由于H+不易达到FeSO4层内部,使Fe表面的pH增大,Fe2O3、Fe3O4开始在Fe表面生成,形成了致密的氧化膜,极大地阻滞了Fe的溶解,因而出现钝化现象。
ef段称为过钝化区。
图3中W表示研究电极、C表示辅助电极、r表示参比电极。
参比电极和研究电极组成原电池,可确定研究电极的电位。
辅助电极与研究电极组成电解池,使研究电极处于极化状态。
阴极极化曲线测定实验报告

阴极极化曲线测定实验报告实验目的本实验旨在通过阴极极化曲线测定的方法,研究金属在不同电位下的电化学行为,并探索阴极极化曲线在材料表征中的应用。
实验原理阴极极化曲线是一种描述金属在电解质溶液中的电化学行为的曲线。
通过在恒定电流下改变电位,可以得到一条曲线,称为阴极极化曲线。
该曲线通常包括三个区域:Tafel区、过渡区和析气区。
Tafel区是曲线的起点,对应着金属表面的电化学反应速率受到电势控制的过程。
在该区域,电流随电位的变化呈线性关系。
过渡区是在Tafel区和析气区之间的区域,此时电流密度增加,但电位变化较小。
析气区是曲线的终点,电流密度随电位的变化呈非线性关系,电位继续增加但电流密度不再增加。
阴极极化曲线可以提供有关金属电化学反应动力学和电极过程的信息。
通过分析曲线的斜率和形态,可以了解金属在特定电位下的电极反应速率、电子传递速率和电化学反应机制。
实验步骤1.准备实验材料:金属试样、电解质溶液、参比电极等。
2.清洗金属试样:使用去离子水和乙醇等溶剂,将金属试样表面的杂质彻底清洗干净。
3.准备电解质溶液:根据实验要求配制合适的电解质溶液,确保其浓度和pH值符合要求。
4.搭建实验电化学池:将准备好的电解质溶液倒入电化学池中,将金属试样和参比电极分别插入池中,并连接电位计和电流计等仪器设备。
5.开始实验:通过改变电位,记录不同电位下的电流密度,并根据测量数据绘制阴极极化曲线。
6.数据处理:根据阴极极化曲线的斜率和形态,分析金属试样在不同电位下的电化学行为,如电极反应速率、电子传递速率等。
7.结果分析:根据实验结果,对金属试样的电化学性能进行评估,并与理论预期进行比较和讨论。
实验结果与讨论根据测得的阴极极化曲线,我们可以得到金属试样在不同电位下的电流密度随电位的变化关系。
通过分析曲线的斜率和形态,我们可以得到以下结论: 1. 在Tafel区,金属试样表面的电化学反应速率受到电势控制,电流密度随电位的变化呈线性关系。
阳极极化曲线实验报告

阳极极化曲线实验报告阳极极化曲线实验报告引言:阳极极化曲线实验是一种常见的电化学实验方法,用于研究金属在电化学腐蚀过程中的行为。
通过测量阳极电流与阳极电位之间的关系,可以了解金属的耐蚀性和腐蚀速率。
本实验旨在通过测量不同金属在不同电位下的阳极电流,探究金属的耐蚀性差异。
实验方法:1. 实验材料准备:本实验选取了铝、铜和铁三种金属作为实验材料。
将这三种金属切割成片状,并用砂纸打磨表面,以确保金属表面的光洁度。
2. 实验仪器准备:实验所需仪器包括:电化学工作站、电化学池、参比电极、阳极电流检测电极、电位扫描电极和数据采集系统。
3. 实验步骤:a. 将电化学池中的电解液(如盐酸)加热至适宜温度,并保持恒温。
b. 将实验材料片依次放入电化学池中,确保每块材料片的表面都与电解液充分接触。
c. 将阳极电流检测电极和电位扫描电极分别连接到电化学工作站上,并将参比电极插入电解液中。
d. 在电化学工作站上设置实验参数,如电位范围和扫描速率。
e. 开始实验,记录不同电位下的阳极电流。
实验结果:将实验数据进行整理和分析后,得到了以下结果:1. 阳极极化曲线图:通过绘制不同金属在不同电位下的阳极电流与电位之间的关系曲线,得到了阳极极化曲线图。
曲线的形状和趋势反映了金属的耐蚀性和腐蚀速率。
在曲线中,存在两个重要参数:极化电流密度和极化电位。
2. 极化电流密度:极化电流密度是指单位面积上的阳极电流。
通过实验数据计算得到不同金属的极化电流密度,可以比较它们的耐蚀性。
结果显示,铝的极化电流密度最小,说明铝具有较好的耐蚀性;铜的极化电流密度次之;而铁的极化电流密度最大,表明铁的耐蚀性相对较差。
3. 极化电位:极化电位是指金属表面的电位与标准电极之间的差值。
通过实验数据计算得到不同金属的极化电位,可以了解金属在不同电位下的腐蚀行为。
结果显示,铝的极化电位最高,说明铝的腐蚀速率较慢;铜的极化电位次之;而铁的极化电位最低,表明铁的腐蚀速率较快。
极化曲线的测定
实验一极化曲线的测定一实验目的1.1掌握用“三电极”法测定金属沉积过程的电极电势。
1.2 通过对镍在玻碳电极上的沉积电势的测量加深理解过电位和极化曲线的概念。
1.3 了解控制电位法测量极化曲线的方法。
二实验原理2.1当把金属插入其盐溶液中时,金属表面上的正离子受到极性水分子的作用,有变成溶剂化离子进入溶液而将电子留在金属表面的倾向。
与此同时,溶液中的金属离子也有从溶液中沉积到金属表面的倾向。
当这种溶解与沉积达到平衡时,形成了双电层,在金属/溶液界面上建立起一个不变的电位差值,这个电位差值就是金属的平衡电位,E R表示。
当有电流通过电极时,电极电势偏离平衡电极电势,成为不可逆电极电势,用E IR表示;电极的电极电势偏离平衡电极电势的现象称为电极的极化。
通常把某一电流密度下的电势E R与E IR 之间的差值的绝对值称为超电势,即:η=│E IR-E R│。
影响超电势的因素很多,如电极材料,电极的表面状态,电流密度,温度,电解质的性质、浓度及溶液中的杂质等。
测定镍沉积超电势实际上就是测定电极在不同外电流下所对应的极化电极电势,以电流对电极电势作图I~E(阴极),所得曲线称为极化曲线。
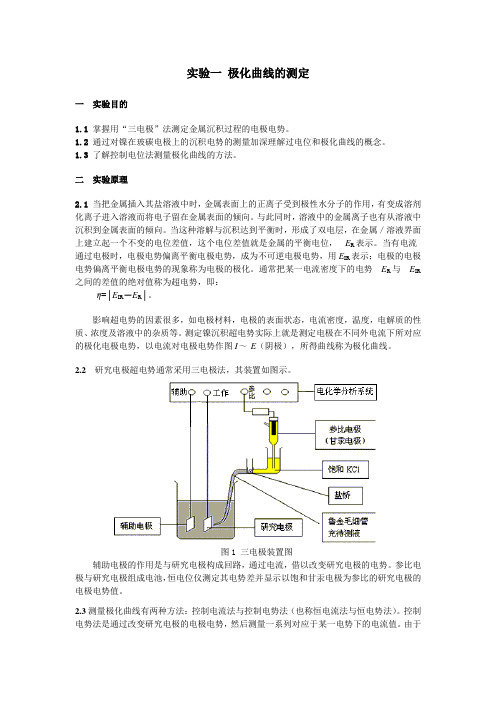
2.2研究电极超电势通常采用三电极法,其装置如图示。
图1 三电极装置图辅助电极的作用是与研究电极构成回路,通过电流,借以改变研究电极的电势。
参比电极与研究电极组成电池,恒电位仪测定其电势差并显示以饱和甘汞电极为参比的研究电极的电极电势值。
2.3测量极化曲线有两种方法:控制电流法与控制电势法(也称恒电流法与恒电势法)。
控制电势法是通过改变研究电极的电极电势,然后测量一系列对应于某一电势下的电流值。
由于电极表面状态在未建立稳定状态前,电流会随时间改变,故一般测出的曲线为“暂态”极化曲线。
本实验采用控制电势法测量极化曲线:控制电极电势以较慢的速度连续改变,并测量对应该电势下的瞬时电流值,以瞬时电流对电极电势作图得极化曲线。
图2 阴极极化曲线三仪器与试剂LK98A微机电化学分析系统一台;甘汞电极一枝;铂电极一枝;玻碳电极一枝;100ml 烧杯3个,500ml烧杯1个;瓦特型镀镍液50ml;稀硝酸50ml;乙醇50ml;蒸馏水500ml。
极化曲线-实验报告

四、实验结果及数据分析
图12205双相不锈钢在0.4mol/L HCl溶液中极化曲线
图22205双相不锈钢在3.5%NaCl溶液中极化曲线
经过拟合可以得出2205双相不锈钢在3.5%NaCl中自腐蚀电位为-0.397V、自腐蚀电流为1.3517E-06A/cm2;在0.4mol/L盐酸中自腐蚀电位为-0.38836V
、自腐蚀电流为1.0524E-05A/cm2
上述两种方法都已经获得了广泛应用,尤其是动态法,由于可以自动测绘,扫描速度可控制一定,因而测量结果重现性好,特别适用于对比实验。
(2)恒电流法
恒电流法就是控制研究电极上的电流密度依次恒定在不同的数值下,同时测定相应的稳定电极电势值。采用恒电流法测定极化曲线时,由于种种原因,给定电流后,电极电势往往不能立即达到稳态,不同的体系,电势趋于稳态所需要的时间也不相同,因此在实际测量时一般电势接近稳定(如1min~3min内无大的变化)即可读值,或人为自行规定每次电流恒定的时间。
2怛电流法恒电流法就是控制研究电极上的电流密度依次恒定在不同的数值下同时测定相应的稳定电极电势采用恒电流法测定极化曲线时由于种种原因给定电流后电极电势往往不能立即达到稳态不同的体系电势趋于稳态所需要的时间也不相同因此在实际测量时一般电势接近稳定如lmin?3min内无大的变化即可读值或人为自行规定每次电流恒定的时间
动态法:控制电极电势以较慢的速度连续地改变(扫描),并测量对应电位下的瞬时电流值,以瞬时电流与对应的电极电势作图,获得整个的极化曲线。一般来说,电极表面建立稳态的速度愈慢,则电位扫描速度也应愈慢。因此对不同的电极体系,扫描速度也不相同。为测得稳态极化曲线,人们通常依次减小扫描速度测定若干条极化曲线,当测至极化曲线不再明显变化时,可确定此扫描速度下测得的极化曲线即为稳态极化曲线。同样,为节省时间,对于那些只是为了比较不同因素对电极过程影响的极化曲线,则选取适当的扫描速度绘制准稳态极化曲线就可以了。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
金属极化曲线的测定实验报告
实验名称:金属极化曲线的测定
实验目的:通过测定金属极化曲线,了解金属的电化学特性,并探讨金属的腐蚀行为。
实验原理:金属在溶液中的电极反应可以通过极化曲线来了解。
极化曲线是通过在不同电位下测量电流得到的。
极化曲线可分为阳极极化曲线和阴极极化曲线。
阳极极化曲线反应了金属发生氧化反应时的电化学特性,阴极极化曲线反应了金属发生还原反应时的电化学特性。
实验仪器:电极测试仪、电位计、电流计、溶液槽、参比电极、工作电极等。
实验步骤:
1. 准备工作:清洗和磨光工作电极,并固定在电极测试仪上。
准备好参比电极和电解槽。
2. 将工作电极和参比电极依次插入电解槽中,保证电极完全浸入溶液中。
3. 打开电极测试仪和电位计,进行零点校准,并调节电位计的电位为初始电位。
4. 开始测量:逐渐改变电位,记录对应的电流值。
首先记录阳极极化曲线,然后通过反向电流去极化,并记录阴极极化曲线。
5. 根据测量数据绘制极化曲线。
实验结果:根据测量得到的数据,绘制得到阳极极化曲线和阴
极极化曲线。
根据曲线形状和电流值的变化,分析金属在溶液中的电化学特性和腐蚀行为。
实验讨论和结论:根据测得的极化曲线,可以分析金属的电化学特性和腐蚀行为。
比如当曲线向高电位延伸时,说明金属发生氧化反应,存在腐蚀现象;当曲线向低电位延伸时,说明金属发生还原反应,有防腐效果。
实验注意事项:
1. 实验中要谨慎操作电位计和电流计,避免出现误差。
2. 注意溶液的配制和浓度的选择,保证实验的可靠性。
3. 实验结束后要将仪器清洗干净,保养好。
实验总结:通过金属极化曲线的测定,我们可以了解金属的电化学特性以及其在溶液中的腐蚀行为。
这对于研究金属材料的耐蚀性以及腐蚀机理有着重要的意义。
通过实验,我们可以得到有关金属的极化曲线,结合实验结果进行分析,有助于我们深入了解金属在不同环境下的电化学特性和腐蚀行为。
