实验2金属Zn阳极极化曲线的测量
阳极极化曲线的测定实验报告

阳极极化曲线的测定实验报告
实验名称:阳极极化曲线的测定实验报告
实验目的:
1. 了解阳极极化现象的基本概念和原理;
2. 掌握测量阳极极化曲线的方法;
3. 分析影响阳极极化的因素及其机理。
实验仪器:
1. 电化学工作站
2. 参比电极:银/氯化银电极
3. 氧化铁电极
4. 稳定电源
实验原理:
阳极极化是指阳极在电解液中发生氧化反应,并在阳极表面生成一层氧化物(如铁在铁离子存在下变成铁离子)后,加速极化的现象。
阳极极化曲线是通过测定阳极的Tafel曲线得出的,Tafel曲线的斜率与阳极极化速率成比例。
实验步骤:
1. 将氧化铁电极固定在电化学工作站的阳极位,并连接稳定电源;
2. 将银/氯化银电极作为参比电极固定在电化学工作站的参比电极位,并用KCl溶液饱和;
3. 连接液路,使氧化铁电极与电化学工作站连接;
4. 对氧化铁电极进行阳极极化,启动电化学工作站,并在一定电位上
进行一段时间的绝化等待稳定;
5. 循环扫描电位,记录电位与电流的变化,得到Tafel曲线;
6. 对Tafel曲线进行分析,得出阳极极化的速率及其机理。
实验结果:
从实验数据中得出,阳极极化速率与阳极表面氧化物的生成速率成正比,同时还受到电流密度、溶液浓度、温度等因素的影响。
实验结论:
通过实验结果得出,阳极极化是一种加速极化现象,其速率受到多种
因素的影响。
在化学反应工业生产中,应该重视阳极极化现象的影响。
极化曲线的测定
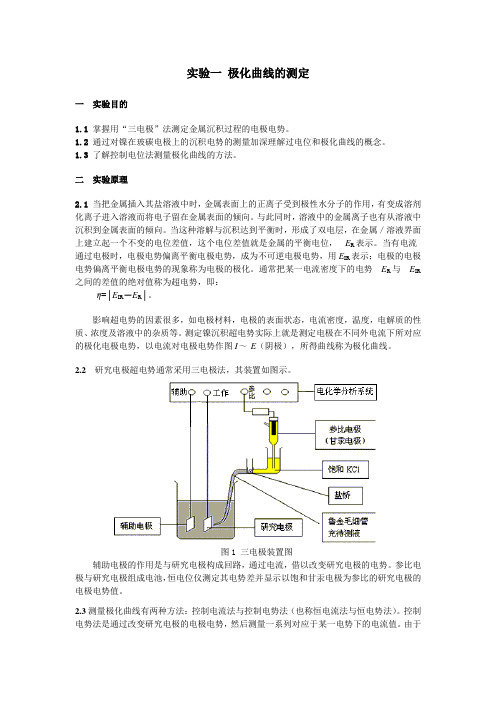
实验一极化曲线的测定一实验目的1.1掌握用“三电极”法测定金属沉积过程的电极电势。
1.2 通过对镍在玻碳电极上的沉积电势的测量加深理解过电位和极化曲线的概念。
1.3 了解控制电位法测量极化曲线的方法。
二实验原理2.1当把金属插入其盐溶液中时,金属表面上的正离子受到极性水分子的作用,有变成溶剂化离子进入溶液而将电子留在金属表面的倾向。
与此同时,溶液中的金属离子也有从溶液中沉积到金属表面的倾向。
当这种溶解与沉积达到平衡时,形成了双电层,在金属/溶液界面上建立起一个不变的电位差值,这个电位差值就是金属的平衡电位,E R表示。
当有电流通过电极时,电极电势偏离平衡电极电势,成为不可逆电极电势,用E IR表示;电极的电极电势偏离平衡电极电势的现象称为电极的极化。
通常把某一电流密度下的电势E R与E IR 之间的差值的绝对值称为超电势,即:η=│E IR-E R│。
影响超电势的因素很多,如电极材料,电极的表面状态,电流密度,温度,电解质的性质、浓度及溶液中的杂质等。
测定镍沉积超电势实际上就是测定电极在不同外电流下所对应的极化电极电势,以电流对电极电势作图I~E(阴极),所得曲线称为极化曲线。
2.2研究电极超电势通常采用三电极法,其装置如图示。
图1 三电极装置图辅助电极的作用是与研究电极构成回路,通过电流,借以改变研究电极的电势。
参比电极与研究电极组成电池,恒电位仪测定其电势差并显示以饱和甘汞电极为参比的研究电极的电极电势值。
2.3测量极化曲线有两种方法:控制电流法与控制电势法(也称恒电流法与恒电势法)。
控制电势法是通过改变研究电极的电极电势,然后测量一系列对应于某一电势下的电流值。
由于电极表面状态在未建立稳定状态前,电流会随时间改变,故一般测出的曲线为“暂态”极化曲线。
本实验采用控制电势法测量极化曲线:控制电极电势以较慢的速度连续改变,并测量对应该电势下的瞬时电流值,以瞬时电流对电极电势作图得极化曲线。
图2 阴极极化曲线三仪器与试剂LK98A微机电化学分析系统一台;甘汞电极一枝;铂电极一枝;玻碳电极一枝;100ml 烧杯3个,500ml烧杯1个;瓦特型镀镍液50ml;稀硝酸50ml;乙醇50ml;蒸馏水500ml。
线性电势扫描法测试金属镍的阳极极化曲线1实验目的2实验原理线性

1实验目的2实验原理线性电势扫描法是指在一定的范围内控制施加在WE 上的电极电势,以一定的速度均匀变化,同时记录对应电极电势下电化学反应的响应电流密度,以电极电势为自变量,电流密度为因变量,用电极电势-电流密度曲线表示实验结果,即极化曲线。
线性电势扫描法可测定电极的阴极和阳极极化曲线。
用该法测得的阳极钝化曲线常为下图所示。
E E 钝化 ii 钝化 图1 线性电势扫描法得到的金属阳极钝化曲线示意图上图中整条曲线分为四个区域:(1)AB 区间为活性溶解区。
金属发生阳极溶解,阳极电流密度与电极电势(或超电势)符合Tafel 规律;(2)BC 区间为过渡钝化区。
由于金属表面开始发生钝化,随着电极电势逐渐正移,金属的溶解速率迅速减小;(3)CD 区间为钝化稳定区。
由于金属表面已经覆盖一层致密的钝化膜,金属的溶解速度保持在一个比较小的水平,溶解速率基本不随电极电势的正移而改变;(4)DE 区间为过度钝化区。
由于在高极化状态下,电极表面发生了析氧反应或生成更高价金属离子的反应,电流密度随电极电势的正移而增大。
从极化曲线可以看出,具有钝化现象的阳极极化曲线的一个重要特点是:在BCD 区间,同一电流密度值下对应几个不同的电极电势值。
这种极化曲线是无法用恒电流法进行测量的。
可见,线性电势扫描法是研究金属钝化现象的重要方法。
影响金属钝化的因素很多。
主要有:(1)金属的组成和结构。
各种金属的钝化能力不同,即所谓的“化学因素”。
在金属中引入其它金属成分,可以改变金属的钝化行为。
如,铁中掺入镍、铬可促进钝化,并提高钝化状态的稳定性。
(2)电解质溶液的组成。
溶液的pH 值、卤素离子和氧化性阴离子对金属的钝化行为存在显著影响,即所谓“溶液因素”。
在酸性和中性溶液中,随着pH 值的增大,有利于钝化的形成。
卤素离子,特别是Cl -离子则阻碍金属的钝化,并能破坏金属的钝态。
有些氧化性的阴离子,如NO 2-等,则可促进金属进入钝态。
(3)其它因素。
阳极极化曲线的测定实验报告

阳极极化曲线的测定实验报告实验目的:1. 理解阳极极化曲线的概念和测定方法;2. 掌握阳极极化的过程,以及控制因素。
实验原理:阳极极化曲线是指阳极电流随阳极电位变化而变化的曲线。
阳极极化是指在阳极表面形成的一种电化学现象。
它与电极材料、电解质、溶液pH值、温度等因素有关。
阳极极化曲线一般呈S形,可分为三个部分:A、B、C。
A区为初级平台区,B区为过渡区,C区为稳态极化区。
初级平台区的电流基本稳定,过渡区的电流逐渐变大,稳态极化区的电流趋于稳定。
实验步骤:1. 准备实验室所需试剂和仪器;2. 将实验用的电极插入电极夹;3. 将电极放置于试剂中,初始电势设置为负电平(如-30V);4. 保持电极稳定,记录其电势和电流数据;5. 在读数器上重复几次实验,确保数据收集稳定和准确;6. 处理和分析数据;7. 根据数据结果得出结论。
实验注意事项:1. 在实验过程中,应注意电极电势的精确度和测量精度;2. 试剂要求纯度高,避免可能的干扰;3. 电极插入溶液后,应尽量避免抖动电极;4. 实验操作过程中,需注意个人安全措施。
实验数据处理:首先,将收集的数据绘制成阳极极化曲线。
然后,通过曲线的三个部分(A、B、C)分析和学习阳极极化的过程和变化。
最后,结合实验原理和结论,探究阳极极化的根本机理。
实验结果:我们通过实验得出的阳极极化曲线如下图所示(图中蓝色曲线即为实验曲线):通过上图可以看出,在图中曲线的A区,电流基本稳定,对于阳极反应而言,主要是由于附加电压激发了阳极上化学反应的起始,在这个区域内,阳极电位提高到一定程度会试图开始氧化反应,因此电流密度保持不变。
曲线的B区是过渡区,电流密度逐渐变大直到到达最大值。
在这个区域内,阳极氧化反应的速率增加,使电流密度增大。
曲线的C区是稳态极化区,电流达到最大值,且在稳定状态下基本固定。
在这个区域内,阳极氧化反应抵消了加在极上的电位增加,形成了稳态极化。
综上所述,阳极极化实验是一项针对钴合金的研究以及试图发现阳极极化曲线的实验。
镍在不同电解质中阳极极化曲线的测定

镍在不同电解质中阳极极化曲线的测定1电极极化当有电流通过电极时,电极电位偏离平衡电极电位的现象叫电极的极化。
1)阴极极化:电流通过阴极时,电极电位向负方向移动,即 EK 比 EK,e负 ,叫阴极极化。
2)阳极极化电流通过阳极时,电极电位向正方向移动 ,即EA 比EA, e正,叫阳极极化。
3)过电位当电极上有电流通过时,电极电位( EK 或 EA )将偏离平衡电极电位( EK,e 或 EA,e),二者之差值叫过电位,以ΔE表示。
ΔE= E –Ee阴极极化时, EK < EK,e,故ΔE < 0,阳极极化时, EA > EA,e,故ΔE > 0。
1.1稳态极化曲线稳态是指电极上通过的电流以及电极电位不随时间改变的状态。
在稳态下测量得到的电流密度与电极电位 (或过电位 )之间的关系曲线叫做极化曲线。
图1和图 2为典型的稳态阴极极化曲线和阳极极化曲线。
1.2电化学极化1)交换电流密度将金属 M 浸入含有 M z+离子的溶液中 ,在两相界面间便发生了物质的转移和电荷的转移 ,最后建立了物质平衡和电荷平衡 ,其电极电位即为平衡电极电位。
此时界面间金属离子的还原速度等于金属的氧化速度 ,电流密度J表示 ,叫做交换电流密度。
2)电化学极化以金属电沉积的阴极过程为例 ,当对镀液进行强烈搅拌 ,使液相传质步骤无任何困难 ,将处于平衡状态下的阴极通以外电流 ,此时电极与镀液界面间的还原反应速度一定大于氧化反应速度 ,由于电子转移步骤存在着阻力 ,还原反应不能将外电源输送的电子全部消耗 ,电极表面负的剩余荷增加 ,使得电极电位向负方向移动 ,即产生了极化。
这种由于电子转移步骤的阻力引起的电极的极化叫做电化学极化。
3)交换电流密度与电化学极化的关系交换电流密度 J是描述电极处于平衡状态的参量 ,但是它与平衡电极电位 Ee不同 , Ee 是热力学函数 ,而J是动力学函数。
两个 Ee相同的电极 ,其J0可以相差几千倍。
极化曲线的测定

实验九极化曲线的测定【目的要求】1. 掌握稳态恒电位法测定金属极化曲线的基本原理和测试方法。
2. 了解极化曲线的意义和应用。
3. 掌握恒电位仪的使用方法。
【实验原理】1. 极化现象与极化曲线为了探索电极过程机理及影响电极过程的各种因素,必须对电极过程进行研究,其中极化曲线的测定是重要方法之一。
我们知道在研究可逆电池的电动势和电池反应时,电极上几乎没有电流通过,每个电极反应都是在接近于平衡状态下进行的,因此电极反应是可逆的。
但当有电流明显地通过电池时,电极的平衡状态被破坏,电极电势偏离平衡值,电极反应处于不可逆状态,而且随着电极上电流密度的增加,电极反应的不可逆程度也随之增大。
由于电流通过电极而导致电极电势偏离平衡值的现象称为电极的极化,描述电流密度与电极电势之间关系的曲线称作极化曲线,如图2-19-1所示。
图2-19-1 极化曲线A-B:活性溶解区;B:临界钝化点B-C:过渡钝化区;C-D:稳定钝化区D-E:超(过)钝化区金属的阳极过程是指金属作为阳极时在一定的外电势下发生的阳极溶解过程,如下式所示:M→M n++n e此过程只有在电极电势正于其热力学电势时才能发生。
阳极的溶解速度随电位变正而逐渐增大,这是正常的阳极溶出,但当阳极电势正到某一数值时,其溶解速度达到最大值,此后阳极溶解速度随电势变正反而大幅度降低,这种现象称为金属的钝化现象。
图2-19-1中曲线表明,从A点开始,随着电位向正方向移动,电流密度也随之增加,电势超过B点后,电流密度随电势增加迅速减至最小,这是因为在金属表面生产了一层电阻高,耐腐蚀的钝化膜。
B点对应的电势称为临界钝化电势,对应的电流称为临界钝化电流。
电势到达C点以后,随着电势的继续增加,电流却保持在一个基本不变的很小的数值上,该电流称为维钝电流,直到电势升到D点,电流才有随着电势的上升而增大,表示阳极又发生了氧化过程,可能是高价金属离子产生也可能是水分子放电析出氧气,DE段称为过钝化区。
阳极极化曲线实验报告
阳极极化曲线实验报告阳极极化曲线实验报告引言:阳极极化曲线实验是一种常见的电化学实验方法,用于研究金属在电化学腐蚀过程中的行为。
通过测量阳极电流与阳极电位之间的关系,可以了解金属的耐蚀性和腐蚀速率。
本实验旨在通过测量不同金属在不同电位下的阳极电流,探究金属的耐蚀性差异。
实验方法:1. 实验材料准备:本实验选取了铝、铜和铁三种金属作为实验材料。
将这三种金属切割成片状,并用砂纸打磨表面,以确保金属表面的光洁度。
2. 实验仪器准备:实验所需仪器包括:电化学工作站、电化学池、参比电极、阳极电流检测电极、电位扫描电极和数据采集系统。
3. 实验步骤:a. 将电化学池中的电解液(如盐酸)加热至适宜温度,并保持恒温。
b. 将实验材料片依次放入电化学池中,确保每块材料片的表面都与电解液充分接触。
c. 将阳极电流检测电极和电位扫描电极分别连接到电化学工作站上,并将参比电极插入电解液中。
d. 在电化学工作站上设置实验参数,如电位范围和扫描速率。
e. 开始实验,记录不同电位下的阳极电流。
实验结果:将实验数据进行整理和分析后,得到了以下结果:1. 阳极极化曲线图:通过绘制不同金属在不同电位下的阳极电流与电位之间的关系曲线,得到了阳极极化曲线图。
曲线的形状和趋势反映了金属的耐蚀性和腐蚀速率。
在曲线中,存在两个重要参数:极化电流密度和极化电位。
2. 极化电流密度:极化电流密度是指单位面积上的阳极电流。
通过实验数据计算得到不同金属的极化电流密度,可以比较它们的耐蚀性。
结果显示,铝的极化电流密度最小,说明铝具有较好的耐蚀性;铜的极化电流密度次之;而铁的极化电流密度最大,表明铁的耐蚀性相对较差。
3. 极化电位:极化电位是指金属表面的电位与标准电极之间的差值。
通过实验数据计算得到不同金属的极化电位,可以了解金属在不同电位下的腐蚀行为。
结果显示,铝的极化电位最高,说明铝的腐蚀速率较慢;铜的极化电位次之;而铁的极化电位最低,表明铁的腐蚀速率较快。
极化曲线等的实验原理 2
极化曲线
是一种快速测定金属腐蚀速度和腐蚀倾向的方法,极化曲线的自腐蚀电位表明了材料的腐蚀趋势,电位越负说明腐蚀趋势越大,而自腐蚀电流密度icorr表明了腐蚀速度的快慢, icorr越大,说明腐蚀速度越快。
icorr是阴极极化曲线和阳极化曲线的塔菲尔区的切线交点对应的电流密度值。
操作参数:采用动电位极化曲线法评价耐蚀性能,测量溶液是3.5%NaCl,在自腐蚀电位±300mV进扫描,扫描速率为50mV/s。
显微硬度评价膜层性能
测定之前,先要将待测磨料制成反光磨片试样,置于显微硬度计的载物台上,通过加负荷装置对四棱锥形的金刚石压头加压负荷的大小可根据待测材料的硬度不同而增减。
金刚石压头压入试样后,在试样表面上会产生一个凹坑。
把显微镜十字丝对准凹坑,用目镜测微器测量凹坑对角线的长度。
根据所加负荷及凹坑对角线长度就可计算出所测物质的显微硬度值。
HV = 常数×试验力/压痕表面积≈0.1891 F/d2。
其最大的优点在于其硬度值与试验力的大小无关,只要是硬度均匀的材料,任意试验力性能不受影响;缺点在于试样要求高,技术要求高,多数停留在实验室使用,致使试验效率低。
仪器操作参数:试验力1.961N(200g),测量系统放大倍数400倍(测量)、100倍(观察),加载时间10s,电源交流电220V。
实验原理
阳极氧化,
它是一种比较传统的表面处理技术,就是把金属或合金放在合适的电解液中作为阳极进行通电、处理,使得金属或合金表面生成一种氧化薄膜的电化学氧化方法。
阳极极化曲线的测定阳极极化曲线的测定与分析
阳极极化曲线的测定阳极极化曲线的测定与分析导读:就爱阅读网友为您分享以下“阳极极化曲线的测定与分析”资讯,希望对您有所帮助,感谢您对的支持!阳极极化曲线的测定与分析了解自腐蚀电位、致钝电位和维钝电位、过钝解自腐蚀电位、致钝电位和维钝电位、过钝化电位以及致钝电流密度和维钝电流密度等概化电位以及致钝电流密度和维钝电流密度等概念;念; 2. 2. 掌握恒电位法测定阳极极化曲线的原理和方掌握恒电位法测定阳极极化曲线的原理和方法;法;3. 3. 通过阳极极化曲线的测定,判定实施阳极保护通过阳极极化曲线的测定,判定实施阳极保护的可能性,初步选取阳极保护的技术参数;的可能性,初步选取阳极保护的技术参数; 4. 4. 掌握掌握IM6ex IM6ex电化学工作站的使用方法。
电化学工作站的使用方法。
将一种金属将一种金属((电极电极))浸在电解液中,在金属与溶液之间就会浸在电解液中,在金属与溶液之间就会形成电位,这种电位称为该金属在该溶液中的电极电位。
形成电位,这种电位称为该金属在该溶液中的电极电位。
当有外加电流通过此电极时,其电极电位会发生变化,这当有外加电流通过此电极时,其电极电位会发生变化,这种现象称为电极的极化。
如果电极为阳极,则电极电位将种现象称为电极的极化。
如果电极为阳极,则电极电位将向正方向偏移,称为阳极极化;对于阴极,电极电位将向向正方向偏移,称为阳极极化;对于阴极,电极电位将向负方向偏移,称为阴极极化。
负方向偏移,称为阴极极化。
电极电位随电流密度变化的电极电位随电流密度变化的关系曲线称为极化曲线关系曲线称为极化曲线。
为了判定金属在电解质溶液中采。
为了判定金属在电解质溶液中采取阳极保护的可能性,选择阳极保护的取阳极保护的可能性,选择阳极保护的33个主要技术参个主要技术参数数——致钝电流密度致钝电流密度、、维钝电流密度维钝电流密度和和钝化区的电位范围钝化区的电位范围,,需要测定阳极极化曲线。
需要测定阳极极化曲线。
实验2-Zn电极极化曲线测定
华南师范大学实验报告学生姓名学号专业新能源材料与器件年级、班级2014课程名称电化学基础实验实验项目Zn电极阳极极化曲线的测量实验类型验证实验时间2016年4月11日实验指导老师吕老师实验评分、一.实验目的1.掌握阳极极化曲线测试的基本原理和方法2.测定Zn电极在1M NaOH溶液和1MZnCl2溶液中的阳极极化曲线3.通过实验理解金属电极钝化与活化过程二.实验原理线性电位扫描法是指控制电极电位在一定的电位范围内,以一定的速度均匀连续变化,同时记录下各电位下反应的电流密度,从而得到电位电流密度曲线,即稳态极化曲线,在这种情况下,电位是自变量,电流密度是因变量,极化曲线表示稳态电流密度与电位之间的函数关系:i=f(ψ)线性电位扫描发可测定阳极极化曲线,特别适用于测定电极表面状态有特殊变化的极化曲线,如测定具有阳极钝化行为的阳极极化曲线。
阳极极化:金属作为阳极时在一定的外电势下发生的阳极溶解过程叫做阳极极化:M=Mn++ne-金属的钝化现象:阳极的溶解速度随电位变正而逐渐增大,这是正常的阳极溶出。
但当阳极电位正到某一数值时,其溶解速度达到一最大值。
此后阳极溶解速度随着电位变正,反而大幅度降低,这种现象称为金属的钝化现象。
三.仪器与试剂1.实验仪器:CHI电化学工作站一台Zn电极Hg/HgO电极甘汞电极铂电极三口电解槽2.实验试剂:1MKOH溶液250ml 1MZnCl2溶液250ml四.实验步骤1.电极预处理:将锌电极沾一点去离子水后用砂纸轻轻打磨,除去氧化膜,将电极表面磨平,用去离子水冲洗干净用滤纸吸干之后轻放进电解池中。
电解池中的辅助电极为铂电极,参比电极为甘汞电极(酸性或中性电解液),Hg/HgO 电极(碱性电解液),往电解池中加入KOH(ZnCl2)溶液。
2.极化曲线的测定:1)启动电化学工作站,运行软件,首先测试开路电压。
再选择Setup菜单中电极“Technique”选项,在弹出菜单中选择“Linear SweepVoltammentry”技术,分别根据电解液的不同输入测试条件。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验2:金属Zn阳极极化曲线的测量
一、实验目的
1.掌握阳极极化曲线测试的基本原理和方法;
2.测定Zn电极在1M KOH溶液和1M ZnCl2溶液中的阳极极化曲线;
3.通过实验理解金属电极钝化与活化过程。
二、实验原理
线性电位扫描法是指控制电极电位在一定的电位范围内,以一定的速度均匀连续的变化,同时记录下各电位下反应的电流密度,从而得到电位-电流密度曲线,即稳态电流密度与电位之间的函数关系:i= f(ψ)。
特别适用于测量电极表面状态有特殊变化的极化曲线。
如下:如阳极钝化行为的阳极极化曲线。
阳极极化:金属作为阳极时在一定的外电势下发生的阳极溶解过程叫做阳极极化,金属
的钝化现象:阳极的溶解速度随电位变正而逐渐增大。
这是正常的阳极溶出。
但当阳极电位正到某一数值时,其溶解速度达到一最大值。
此后阳极溶解速度随着电位变正,反而大幅度的降低,这种现象称为金属的钝化现象。
线性电位扫描法不但可以测定阴极极化曲线,也可以测定阳极极化曲线,特别适用于测定电极表面状态有特殊变化的极化曲线,如测定具有阳极钝
化行为的阳极极化曲线,用线性电位扫描法测得的阳极极化曲线,如下图所示
•AB段-----称为活性溶解区;此时金属进行正常的阳极溶解,阳极电流随电位改变服Tafel 公式的半对数关系。
•BC段-----称为钝化过渡区;此时是由于金属开始发生钝化,随着电极电位的正移,金属的溶解速度反而减小了。
•CD段-----称为钝化稳定区;在该区域中金属的溶解速度基本上不随电位二改变;
•DE段-----称为过度钝化区;此时金属溶解速度重新随电位的正移而增大,为氧的析出或者高价金属离子的生成。
从阳极极化曲线上可以得到下列参数:c点对应的电位---临界钝化电位;c点对应的电流—临界钝化电流密度;而这些参数恒电流法是测不出来的。
影响金属钝化的因素很多,包括溶液的组成、金属的组成和结构以及外界条件。
三、仪器与试剂
CHI电化学工作站、锌电极、Hg/HgO电极、甘汞电极、铂电极、三口电解槽、
1M KOH溶液250ml、1M ZnCl2溶液250ml
金属Zn是中性锌锰电池、碱性锌锰电池和锌-空气电池等的负极材料,其电化学行为受到广泛的研究。
本实验应用线性电位扫描法测量金属Zn电极在1M KOH和1M ZnCl2 中阳极极化曲线。
四、实验步骤
(1) 电极预处理
将锌电极在砂纸上轻轻打磨至光亮,除去氧化膜,用去离子水冲洗干净,铂电极用硫酸浸泡以除去表面杂质,并用去离子水冲洗。
(2) 极化曲线测定
采用电化学工作站中的线性电位扫描技术(Linear Sweep Voltammetry)分别测量Zn 电极在1M KOH 溶液和1M ZnCl 2溶液中常温和450C 的阳极极化曲线(扫描速率5mV/s ,从开路到截止电压分别为-1.0V 和-0.5V) 。
五、结果分析和讨论
1. 每种溶液中不同温度下的极化曲线叠加在同一张图中。
结果分两张图表示。
C u r r e n t /A
Potential/V
图1:1mol/L 的KOH 溶液中Zn 电极分别在25℃和45℃下的阳极极化曲线
C u r
r e n t /A
Potential/V
图2:1mol/L 的ZnCl 2溶液中Zn 电极分别在25℃和45℃下的阳极极化曲线 2. 结合文献,指出图中的活性溶解区、过渡钝化区、稳定钝化区和过度钝化区。
-1.4
-1.2
-1.0
0.000
0.001
0.002
C u r r e n t /A
Potential/V
b
a
c
d
e
图3:1mol/LKOH 溶液中Zn 电极在25℃下的阳极极化曲线
abc 段:活性溶解区;cd 段:过渡钝化区;de 段:稳定钝化区
-1.4
-1.2
-1.0
-0.001
0.0000.0010.0020.0030.004
0.005
0.006C u r r e n t /A
P otential/V
a
b
c
d
图4:1mol/LKOH 溶液中Zn 电极在45℃下的阳极极化曲线 ab 段:活性溶解区;bc 段:过渡钝化区;cd 段:稳定钝化区
C u r r e n t /A
Potential/V
图5:1mol/L的ZnCl2溶液中Zn电极分别在25℃和45℃下的阳极极化曲线
ab段:活性溶解区;bc段:活性溶解区
3.比较不同溶液中电极的阳极极化行为。
尝试分析原因。
KOH溶液中,金属Zn发生阳极氧化产生的Zn2+与OH-反应生成难溶的Zn(0H)2阻碍金属Zn的继续氧化,而在ZnCl2溶液中则不会出现这种问题。
4.根据不同温度下氧化峰面积的大小,比较温度对氧化电量的影响。
经过对不同温度下的Zn在1mol/L的KOH溶液中的阳极极化曲线积分,图3峰面积:4.099020035E-4
图4峰面积:9.13397448E-4
可见,温度越高,氧化电量越高。
