专题69 有机物制备综合实验(教师版)十年(2013-2022)高考化学真题分项汇编(全国通用)
专题71 探究性综合实验(学生版)-十年(2013-2022)高考化学真题分项汇编(全国通用)
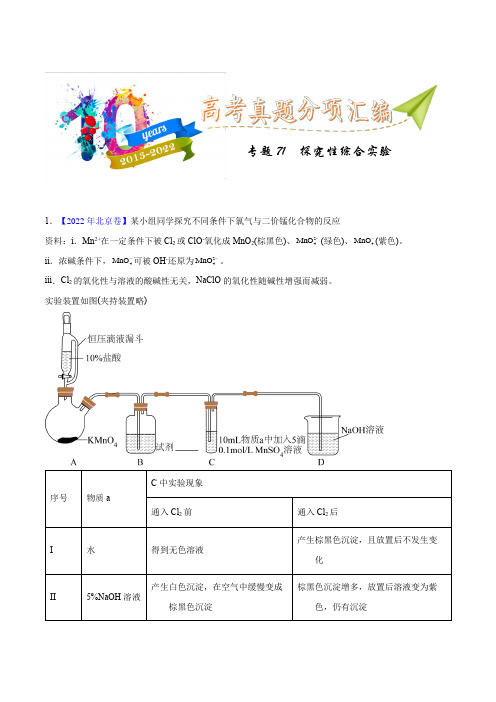
1.【2022年北京卷】某小组同学探究不同条件下氯气与二价锰化合物的反应资料:i .Mn 2+在一定条件下被Cl 2或ClO -氧化成MnO 2(棕黑色)、24MnO -(绿色)、4MnO -(紫色)。
ii .浓碱条件下,4MnO -可被OH -还原为24MnO -。
iii .Cl 2的氧化性与溶液的酸碱性无关,NaClO 的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)序号物质aC 中实验现象通入Cl 2前通入Cl 2后I水得到无色溶液产生棕黑色沉淀,且放置后不发生变化II5%NaOH 溶液产生白色沉淀,在空气中缓慢变成棕黑色沉淀棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀专题71 探究性综合实验(1)B 中试剂是___________。
(2)通入Cl 2前,II 、III 中沉淀由白色变为黑色的化学方程式为___________。
(3)对比实验I 、II 通入Cl 2后的实验现象,对于二价锰化合物还原性的认识是___________。
(4)根据资料ii ,III 中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因: 原因一:可能是通入Cl 2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将24MnO -氧化为4MnO -。
①化学方程式表示可能导致溶液碱性减弱的原因___________,但通过实验测定溶液的碱性变化很小。
②取III 中放置后的1 mL 悬浊液,加入4 mL40%NaOH 溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。
溶液紫色变为绿色的离子方程式为___________,溶液绿色缓慢加深,原因是MnO 2被___________(填“化学式”)氧化,可证明III 的悬浊液中氧化剂过量;③取II 中放置后的1 mL 悬浊液,加入4 mL 水,溶液紫色缓慢加深,发生的反应是___________。
④从反应速率的角度,分析实验III 未得到绿色溶液的可能原因___________。
专题27 化学反应与能量变化(教师版)十年(2013-2022)高考化学真题分项汇编(全国通用)
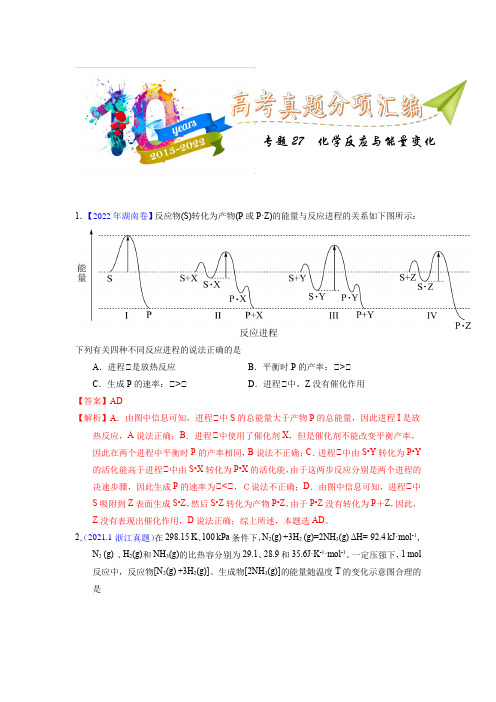
专题27 化学反应与能量变化1.【2022年湖南卷】反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:下列有关四种不同反应进程的说法正确的是A.进程Ⅰ是放热反应B.平衡时P的产率:Ⅰ>ⅠC.生成P的速率:Ⅰ>ⅠD.进程Ⅰ中,Z没有催化作用【答案】AD【解析】A.由图中信息可知,进程Ⅰ中S的总能量大于产物P的总能量,因此进程I是放热反应,A说法正确;B.进程Ⅰ中使用了催化剂X,但是催化剂不能改变平衡产率,因此在两个进程中平衡时P的产率相同,B说法不正确;C.进程Ⅰ中由S•Y转化为P•Y 的活化能高于进程Ⅰ中由S•X转化为P•X的活化能,由于这两步反应分别是两个进程的决速步骤,因此生成P的速率为Ⅰ<Ⅰ,C说法不正确;D.由图中信息可知,进程Ⅰ中S吸附到Z表面生成S•Z,然后S•Z转化为产物P•Z,由于P•Z没有转化为P+Z,因此,Z没有表现出催化作用,D说法正确;综上所述,本题选AD。
2.(2021.1·浙江真题)在298.15 K、100 kPa条件下,N2(g) +3H2 (g)=2NH3(g) ΔH=-92.4 kJ·mol-1,N2 (g) 、H2(g)和NH3(g)的比热容分别为29.1、28.9和35.6J·K-1·mol-1。
一定压强下,1 mol 反应中,反应物[N2(g) +3H2(g)]、生成物[2NH3(g)]的能量随温度T的变化示意图合理的是A.B.C.D.【答案】B【解析】该反应为放热反应,反应物的总能量大于生成物的总能量,根据题目中给出的反应物与生成物的比热容可知,升高温度反应物能量升高较快,反应结束后反应放出的热量也会增大,比较4个图像B符合题意,故答案选B。
3.(2018·上海高考真题)H2(g)和I2(g)、H2(g)和I2(s)以及HI(g)的能量高低如图所示,下列判断错误的是()A.1molH2(g)和1molI2(g)的能量总和高于2molHI(g)的能量B.I2(g)→I2(s)+QkJ(Q>0)C.H2(g)+I2(g)→2HI(g)+9.3kJD.H2(g)+I2(s)→2HI(g)+53.0kJ【答案】D【解析】A.由能量高低图分析可知,2molHI(g)→1molH2(g)和1molI2(g)需要吸收9.3kJ的能量,故1molH2(g)和1molI2(g)的能量总和高于2molHI(g)的能量,正确;B.由能量高低图可知,I2(g)→I2(s)放出能量,即I2(g)→I2(s)+QkJ(Q>0),正确;C.根据能量高低图分析可知,H2(g)+I2(g)→2HI(g)放出9.3kJ的能量,故H2(g)+I2(g)→2HI(g)+9.3kJ,正确;D.根据能量高低图分析可知,H2(g)+I2(s)→2HI(g)吸收53.0kJ的能量,故H2(g)+I2(s)→2HI(g)-57.3kJ,错误;答案选D。
十年(2013-2022)高考化学真题分项汇编(全国通用):专题34 电解应用(教师版)

1.【2022 年北京卷】利用下图装置进行铁上电镀铜的实验探究。
装置示意图
序号 电解质溶液
①
0.1mol / LCuSO4 少量H2SO4
②
0.1mol / LCuSO4 过量氨水
实验现象
阴极表面有无色气体,一段时 间后阴极表面有红色固 体,气体减少。经检验电 解液中有 Fe2+
1molLi
P
CN
2
,理论上外电路需要转移
2mol
电子
B.阴极上的电极反应为:
P4
+8CN-
-4e-
=4
P
CN 2
-
C.在电解过程中 CN- 向铂电极移动
D.电解产生的 H2 中的氢元素来自于 LiOH
【答案】D
【解析】A.石墨电极发生反应的物质:P4→
Li
P
CN
2
化合价升高发生氧化反应,所以石墨电极为阳极,
CN
-
应该向
阳极移动,即移向石墨电极,C 错误;D.由所给图示可知 HCN 在阴极放电,产生 CN- 和 H2 ,而
HCN 中的 H 来自 LiOH ,则电解产生的 H2 中的氢元素来自于 LiOH ,D 正确;故选 D。 4.(2021·广东真题)钴( Co )的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制
对应的电极反应式为:
P4
+8CN-
-4e-
=4
P
CN 2
-
,则生成
1molLi
P
CN
2
,理论上外电路需要转移
1mol
电子,A
错误;B.阴极上发生还原反应,应该得电子,
专题77 物质结构综合(选考)(学生版)十年(2013-2022)高考化学真题分项汇编(全国通用)

专题77物质结构综合(选考)(B)1.【2022年全国乙卷】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。
回答下列问题:(1)氟原子激发态的电子排布式有_______,其中能量较高的是_______。
(填标号)A .22411s 2s 2p 3s B .22421s 2s 2p 3d C .2121s 2s 2p D .22321s 2s 2p 3p (2)①一氯乙烯()23C H Cl 分子中,C 的一个_______杂化轨道与Cl 的x 3p 轨道形成C-Cl _______键,并且Cl 的3p z 轨道与C 的z 2p 轨道形成3中心4电子的大π键()43∏。
②一氯乙烷()25C H Cl 、一氯乙烯()23C H Cl 、一氯乙炔()2C HCl 分子中,C-Cl 键长的顺序是_______,理由:(ⅰ)C 的杂化轨道中s 成分越多,形成的C-Cl 键越强;(ⅱ)_______。
(3)卤化物2CsICl 受热发生非氧化还原反应,生成无色晶体X 和红棕色液体Y 。
X 为_______。
解释X 的熔点比Y 高的原因_______。
(4)α-AgI 晶体中-I 离子作体心立方堆积(如图所示),+Ag 主要分布在由-I 构成的四面体、八面体等空隙中。
在电场作用下,+Ag 不需要克服太大的阻力即可发生迁移。
因此,α-AgI 晶体在电池中可作为_______。
已知阿伏加德罗常数为A N ,则α-AgI 晶体的摩尔体积m V =_______3-1m mol ⋅(列出算式)。
2.【2022年山东卷】研究笼形包合物结构和性质具有重要意义。
化学式为366Ni(CN)x Zn(NH )y zC H ⋅⋅的笼形包合物四方晶胞结构如图所示(H 原子未画出),每个苯环只有一半属于该晶胞。
晶胞参数为a b c,α=β=γ=90︒=≠。
回答下列问题:(1)基态Ni 原子的价电子排布式为_______,在元素周期表中位置为_______。
专题04 化学与传统文化(教师版)十年(2013-2022)高考化学真题分项汇编(全国通用)

1.【2022年山东卷】古医典富载化学知识,下述之物见其氧化性者为A.金(Au):“虽被火亦未熟"B.石灰(CaO):“以水沃之,即热蒸而解”C.石硫黄(S):“能化……银、铜、铁,奇物”D.石钟乳(3CaCO):“色黄,以苦酒(醋)洗刷则白”【答案】C【解析】A.金“虽被火亦未熟”是指金单质在空气中被火灼烧也不反应,反应金的化学性质很稳定,与其氧化性无关,A不合题意;B.石灰(CaO):“以水沃之,即热蒸而解”是指CaO+H2O=Ca(OH)2,反应放热,产生大量的水汽,而CaO由块状变为粉末状,未发生氧化还原反应,与其氧化性无关,B不合题意;C.石硫黄即S:“能化……银、铜、铁,奇物”是指2Ag+S ΔAg2S、Fe+SΔFeS、2Cu+SΔCu2S,反应中S作氧化剂,与其氧化性有关,C符合题意;D.石钟乳(CaCO3):“色黄,以苦酒(醋)洗刷则白”是指CaCO3+2CH3COOH=(CH3COO)2Ca+H2O+CO2↑,未发生氧化还原反应,与其氧化性无关,D 不合题意;故答案为:C。
2.【2022年广东卷】中华文明源远流长,在世界文明中独树一帜,汉字居功至伟。
随着时代发展,汉字被不断赋予新的文化内涵,其载体也发生相应变化。
下列汉字载体主要由合金材料制成的是专题04 化学与传统文化【答案】B【解析】A.兽骨,甲骨文的契刻载体之一,主要是牛的肩胛骨,一小部分是羊、猪、鹿的肩胛骨,还有极少部分的牛肋骨,其主要成分是碳酸钙和其它钙盐,故A不符合题意;B.青铜器是红铜与其他化学元素锡、铅等的合金,属于合金材料,故B项符合题意;C.纸张的主要成分是纤维素,故C不符合题意;D.液晶显示器是一种采用液晶为材料的显示器,液晶是一类介于固态和液态间的有机化合物,故D不符合题意;综上所述,答案为B项。
3.(2021·广东真题)今年五一假期,人文考古游持续成为热点。
很多珍贵文物都记载着中华文明的灿烂成就,具有深邃的文化寓意和极高的学术价值。
专题02 化学与材料(学生版)十年(2013-2022)高考化学真题分项汇编(全国通用)

专题02化学与材料1.【2022年河北卷】定窑是宋代五大名窑之一,其生产的白瓷闻名于世。
下列说法正确的是SiO和MgO A.传统陶瓷是典型的绝缘材料B.陶瓷主要成分为2C.陶瓷烧制的过程为物理变化D.白瓷的白色是因铁含量较高2.【2022年江苏卷】我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精PbO是铅蓄电池的电极材料,不同铅化合物一般具有不同颜色,历美的青铜器;PB.2史上曾广泛用作颜料,下列物质性质与用途具有对应关系的是A.石墨能导电,可用作润滑剂B.单晶硅熔点高,可用作半导体材料C.青铜比纯铜熔点低、硬度大,古代用青铜铸剑D.含铅化合物颜色丰富,可用作电极材料3.【2022年河北卷】化学是材料科学的基础。
下列说法错误的是A.制造5G芯片的氮化铝晶圆属于无机非金属材料B.制造阻燃或防火线缆的橡胶不能由加聚反应合成C.制造特种防护服的芳纶纤维属于有机高分子材料D.可降解聚乳酸塑料的推广应用可减少“白色污染”4.【2022年广东卷】广东一直是我国对外交流的重要窗口,馆藏文物是其历史见证。
下列文物主要由硅酸盐制成的是文物选项A.南宋鎏金饰品B.蒜头纹银盒C.广彩瓷咖啡杯D.铜镀金钟座5.【2022年辽宁卷】北京冬奥会备受世界瞩目。
下列说法错误的是A.冰壶主材料花岗岩属于无机非金属材料B.火炬“飞扬”使用的碳纤维属于有机高分子材料C.冬奥会“同心”金属奖牌属于合金材料D.短道速滑服使用的超高分子量聚乙烯属于有机高分子材料6.【2022年6月浙江卷】下列说法不正确...的是A.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维B.高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明C.氧化铝熔点高,常用于制造耐高温材料D.用石灰石-石膏法对燃煤烟气进行脱硫,同时可得到石膏7.【2022年湖北卷】武当山金殿是铜铸鎏金大殿。
传统鎏金工艺是将金溶于汞中制成“金汞漆”,涂在器物表面,然后加火除汞,使金附着在器物表面。
十年(2013-2022)高考化学真题分项汇编(全国通用):专题37 金属的腐蚀与防护(教师版)

A.铁被氧化的电3;
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替 NaCl 溶液,铁不能发生吸氧腐蚀
【答案】C
【解析】根据实验所给条件可知,本题铁发生的是吸氧腐蚀,负极反应为:Fe-2e-=Fe2+;正极反应为:
O2+2H2O +4e-=4OH-;据此解题;A.在铁的电化学腐蚀中,铁单质失去电子转化为二价铁离子,即负 极反应为:Fe-2e-=Fe2+,错误;B.铁的腐蚀过程中化学能除了转化为电能,还有一部分转化为热能,
累大量电子,自身金属不再失电子从而被保护,正确;D.海水中的离子浓度大于河水中的离子浓度, 离子浓度越大,溶液的导电性越强,因此钢铁设施在海水中的腐蚀速率比在河水中快,错误;故选: C。 4.(2019·江苏高考真题)将铁粉和活性炭的混合物用 NaCl 溶液湿润后,置于如图所示装置中,进行铁的 电化学腐蚀实验。下列有关该实验的说法正确的是
2.(2021·全国乙卷真题)沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排
放并降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。
下列叙述错误的是 A.阳极发生将海水中的 Cl 氧化生成 Cl2 的反应 B.管道中可以生成氧化灭杀附着生物的 NaClO C.阴极生成的 H2 应及时通风稀释安全地排入大气 D.阳极表面形成的 Mg(OH)2 等积垢需要定期清理
D.加入
K
3
Fe
CN
6
溶液无蓝色沉淀生成
【答案】D
【解析】镀层有破损的镀锌铁片被腐蚀,则将其放入到酸化的 3%NaCl 溶液中,会构成原电池,由于锌比
铁活泼,作原电池的负极,而铁片作正极,溶液中破损的位置会变大,铁也会继续和酸化的氯化钠溶
专题67 实验设计与评价(学生版)十年(2013-2022)高考化学真题分项汇编(全国通用)

1.【2022年全国甲卷】根据实验目的,下列实验及现象、结论都正确的是选项实验目的实验及现象结论A 比较3CH COO-和3HCO-的水解常数分别测浓度均为10.1mol L-⋅的34CH COONH和3NaHCO溶液的pH,后者大于前者()()--h33hK CH COO<K HCOB 检验铁锈中是否含有二价铁将铁锈溶于浓盐酸,滴入4KMnO溶液,紫色褪去铁锈中含有二价铁C 探究氢离子浓度对2-4CrO、2-27Cr O相互转化的影响向24K CrO溶液中缓慢滴加硫酸,黄色变为橙红色增大氢离子浓度,转化平衡向生成2-27Cr O的方向移动D 检验乙醇中是否含有水向乙醇中加入一小粒金属钠,产生无色气体乙醇中含有水2.【2022年辽宁卷】下列实验能达到目的的是实验目的实验方法或操作A测定中和反应的反应热酸碱中和滴定的同时,用温度传感器采集锥形瓶内溶液的温度B 探究浓度对化学反应速率的影响量取同体积不同浓度的NaClO溶液,分别加入等体积等浓度的23Na SO溶液,对比现象专题67 实验设计与评价.....6.虑存放试剂的容器)10下列说法不正确的是A .根据I 中试纸变蓝,说明NH 4Cl 发生了分反解反应B .根据I 中试纸颜色变化,说明氨气比氯化氢气体扩散速率快C .I 中试纸变成红色,是由于NH 4Cl 水解造成的D .根据试管中部有白色固体附着,说明不宜用加热NH 4Cl 的方法制备NH 3 11.(2019·北京高考真题)探究草酸(H 2C 2O 4)性质,进行如下实验。
(已知:室温下,0.1 mol·L −1 H 2C 2O 4的pH=1.3)A .H 2C 2O 4有酸性,Ca(OH)2+ H 2C 2O 4CaC 2O 4↓+2H 2OB .酸性:H 2C 2O 4> H 2CO 3,NaHCO 3+ H 2C 2O 4NaHC 2O 4+CO 2↑+H 2O C .H 2C 2O 4具有还原性,24MnO -+5224C O -+16H +2Mn 2++10CO 2↑+ 8H 2OD.H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH浓硫酸C2H5OOCCOOC2H5+2H2O12.(2017·浙江高考真题)某兴趣小组查阅资料得知,连苯三酚的碱性溶液能定量吸收O2;CuCl的盐酸溶液能定量吸收CO,且易被O2氧化。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.【2022年1月浙江卷】某兴趣小组用四水醋酸锰[(CH 3COO)2Mn·4H 2O]和乙酰氯(CH 3COCl)为原料制备无水二氯化锰,按如图流程开展了实验(夹持仪器已省略):已知:①无水二氯化锰极易吸水潮解,易溶于水、乙醇和醋酸,不溶于苯。
②制备无水二氯化锰的主要反应:(CH 3COO)2Mn+CH 3COCl −−−−→Δ苯MnCl 2↓+2(CH 3COO)2O 。
③乙酰氯遇水发生反应:CH 3COCl+H 2O→CH 3COOH+HCl 。
请回答:(1)步骤Ⅰ:所获固体主要成分是_________(用化学式表示)。
(2)步骤Ⅰ在室温下反应,步骤Ⅰ在加热回流下反应,目的分别是________。
(3)步骤Ⅰ:下列操作中正确的是_________。
A .用蒸馏水润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上B .用倾析法转移溶液,开大水龙头,待溶液快流尽时再转移沉淀C .用乙醇作为洗涤剂,在洗涤沉淀时,应开大水龙头,使洗涤剂快速通过沉淀物D .洗涤结束后,将固体迅速转移至圆底烧瓶进行后续操作(4)步骤Ⅰ:①将装有粗产品的圆底烧瓶接到纯化装置(图2)上,打开安全瓶上旋塞,打开抽气泵,关闭安全瓶上旋塞,开启加热器,进行纯化。
请给出纯化完成后的操作排专题69 有机物制备综合实验序:________。
纯化完成→(_____)→(_____)→(_____)→(_____)→将产品转至干燥器中保存A .拔出圆底烧瓶的瓶塞B .关闭抽气泵C .关闭加热器,待烧瓶冷却至室温D .打开安全瓶上旋塞②图2装置中U 形管内NaOH 固体的作用是________。
(5)用滴定分析法确定产品纯度。
甲同学通过测定产品中锰元素的含量确定纯度;乙同学通过测定产品中氯元素的含量确定纯度。
合理的是_________(填“甲”或“乙”)同学的方法。
【答案】(1)(CH 3COO)2Mn(2)步骤Ⅰ脱去四水醋酸锰的结晶水并防止生成MnCl 2;步骤Ⅰ加热回流促进反应生成MnCl 2(3)ABD(4) cdba 防止可能产生的酸性气体进入抽气泵;防止外部水气进入样品 (5)乙【解析】(1)根据制备无水二氯化锰的主要反应:(CH 3COO)2Mn+CH 3COCl −−−−→Δ苯MnCl 2↓+2(CH 3COO)2O 以及乙酰氯遇水发生反应:CH 3COCl+H 2O→CH 3COOH+HCl 可判断步骤Ⅰ中利用CH 3COCl 吸水,因此所获固体主要成分是(CH 3COO)2Mn 。
(2)由于步骤Ⅰ脱去四水醋酸锰的结晶水并防止生成MnCl 2,因此步骤Ⅰ在室温下反应;而步骤Ⅰ加热回流促进反应生成MnCl 2,所以步骤Ⅰ需要在加热回流下反应。
(3)A .滤纸略小于布氏漏斗,但要把所有的孔都覆盖,并用蒸馏水润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上,故A 正确;B .用倾析法转移溶液,开大水龙头,待溶液快流尽时再转移沉淀,故B 正确;C .用抽滤洗涤沉淀时,抽滤速率不能过快,故C 错误;D .由于无水二氯化锰极易吸水潮解,洗涤结束后,将固体迅速转移至圆底烧瓶进行后续操作,故D 正确;故答案为ABD ;(4)①纯化完成后首先关闭加热器,待烧瓶冷却至室温,然后打开安全瓶上旋塞,关闭抽气泵,最后拔出圆底烧瓶的瓶塞,将产品转至干燥器中保存,故答案为cdba ;②由于可能混有酸性气体且无水二氯化锰极易吸水潮解,因此图2装置中U 形管内NaOH固体的作用是防止可能产生的酸性气体进入抽气泵,同时防止外部水气进入样品。
(5)由于无水二氯化锰极易吸水潮解,且锰离子水解,所以应该通过测定产品中氯元素的含量确定纯度,所以合理的是乙同学的方法。
2.(2020年新课标Ⅰ)苯甲酸可用作食品防腐剂。
实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:+KMnO4→+ MnO2+HCl→+KCl(1)在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 mol)高锰酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
(2)停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。
合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。
将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。
称量,粗产品为1.0 g。
(3)纯度测定:称取0. 122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。
每次移取25. 00 mL溶液,用0.01000 mol·L−1的KOH标准溶液滴定,三次滴定平均消耗21.50 mL的KOH标准溶液。
回答下列问题:(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为______(填标号)。
A.100 mL B.250 mL C.500 mL D.1000 mL(2)在反应装置中应选用______冷凝管(填“直形”或“球形”),当回流液不再出现油珠即可判断反应已完成,其判断理由是______。
(3)加入适量饱和亚硫酸氢钠溶液的目的是___________;该步骤亦可用草酸在酸性条件下处理,请用反应的离子方程式表达其原理__________。
(4)“用少量热水洗涤滤渣”一步中滤渣的主要成分是_______。
(5)干燥苯甲酸晶体时,若温度过高,可能出现的结果是_______。
(6)本实验制备的苯甲酸的纯度为_______;据此估算本实验中苯甲酸的产率最接近于_______(填标号)。
A .70%B .60%C .50%D .40%(7)若要得到纯度更高的苯甲酸,可通过在水中__________的方法提纯。
【答案】(1)B (2)球形 无油珠说明不溶于水的甲苯已经被完全氧化(3)除去过量的高锰酸钾,避免在用盐酸酸化时,产生氯气 24MnO -+5H 2C 2O 4+6H +=2Mn 2++10CO 2↑+8H 2O (4)MnO 2 (5)苯甲酸升华而损失 (6)86.0% C(7)重结晶【解析】甲苯用高锰酸钾氧化时生成苯甲酸钾和二氧化锰,为增加冷凝效果,在反应装置中选用球形冷凝管,加热回流,当回流液中不再出现油珠时,说明反应已经完成,加入适量的饱和亚硫酸氢钠溶液除去过量的高锰酸钾,用盐酸酸化得苯甲酸,过滤、干燥、洗涤得粗产品;用KOH 溶液滴定,测定粗产品的纯度。
(1)加热液体,所盛液体的体积不超过三颈烧瓶的一半,三颈烧瓶中已经加入100m 的水,1.5mL 甲苯,4.8g 高锰酸钾,应选用250mL 的三颈烧瓶,故答案为:B ;(2)为增加冷凝效果,在反应装置中宜选用球形冷凝管,当回流液中不再出现油珠时,说明反应已经完成,因为:没有油珠说明不溶于水的甲苯已经完全被氧化;(3)高锰酸钾具有强氧化性,能将Cl -氧化。
加入适量的饱和亚硫酸氢钠溶液是为了除去过量的高锰酸钾,避免在用盐酸酸化时,产生氯气;该步骤亦可用草酸处理,生成二氧化碳和锰盐,离子方程式为:5H 2C 2O 4+2MnO 4-+6H +=2Mn 2++10CO 2↑+8H 2O ; (4)由信息甲苯用高锰酸钾氧化时生成苯甲酸钾和二氧化锰,“用少量热水洗涤滤渣”一步中滤渣的主要成分是:MnO 2;(5)苯甲酸100Ⅰ时易升华,干燥苯甲酸时,若温度过高,苯甲酸升华而损失; (6)由关系式C 6H 5COOH ~KOH 得,苯甲酸的纯度为:-1-3-11000.01000mol?L 21.5010L 122g?mol 250.122g ⨯⨯⨯⨯ ×100%=86.0%;1.5mL 甲苯理论上可得到苯甲酸的质量:-1-1-11.5mL 0.867g?mL ×122g?mol 92g?mol ⨯ =1.72g ,产品的产率为1g 86%1.72g⨯ ×100%=50%; (7)提纯苯甲酸可用重结晶的方法。
3.(2020年江苏卷)羟基乙酸钠易溶于热水,微溶于冷水,不溶于醇、醚等有机溶剂。
制备少量羟基乙酸钠的反应为222ClCH COOH 2NaOH HOCH COONa NaCl H O 0H +→++∆<实验步骤如下:步骤1:如图所示装置的反应瓶中,加入40g 氯乙酸、50mL 水,搅拌。
逐步加入40%NaOH 溶液,在95Ⅰ继续搅拌反应2小时,反应过程中控制pH 约为9。
步骤2:蒸出部分水至液面有薄膜,加少量热水,趁热过滤。
滤液冷却至15Ⅰ,过滤得粗产品。
步骤3:粗产品溶解于适量热水中,加活性炭脱色,分离掉活性炭。
步骤4:将去除活性炭后的溶液加到适量乙醇中,冷却至15Ⅰ以下,结晶、过滤、干燥,得羟基乙酸钠。
(1)步骤1中,如图所示的装置中仪器A 的名称是___________;逐步加入NaOH 溶液的目的是____________。
(2)步骤2中,蒸馏烧瓶中加入沸石或碎瓷片的目的是_______________。
(3)步骤3中,粗产品溶解于过量水会导致产率__________(填“增大”或“减小”);去除活性炭的操作名称是_______________。
(4)步骤4中,将去除活性炭后的溶液加到适量乙醇中的目的是_______________。
【答案】(1)(回流)冷凝管 防止升温太快、控制反应体系pH(2)防止暴沸 (3)减小 趁热过滤(4)提高羟基乙酸钠的析出量(产率)【解析】制备少量羟基乙酸钠的反应为222ClCH COOH 2NaOH HOCH COONa NaCl H O 0H +→++∆<,根据羟基乙酸钠易溶于热水,粗产品溶解于适量热水中,加活性炭脱色,分离掉活性炭,趁热过滤,根据羟基乙酸钠不溶于醇,将去除活性炭后的溶液加到适量乙醇中,冷却至15Ⅰ以下,结晶、过滤、干燥,得羟基乙酸钠。
(1)根据图中仪器得出仪器A 的名称为冷凝管,根据题中信息可知制备羟基乙酸钠的反应为放热反应,逐步加入NaOH 溶液的目的是防止升温太快,同时控制反应体系的pH ;故答案为:(回流)冷凝管;防止升温太快,控制反应体系的pH 。
(2步骤2中烧瓶中加入沸石或碎瓷片的目的是防止暴沸;故答案为:防止暴沸。
(3)粗产品溶于过量水,导致在水中溶解过多,得到的产物减少,因此导致产率减小;由于产品易溶于热水,微溶于冷水,因此去除活性炭的操作名称是趁热过滤;故答案为:减少;趁热过滤。
(4)根据信息,产品不溶于乙醇、乙醚等有机溶剂中,因此步骤4中,将去除活性炭后的溶液加到适量乙醇中的目的是降低产品的溶解度,提高羟基乙酸钠的析出量(产量);故答案为:提高羟基乙酸钠的析出量(产量)。
4.[2019新课标Ⅰ]乙酰水杨酸(阿司匹林)是目前常用药物之一。
实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:解。
