对甲苯乙酮的制备概论
精细化工4-苯乙酮的合

精细化工-4-苯乙酮的合成引言精细化工是一门用于合成复杂有机化合物的工艺。
本文将介绍精细化工中的一种常用合成反应——苯乙酮的合成。
我们将从合成方法、反应机理以及工业应用等方面进行讨论。
1. 合成方法苯乙酮的合成有多种方法,其中最常用的方法是酸碱催化法和氧化法。
1.1 酸碱催化法酸碱催化法是将苯乙酮的前体苯乙烯与乙酸酐进行缩合反应。
一般情况下,使用硫酸为催化剂,将苯乙烯和乙酸酐加热反应,生成苯乙酮。
反应方程式如下:C6H5CH=CH2 + CH3COOH → C6H5CH2C(O)CH3 + H2O1.2 氧化法氧化法是通过将苯乙烯氧化为苯乙酮。
该方法一般使用氧气或过氧化氢等氧化剂进行反应。
反应方程式如下:C6H5CH=CH2 + O2 → C6H5CH2C(O)CH3 + H2O2. 反应机理2.1 酸碱催化法反应机理酸碱催化法的反应机理主要分为几个步骤:1.乙酸酐与硫酸反应生成酸性环境,促进反应进行。
2.苯乙烯与乙酸酐在酸性环境下发生缩合反应,生成中间产物。
3.中间产物经水解得到苯乙酮。
整个反应过程的机理较为复杂,其中每个步骤都可进一步分解,具体的细节和机理需要进一步研究。
2.2 氧化法反应机理氧化法的反应机理主要涉及苯乙烯的氧化反应。
1.苯乙烯通过氧化剂的作用氧化为过渡态,生成中间产物。
2.中间产物进一步发生转化反应,生成苯乙酮。
由于该方法的氧化剂和反应条件不同,反应机理也会有所差异。
3. 工业应用苯乙酮是一种重要的化工原料,广泛应用于染料、涂料、香料和药物等领域。
在染料工业中,苯乙酮可作为染料的合成原料或溶剂,用于染料的合成和提取等过程。
在涂料工业中,苯乙酮广泛用于各种涂料的合成和稀释。
同时,苯乙酮作为有机溶剂,具有良好的挥发性和溶解性,可以帮助涂料更好地附着在被涂物表面。
在香料工业中,苯乙酮可用于合成多种香精,如玫瑰香精、松香精等。
苯乙酮的独特气味使其成为很多香水和香料的重要成分。
在医药领域中,苯乙酮是合成多种药物的重要中间体。
实验十四 苯乙酮的制备(预习指导)

实验十四 苯乙酮的制备(6学时)一、实验目的1.学习利用Friedel-Crafts 酰基化反应制备芳香酮的原理与方法。
2.巩固无水实验操作的基本技巧。
3.学会电磁搅拌器的作用,掌握有毒气体的处理方法。
4.巩固醛酮的化学性质及鉴别方法。
二、实验原理Friedel-Crafts 酰基化反应是制备芳香酮的最重要和常用的方法之一,酸酐是常用的酰化试剂,无水FeCl 3,BF 3,ZnCl 2 和AlCl 3等路易斯酸作催化剂,分子内的酰基化反应还可用多聚磷酸PPA 作催化剂。
酰基化反应常用过量的液体芳烃、二硫化碳、硝基苯、二氯甲烷等作为反应的溶剂。
该类反应一般为放热反应,通常是将酰基化试剂配成溶液后,慢慢滴加到盛有芳香族化合物的反应瓶中。
用苯和乙酸酐制备苯已酮的反应方程式如下:主反应: + (CH 3CO )2O3COCH 3CH 3COOHCOCH 3AlCl 3CH 3COOAlCl 2HClAlCl 3CH 3COOH3O AlCl 3+3O反应机理:傅—克酰基化反应催化剂的用量大,乙酸酐:AlCl 3=1:2.2(苯乙酮和乙酸都与当量的三氯化铝生成络合物,三氯化铝不能再参与反应,失去催化活性,故必须过量)。
三、试剂及器材1.器材: 50mL 三颈烧瓶,25mL 圆底烧瓶,球形冷凝管,空气冷凝管,恒压滴液漏斗,温度计,电磁搅拌器,电热套(酒精灯),分液漏斗,250 mL烧杯1个,长颈漏斗1个,干燥管,10 mL、5 mL、100mL量筒。
2.试剂:醋酸酐、无水苯、无水三氯化铝、浓盐酸、氢氧化钠、无水硫酸镁,沸石,碎冰四、主要试剂及产品的物理常数五、实验内容与仪器装置1.实验内容(1)合成向装有恒压滴液漏斗、电磁加热搅拌器和回流冷凝管(上端通过一氯化钙干燥管与氯化氢气体吸收装置相连)的50 mL三颈(或二颈)烧瓶中迅速加入研细的6.0g无水三氯化铝和8.0mL无水苯。
在电磁搅拌下自滴液漏斗慢慢滴加2 mL乙酐(加2 mL苯稀释),开始少加几滴,待反应发生后再继续滴加,切勿使反应过于激烈,滴加速度以烧瓶稍热为宜。
对羟基苯乙酮的合成
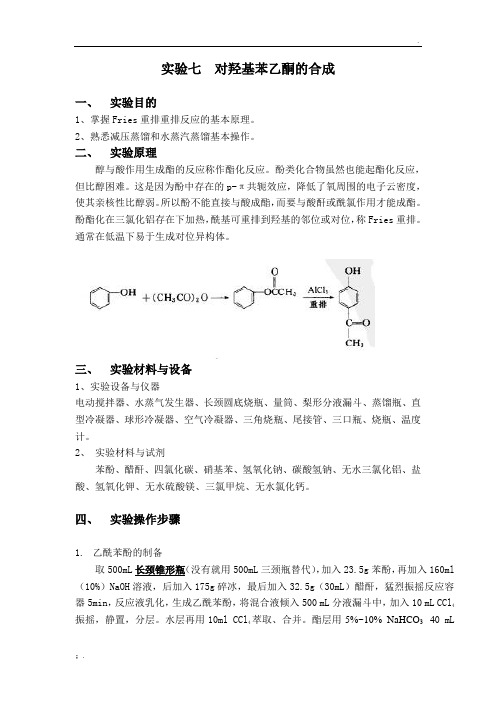
实验七对羟基苯乙酮的合成一、实验目的1、掌握Fries重排重排反应的基本原理。
2、熟悉减压蒸馏和水蒸汽蒸馏基本操作。
二、实验原理醇与酸作用生成酯的反应称作酯化反应。
酚类化合物虽然也能起酯化反应,但比醇困难。
这是因为酚中存在的p-π共轭效应,降低了氧周围的电子云密度,使其亲核性比醇弱。
所以酚不能直接与酸成酯,而要与酸酐或酰氯作用才能成酯。
酚酯化在三氯化铝存在下加热,酰基可重排到羟基的邻位或对位,称Fries重排。
通常在低温下易于生成对位异构体。
三、实验材料与设备1、实验设备与仪器电动搅拌器、水蒸气发生器、长颈圆底烧瓶、量筒、梨形分液漏斗、蒸馏瓶、直型冷凝器、球形冷凝器、空气冷凝器、三角烧瓶、尾接管、三口瓶、烧瓶、温度计。
2、实验材料与试剂苯酚、醋酐、四氯化碳、硝基苯、氢氧化钠、碳酸氢钠、无水三氯化铝、盐酸、氢氧化钾、无水硫酸镁、三氯甲烷、无水氯化钙。
四、实验操作步骤1.乙酰苯酚的制备取500mL长颈锥形瓶(没有就用500mL三颈瓶替代),加入23.5g苯酚,再加入160ml (10%)NaOH溶液,后加入175g碎冰,最后加入32.5g(30mL)醋酐,猛烈振摇反应容器5min,反应液乳化,生成乙酰苯酚,将混合液倾入500 mL分液漏斗中,加入10 mL CCl4振摇,静置,分层。
水层再用10ml CCl萃取、合并。
酯层用5%~10% NaHCO3 40 mL4溶液洗涤至pH7到8,酯层(即CCl4层)置于250mL三角锥瓶中。
用适量无水CaCl2约6克干燥,不时地振摇约1h,然后滤至100 mL蒸馏烧瓶中,旋蒸除去CCl4,然后减压蒸馏收集常压下192~197℃的馏分,称重,计算收率。
(油浴开始加热,阶段梯度加热(10+10+5+5+5…℃,当油浴锅指示温度为115℃,温度计指示温度为74℃时开始有馏出液溜出;馏出液呈无色透明。
)2.对羟基苯乙酮的制备(Fries重排反应)在烘干的装有转子、温度计100mL的三口烧瓶中加入乙酸苯酚10g,硝基苯25mL,剧烈搅拌下分数次缓慢加入无水三氯化铝16g,加完后开始油浴加热回流升温至60℃反应2h,停止加热,慢慢倾入到150g冰水中,并迅速搅拌。
第八章+塞来克西的生产工艺原理

Claisen(克莱森)缩合反应
1) H3C O C CH3 + O C OCH3 H3C CH2 + CH3OH
一、1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮的合成
O H3 C CH3 (CH3CO)2O/AlCl3 or CH3COCl/AlCl3 H3 C (8-5) O CH3 F3C O O O (8-7) CF3 H3 C (8-3) CF3 O O CF3
1. 对甲基苯乙酮(8-5)与三氟乙酸乙酯(8-6)缩合的路线。 对甲基苯乙酮(8-5)在甲醇钠作用下与三氟乙酸乙酯(8-6)缩合 得1-(4-甲基苯基)-4,4,4-三氟丁烷-1,3-二酮(8-3),收率为94 %。该路 线原料价廉易得,总收率高。 2. 对甲基苯乙酮(8-5)与三氟乙酸-β-三氟乙酯(8-7)缩合的路线 在六甲基二硅叠氮锂(LHMDS)作用下,对甲苯乙酮(8-5)与三 氟乙酸-β-三氟乙酯(8-7)在四氢呋喃中缩合得(8-3)。收率为86 %。 该法所用试剂昂贵,收率也低于三氟乙酸乙酯(8-6)路线。
O C H3C
C H2
O C
CF3
(8-3)
2. 工艺过程 氩气保护下,将(8-5)溶于甲醇中并加入25%的甲醇 钠甲醇溶液。将混合物搅拌5 分钟,加入(8-6)。回流24 小时后,将混合物冷至室温并浓缩。加入100mL10%盐酸 并将混合物用乙酸乙酯萃取四次,萃取液用无水硫酸镁干 燥,过滤并浓缩,得棕色油状物,收率94%。产物无需进 一步纯化,可直接投入下一步反应。 3. 反应条件及影响因素 (8-5)的α-氢活性较小,在甲醇钠作用下缩合效果较 好。甲醇钠与(8-5)的摩尔比应为1:1.1 左右;反应在无 水条件下进行。
苯乙酮的制备

苯乙酮的制备
一、实验目的
学习用Friedel-Crafts酰基化反应制备芳酮的原理和操作方法; 掌握无水操作及防潮气体吸收回流装置的安装和使用。
二、实验原理
F-K反应:芳香烃在无水三氯化铝等催化剂存在下。同酰氯或酸酐作用, 在苯环上引入酰基的反应。 当苯环上有一个酰基取代后,因它是间位定位基,使苯环的活性降低,不 会生成多元取代物的混合物。用酸酐做酰基化试剂时,因有一部分三氯化铝 与酸酐作用和能与芳酮生成配合物,所以1mol的酸酐需要3mol的三氯化铝, 实际上还要过量10~20%。 此反应为放热反应,常有一个诱导期,操作时要注意温度变化,不可盲目 快加。
有机基础实验:正溴丁烷的制备
五、注意事项
1. 严防倒吸!(会爆炸)
2. 滴加过程要控制反应速度,注意诱导期
3. 反应液倒入盐酸溶液中,一定要慢、搅拌、通风橱进行操作 4. 有机层干燥后所有使用的仪器要干燥
5. 前馏分和正馏分均有毒,注意密封,回收。
六、实验结果
状态、颜色、气味、沸程、实际产量、理论产量、产率等
有机基础实验:正溴丁烷的制备
三、试剂与原料
反 应 瓶
25.0g三氯化铝 20mL 苯
恒压 滴液 漏斗
8.0mL乙酸酐 10mL 苯
其它:浓盐酸,水,石 油醚,5%碳酸氢钠,无 水Байду номын сангаас酸镁,无水氯化钙
有机基础实验:正溴丁烷的制备
四、实验装置
拉直或用夹子固定,切 忌漏斗完全浸入水中, 可使漏斗倾斜,露出至 少1/2, 防止倒吸!!!
杯中(慢、搅拌、在通风橱进行,可戴护目镜),固体完全溶
解后冷至室温,转移至分液漏斗,分出有机层,水层用石油醚 萃取两次(每次15mL)。合并有机层,依次用5%氢氧化钠溶 液、水各20mL洗涤。 3. 有机层用无水硫酸镁干燥。 4. 简单蒸馏装置,回收前馏分,收集198~202oC的馏分(注意放 水或换空气冷凝管)
苯亚甲基苯乙酮的制备实验报告

苯亚甲基苯乙酮的制备实验报告实验十二苯亚甲基苯乙酮的制备实验十二苯亚甲基苯乙酮的制备一、实验目的1、掌握羟醛缩合反应原理和方法;2、掌握反应温度控制方法;巩固滴液漏斗、搅拌器的使用。
3、巩固产物重结晶的方法。
二、反应原理NaOH -H20C6H5CH0 + CH3C0C6H5 C6H5CH0HCH2C0C6H5C6H5CH=CHC0C6H5 反应历程:0H+HH2C+H2H2CCH2CH2+CH2+0H-H20C6H3CH二CHC0C6H5四、实验装置图五、反应步骤苯亚屮基苯乙酮是山苯屮醛与苯乙酮在10%氢氧化钠溶液催化下缩合而合成。
为了使反应顺利进行和控制苯屮醛的滴加速度,通常在装有搅拌器、温度计和滴液漏斗的三颈瓶中进行。
在装有搅拌器、温度计和恒压漏斗的250ml三口烧瓶中,加入25mL10%氢氧化钠溶液、50mL 95%乙醇和12ml苯乙酮。
保持反应温度在20~250C之间,搅拌下由恒压漏斗滴加10mL 苯屮醛,控制滴加速度(5-10min滴完)。
滴加完毕后,继续保持此温度搅拌搅拌「1.5h,即有固体析出。
反应结束后将三口烧瓶置于冰水浴中冷却15~30min,使结晶完全。
抽滤收集产物,用水充分洗涤,至洗涤液对PH试纸显中性,得苯亚甲基苯乙酮粗品。
粗产物用95%乙醇重结晶(每克产物约需4、5mL溶剂),若溶液颜色较深可加少量活性炭脱色,得浅黃色片状结晶产物,熔点56〜570C。
六、实验流程七、注意要点(1)稀碱最好新配(浓度要够)。
(2)控制好反应温度,温度过低产物发粘,过高副反应多。
(3)洗涤要充分,可转移至烧杯中进行。
(3)产物熔点较低,重结晶加热时易呈熔融状,故须加乙醇作溶剂使呈均相。
八、思考题1 (本实验中如何避免副反应的发生,答:先将苯乙酮与碱混合,产生碳负离子,控制低温,防止苯乙酮的自身缩合;采取控温滴加与搅拌,有利于发生交义疑醛缩合而防止苯屮醛的岐化。
3(本实验中,苯屮醛与苯乙酮加成后为什么不稳定并会立即失水,答:生成的反式烯桂稳定,或者说亚屮基氢受拨基和羟基的影响比较活泼,易于消除。
对甲氧基苯乙酮合成工艺

对甲氧基苯乙酮合成工艺
嘿,今天咱就来聊聊对甲氧基苯乙酮的合成工艺哈。
你们知道不,有一次我在实验室里捣鼓这个合成的时候,那可真是状况百出啊!我就像个好奇的小猴子,这儿摸摸那儿碰碰。
我小心翼翼地把各种试剂按比例加进去,心里还默默祈祷着可千万别出错呀。
然后就开始加热搅拌,眼睛死死地盯着那反应瓶,感觉那瓶子就像个宝贝似的。
随着温度慢慢升高,我那心也跟着提起来了,生怕有啥意外。
突然,我发现搅拌子好像有点不对劲,怎么转得有点怪怪的呢!哎呀呀,我赶紧凑近了仔细看,原来是被一些没溶解的东西给缠住了。
我那个着急呀,这可咋办呢!我赶紧拿个小镊子去摆弄,就跟解救被困的小动物似的,费了好大劲才把搅拌子弄好。
经过这么一番折腾,我才更加深刻地体会到合成对甲氧基苯乙酮可真不是件容易的事儿呀!每一个步骤都得小心翼翼,就像走钢丝一样。
但也就是这样的过程,让我对这个合成工艺有了更特别的感情呢。
总之呢,对甲氧基苯乙酮的合成工艺就是这样,充满了挑战和乐趣,哈哈!。
苯乙酮的合成

注意事项
1. 干燥管的作用及填装方法 2. 气体吸收装置的作用和装法和拆的时间 3. 控制反应温度60度左右,反应完毕后加酸 水要控制白烟不要超过两个球,待反应高 峰过后再加入大量酸水混合物 4. 碱洗有机相时,应轻轻较长时间摇动,较 长时间静置分液,以防止乳化和分离不佳。
思考题
1. 2. 为什么要用过量的苯和无水AlCl3?答:苯既作为溶剂, 又参与反应,极易吸水,称量和加入反应瓶的速度要快。 为什么用盐酸的冰水来分解反应混合物?答:因为苯乙 酮和AlCl3在苯中形成黑黄色的稳定络合物,必须通过酸 解才能析出产物。而酸解氏剧烈的放热反应,冒大量白 烟。为了减少剧烈程度,所以加入用冰水稀释的浓盐酸。 若仍又不溶物,可多加水使之溶解。 室温20度以下时,加酸水解混合液回呈现混浊状。答: 因为苯乙酮的凝固点为196度。若在20度以下加酸水解, 会使苯乙酮呈固体状不溶解,变混浊,即溶解度变小。
试验十 苯乙酮的合成
简介
• 苯乙酮,英文:acetophenone, 或者 methylphenyl ketone, acetylbenzene。分子式 C8H8O,分子量:120.15. • 苯乙酮是由C.Friedel于1857年首先制备出来的。 将苯甲酸钙和乙酸钙的混合物蒸馏得到。在褐煤 焦油的重油馏分中含有少量苯乙酮。自然界中存 在于Stirlingia latifolia的精油中,可以从其中分馏 结晶得到;也存在于岩蔷薇、大鄩麻、香熏草及 各种植物中,还存在于海狸香净油中。
化学性质
制备方法
产品规格及用途
实验目的
• 学习付氏酰基化反应原理和操作 • 学习使用气体吸收装置以及巩固萃取、洗 涤和蒸馏等基本反应操作。
实验原理
付氏酰基化反应就是芳香化合物利用Lewis酸,如AlCl3、BF3、 H2SO4等作催化剂,与酰基化试剂,如酰氯、酸酐和羧酸等发生亲 核取代反应
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Author:xxx
Number:xxx
Abstract:Tolueneand acetic anhydrideisas raw materials,Anhydrous aluminium chlorideisas catalysttopreparate formethyl acetophenone.In the experimental process,werequireto master theprinciple and method ofpreparingmethyl acetophenoneusing FriedelCrafts acyllaboratory.At the same time,werequireto masterwith gasabsorptionheating refluxdeviceand other basic operations,tolearn to controlthe anhydrousreaction conditions.
1.3产物产率误差分析及波谱分析
经计算,理论产量为2.43,实验过程中实际产量为1.80克,产率为74.1%
用恒压滴液漏斗向三颈瓶中滴加乙酸酐时,由于恒压滴液漏斗有漏液现象,故乙酸酐有所损失。部分未反应的乙酸酐,在冰解的过程中水解了,生成了醋酸,醋酸与氯化铝反应,该反应作为该试验的副反应而使乙酸酐不能完全反应转化生成为对甲基苯乙酮。在刚开始反应时,还可能因为乙酸酐的滴加速度过快而导致反应放热过多,一部分乙酸酐碳化了,又损失了一部分的反应原料,故反应产物的产率只有74.1%。
3.实验部分
3.1仪器与试剂
仪器:三颈瓶、恒压滴液漏斗、温度计、球型冷凝管、干燥器、磁力加热搅拌器、铁架台、烧杯、过滤漏斗、橡胶管、分液漏斗、锥形瓶、蒸馏烧瓶、直型冷凝管、尾接管
试剂:7.00ml甲苯、5.00g无水氯化铝、1.5ml乙酸酐、20ml石油醚、12.5g冰、10ml浓盐酸、5%氢氧化钠溶液、无水硫酸钠
16:02
向水相中加入5毫升石油醚萃取
液体分为两层,上层为橘黄色,下层为无色
16:04
将水相再次用10毫升石油醚萃取
液体分为两层,上层为淡黄色,下层为无色
16:06
将有机相混合到蒸馏烧瓶中,加入一定量的5%氢氧化钠溶液,分液
液体分为两层,上层为红棕色,下层无色
16:10
向有机相中加入一定量的清水
液体分层
16停止蒸馏拆卸装置称量产品产物红外和核磁共振谱图对甲基苯乙酮的核磁共振谱图对甲基苯乙酮的红外光谱图书是我们时代的生命别林斯基书籍是巨大的力量列宁书是人类进步的阶梯高尔基书籍是人类知识的总统莎士比亚书籍是人类思想的宝库乌申斯基书籍举世之宝梭罗好的书籍是最贵重的珍宝别林斯基书是唯一不死的东西丘特书籍使人们成为宇宙的主人巴甫连柯书中横卧着整个过去的灵魂卡莱尔人的影响短暂而微弱书的影响则广泛而深远普希金人离开了书如同离开空气一样不能生活科洛廖夫书不仅是生活而且是现在过去和未来文化生活的源泉法耶夫书籍把我们引入最美好的社会使我们认识各个时代的伟大智者书籍便是这种改造灵魂的工具
2.结论
该反应,乙酸酐的滴加速度很关键,由于乙酸酐的总量本身就很少,因此在控制滴加速度时,可能因为操作的问题使乙酸酐的滴加速度过快,反应剧烈,放热迅速,使乙酸酐碳化,大大的降低的对甲基苯乙酮的产率。若是在反应前将一部分甲苯与乙酸酐混合,一部分甲苯盛放在三颈瓶中,可以在一定程度上解决。其次将三颈瓶中的溶液进行冰解时,用玻璃棒引流,可以改为用滴定管等缓慢往下滴。掌握傅克酰基化反应在实验过程中是及其有利的,了解了反应原理,在该反应中,对一些副产物的生成可以更加了解,可以根据个人实验情况调整反应温度。
对甲苯乙酮的制备
作者:xxx
学号:xxx
摘要:以甲苯和乙酸酐为原料,无水氯化铝为催化剂,制备对甲基苯乙酮。在实验过程中,要求掌握实验室中利用Friedel Crafts酰基化制备对甲基苯乙酮的原理和方法。同时要求掌握带有气体吸收装置的加热回流等基本操作,学会控制无水的反应条件。
关键词:对甲苯乙酮、傅克酰基化反应、乙酸酐、尾气吸收
1.结果与讨论
1.1.实验装置的选取
制备反应中,常用酸酐代替酰氯作酰化试剂,这是由于与酰氯相比,酸酐原料易得、纯度高、操作方便,无明显的副反应或有害气体放出;反应平稳且产率高,产生的芳酮容易提纯。与烷基化反应的另一不同点是,酰化反应由于酮基的致钝作用,阻碍了进一步的取代反应,故产物纯度高,不存在烷基化反应的多元取代物,因此,制备纯净的侧链烷基苯通常是通过酰化反应接着还原羧基来实现的。酰基反应也不存在于烃基化反应中的重排反应,这是由于酰基阳离子通过共振作用增加了稳定性。
实验装置:
在反应的过程中,由于催化剂无水氯化铝能够在有水的条件下发生水解,而失去催化剂的效应,故体系中应该保持无水。在进行反应前,相关的实验仪器应该进行烘干处理,相应的反应试剂也应该进行除水。恒压滴液漏斗的使用,一方面可以避免空气中的水蒸气进入反应体系,另一方面可以很好的控制反应速率。因为甲苯和乙酸酐在无水氯化铝作为催化剂的条件下发生反应时,反应速率非常迅速,同时会放出大量的热量。其次,由于甲苯的沸点较低,因此在反应过程中,应该加入一个回流装置,减少甲苯的蒸出,提高反应的产率。由实验原理可知,在反应的过程中有有毒气体氯化氢的产生,故该反应装置中应该再加一个尾气吸收装置,为了避免水蒸气进入反应体系,在球型冷凝管和尾气吸收装置之间还应该加入一个干燥管。后将反应液进行冰解,由于甲苯,对甲基苯乙酮,副产物领甲基苯乙酮等都不溶于水,故可以用分液装置将体系中的水溶液分离。最后由于甲苯等不能通过分液的方法将其与产物对甲基苯乙酮分开,且甲苯的沸点为110.6度,对甲基苯乙酮的沸点为225度,故可以用蒸馏的方式将甲苯从产物中分离出来。
266
1124
----
溶于水、乙醇、甘油
3.反应和后处理实验步骤和现象
时间
温度
操作
现象
14:0
如图搭好实验装置图
14:40
向三颈瓶中加入7毫升甲苯和5克无水氯化铝
开启搅拌和冷凝水
溶液变成浅黄色
溶液黄色加深逐渐变为橙色
14:42
向恒压漏斗中加入1.5毫升乙酸酐,缓慢向三颈瓶中滴加
溶液橙色加深,有少量气泡产生
性状
折光率
密度
熔点
沸点
溶解度
无水三氯化铝
133.5
白色颗粒粉末,有强盐酸气味
---
244
190
----
易溶于水、醇、氯仿、四氯化碳,微溶于水
甲苯
92.14
无色透明液体,有类似苯的芳香味
1.4961
0.8669
-94.7
110.6
不溶于水,可溶于苯、醇等多数有机溶剂
乙酸酐
102.09
无色透明液体,有刺激性气味
参考文献:
1.基础化学实验对甲苯乙酮的合成-----湖大版
2.化学品数据库------对甲基苯乙酮
3.真空精馏技术提纯对甲基苯乙酮的研究,广州化工,贾鹏飞
4.精编有机化学教程第二版,山东大学出版社
5.有机化学第二版,郭灿城主编
附加材料:
1.实验室装置图
反应装置
分液装置
蒸馏装置
2.物性常数
化合物名称
分子量
16:15
向蒸馏烧瓶中加入少量无水硫酸钠干燥
16:17
如图搭好实验装置
16:30
设置温度160,开启加热搅拌和冷凝水
液体为橘红色
16:38
开始有液体蒸出
16:47
153
温度计温度显示60
17:00
172
液体缓慢蒸出,温度计温度显示64,蒸馏烧瓶中有晶体析出
17:10
179
17:12
187
设置温度为200
1.2实验现象的分析
无水氯化铝为浅黄色或者白色的晶体,往甲苯中加入无水氯化铝后,溶液就变为了浅黄色。后用恒压滴液漏斗向三颈瓶中加入乙酸酐,因为产生了氯化氢有毒气体,故液面有气泡产生。加入乙酸酐后,由于三氯化铝与醋酐的铝合物或者三氯化铝和对甲基苯乙酮羰基络合,使溶液呈现较深的橘色。开始加热后,由于无水氯化铝水解生成碱式氯化铝,由于碱式氯化铝为灰黑色的沉淀,且反应体系中磁子在搅拌导致碱式氯化铝不能够沉淀下来形成了悬浊液,使溶液整体呈现黄褐色。烧瓶中的白雾可能为甲苯和氯化氢的混合物。对反应体系进行加热后,由于甲苯的沸点并不是很高,因此会在球型冷凝管中冷凝回流。反应完全后,将三颈瓶中的反应液倒入到12.5克的冰水中进行冰解时,溶液先变成了紫色,后变为棕褐色,底部出现白色沉淀。因为加入了冰和盐酸,其破坏了三氯化铝和酰基氧的络合,释放了产物,因为对甲基苯乙酮为略带黄色的透明液体,故由于对甲基苯乙酮和碱式氯化铝的同时存在,导致溶液为黄褐色。加入的盐酸的量不够多,无法溶液因水解产生的氢氧化铝的沉淀,故溶液底部还有一层白色沉淀。将溶液分液时,由于甲苯作为溶剂,密度为0.87,产物对甲基苯乙酮的密度为1.0051,略大于水,故有机相浮在水相上。后两次用石油醚进行萃取时,由于石油醚的密度比水的小,故有机相都在水相上,且水相中溶解的产物对甲基苯乙酮的量越来越少,故每次有机相的颜色都越来越浅,从橘黄色变为浅黄色。最后对有机相进行蒸馏时,由于甲苯的沸点较低,且在混合物中的量是最大的,因此在蒸馏过程中,首先会有大量的无色透明液体蒸出,该无色透明液体就为甲苯,蒸馏烧瓶中剩余的液体则被视为产物对甲基苯乙酮。
3.2实验方法
在装有回流冷凝管和恒压滴液漏斗的三颈烧瓶中,加入5.00克无水三氯化铝和7.0毫升甲苯,冷凝管上口接一个氯化钙干燥管,干燥管与氯化氢吸收装置连接。从滴液漏斗中慢慢加入1.5毫升乙酸酐,滴加速度以三口烧瓶稍热为宜,约十几分钟滴加完毕。反应过程中要充分搅拌使反应充分。在水浴上加热回流至反应体系内不再有盐酸气体产生为止,待反应液冷却后冰解。将反应液倒入盛有10毫升浓盐酸和12.5克碎冰的烧杯中冰解。若有固体不溶物,可加入少量盐酸使之溶解。然后将该溶液倒入分液漏斗中,分出有机相,水相用10毫升石油醚分两次提取,提取液和有机相合并,依次用等体积的5%的氢氧化钠水溶液和水各洗一次至中性。经无水硫酸钠干燥。先蒸出甲苯,加热收集198-202度的馏分,得产品承重计算产率。
