天然药物化学.ppt
合集下载
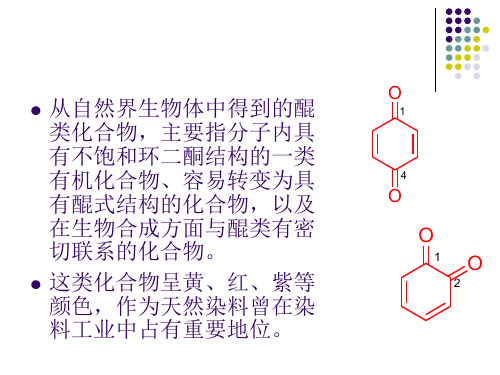
天然药物化学最新PPT课件
O O OH Glc
Glc O O OH
HH
COOH
CH2OH O O OH Glc
O O
长时间存放 2
H
O
Glc
O
O
OH
O 蒽醌
H
H
COOH
COOH
O
O
OH
Glc
OH O OH COOH
中位萘并二蒽酮类
OH O OH
HO
CH3
H3C
OH
OH O OH
hypericin
醌类化合物的理化性质
(一)物理性质 1.性 状 2.升华性 3.溶解度
高效液相色谱法(HPLC)
蒽醌类化合物的波谱特征
UV
O
O A
O
峰1 ~230nm
峰2 240~260nm (A)
峰3 262~295nm (B)
峰4 305~389nm (A)
O
峰5 >400nm
B
(B中的羰基引起)
蒽醌类化合物的波谱特征
核磁共振氢谱(1H-NMR或PMR)
5.0
5.0
OH
H OOH
O
O
应用:pH梯度萃 取
游离蒽醌酸性顺序:
-COOH>2个β-OH>1个β-OH>2个α-OH>1个α-OH
5%NaHCO3
5%Na2CO3 1%NaOH 5%NaOH
由于醌类化合物多具有酸性,在碱液中成盐而溶解, 加酸酸化后重新游离而沉淀析出。故常利用碱溶解酸 沉淀法提取醌类化合物。
OH O OH
H3CO O
O H3CO H3CO
O
arnebinone
O
arnebifuranon
Glc O O OH
HH
COOH
CH2OH O O OH Glc
O O
长时间存放 2
H
O
Glc
O
O
OH
O 蒽醌
H
H
COOH
COOH
O
O
OH
Glc
OH O OH COOH
中位萘并二蒽酮类
OH O OH
HO
CH3
H3C
OH
OH O OH
hypericin
醌类化合物的理化性质
(一)物理性质 1.性 状 2.升华性 3.溶解度
高效液相色谱法(HPLC)
蒽醌类化合物的波谱特征
UV
O
O A
O
峰1 ~230nm
峰2 240~260nm (A)
峰3 262~295nm (B)
峰4 305~389nm (A)
O
峰5 >400nm
B
(B中的羰基引起)
蒽醌类化合物的波谱特征
核磁共振氢谱(1H-NMR或PMR)
5.0
5.0
OH
H OOH
O
O
应用:pH梯度萃 取
游离蒽醌酸性顺序:
-COOH>2个β-OH>1个β-OH>2个α-OH>1个α-OH
5%NaHCO3
5%Na2CO3 1%NaOH 5%NaOH
由于醌类化合物多具有酸性,在碱液中成盐而溶解, 加酸酸化后重新游离而沉淀析出。故常利用碱溶解酸 沉淀法提取醌类化合物。
OH O OH
H3CO O
O H3CO H3CO
O
arnebinone
O
arnebifuranon
苯丙素(天然药物化学课件)

9
O O
荜澄茄脂素
H3CO HO
9’
O
7
OH
OCH3 OH
落叶松脂素
55
第三节
木脂素类
lignans
(三)木脂内酯
二芳基丁内酯
O
O
O
O
O
O
56
第三节
木脂素类
lignans
木脂内酯例子
O
O
O
H3CO
O
O
O
O
O
RO
O
O
OCH3 OCH3
R=H 牛蒡子苷元 R=glc 牛蒡子苷
O O
台湾脂素A
O O
台湾脂素B
coumarins
三、提取分离方法
(一)系统溶剂分离法
前胡→乙醇提取物→水分散
乙酸乙酯萃取 正丁醇萃取物 物(游离) (苷)
33
第二节
香豆素类
coumarins
(二)水蒸气蒸馏法
小分子香豆素
34
第二节
香豆素类
coumarins
(三)碱溶酸沉法
内酯环
条件的控制
C-8有酰基
侧链酯基水解
烯丙醚或邻二醇重排
HO
OH
HO
O
OH
绿原O酸
抑制组胺释放
COOH
OH OH
O O
OHOH
OH
绿原酸
CH2OH
O OH
H3CO O
HO
H3CO
OH
OH OH
OH
丁香苷
8
第一节
简单苯丙素
Simple phenylpropane
二、提取和分离
天然药物化学(ppt)

二、分离纯化
(一)溶剂法
酸碱法:是将总提取物溶于有机溶剂,用酸水、碱水 分别萃取,难溶于水的有机碱性成分可与酸成盐溶于水, 从而达到分离纯化的目的。 溶剂分配法:利用混合物中各组分在两相溶剂中分配 系数差进行分离纯化的方法。
(二)沉淀法
基于有些天然药物化学成分能与某些试剂生成沉 淀;或降低某些成分在溶液中的溶解度而自溶液中析出 的一种分离方法。
多孔凝胶过滤色谱
第五节 天然药物化学成分结构鉴定方法
结构鉴定的程序一般是: (1)确定纯度 (2)测定物理常数 (3)确定分子量、分子式 (4)波谱分析 (5)确定结构式
确定化合物结构常用几种光谱分析技术: ① 紫外光谱 ② 红外光谱 ③ 磁共振 ④ 质谱
紫外光谱
测定范围:通常在200~600nm的紫外可见光区 原理:基于分子中的电子可因光照射由基态跃迁到激
第四节 天然药物化学成分的提取分离方法
一、天然药物化学成分的提取
(一)溶剂提取法 1、溶剂
原理:相似者相溶,根据欲提取成分的性质确定,充分地提取 所需成分、沸点适中、易回收、安全低毒。 常用溶剂:以溶剂极性弱到强的顺序排列为: 石油醚<四氯化碳<苯< 二氯甲烷<氯仿<氯仿<乙醚<乙酸 乙酯<正丁醇<丙酮<乙醇<甲醇<水
天然药物化学(ppt)
优选天然药物化学
第一节 天然药物化学的性质与任务
一、天然药物化学的性质
1、概念:“天然药物化学”是应用现代科学理论 与方法研究天然药物中的化学成分的学科. 2、性质:“天然药物化学”是从分子水平研究天 然药物的药效物质基础及其防治疾病规律的一门综 合性学科。
“天然药物化学”是药学二级学科“药物化学”下设置的三级学 科. “天然药物化学”是药学类专业规定设置的一门主要专业课程.
强心苷—结构类型(天然药物化学课件)

(1)甲型强心苷元
HO
C17位连接五元Δαβ-γ-内酯。
大多数属于此种类型。
O
O
HO
洋地黄毒苷元
(2) 乙型强心苷元
C17连接六元的Δαβ,γδδ-内酯。
HO
O
O
HO
海葱苷元
糖部分
根据C2位上有无羟基可以将他们分成两大类:
α-去氧糖和α-羟基糖。
α-去氧糖
CH3 O OH
(2,6-二去氧糖) OH 只存在于强心苷中 OH
D-洋地黄毒糖
O OH CH3
OH OCH3
α-羟基糖 (6-去氧糖、 葡萄糖)
OH
O OH
CH3
OH OH L-鼠李糖
OH
O OH
CH3 O多为单糖链苷,大多与苷元C3羟基缩合,最多可连接 5个糖分子。
Ⅰ型强心苷:苷元C3-O-(2,6-二去氧糖)x-(D-葡萄糖)y
(一)西地兰的提取分离 西地兰的提取分离可分为三个步骤:提取总苷、分
离苷丙、苷丙脱乙酰基。 (二)地高辛的提取分离
地高辛的提取分离过程为:原药材酶水解、乙醇提 取、除脂溶性杂质,分离次生苷、脱去乙酰基、分离地 高辛。
从毛花洋地黄叶中提取分离地高辛的流程
流程分析: 1、利用叶中存在的β-D-葡萄糖酶水解去除葡萄糖,再用乙醇提取; 2、提取液浓缩至20%时脂溶性杂质溶解度小,析胶效果好,可去 除脂溶性杂质; 3、次生苷在三氯甲烷中溶解度较大; 4、NaOH洗涤去乙酰基并除去残留的叶绿素; 5、地高辛在三氯甲 烷中溶解度较大; 6、地高辛的精制利用其在乙醇中溶解度相关悬殊的性质进行。
强心苷-结构类型
1
概述
2
结构类型
3
醌类化合物(天然药物化学课件)

O
O OH
OH O OH
金丝桃素 O
OH O OH
天精
CH3 OH O OH
OH O OH H3C O
山扁豆双醌
22
结构、分类 第一节 与生物活性
classification, structure and bioactivity of quinones
O
二蒽酮继续氧化产物
O
O
去氢二蒽酮
O
日照蒽酮
天然药物化学
HH
COOH COOH
glc O O OH
OH O OH glc
COOH
大黄酸蒽酮
番泻叶苷A
21
结构、分类 第一节 与生物活性
classification, structure and bioactivity of quinones
OH O
OH
其他结合方式
OH O OH
HO
CH3
HO
CH3
HO
CH3 H3C
(二)溶解性
游离者极性小
–乙醇、丙酮、三氯甲烷、乙醚
成苷后极性大
–甲醇、乙醇、热水
碳苷
–吡啶
26
理化性质 第二节 显色反应
physicochemical property and reaction
(三)升华性和挥发性
游离的一般有升华性
小分子苯醌和萘醌具挥发性
有些注意避光
27
理化性质 第二节 显色反应
番泻叶苷B
glc O O OH
HH
COOH CH2OH
H
COOH
H
CH2OH
glc O O OH
番泻叶苷C
glc O O OH
蒽醌类化合物—提取分离(天然药物化学课件)

试剂:碱性试剂+活性亚甲基试剂
判断:苯醌及萘醌类化合物未取代为阳性;蒽醌为阴性。
O
O
O
O
醌环上未取代位置
在氨碱性下 兰蓝绿绿色色
+ 活性次甲基试剂
或or
(丙二酸酯、乙酰醋酸脂/醇液)
兰紫色
蓝紫色
不同颜色反应鉴别特点及意义
反应类型
Feigl反应
无色亚甲蓝 Bornträge反
应
反应试剂
反应特征
鉴别特点
引力或产生氢键的结果;分子筛是其多孔性结构性质 ❖ 3、影响吸附因素:溶剂本身的性质;物质在溶剂中的
溶解度(溶解度大,树脂对其吸附力降低);化合物 的性质
五、蒽醌类化合物(三) ——显色反应
一、碱液呈色反应( Bornträge反应)
❖ 羟基蒽醌类遇碱显红—紫红色。 ❖ 检识羟基蒽醌成分的最常用方法。 ❖ 蒽酚、蒽酮、二蒽酮类成分需氧化形成羟基
五、蒽醌类化合物(四)
一、提取方法
(一)亲脂性有机溶剂提取法 (二)醇提取法 (三)碱提酸沉法 (四)水蒸气蒸馏法 (五)其它方法
(一)亲脂性有机溶剂提取法
(1)用于提取苷元(游离醌类)。 (2)可用苯、氯仿等极性较小的溶剂提取。 (3)蒽醌类在植物体内多以苷或盐的形式存在。
药材 酸 苷水解,盐游离
(2)色谱分离法 ❖ 多用吸附柱层析,以硅胶、磷酸氢钙、聚酰胺
粉为吸附剂,不宜用氧化铝,尤其是碱性氧化铝 ,因为羟基蒽醌能与氧化铝形成牢固螯合物,难 以洗脱。
(3)大孔吸附树脂 ❖ 1、特点:白色球形颗粒,分为非极性和极性两类,理
化性质稳定,不溶于酸、碱及有机溶媒中 ❖ 2、原理:吸附性和分子筛性相结合。吸附性由范德华
判断:苯醌及萘醌类化合物未取代为阳性;蒽醌为阴性。
O
O
O
O
醌环上未取代位置
在氨碱性下 兰蓝绿绿色色
+ 活性次甲基试剂
或or
(丙二酸酯、乙酰醋酸脂/醇液)
兰紫色
蓝紫色
不同颜色反应鉴别特点及意义
反应类型
Feigl反应
无色亚甲蓝 Bornträge反
应
反应试剂
反应特征
鉴别特点
引力或产生氢键的结果;分子筛是其多孔性结构性质 ❖ 3、影响吸附因素:溶剂本身的性质;物质在溶剂中的
溶解度(溶解度大,树脂对其吸附力降低);化合物 的性质
五、蒽醌类化合物(三) ——显色反应
一、碱液呈色反应( Bornträge反应)
❖ 羟基蒽醌类遇碱显红—紫红色。 ❖ 检识羟基蒽醌成分的最常用方法。 ❖ 蒽酚、蒽酮、二蒽酮类成分需氧化形成羟基
五、蒽醌类化合物(四)
一、提取方法
(一)亲脂性有机溶剂提取法 (二)醇提取法 (三)碱提酸沉法 (四)水蒸气蒸馏法 (五)其它方法
(一)亲脂性有机溶剂提取法
(1)用于提取苷元(游离醌类)。 (2)可用苯、氯仿等极性较小的溶剂提取。 (3)蒽醌类在植物体内多以苷或盐的形式存在。
药材 酸 苷水解,盐游离
(2)色谱分离法 ❖ 多用吸附柱层析,以硅胶、磷酸氢钙、聚酰胺
粉为吸附剂,不宜用氧化铝,尤其是碱性氧化铝 ,因为羟基蒽醌能与氧化铝形成牢固螯合物,难 以洗脱。
(3)大孔吸附树脂 ❖ 1、特点:白色球形颗粒,分为非极性和极性两类,理
化性质稳定,不溶于酸、碱及有机溶媒中 ❖ 2、原理:吸附性和分子筛性相结合。吸附性由范德华
鞣质及其他酚类(天然药物化学课件)
31
第一节
鞣质
Tannins
(三)复合鞣质
黄烷醇和可水解鞣质通过碳 碳键连接而成
OH
HO O
HO
C
O
O
HO
C
HO OH
O O
CH2 OH HO H
O HO
OC CO
HO
OH
OH OH
O
OH
山茶素 B
HO OH OH OH
32
第一节
鞣质
Tannins
番石榴素 A
33
第一节
鞣质
Tannins
HO HO
O
OH C O C O
HO
OH
OH
HO
OH
OH
HO
OH
HO OH HO OH
OH OH
OH OH
OH OH
21
第一节
鞣质
Tannins
老鹳草素
HO OH OH OH
HO
OH
DHHDP
OC CO
O
O
脱氢六羟基联苯二酰基
CH2 O O
OC
OH
O
O
O
C
CO
OH HO
H
O HO
OH
HO
OH
OH
O
22
第一节
25
第一节
鞣质
Tannins
(二)缩合鞣质
黄烷醇以碳碳缩合而成
可缩合为鞣红
茶叶、翻白草、大黄
主要结构单元以儿茶素为代 表的黄烷醇类
26
第一节
鞣质
Tannins
HO
O
1.黄烷-3-醇类
OH
制药工程专业《天然药物化学》PPT课件
卫生部规划教材(第四版)
制药工程专业 天然药物化学
天然药物化学(medicinal chemistry of natural products) 是系指运用现代科学理论与方法研究药用植物或植物中具有生理活性 成分的化学分支学科。
它是随着分离技术和鉴定方法趋于微量、快速而发展的。其研究 内容主要是药用植物或植物中活性成分的提取、分离、结构测定,必 要的结构改造以及合成,以探索安全高效的新的化合物。
发展史_4
青蒿素(Qinghaosu, arteannuin, artemisimnin)是我国科学家从黄花蒿 Artemisia annua L.叶中得到的新型抗虐倍半萜过氧化物,是我国自主开发的在该领域 最杰出的工作,1977 年3 月在《科学通报》上首次发表了其独特的结构,2002 年4 月 22 日,复方蒿甲醚被列入WHO 第12 版基本药物名录的核心目录。中国发现者屠呦呦因 此获2015诺贝尔生理学或医学奖。
我国明代李挺所著的《医学入门》(1575年)记载了用发酵法从五倍子中得到没 食子酸的过程。书中所谓“五倍子粗粉并矾,曲和匀作酒曲样入瓷器避不见风,候生白 取出”,“生白”即没食子酸生成之意,这是世界上最早从天然产物中得到的有机酸。 李时珍在《本草纲目》(1596年)中详细记载了用升华法制备、纯化樟脑的过程。
发展史_1
人类发展和进化的过程同时也是人类不断与疾病做斗争的过程。据记载人类利用 天然产物作为药物已有几千年的历史,在远古时代,人类有了身体上的痛苦或称谓“疾 病”就开始从自然界中寻找被称为“药”的物质来缓解疾病带来的痛苦。这种来自自然 界的可以缓解或治疗疾病的物质就是最原始的“药物”,并一代代流传下来,国外称之 为“天然药物(natural medicines)”,我国称之为“中草药(Chinese herbal medicines)或中药(Chinese materia medica,CMM)”。之所以能防病治病,其物质基础 在于其中所含的具有活性的化学成分。
制药工程专业 天然药物化学
天然药物化学(medicinal chemistry of natural products) 是系指运用现代科学理论与方法研究药用植物或植物中具有生理活性 成分的化学分支学科。
它是随着分离技术和鉴定方法趋于微量、快速而发展的。其研究 内容主要是药用植物或植物中活性成分的提取、分离、结构测定,必 要的结构改造以及合成,以探索安全高效的新的化合物。
发展史_4
青蒿素(Qinghaosu, arteannuin, artemisimnin)是我国科学家从黄花蒿 Artemisia annua L.叶中得到的新型抗虐倍半萜过氧化物,是我国自主开发的在该领域 最杰出的工作,1977 年3 月在《科学通报》上首次发表了其独特的结构,2002 年4 月 22 日,复方蒿甲醚被列入WHO 第12 版基本药物名录的核心目录。中国发现者屠呦呦因 此获2015诺贝尔生理学或医学奖。
我国明代李挺所著的《医学入门》(1575年)记载了用发酵法从五倍子中得到没 食子酸的过程。书中所谓“五倍子粗粉并矾,曲和匀作酒曲样入瓷器避不见风,候生白 取出”,“生白”即没食子酸生成之意,这是世界上最早从天然产物中得到的有机酸。 李时珍在《本草纲目》(1596年)中详细记载了用升华法制备、纯化樟脑的过程。
发展史_1
人类发展和进化的过程同时也是人类不断与疾病做斗争的过程。据记载人类利用 天然产物作为药物已有几千年的历史,在远古时代,人类有了身体上的痛苦或称谓“疾 病”就开始从自然界中寻找被称为“药”的物质来缓解疾病带来的痛苦。这种来自自然 界的可以缓解或治疗疾病的物质就是最原始的“药物”,并一代代流传下来,国外称之 为“天然药物(natural medicines)”,我国称之为“中草药(Chinese herbal medicines)或中药(Chinese materia medica,CMM)”。之所以能防病治病,其物质基础 在于其中所含的具有活性的化学成分。
蒽醌类化合物—鉴定与结构测定(天然药物化学课件)
几种常见蒽醌苷类纸色谱的Rf值
④三个α-OH
在λmax485~530nm有两个或两个以上
的吸收峰
⑤四个α-OH
在λmax540~560nm出现多重峰
二、红外光谱(IR):
醌类化合物的主要特征是羰基吸收峰以及苯 环和双键的吸收峰。
羟基蒽醌类化合物的红外区域有:
VC=O 1675~1653 cm-1 (羰基的伸缩振动)
V-OH
3600~3150 cm-1 (羟基的伸缩振动)
第Ⅳ峰:如α位有供电子基,则峰位红移,强度降 低;如取代基处于β位,则吸收峰强度增大。 第Ⅴ峰:主要受α羟基影响,α羟基数目越多, λmax红移就越多
第V峰一般有如下规律:
①无α-OH
λmax:356~362.5nm
②一个α-OH ③二个α-OH
λmax:400~420nm 1,8位二羟基蒽醌λmax:400~420nm; 1,5位二羟基蒽醌λmax:418~440nm; 1,4位二羟基蒽醌λmax:430~500nm
α-酚OH数 0 1 2 2 3 4
羟基位置 无α-OH 1-OH 1,4或1,5-OH 1,8-二OH 1,4,5-三OH 1,4,5,8-四OH
游离C=O频率 (cm-1)
1678~1653 1675~1647
-
1678~1661
-
-
缔合C=O频率 (cm-1) -
1637~1621
1645~1608
-OH取代将影响相应的吸收带向红位移
与结构的关系:
第Ⅰ峰与结构中羟基数目有关,羟基越多,其位置 吸收峰波长越长,峰1波长与羟基位置(α、β)无关,强 度主要取决于α羟基的数目。
第Ⅲ峰由醌样结构引起,峰位和强度主要受β酚羟 基的影响,β酚羟基能够通过蒽醌母核向羰基供电,使 该峰红移,强度亦增强。若吸收强度lgε低于4.1,表示 无β酚羟基。
黄酮类化合物—理化性质(天然药物化学课件)
醇及黄酮苷类(糖),结构中有手性碳,故均
具有旋光性。
O
*
O
O
O
*
* OH
*
O
O
O* * OH
O* ** OH
OH
黄酮类化合物-理化性质(2)
4.溶解性
黄酮类化合物的溶解性因结构不同而有很大 差异。一般情况下
水 黄酮苷元 (亲脂性) 黄酮苷 (亲水性) +
甲(乙)醇 乙醚(苯)
+
+
+
+--石油醚苷元溶解度:取决于存在状态
总结: 花色素(平面性分子,离子型) > 非平面性分子 > 平面性分子
5.酸碱性:以黄酮为例
(1)酸性
❖ 黄酮类化合物因分子中具有酚羟基,故显酸性,黄
酮中各酚羟基酸性由强到弱的顺序是:
羟基位置
酸性 溶解性
7,4'-二羟基
强 溶于5%NaHCO3
7或4'-羟基 一般酚羟基
溶于5%Na2CO3 溶于0.2%NaOH
黄酮类化合物-理化性质(1)
1.性状
❖黄酮类化合物多为结晶性固体,少数(如黄 酮苷类)为无定形粉末。
2.颜色
(1)颜色与分子中是否存在交叉共轭体系有
1
2
关。
3
O
(2)在黄酮(醇)7 、4′引入OH 、OCH3 等助色
团,促进电子移位、重排,化合物的颜色加深 (3)pH不同而颜色改变, pH 〈7显红色, pH =8.5显
1.结构:平面型分子
难溶于水:
黄酮(醇)、查耳酮
非平面型分子 溶解度稍大: 二氢黄酮(醇)
离子型分子
具有盐的通性,水溶性大 :花青素
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.原始和萌芽阶段(——18世纪末)
天然药物识别、使用经验——巫术、迷信色彩 文明的进步——对疾病、天然药物的认识趋于客观
231—341,晋,葛洪,《抱卜子》
1575, 明,李, 《医学入门》,没食子酸
1711,
清,洪遵,《集验方》,樟脑
1769-1786,舍勒,酒石酸、
苯甲酸、乳酸、苹果酸、没食子酸
正确理解成分的划分
生理活性成分并不一定真正代表有效成分
有效成分与无效成分的划分是相对的、发展的
A. 不同类型成分,在不同天然药物中作用不同
B. 原来视为无效成分,可能成为有效成分
C. 过去视为有效成分,被修正、完善
麝香 抗炎成分 麝香酮————多肽
丹参 扩冠
丹参醌————丹参酚酸
D. 加工、代谢等过程,可转化非活性成分为活性成分
第一章 总 论
第一节 绪论 第二节 生物合成 第三节 提取分离方法 第四节 结构研究法
第一节 绪 论
一、天然药物及其相关术语 二、天然药物化学的定义、研究对象、研究内容 三、天然药物化学发展历史沿革和现状 四、天然药物化学在中药现代化中的作用
一、天然药物及其相关术语
1.天然药物的定义: 天然来源 2.天然药物的来源:
2.学科真正形成阶段(19世纪)
特点二:结构鉴定以化学方法为主 氧化、还原等降解反应——推导结构 碎片合成、全合成————证明结构
2.学科真正形成阶段(19世纪)
特点三:生源合成途径、本质的揭示 生源前体的识别:萜类———MVA 生物碱——α-Aa 生源合成本质的揭示:生物细胞内多步酶促反应 有机反应理论来解释机制 生物合成物质用于结构确定
2.学科真正形成阶段(19世纪)
特点一:以化学成分的发现和分离为主 1806, 阿片——————吗啡(morphine) 1820, 金鸡纳树皮———奎宁 (quinine) 1828, 烟草——————烟碱(nicotine) 1885, 麻黄——————麻黄碱(ephedrine) 吐根碱、士的宁、小檗碱,阿托品、可卡因等
1. 天然药物化学定义及相关术语:
天然药物化学
Chemistry of natural medicine
Medicinal chemistry of natural products
运用现代科学理论与方法研究天然药物中化学成分 (以生理活性成分或有效成分为主)
中药化学
Chemistry of TCM
4. 天然药物研究现状
世界各地加强天然药物研发的投入 1983-1994年,上市522种新药,44%天然来源 1984-1995,FDA,31种抗癌新药,61%天然来源 93种抗感染新药,63%天然来源
关于天然产物的学术交流日渐活跃
二、天然药物化学的定义、研究对象、研究内容
1.定义及相关术语 2.研究对象 3.研究内容
3. 天然药物化学的研究内容
结构特点 理化性质 提取分离方法 结构鉴定方法 生物合成
结构修饰 构效关系 生物转化 体内代谢过程等
三、天然药物化学发展历史沿革和现状
大体分为以下3个阶段: 1. 原始和萌芽阶段(——18世纪末) 2. 学科真正形成阶段(19世纪) 3. 学科迅速发展时期(20世纪——)
天然化合物的分离向高效、快速、微量发展
3.学科迅速发展时期(20世纪——)
特点二:波谱技术用于天然化合物的结构鉴定
IR: 1944,Pekin-Elmer公司,第一台红外光谱仪 MS: 20世纪,质谱仪
EI、CI,FD,FAB,ESI,MALDI ESI-TOF,MALDI-TOF NMR:1953,30MHZ的连续波核磁共振仪 70年代,脉冲傅立叶变换核磁共振仪 1D NMR——2D NMR 30—60—100—300MHz 400—500—600—800—900MHz UV,X-ray,ORD,CD等
2.天然药物化学的研究对象
生理活性成分 active compound / constituent 非生理活性成分 inactive compounds
有效成分 无效成分 有效部位 active fraction
一种主要有效成分/一组结构相近的有效成分 有毒成分 toxic compound
植物 动物 矿物 微生物 海洋天然药物
3.天然药物相关术语
天然药物 natural medicine 中草药 chinese herbal medicine
《本草纲目》,1892种 / 《本草纲目拾遗》,1021种 目前我国药用植物总数,15000余种
中药 Traditional Chinese Medicine 草药 herbal drug 民族药 Ethnic Medicine 蒙药 Mongolia Medicine
藏药 Tibetan Medicine 苗药 Miao drug
生药 Crude drug
4. 天然药物研究现状
疾病谱、医疗模式、药物结构的改变 传染、感染性疾病 —— 身心疾病、现代病 治疗 —— 预防、保健、治疗、康复 化药 —— 化药 天然药
国际市场对天然药物的需求日益增大 2000年全球植物药销售额,300亿美元 天然药物销售额年增长幅度,欧共体,30% 美国, 20% 日本, 15%
3.学科迅速发展时期(20世纪——)
特点一:色谱技术用于天然化合物的分离和纯化
1906,俄,Tsweet,碳酸钙为吸附剂,石油醚为洗脱剂, 1931,德,Kuhn and Lederer,氧化铝、碳酸钙为吸附剂, 1940,提出了液液色谱法,如逆流分配 1952,James and Martin,提出气液色谱理论 20世纪60年代,高效液相色谱出现
植Hale Waihona Puke 化学Phytochemistry
天然产物化学 Chemistry of natural products
2.天然药物化学的研究对象
研究对象:化学成分 chemical constituents 特别是生理活性成分或有效成分 active compound
成分的复杂性: 不同药物所含成分类型不同 每种类型成分的数目相当多 同种药物所含成分结构、性质各异
