九年级上册化学化学方程式归纳练习及答案
人教版初中九年级化学上册第五单元《化学方程式》(含答案解析)

一、选择题1.下列说法中正确并符合质量守恒定律解释的是( ) A .10g 酒精和50g 水混匀后形成60g 酒精溶液B .红磷在氧气中燃烧,反应后得到30g P 2O 5,则参加反应的O 2和磷的总质量一定为30gC .2L 氢气和1L 氧气反应,生成3L 水,这符合质量守恒定律D .2g 氢气和8g 氧气完全反应,生成10g 水,这符合质量守恒定律B 解析:BA 、10g 酒精和50g 水混匀后形成60g 酒精溶液,无新物质生成,属于物理变化,不符合质量守恒定律,不符合题意;B 、根据质量守恒定律,化学反应前后,物质的总质量不变,红磷在氧气中燃烧,反应后得到30g P 2O 5,则参加反应的O 2和磷的总质量一定为30g ,符合题意;C 、质量守恒定律,是化学反应前后,物质的总质量相等,不是体积,不符合题意;D 、氢气和氧气反应:2222H +O 2H O 点燃,参加反应的氢气、氧气和生成水的质量比为:4:32:36=1:8:9,故2g 氢气和8g 氧气反应,氢气剩余,不能生成10g 水,不符合题意。
故选B 。
2.化学现象中有许多“相等”,下列有关“相等”的说法错误的是( ) A .原子中的质子数和核外电子数一定相等 B .化学反应前后各原子总数相等C .50mL 酒精和50mL 水混合,其体积与混合前二者的体积之和相等D .化合物中,正负化合价数值一定相等C 解析:C 【分析】A 、根据原子的构成分析;B 、根据化学反应的实质及质量守恒定律分析;C 、根据分子的基本性质进行分析;D 、根据化合价分析。
A 、原子中核内质子数和核外电子数一定相等, 故说法正确;B 、化学反应的实质是分子分解成原子,原子重新组合成新的分子,反应前后各原子总数相等, 故说法正确;C 、由于分子间有间隔,50mL 酒精和50mL 水混合,其体积一定小于混合前二者的体积之和, 故说法错误;D 、化合物中,正负化合价数值一定相等, 故说法正确。
(必考题)初中九年级化学上册第五单元《化学方程式》经典习题(含答案解析)

(必考题)初中九年级化学上册第五单元《化学方程式》经典习题(含答案解析)一、选择题1.如图是“尾气催化转换器”将汽车尾气中有毒气体转化为无毒气体的微观示意图,其中不同的圆球代表不同的原子。
下列说法错误的是( )A .该反应一定不是化合反应B .图中的反应物全部是化合物C ..参加反应的两种分子个数比为1:1D .该反应生成了三种生成物 2.图中表示氢原子,表示氮原子,在一定条件有如下图反应发生,下列有关叙述错误的是A .该反应为化合反应B .该反应前两种物质均为单质C .该反应前后三种物质的化学计量数之比为4:1:2D .一个分子中含有三个氢原子和一个氮原子3.下图是某个化学反应的微观模拟示意图。
从图中获得的有关信息不正确...的是A .反应前后原子种类和个数个数不变B .反应前是混合物,反应后是化合物C .化学反应中分子可分为原子D .该反应为分解反应4.刚刚过去的9月27日,我省太原卫星发射中心用长征四号乙运载火箭,以一箭双星的方式成功发射环境减灾二号A 、B 卫星。
此次发射所使用的燃料为四氧化二氮和偏二甲肼,其燃烧的反应为2822422C H N +2N O 2CO 3N 4X ↑+↑+点燃,其中X 的化学式为A .NH 3B .N 2OC .H 2OD .C 2H 45.在一个密闭的容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下,下列说法正确的是物质甲乙丙丁反应前质量/g93221反应后质量/g x3417A.乙是该反应的催化剂B.x的值为2C.丙可能是单质D.该反应可能是水通电分解6.甲型H1N1流感的蔓延,是对人类健康的重大威胁。
从中草药“八角”中提取莽草酸是生产抗甲型H1N1流感药物“达菲”的主要原料,其化学式为C7H10O5.下列关于莽草酸的说法中,不正确的是A.莽草酸是由碳、氢、氧三种元素组成的B.莽草酸可在氧气中完全燃烧生成CO2和H2OC.莽草酸中含有7个碳原子、10个氢原子和5个氧原子D.莽草酸的相对分子质量为1747.某反应的微观示意图如下,下列说法正确的是A.生成物一定是混合物B.化学反应前后原子的种类不变C.该反应的生成物一定是氧化物D.反应后各元素化合价不变8.一定条件下,甲、乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示,下列说法正确的是()A.丁一定是该反应的催化剂B.该反应中甲、丙的质量比为 1∶5C.该反应中乙、丙的质量比为 2∶5D.该反应一定是分解反应9.某反应过程的微观示意图如图。
九年级化学上册第五单元化学方程式知识点总结归纳完整版(带答案)

九年级化学上册第五单元化学方程式知识点总结归纳完整版单选题1、兴趣小组的同学利用下图装置,探究化学反应前后物质的质量是否守恒。
应选用的药品是A.铁粉和稀盐酸液体中B.硝酸钾晶体和水C.碳酸钡粉末和稀硫酸D.铜粉和硝酸银溶液答案:D分析:由题意,如图所示用敞口容器探究质量守恒,应选择反应物和生成物均无气体的化学反应。
A、铁粉和稀盐酸反应生成氢气,烧杯敞口,气体逸出反应体系,A选项药品不能用来探究化学反应前后物质的质量是否守恒,不符合题意;B、硝酸钾晶体和水不会发生反应,B选项没有发生化学反应,药品不能用来探究化学反应前后物质的质量是否守恒,不符合题意;C、碳酸钡和稀硫酸反应生成二氧化碳,烧杯敞口,气体逸出反应体系,C选项药品不能用来探究化学反应前后物质的质量是否守恒,不符合题意;D、铜粉和硝酸银溶液发生置换反应生成硝酸铜和银,无气体生成,D选项药品能用来探究化学反应前后物质的质量是否守恒,符合题意。
故选D。
小提示:本题考查探究化学反应前后物质的质量是否守恒的药品的选择,所选择的药品要能够发生化学反应,再结合实验装置进行分析,若为敞口容器的装置,应选择反应物和生成物均无气体的化学反应,否则因为空气的参与或者气体生成逸散出容器,就不能探究化学反应前后物质的质量是否守恒。
2、在一个密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法正确的是C .X 的值为13D .乙、丁变化的质量比为1:2答案:C 分析:反应前物质的总质量为30+5+10+0=45,反应后物质的总质量为12+X+10+10=45,则X=13。
A 、甲的质量减少为反应物;乙质量增加为生成物;丙质量不变为催化剂或不参与反应;丁质量增加为生成物;故是甲生成乙和丁,为分解反应,错误;B 、丙的质量没变,可能是催化剂,错误;C 、X 的值为13,正确;D 、乙、丁变化的质量比为(13-5):(10-0)=4:5,错误。
人教版初中九年级化学上册第五单元《化学方程式》知识点总结(含答案解析)(1)
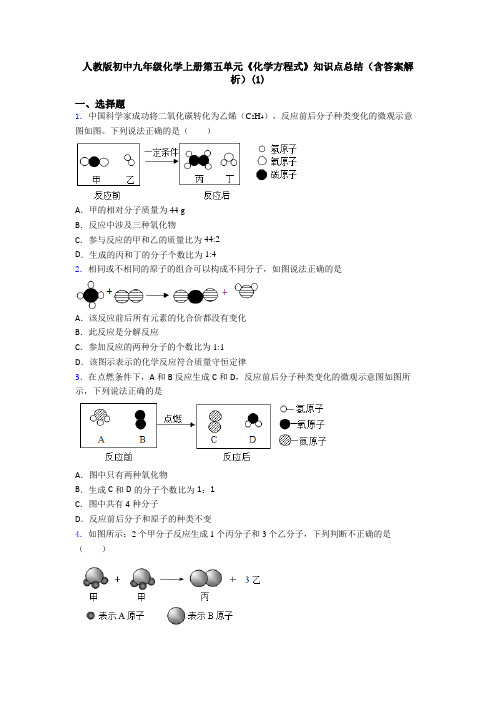
人教版初中九年级化学上册第五单元《化学方程式》知识点总结(含答案解析)(1)一、选择题1.中国科学家成功将二氧化碳转化为乙烯(C2H4),反应前后分子种类变化的微观示意图如图。
下列说法正确的是()A.甲的相对分子质量为44 gB.反应中涉及三种氧化物C.参与反应的甲和乙的质量比为44:2D.生成的丙和丁的分子个数比为1:42.相同或不相同的原子的组合可以构成不同分子,如图说法正确的是A.该反应前后所有元素的化合价都没有变化B.此反应是分解反应C.参加反应的两种分子的个数比为1:1D.该图示表示的化学反应符合质量守恒定律3.在点燃条件下,A和B反应生成C和D,反应前后分子种类变化的微观示意图如图所示,下列说法正确的是A.图中只有两种氧化物B.生成C和D的分子个数比为1:1C.图中共有4种分子D.反应前后分子和原子的种类不变4.如图所示:2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是()A .根据质量守恒定律可推知,1个乙分子中含有2个A 原子B .该反应前后一定有元素的化合价发生了改变C .该反应中甲、乙和丙的分子个数比是2:2:3D .该反应属于分解反应5.在一密闭容器中有A 、B 、C 、D 四种物质,一定条件下充分反应测得反应前后各物质的质量如表所示。
则下列说法中正确的是 物质 A B C D 反应前的质量/g 18 18 5 3 反应后的质量/g30待测9A .该反应一定是化合反应B .C 物质在该反应中一定是催化剂 C .反应后待测的C 物质的质量为0gD .参加反应的A 、B 、D 三种物质的质量比为3:2:16.当空气中受到 SO 2污染时,可通过飞机喷洒石灰石粉末,使空气中 SO 2含量降低,该过程发生反应为:32422CaCO +2SO +X=2CaSO +2CO ,则 X 的化学式为( ) A .CaO B .O 3C .O 2D .CO7.用和分别代表两种不同单质A 2和B 2的分子,A 2和B 2在一定条件下发生化学反应生成新物质X ,微观过程如下图所示。
人教九年级化学上册期末复习:初三1-8单元化学方程式(含答案)

上学期初三化学期末复习——1-8单元化学方程式一、气体的实验室制法和工业制法1.过氧化氢与二氧化锰混合(二氧化锰起作用)2.加热氯酸钾与二氧化锰混合物(加热一段时间才产生O2)3.加热高锰酸钾(加热一段时间才产生O2,塞一团棉花)4.实验室用和制取CO2(现象:产生大量,固体逐渐。
所制得的CO2会带来的杂质气体除了水蒸气,还有)5.实验室用锌粒和稀硫酸制氢气(现象:产生大量,固体逐渐)6.工业高温煅烧大理石制取CO2(《石灰吟》所包含的反应)二、物质的燃烧(物质与氧气的反应)7.红磷在空气中燃烧(测定空气中氧气含量的反应,现象:发光,生成)8.硫燃烧(现象:在空气中色火焰,在氧气中色火焰,生成气味的气体)9.铁丝在氧气中燃烧(现象:火星四射,剧烈燃烧,生成色固体)10.镁条燃烧(现象:发出耀眼的,生成色固体)11.铝在氧气中燃烧(铝在常温下也和O2反应,形成致密的)12.铜在空气中加热(紫红色的固体变色)13.木炭不充分燃烧(当碳和氧气质量比为3:4时,则生成CO)14.木炭氧气中充分燃烧(现象:发出光。
当碳和氧气质量比为3:8时,则生成CO2)15.CO的燃烧(现象:产生色火焰,CO作为尾气时可以用燃着的酒精灯烧掉)16.氢气燃烧(爆炸)(现象:产生色火焰,罩在火焰上方干冷烧杯内壁有)17.甲烷的燃烧(天然气)(现象:产生色火焰)18.乙醇的燃烧(乙醇俗称)三、还原反应(三大还原剂是,它们在反应中发生氧化反应)19.木炭还原氧化铜(现象:色的固体变成色,澄清石灰水变)20.木炭还原氧化铁21.CO还原氧化铜(先通一会CO,才加热,防止)22.CO还原氧化铁(现象:色的固体变成色,澄清石灰水变)23.CO还原四氧化三铁(此反应属于置换反应吗?)24.氢气还原氧化铜(现象:黑色的固体变成色,试管内壁有)25.氢气还原氧化铁26.木炭还原CO2(此反应热量,记住是CO2转化为CO的方法)四、金属与溶液的反应(均属于反应)27.锌与稀盐酸(现象:固体逐渐,产生)28.镁与稀硫酸(此反应热量)29.镁与稀盐酸(此反应热量)30.铁和稀硫酸(所得溶液呈色)31.铁和稀盐酸(所得溶液呈色)32.铝和稀硫酸33.铝和稀盐酸34.铜片投入硝酸银溶液中(铜表面出现色固体,溶液由色变色)35.铁钉投入硫酸铜溶液中(铁表面出现色固体,溶液由色变色)36.铝片投入硫酸铜溶液中(铝表面出现色固体,溶液由色变色)37.铝片投入硝酸银溶液中五、要掌握的其它反应38.二氧化碳通入澄清石灰水(检验二氧化碳)(生成色沉淀)39.二氧化碳和水反应(将CO2通入到紫色石蕊溶液中,溶液变色)40.碳酸分解(将通了CO2的石蕊溶液加热,溶液由色变回色)41.水通电分解(负极放出,正极放出,体积比为)42.生石灰(CaO)与水反应(此反应热量。
人教版九年级化学上册第五单元 化学方程式章节练习试题(含答案解析版)

九年级化学上册第五单元化学方程式章节练习考试时间:90分钟;命题人:化学教研组考生注意:1、本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I卷(选择题 30分)一、单选题(10小题,每小题3分,共计30分)1、将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:下列有关说法正确的是A.x=3.2 B.该反应属于分解反应C.反应中a与b的质量比为3:7 D.d一定是催化剂2、下列图像能正确反映对应变化关系的是A.加热一定质量的氯酸钾和二氧化锰的混合物B .在某一密闭装置内点燃红磷C .一定量的镁在过量的氧气中充分燃烧D .将水通电电解一段时间3、硝酸铅(Pb(NO 3)2)时受热分解的化学方程式32222Pb NO 2PbO+xNO +O ↑加热(),则x 为A .2B .3C .4D .54、下列化学方程式书写完全正确的是A .23Fe+2O 点燃 34Fe OB .44Al+CuSO =AlSO +CuC .322Fe+6HCl=2FeCl +3H ↑D .322443Ba(NO )+H SO =BaSO +HNO ↓5、北京冬奥会火种灯的火种燃料为丙烷。
丙烷燃烧前后分子种类变化微观示意图如下、下列说法不.正确..的是A.乙为单质B.丙的相对分子质量为44C.生成丙与丁的分子个数比为3:4D.丙烷由3个碳原子、8个氢原子构成6、化学反应前后,肯定没有变化的是①原子个数②元素种类③分子个数④物质种类⑤物质的总质量A.①②③④B.①②⑤C.①②D.②③⑤7、已知2A+3B=C+3D,用足量的A和49 g B恰好完全反应,生成57 g C和1 g D,若B的相对分子质量为98,则A的相对分子质量为A.16 B.27 C.44 D.548、枯茗醛(C10H12O)是一种食用香料。
人教版九年级化学上册第五单元《化学方程式》测试题(含答案)
人教版九年级化学上册第五单元《化学方程式》测试题(含答案)相对原子质量:H-1;C-12;N-14;O-16;Ca-40。
一、本大题包括12小题,每小题1分,共12分。
每小题的4个备选答案中只有一个答案符合题意。
1、在化学变化前后可能发生改变的是()A.分子种类 B.分子个数 C.元素种类D.原子种类2、纯净物M加热可分解为NH3、H2O和CO2,根据这一实验事实推断M的化学式可能是()A.Na2CO3 B.NaHCO3C.(NH4)2SO4D.(NH4)2CO33、下列化学方程式书写正确的是()A.4P+5O22P2O5 B.2H2O2═2H2O+O2C.S+O2↑SO2 D.Fe+O24O3Fe4、质量守恒定律是自然界的基本规律之一。
下列装置及实验(天平未画出)能用来验证质量守恒定律的是()5、香烟烟雾中有一种强致癌物叫苯并芘,其完全燃烧的方程式X+23O220CO2+6H2O,则苯并芘的化学式为()A.C20H12 B.C20H6C.C20H12O2D.C20H6O6、在一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得反应前后各物质的质量如图所示,下列说法不正确的是()A.x=4B.丙可能为该反应的催化剂C.该反应中,乙、丁的质量变化之比为7:5D.该反应中,甲、乙的质量变化之比为1:47、制备过氧乙酸过程发生反应的微观示意图如图所示,下列说法错误的是()A.过氧乙酸的相对分子质量为76B.物质乙和物质丁中氧元素的化合价相同C.过氧乙酸中,氧元素的质量分数最大D.该反应说明原子在化学反应中不可以再分8、从化学方程式S+O2SO2中无法获得的信息是()A.反应物和生成物是什么 B.参加反应的硫和氧气的质量比C.化学反应速率的快慢 D.反应发生所需要的条件9、下列对质量守恒定律的理解和应用中,正确的是()A.化学反应前后原子的种类、数目和质量不变,所以化学反应遵循质量守恒定律B.10g冰加热融化变成10g水,遵循质量守恒定律C.氢气燃烧时,参加反应的氢气和氧气的体积,一定等于生成水的体积D.蜡烛燃烧后质量减少了,该反应不遵循质量守恒定律10、在A+B=C+D的反应中,9.8gA和8gB完全反应生成14.2gC,同时得到D的质量为()A.1.8g B.3.6g C.7.2g D.14.4g11、分析推理是化学学习的常用方法,下列分析推理正确的是()A.单质是由同种元素组成的,所以同种元素组成的物质一定属于单质B.某物质燃烧后生成CO2和H2O,所以该物质一定含有C、H、O元素C.氧化物中都含有氧元素,所以含有氧元素的化合物都是氧化物D.纯净物都有固定的组成,所以每种纯净物都只能用一个化学式表示12、下列图象能正确反映其对应操作中各量变化关系的是()A.用等质量、等浓度的过氧化氢溶液分别制取氧气B.加热一定量的高锰酸钾固体C.密闭容器中用红磷测定空气中氧气含量D.将水通电,电解一段时间二、本大题包括5小题,共28分13、按要求完成下列问题:(1)配平下列化学方程式①Al+Fe3O4Fe+ Al2O3。
九年级化学上册第五单元化学方程式经典大题例题(带答案)
九年级化学上册第五单元化学方程式经典大题例题单选题1、兴趣小组的同学利用下图装置,探究化学反应前后物质的质量是否守恒。
应选用的药品是A .铁粉和稀盐酸液体中B .硝酸钾晶体和水C .碳酸钡粉末和稀硫酸D .铜粉和硝酸银溶液答案:D分析:由题意,如图所示用敞口容器探究质量守恒,应选择反应物和生成物均无气体的化学反应。
A 、铁粉和稀盐酸反应生成氢气,烧杯敞口,气体逸出反应体系,A 选项药品不能用来探究化学反应前后物质的质量是否守恒,不符合题意;B 、硝酸钾晶体和水不会发生反应,B 选项没有发生化学反应,药品不能用来探究化学反应前后物质的质量是否守恒,不符合题意;C 、碳酸钡和稀硫酸反应生成二氧化碳,烧杯敞口,气体逸出反应体系,C 选项药品不能用来探究化学反应前后物质的质量是否守恒,不符合题意;D 、铜粉和硝酸银溶液发生置换反应生成硝酸铜和银,无气体生成,D 选项药品能用来探究化学反应前后物质的质量是否守恒,符合题意。
故选D 。
小提示:本题考查探究化学反应前后物质的质量是否守恒的药品的选择,所选择的药品要能够发生化学反应,再结合实验装置进行分析,若为敞口容器的装置,应选择反应物和生成物均无气体的化学反应,否则因为空气的参与或者气体生成逸散出容器,就不能探究化学反应前后物质的质量是否守恒。
2、下列关于2CO+O 2点燃2CO 2的说法不正确...的是( ) A .表示一氧化碳与氧气在点燃条件下反应生成二氧化碳B.参加反应的一氧化碳与氧气的质量比为7:8C.反应前后碳原子、氧原子的个数均保持不变D.参加反应的一氧化碳与生成的二氧化碳的分子个数比为1:1答案:BA、该反应可表示一氧化碳与氧气在点燃条件下反应生成二氧化碳,故选项说法正确;B、参加反应的一氧化碳与氧气的质量比为(28×2):32=7:4,故选项说法错误;C、化学反应前后碳原子、氧原子的个数均保持不变,故选项说法正确;D、微观上,点燃条件下,每2个一氧化碳分子和1个氧分子反应生成2个二氧化碳分子,则参加反应的一氧化碳与生成的二氧化碳的分子个数比为2:2=1:1,故选项说法正确。
人教版九年级化学上册第五单元-化学方程式专题训练试卷(解析版含答案)精选全文
可编辑修改精选全文完整版九年级化学上册第五单元 化学方程式专题训练考试时间:90分钟;命题人:化学教研组考生注意:1、本卷分第I 卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I 卷(选择题 30分)一、单选题(10小题,每小题3分,共计30分)1、化学方程式书写错误的是A .铁丝在氧气中燃烧:4Fe +3O 2点燃2Fe 2O 3B .无水硫酸铜检验水:CuSO 4+5H 2O=CuSO 4·5H 2OC .甲烷燃烧:CH 4+2O 2点燃CO 2+2H 2OD .用氯酸钾制取氧气:322MnO 2KCl Δ2KClO +3O2、将15gA 、10gB 、9gC 的固体混合物充分加热,使其完全反应。
待反应结束时,测得A 剩余3g ,B 增至25g ,C 的质量为零,同时生成了气体D ,则D 的质量为A .6gB .9gC .16gD .34g3、甲和乙在点燃条件下反应生成丙和丁。
四种物质微观结构如下图(其中“”代表氢原子,“”代表碳原子,“”代表氧原子)。
则下列叙述不正确的是A.乙分子中碳、氢、氧原子个数比为2:6:1B.生成物均为氧化物C.在该反应中,甲和乙的分子个数比为3:1D.在该反应中,生成物丙和丁的质量比为2:34、将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:下列有关说法正确的是A.x=3.2 B.该反应属于分解反应C.反应中a与b的质量比为3:7 D.d一定是催化剂5、下列是两个关于水的实验。
下列说法正确的是A.实验1,试管a中得到的气体能供给人体呼吸B.实验1,反应前后原子的种类、个数均未改变C.实验1和实验2,是同一个反应D.实验2,水分子空隙没有变化6、下列推理合理的是A.蜡烛燃烧生成CO2和H2O,所以蜡烛的组成中一定含有碳元素和氢元素B.氧气的化学性质比较活泼,所以氧气能与所有的物质反应C.由同种分子构成的物质一定是纯净物,所以纯净物一定是由同种分子构成的D.单质是由同种元素组成的物质,所以由同种元素组成的物质一定是单质7、如图为某反应的微观示意图,“”和“”表示两种不同的原子,下列说法不正确...的是A.参加反应的两种分子个数比为2:1 B.生成物是混合物C.反应前后分子种类改变D.反应前后原子种类不变8、下列关于N2 + O2放电2NO的说法不正确...的是A.表示氮气和氧气在放电条件下反应生成一氧化氮B.反应前后分子的数目不变C.反应前后原子的种类、数目均不变D.参加反应的氮气与生成的一氧化氮的质量比为14∶154Ag+2H S+O=2X+2H O。
九年级化学上册第五单元化学方程式知识汇总大全(带答案)
九年级化学上册第五单元化学方程式知识汇总大全单选题1、根据化学方程式不能获得的信息有( ) A .化学反应发生的条件B .化学反应的快慢C .反应物和生成物的质量比D .化学反应的反应物和生成物 答案:B分析:根据化学反应方程式可知反应物、生成物是什么,反应在什么条件下发生,还能反映出反应体系中各物质的质量关系和微观粒子的数量关系。
根据化学方程式可以获得化学反应发生的条件、反应物和生成物的质量比和化学反应的反应物和生成物,但是无法获得化学反应的快慢。
故选B 。
2、甲酸(HCOOH )具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:下列说法正确的是A .甲酸分子中氢、氧原子个数比为1:2B .乙中碳、氧元素质量比为1:2C .46g 甲酸中氢元素质量为2gD .生成甲与乙的分子个数比为2:1 答案:C分析:由微观示意图可知,反应的化学方程式为HCOOH一定条件H 2↑+CO 2↑。
A 、甲酸化学式为HCOOH ,甲酸分子中氢、氧原子个数比为2:2=1:1,故A 不正确;B 、乙是CO 2,乙中碳、氧元素质量比为12:(2×16)=3:8,故B 不正确;C 、甲酸化学式为HCOOH ,46g 甲酸中氢元素质量为46g ×(1×21×2+12+2×16×100%)=2g,故C 正确;D 、反应的化学方程式为HCOOH一定条件H 2↑+CO 2↑,则生成甲与乙的分子个数比为1:1,故D 不正确。
故选C 。
3、下图是反映某个化学反应里物质质量与时间的变化关系,下列对此变化的描述中,正确的是A .充分反应后,乙+丙=甲的质量B .物质甲的相对分子质量大于乙C .此化学反应中,不遵守质量守恒定律D .反应了此化学反应是分解反应 答案:DA 、根据图示知,参加反应的丙物质的质量等于生成的甲和乙物质质量之和,错误;B 、无法比较甲和乙的相对分子质量大小,错误;C 、一切化学反应都遵守质量守恒定律,错误;D 、甲乙为生成物,丙为反应物,故反应是“一变多”,该反应为分解反应,正确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
九年级上册化学化学方程式归纳练习及答案
集团文件版本号:(M928-T898-M248-WU2669-I2896-DQ586-M1988) 九年级上册化学化学方程式归纳练习及答案 一、各物质在氧气中燃烧方程式及现象 1、磷在空气中燃烧: (验证空气含量,书P27) 现象: 2、碳在氧气中燃烧 现象: 3、硫在 氧气中燃烧 (比较其在空气中燃烧的现象) 现象: 4、铁在 氧气中燃烧 (注:铁在空气中不燃烧) 现象: 5、镁在 氧气中燃烧 现象: 二、实验室制氧气原理:(氧气的物理性质、收集方法、检验、验满) 6、 过氧化氢溶液制氧气: 7、加热氯酸钾制氧气: 8、加热高锰酸钾制氧气:(装置、操作步骤及注意事项 书P37) 三、水的电解(氢气的物理性质、收集方法、验纯及用途,书P79-80)
9、 结论:1、 2、 与正极相连的气体为_______,与负极相连的气体为_______,正负极生成气体的体积比为__________,可用八个字概括_______________________ 四、碳在空气中燃烧(碳几种单质的物理性质及用途,碳的化学性质) 10、 (氧气不足) (氧气充足) 五、碳的还原性 11、碳还原氧化铜: 现象: 12、碳还原氧化铁 13、二氧化碳通入炽热的碳层 六、二氧化碳(物理性质、制取原料、收集方法、验证、验满、注意事项) 14、实验室制法: 15、工业制法: 16、二氧化碳通入紫色石蕊溶液,溶液变红: 17、加热变红的溶液又变红(碳酸的不稳定性) 18、检验CO2:
现象: 七、一氧化碳(物理性质、化学性质) 19、可燃性(火焰呈______色): 20、还原性(还原氧化铁) 21、还原氧化铜: 22、甲烷燃烧 : 23、氢气在空气中燃烧: 24、乙醇在空气中燃烧: 25、实验室制氢气: 答案 一、各物质在氧气中燃烧方程式及现象
1、4P + 5O2 2P2 O5 (验证空气含量,书P27) 现象:
2、C + O2 CO2
现象:
3、S + O2 SO2 (比较其在空气中燃烧的现象) 现象: 4、3Fe + 2O2 Fe3O4 (注:铁在空气中不燃烧) 现象:
5、2Mg + O2 2MgO 现象: 二、实验室制氧气原理:(氧气的物理性质、收集方法、检验、验满)
6、 2H 2O 2 2H 2O+O 2↑ 7、2KClO3 2KCl + 3O2 ↑ 8、2KMnO4 K2 MnO4 + MnO2 + O2 ↑ (装置、操作步骤及注意事项 书P34-35) 三、水的电解(氢气的物理性质、收集方法、验纯及用途,书P46-47)
9、2H2 O 2H2 ↑+ O2↑ 结论:1、 2、 与正极相连的气体为_______,与负极相连的气体为_______,正负极生成气体的体积比为__________,可用八个字概括_______________________ 四、碳在空气中燃烧(碳几种单质的物理性质及用途,碳的化学性质) 10、2C + O2 2CO(氧气不足) C + O2 CO2 (氧气充足) 五、碳的还原性
11、C+ 2CuO 2Cu + CO2 ↑ 现象:
12、3C+ 2Fe2O3 4Fe + 3CO2↑ 13、C+ CO2 2CO 六、二氧化碳(物理性质、制取原料、收集方法、验证、验满、注意事项) 14、CaCO 3+ 2HCl === CaCl2 + H2 O + CO2↑(实验室制法)
15、CaCO3 CaO + CO2 ↑ 16、CO2 + H2O === H2 CO3(碳酸可以使紫色石蕊溶液变_________) 17、H2 CO3 === H2 O + CO2↑(碳酸的不稳定性) 18、Ca(OH) 2 + CO2 ==== CaCO 3↓+ H2 O(检验CO2) 现象: 七、一氧化碳(物理性质、化学性质)
19、CO + O2 2CO2(火焰呈______色) 20、CO + Fe2 O3 2Fe + 3CO2 21、CO+ CuO Cu + CO2
22、CH4 + 2O2 CO2 + 2H2 O 23、2H2 + O2 2H2 O
24、C2 H5OH + 3O2 2CO2 + 3H2 O 25、Zn+H2SO4 === ZnSO4+H2↑(实验室制氢气) 九年级上册化学方程式总结 化 学 反 应 化 学 方 程 式 反应现象 反应现象 反应 类型 1 红磷在空气中燃烧 4 P + 5 O2 点燃 2 P2O5 红磷在空气中燃烧,产生大量白烟 化
合 反 应 2 硫在空气中燃烧 S + O2 点燃 SO2 硫在空气中燃烧淡蓝色火焰,有刺激性气味的气体 硫在氧气中燃烧蓝紫色火焰,有刺
激性气味的气体。
3 铝在氧气中燃烧 4 Al + 3 O2 点燃 2 Al2O3 铝在空气中不能燃烧 在纯氧中可燃,现象是剧烈燃烧,
发出白光,生成白色固体(Al2O3)
4 碳在空气中燃烧(充分) C + O2 点燃 CO2 碳在氧气中燃烧发出白光,没有火
焰 在空气中发出红光 5 铁在氧气中燃烧 3 Fe + 2 O2 点燃 Fe3O4 铁在空气中不能燃烧,而铁粉可以在空气中燃烧。 铁在氧气中剧烈燃烧,火星四射;生成黑色固体;放出大量的热
6 镁在空气中燃烧 2 Mg + O2 点燃 2 MgO 发出耀眼的白光,放出热量,生成白色固体 剧烈燃烧,发出耀眼白光,生成白烟,放出大量的热 7 氢气在空气中燃烧 2 H2 + O2点燃2 H2O 氢气在空气中燃烧淡蓝色火焰; 氢气在氧气中燃烧与空气中相同
8 碳在空气中不充分燃烧 2 C + O2 ( 不足 ) 点燃2 CO 在空气中保持红热 发出白光并且发热,碳消失,生成无色无味的气体,将它导出,发现可以燃烧,生成无色无味的气体,能使澄清石灰水变浑浊 9 一氧化碳在空气中燃烧 2 CO + O2点燃 2 CO2 一氧化碳在空气中燃烧蓝色火焰 在氧气中燃烧与空气中相同。
10 生石灰化成熟石灰 CaO+H2O ==Ca(OH)2 放出大量的热,有白色沉淀(氢氧化钙)生成 11 二氧化碳溶于水 CO2 + H2O === H2CO3 水变酸性,生成碳酸,颜色没变化,
基本上没什么现象,就是冒气泡,应用于常喝的汽水 12 过氧化氢分解制氧气 2 H2O2 MnO2 2 H2O + O2↑ 产生大量的气泡,产生的气体能使带火星的木条复燃 分解反应 13 实验室用高锰酸钾制氧气 2KMnO4 △ K2MnO4+ MnO2+ O2↑ 高锰酸钾制造氧气是最容易控制并且最安全的。 产生大量的气泡,产生的气体能使带火星的木条复燃 分 解 反 应 14 水通电分解 2 H2O通电2 H2↑+ O2↑ 正极氧气,负极氢气
15 氧化汞受热分解 2 HgO △ 2 Hg + O2↑ 生成流体状汞呈圆珠状,空气中极易挥发成汞蒸气,并释放氧气 16 氯酸钾分解制氧气 2 KClO3 MnO2 2 KCl + 3 O2↑ 用集气法收集氧气,发现集气瓶中的水被排出,原因是:氧气很难溶于水 把带有火星的木条深入集气瓶中,观察到木条复燃
17 用石灰石烧生石灰 CaCO3高温 CaO + CO2↑ 18 碳酸易分解 H2CO3==== CO2 ↑+ H2O 产生气泡 如果滴了紫色石蕊指示剂的话 溶液从红色变成紫色 19 氢气还原氧化铜 H2 + CuO △ Cu + H2O 黑色粉末逐渐变成光亮的红色物质,同时试管口有水滴生成 置 换 20 碳还原氧化铜 C + 2 CuO高温 2 Cu + CO2↑ 取氧化铜和研好的木炭粉,按其质量10:1的比放在研钵中充分研磨,使之混合均匀,装入硬质试管并铺开(如图),再用酒精喷灯(或大火焰酒精灯)加热 数分钟后,即可看到石灰水变浑浊,而原来的黑色粉末混合物基本变为红色。 反 应
21 碳还原氧化铁 3 C + 2 Fe2O3 高温 4 Fe + 3 CO2 ↑ 如果把生成的气体通入澄清石灰水,则会出现混浊 红棕色固体逐渐减少 22 铁和硫酸铜反应 Fe + CuSO4=FeSO4 + Cu 铁溶解,有红色物质生成,溶液由蓝色变为浅绿色, 23 镁和盐酸反应 Mg + 2 HCl == MgCl2 + H2↑ 发生剧烈反应,白色固体溶解,在固体表面生成大量气泡 得到无色溶液
24 镁和硫酸反应 Mg + H2SO4 ==MgSO4 + H2↑ 有气泡产生 溶液颜色不变 25 锌和盐酸反应 Zn + 2 HCl == ZnCl2 + H2↑ 金属较快溶解,并放出气体 26 实验室制氢气 Zn + H2SO4==ZnSO4 + H2↑ 金属较快溶解,并放出气体 27 铁和盐酸反应 Fe + 2 HCl==FeCl2 + H2↑ 金属逐渐溶解 产生少量气体 溶液由无色变为浅绿色 28 铁和硫酸反应 Fe + H2SO4 == FeSO4 + H2↑ 金属逐渐溶解 产生少量气体 溶液由无色变为浅绿色 置 换 反 应 29 铝和硫酸铜反应 2 A l + 3 CuSO4 == Al2(SO4)3 + 3Cu 蓝色的硫酸铜溶液会变色成为无色
的硫酸铝。 30 铜和硝酸银反应 Cu + 2 AgNO3 == Cu(NO4)2 + 2 Ag 铜表面有着一层银白色固体, 溶液由无色渐渐变为蓝色
31 盐酸和氧化铜反应 2HCl + CuO △ Cu Cl2+ H2O 黑色粉末逐渐溶解 溶液逐渐变成蓝色 32 硫酸铜和氢氧化钠反应 CuSO4+2NaOH== Cu(OH)2↓+ Na2SO4 生成蓝色沉淀 溶液变无色 33 实验室制二氧化碳 CaCO3+ 2HCl == CaCl2 + CO2↑+ H2O 白色固体减少 生成一种能使澄清石灰水变混浊的气体 复 分 解 反 应
34 铁锈溶解在盐酸中 Fe2O3+6HCl==2FeCl3+3H2O 铁锈逐渐溶解 溶液颜色由无色变黄。
35 三氧化二铁与硫酸反应 Fe2O3+3H2SO4==Fe2(SO4)3+3H2O 铁锈逐渐溶解 溶液颜色由无色变黄。
