ch8-3
AI731-S使用手册

0.6±0.1 mA (0~50)℃
宽温型(-20~70)℃ (-40~70)℃
10%RH~90%RH,无凝露 5%RH~95%RH,无凝露
二线制接法时需要考虑引线电阻,不保证上述精度指标。
1
AI731-S 使用手册
3 使用说明
3.1 LED 指示灯说明
LED 指示灯
意义 状态
通道
I+
V+ CH1
V-
I-
I+
V+ CH2
V-
I-
I+
V+ CH3
V-
I-
I+
V+ CH4
V-
I-
I+
V+ CH5
V-
I-
I+
V+ CH6
V-
I-
I+
V+ CH7
V-
I-
I+
V+ CH8
V-
I不接线
4
AI731-S 使用手册
3.4 基座选型
与 AI731-S 模块匹配的基座有:I/O 模块基座 MB731-S、冗余 I/O 模块基座 MB732-S、I/O 模块 端子转接基座 MB743-S、冗余 I/O 模块端子转接基座 MB744-S,用户可根据需求选择不同的基座。
当现场信号不允许直接连入系统柜时,应选用端子转接基座,并配置相应的端子板。与转接基
座匹配的端子板有:转接端子板 TU751-S 等。
表 3-3 AI731-S 匹配基座/端子板选型表
信号连接要求 直接连接
端子转接
模块工作方式 单模块 冗余 单模块 冗余
数据结构第八章_排序

49 38 65 97 76
三趟排序:4 13 27 38 48 49 55 65 76 97
算法描述
#define T 3 int d[]={5,3,1};
例 13 48 97 55 76 4 13 49 27 38 65 49 27 38 65 48 97 55 76 4 j j j
j
j
i
例 初始: 49 38 65 97 76 13 27 48 55 4 取d1=5 49 38 65 97 76 13 27 48 55 4 一趟分组:
一趟排序:13 27 48 55 4 取d2=3 13 27 48 55 4 二趟分组:
49 38 65 97 76 49 38 65 97 76
二趟排序:13 4 48 38 27 49 55 65 97 76 取d3=1 13 27 48 55 4 三趟分组:
初始时令i=s,j=t
首先从j所指位置向前搜索第一个关键字小于x的记录,并和rp
交换 再从i所指位置起向后搜索,找到第一个关键字大于x的记录, 和rp交换 重复上述两步,直至i==j为止 再分别对两个子序列进行快速排序,直到每个子序列只含有 一个记录为止
快速排序演示
算法描述
算法评价
例
38 49 49 38 65 76 97 13 97 76 97 27 13 30 97 27 97 30 初 始 关 键 字
38 49 65 13 76 27 76 13 30 76 27 76 30 97 第 一 趟
38 49 13 65 27 65 13 30 65 27 65 30
38 13 49
时间复杂度
最好情况(每次总是选到中间值作枢轴)T(n)=O(nlog2n) 最坏情况(每次总是选到最小或最大元素作枢轴)
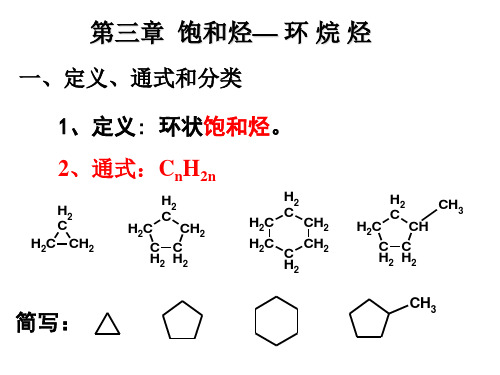
第三章 环烷烃
如何鉴别: 如何鉴别:
CH3-CH=CH2 CH3-CH2-CH3
褪褪 Br2/H2O
褪褪 KMnO4
×
褪褪
×
在强烈条件下,环烷烃也能被氧化。 在强烈条件下,环烷烃也能被氧化。 如:
OH
O
+ O2 (air)
环烷酸钴 140~180℃ ℃ 1-2.5MPa
+
氧化
HOOC
COOH
工业生产己二酸 锦纶-66单体 单体) (锦纶-66单体)
总之: 总之: 三元环的稳定性最小,最易开环; 三元环的稳定性最小,最易开环; 四元环的稳定性次之;也易开环; 四元环的稳定性次之;也易开环; 五元、六元环等,较稳定,不易开环。 五元、六元环等,较稳定,不易开环。 作业 : P73 二(4、5、6) 、 、 )
Ni + H2 200
+ 开环 加
Pt H2 300
CH3-CH2-CH2-CH2-CH3
(2)加成卤素 ) +
常温 Br2 CCl4
Br-CH2-CH2-CH2-Br
+ Br2
CCl4
Br-CH2-CH2-CH2-CH2-Br
棕红色褪去,用以鉴定环丙烷及环丁烷 鉴定环丙烷及环丁烷。 使Br2/CCl4棕红色褪去,用以鉴定环丙烷及环丁烷。
(3)加成卤化氢 )
+ HBr
CH3
CH3CH2CH2Br
+
HBr
CH3CHCH2CH3 Br
带有取代基的小环烷烃加成HX或 带有取代基的小环烷烃加成HX或Br2时,环 HX 的断裂是在取代基最多与最少的两个环碳原子 的断裂是在取代基最多与最少的两个环碳原子 加到含H多的碳上。( P67有错误 。(书 有错误!) 之间, 之间,且H加到含H多的碳上。(书P67有错误!)
高分子化学-第八章开环聚合

高 分 子 化 学
21
8.2 环醚的开环聚合
醇的影响
一些金属烷氧化物和氢氧化物引发的聚合反应体系中, 常加入适量的醇:溶解引发剂,形成均相聚合体系;促进 增长链阴离子与抗衡阳离子的离解,增加自由离子浓度, 加快聚合反应速度。 在醇的存在下,增长链可和醇之间发生如下交换反应:
开环聚合中,对环醚的研究比较详细,尤其是对三节 环和五节环环醚研究得最多。
高 分 子 化 学
9
8.1 开环聚合概述
按环的大小,环醚单体主要有下列几种:
CH2 CH2 O
CH2 CH CH3 O
CH2 CH2 O
CH2 O CH2 C
CH2Cl CH2Cl
环氧乙烷
8.1 开环聚合概述
环状单体的种类
环中含一个杂原子的环状单体有环醚、环硫化合物和 环亚胺等,含有两个杂原子的有环缩醛,含有一个杂原子 和一个羰基的有环酯,环酰胺等。
环醚
环中含有醚键-O-的环状化合物称为环醚;
三节环醚又称为环氧化合物或氧化烯,如环氧乙烷又 称为氧化乙烯,环氧丙烷又称为氧化丙烯;
高 分 子 化 学
17
8.2 环醚的开环聚合
环氧化合物的开环聚合
环氧化合物的阳离子开环聚合仅生成低相对分子质量的 产物,且副反应很多。 环氧化合物可以用醇盐、氢氧化物和负碳离子来引发聚 合,用碱引发聚合可制得端羟基聚醚,目前工业上采用。 环氧化合物的阴离子开环聚合是在二元醇或三元醇存在 下用醇盐和氢氧化物作引发剂来进行的。 醇(作为起始剂)通常用来溶解引发剂形成均相聚合体 系,同时能明显的提高聚合反应的速率,这可能是因为 均相体系增加了自由离子的浓度以及使紧密离子对转变 为松对的缘故。
第八讲 第四章 二烯烃 共轭体系 共振论(1)

越低,分子越稳定。
有 机
共振能:能量最低的极限结构与共振杂化体(分子的真实结构)之间的 能差。共振能越大说明该分子比最稳定的极限结构越稳定。
化
常用CH2=CH-CH=CH2表示,与电子衍射测的事实不符。鲍林指出,
学 这些共振结构本身是不存在的,是假想的。因此,共振论是用假想的共振
结构去近似的描述真实物质的结构理论。
八 讲
CH2 CH CH2
CH2 CH Cl
CH2 CH O R
烯丙基碳正离子
氯乙烯
乙烯基醚
(9)
其电子离域方向如下:
CH2 CH CH2 CH2 CH Cl CH2 CH O R
有 4.3.3 超共轭
机
在C–H 键与 键直接相连的体系中也存在与 , -共轭体系类似的电
化 学
子离域现象。如图4-5所示:
丙二烯
1,2-丁二烯
其结构形式为: C C C C
(3)
CH3
CH2=CH-CH=CH2
CH2 C CH CH2
1,3-丁二烯(或丁二烯)
2-甲基-1,3-戊二烯(或异戊二烯)
4.1.2 二烯烃的命名
有
原则:系统命名与烯烃相似,不同之处在于:分子中含有两个双键,
机 化 学
用二烯代替烯,选择主链时必须包括两个双键在内,同时应标明两个双键 的位次。存在顺反异构时要逐个标明其构型。例如:
H
S-顺-1,3-丁二烯
H
CH2
CC
CH2
H
S-反-1,3-丁二烯
1, 3-环己二烯
或S-(Z)-1,3 -丁二烯 或S-(E)- 1,3-丁二烯
二环 [4.4.0]-1,9-癸二烯
《有机化学》(第四版)第三章-不饱和烃(习题答案)

第三章 不饱和烃思考题习题3.1 写出含有六个碳原子的烯烃和炔烃的构造异构体的构造式。
其中含有六个碳原子的烯烃,哪些有顺反异构?写出其顺反异构体的构型式(结构式)。
(P69)解:C 6H 12有13个构造异构体,其中4个有顺反异构体:CH 2=CHCH 2CH 2CH 2CH 3CH 3CH=CHCH 2CH 2CH 3CH 3CH 2CH=CHCH 2CH 3(Z,E)(Z,E)CH 2=CCH 2CH 2CH 3CH 3CH 2=CHCHCH 2CH 3CH 3CH 2=CHCH 2CHCH 3CH 3CH 3C=CHCH 2CH 3CH 3CH 3CH=CCH 2CH 3CH 3CH 3CH=CH 2CHCH 3CH 3(Z,E)(Z,E)CH 2=CHCCH 3CH 3CH 3CH 2=CCHCH 3CH 3CH 3CH 3C=CCH 3CH 3CH 3CH 2=CCH 2CH 3CH 2CH 3C 6H 10有7个构造异构体:CH CCH 2CH 2CH 2CH 3CH 3C CCH 2CH 2CH 3CH 3CH 2C CCH 2CH 3CH CCHCH 2CH 3CH 3CH CCH 2CHCH 3CH 3CH CC(CH 3)3CH 3C CCHCH 3CH 3习题3.2 用衍生物命名法或系统命名法命名以下各化合物:(P74)(1) (CH 3)2CHCH=CHCH(CH 3)2对称二异丙基乙烯 or 2,5-二甲基-3-己烯(2)(CH 3)2CHCH 2CH=CHCHCH 2CH 3CH 3123456782,6-二甲基-4-辛烯(3)CH 3CH 2C CCH 2CH 3123456二乙基乙炔 or 3-己炔(4)CH 3CH 2C(CH 3)2C CH 12345 3,3-二甲基-1-戊炔(5)CH 2=CHCH 2C CH 123451-戊烯-4-炔(6) HCC C=CCH=CH 2CH 2CH 2CH 3CH 2CH 2CH 31234563,4-二丙基-1,3-己二烯-5-炔(7)CH 3CH 32,3-二甲基环己烯(8)CH 3CH 35,6-二甲基-1,3-环己二烯习题3.3 用Z,E-命名法命名以下各化合物:(P74)(1) ↑C=CCH 2CH 3H ClBr↑(Z)-1-氯-1-溴-1-丁烯(2) ↓C=CF CH 3ClCH 3CH 2↑(E)-2-氟-3-氯-2-戊烯 (3) ↑C=CCH 2CH 3CH 2CH 2CH 3HCH 3↓ (E)-3-乙基-2-己烯(4) ↓C=CCH(CH 3)2CH 2CH 2CH 3CH 3H↑ (E)-3-异丙基-2-己烯习题3.4 完成以下反应式:(P83)(1) C 3H 7C CC 3H7C=C H C 3H 7HC 3H 7(2)3C 3H 7C CC 3H 7C=C H C 3H 7C 3H 7H(3)+ Br 2C=C HC 2H 5C 2H 5H25(4)CCHOOC COOH C=CHOOCBr Br COOH+ Br 2习题3.5 以下各组化合物分别与溴进行加成反应,指出每组中哪一个反应较快。
有机化学第1-4章 作业
第1章 绪论思考题1–1 典型有机物和典型无机物性质上有何不同?举例说明。
有机物易燃烧,不易溶于水,熔点和沸点都比较低。
如:有机物的熔点一般低于300℃,通常在40~300℃之间,而食盐的熔点为808℃。
思考题1–2 解释为何C=C 的键能比C –C 的键能的2倍要小。
σ键的键能比π键的键能大得多。
如C –C 键能为348 kJ·mol -1,而C=C 键能为610 kJ·mol -1,这表明π键的键能只有264 kJ·mol -1。
表1–1是一些常见共价键的键能。
思考题1–3 用δ+和δ-分别表示下列化合物的正负极(1)CH 3-NH 2 (2)CH 3-OHδ+ δ-δ+δ-思考题1–4 下列化合物哪些是极性化合物,哪些是非极性化合物? 极性化合物:CH 3Cl ,CH 3OH 非极性化合物:CCH 4, CCl 4, CH 3COCH 3思考题1–5 酸碱的质子理论中,下列化合物中哪些为酸?哪些为碱?哪些既为酸,又能为碱?酸:NH 4+, HI 碱:CN –既为酸,又能为碱:HS – ,H 2O思考题1–6 按酸碱的电子理论下列反应中,哪个反应物为酸,哪个反应物为碱? AlCl 3为酸,COCl 2为碱思考题1–7 下列化合物沸点由高到低的顺序为:CH 3(CH 2)4OHCH 3(CH 2)3CH 3(CH 3)4C abcd(CH 3)2CHCH 2CH 3c>a>d>b思考题1–8 矿物油(相对分子质量较大的烃的混合物)能溶于己烷,但不溶于乙醇和水,说明原因。
根据“相似相溶”原理,矿物油是非极性分子,而水和乙醇是极性分子,故不宜互溶。
习 题1.下列化合物各属于有机化合物还是无机化合物,分别属于哪一类别? 有机化合物:(1)(3)(4)(5)(6)(7)(8)(9)(10) 无机化合物:(2)2.写出甲烷CH 4分子的一个C –H 键均裂产生的自由基结构。
有机化学第十四章-二羰基化合物
有机化学第十四章-二羰 基化合物
第十四章 -二羰基化合物
(4):分子内酯缩合——成环
作业5(4)
成环
(3)酮与酯在乙醇钠作• 常用丙酮或其他甲基酮和酯缩合来合成 -二酮。
• 注意:与羟醛缩合反应不同(稀碱条件下,生成 ,-不饱和醛)。P286
(4)克诺文格尔缩合反应 *——制备,-不饱和酸
• 醛、酮还可以和-二羰基化合物(一般是丙二酸及 其衍生物),在弱碱(氨或胺)作用下缩合:
•烯醇负离子的共振式:
• 由于有烯醇式的存在,所以叫烯醇负离子;又由于亚 甲基上也带有负电荷,反应往往发生在此碳原子上, 所以这种负离子也称为碳负离子。
14.2 -二羰基化合物碳负离子的反应
主 要
• 碳负离子的反应类型: (1)与卤烷反应:即羰基碳原子的烷基化或烷基化反应 (2)与羰基化合物反应:常称为羰基化合物和-二羰基化合 物的缩合反应;当与酰卤或酸酐作用可得酰基化产物; (3)与, -不饱和羰基化合物的共轭加成反应或1,4-加成 反应.
与“三乙”可再 反应合成二酮!
(5) 与酰卤或酸酐作用——羰基亲核加成-消除反应
例:与酰氯的反应(得到酰基化产物)
NaH
•在 非 质 子 溶 液中进行
• 酮式分解得:-二酮
• 在合成上乙酰乙酸乙酯更多的用来合成 酮类。(合成羧酸时,常有酮式分解)
补充7
与酰卤作用
• 酮式分解得:-二酮
补充8
ch8 旋光异构
CH3
HO
H
COOH
CH3 H COOH
OH
因为这些操作不会改变物质构型。
不允许下列操作,因这些操作改变了物质的构型。 (1)不允许投影式在纸面上旋转90或270度 (2)不允许投影式离开纸面翻转 (3)不允许中心原子上的两个基团经一次或奇次交换
投影式旋转90° 得到另一个分子
COOH ≠
COOH
C6
判别手性分子的依据
具有对称面或对称中心——对称分子,为非手性分子 不具备任何对称因素——不对称分子,为手性分子 只含对称轴——非对称分子,为手性分子 手性分子具有光学活性
手性中心(chiral center):能引起分子具有手性的一个原子 或分子骨架的中心。最常见的手性中心为手性碳原子(chiral carbon),即连接四个不同原子或基团的碳原子。其他杂原子 也可形成手性中心。
C(CH3)3
CH3 C CH3 CH3
CH CH2 (C) (C) CCH HH
试比较下列基团的优先顺序:
NH2
CH2COOH
COCH3
第一节 旋光性与旋光度
一、物质的旋光性与化学结构的关系 1. 平面偏振光
光是一种电磁波,光波的振动方向与光的前进 方向垂直。
光束先进方向
光源
平面偏振光
普通光
Nicol prism
H OH 对调一次 HO
H
CH3
CH3
旋转90度 ≠
翻转
≠
H
H3C
COOH
CH3
H
OH
COOH
OH
如分子中有两个相邻的碳原子都需观察基团的空间 位置关系,可写成费歇尔投影式如下:
CHO
ch.8大气行星边界层
这种二级环流所造成地自由大气与边界层之间的 动量、热量和水汽交换比单纯的湍流扩散效应要有效 的多 。
在准地转涡旋流场中,由于湍流摩擦效应将会在埃克曼层中造成强迫的垂 直环流,它迭加在准地转水平环流之上,称之为二级环流。
研究边界层问题的思路方法
由于湍流运动的复杂性,相应的理论还不成 熟。因此,本章将采用半经验半理论的方法,首 先推导出平均运动方程组,再采用参数化方法模 拟湍流运动对平均运动的影响,从而研究行星边 界层中大气运动的具体规律。
§8.1 湍流平均动量方程,混合长理论
本节主要内容 1. 推导和建立平均动量方程。 2. 平均动量方程的特点和物理意义 3. 参数化与混合长理论。
此外,还可证明地表面上涡动应力与该层次中风速的平方成正比。
又由(8.45)式知:
2
u2
ln z
z0
u2
故有:
2
zx s
ln z
z0
su2
上式可改写为:
zx s sCDu 2
其中u常取为10m高度上的平均风速,而:
CD
2
ln
10 z0
2
(8.47) (8.48)
§8.2.2 埃克曼层
观测表明,中性层结下埃克曼层中湍涡的铅直尺度与离地表面高 度关系不大,可以假定涡动粘性系数 k 不随高度改变,因此有:
fv
1
p K x
2u z 2
fu 1 p K 2v
y
z 2
科氏力 水平气压梯度力 湍流粘性力
K Az
地转风
ug
1
