稀土荧光探针检测多巴胺及类似物
CdSeCdS量子点荧光探针检测Cu2+

第42卷第1期2023年2月沈㊀阳㊀理㊀工㊀大㊀学㊀学㊀报JournalofShenyangLigongUniversityVol 42No 1Feb 2023收稿日期:2022-05-24基金项目:广西自然科学基金项目(2019GXNSFAA185013)作者简介:汪登鹏(1995 )ꎬ男ꎬ硕士研究生ꎻ通信作者:高锋(1976 )ꎬ男ꎬ副教授ꎬ研究方向:稀土功能材料ꎮ文章编号:1003-1251(2023)01-0061-07CdSe/CdS量子点荧光探针检测Cu2+汪登鹏ꎬ高㊀锋ꎬ藤田澧久(广西大学资源环境与材料学院ꎬ南宁530000)摘㊀要:采用液相反应法在水介质中合成巯基乙酸封端的CdSe/CdS核壳结构量子点ꎬ基于Cu2+对量子点荧光的猝灭效应ꎬ以CdSe/CdS核壳量子点为荧光探针定量检测水溶液中Cu2+的浓度ꎮ研究结果表明:Cu2+的浓度为0.5~60μmol/L时ꎬCdSe/CdS量子点的荧光强度与Cu2+的浓度成良好的分段线性关系ꎬ浓度检测限为0.06μmol/Lꎻ该荧光探针对Cu2+的检测具有高选择性ꎻ对实际自来水样品中Cu2+的检测结果准确可靠ꎻ量子点的淬灭机理为动态淬灭ꎮ关㊀键㊀词:量子点ꎻ荧光淬灭ꎻCu2+检测ꎻ荧光探针中图分类号:O657.3文献标志码:ADOI:10.3969/j.issn.1003-1251.2023.01.010CdSe/CdSQuantumDotFluorescenceProbeforDetectionofCu2+WANGDengpengꎬGAOFengꎬFUJITAToyohisa(CollegeofResourcesEnvironmentandMaterialsꎬGuangxiUniversityꎬNanning530000ꎬChina)Abstract:CdSe/CdScore ̄shellquantumdots(QDs)withthioglycolicacidweresuccessful ̄lysynthesizedinaqueousmediumbyliquidphasereaction.BasedonthequenchingeffectofCu2+onQDfluorescenceꎬtheCdSe/CdScore ̄shellQDfluorescenceprobewasestablishedtoquantitativelyanalyzeCu2+inaqueoussolution.Theresultsshowthatthefluorescencein ̄tensityofCdSe/CdSQDshasagoodfractionallinearrelationshipwiththeconcentrationofCu2+intherangeof0.5~60μmol/LꎬandthedetectionlimitofCu2+is0.06μmol/L.ThefluorescenceprobehasahigherselectivityforCu2+thanothermetalionsꎬandthedetectionofCu2+inactualtapwatersamplesareaccurateandreliable.ThequenchingmechanismofQDsisdynamicquenching.Keywords:quantumdotꎻfluorescencequenchingꎻCu2+detectionꎻfluorescenceprobe㊀㊀河流和湖泊中的有毒重金属ꎬ如铬㊁镉㊁铜㊁铅和汞等ꎬ对动物㊁植物及人类的生存和健康影响很大[1]ꎮ其中铜是生物必需的元素之一ꎬ铜的缺乏会导致生物体的某些功能障碍ꎬ但过度摄入铜会导致铜中毒ꎬCu2+是铜最常见的价态ꎬ痕量Cu2+的测定具有重要的意义ꎮ目前检测Cu2+的方法主要有原子吸收光谱法[2]㊁原子荧光分光光度法[3]㊁电感耦合等离子体质谱法㊁电化学法[4]和荧光探针法[5]等ꎮ与荧光探针法相比较ꎬ其他几种方法虽然都具备一定的检测能力ꎬ但存在选择性差㊁灵敏度不高ꎬ或具有高选择性与灵敏度但设备复杂㊁昂贵ꎬ或存在样品制备程序复杂等问题ꎬ故其应用受到一定限制ꎮ荧光探针法最大的优势是其荧光响应迅速ꎬ此外还具有可视性和灵敏度高㊁检测重金属离子的选择性好㊁线性范围宽等优点ꎬ且该检测方法成本低㊁操作简单ꎮ上述诸多优势使得荧光探针成为当前研究的热点ꎬ并广泛应用于生物医学和分析化学等领域[6]ꎮ荧光探针大致可分为有机荧光探针和无机荧光探针ꎮ与有机荧光探针相比ꎬ无机量子点具有高荧光量子产率㊁荧光发射光谱可调㊁多种荧光颜色可视性的优点ꎮ用于检测Cu2+的量子点荧光探针较多ꎬ如CdX(X代表Te㊁Se㊁S)[7]㊁ZnS㊁C[8]和Au量子点[9]等ꎮ根据光谱特性ꎬ量子点荧光探针可分为基于单一荧光峰强度变化的普通荧光探针和基于两个发射峰相对强度的比率荧光探针[10]ꎻ根据结构ꎬ量子点可分为单晶体型㊁核壳型和混晶型等[11-13]ꎮ量子点检测Cu2+有Turn ̄offꎬOff ̄on两种方式ꎮ本文首先制备疏基乙酸封端的CdSe/CdS核壳型量子点ꎬ并通过X射线衍射仪(XRD)㊁透射电子显微镜(TEM)和光致发光光谱(PL)对其进行表征ꎻ然后以该量子点作为Cu2+浓度检测探针ꎬ基于Turn ̄off模式定量检测水溶液中Cu2+的浓度ꎻ最后使用该荧光探针对自来水样品中的Cu2+浓度进行检测ꎮ1㊀实验部分1.1㊀实验试剂疏基乙酸(TGA)㊁硼氢化钠(NaBH4)㊁氯化镉(CdCl2 2.5H2O)㊁硫化钠(Na2S 9H2O)和各种金属离子标准溶液(K+㊁Na+㊁Mg2+㊁Ba2+㊁Al3+㊁Mn2+㊁Fe3+㊁Ca2+㊁Pb2+㊁Cu2+㊁Zn2+㊁Cd2+)ꎬ均购自国药集团化学试剂有限公司ꎻ盐酸(HCl)㊁三羟甲基氨基甲烷(Tris)ꎬ购自阿拉丁试剂(上海)有限公司ꎮ所有试剂均为分析纯ꎮ1.2㊀实验仪器透射电子显微镜(F200X型ꎬ赛默飞世尔科技公司)ꎻ高灵敏稳瞬态荧光光谱仪(FL3C ̄111TC ̄SPC型ꎬ堀场仪器(上海)有限公司)ꎻX射线衍射仪(D/MAX2500V型ꎬ日本理学公司)ꎻ傅里叶红外光谱仪(NicoletiS20型ꎬ赛默飞世尔科技公司)ꎮ1.3㊀CdSe/CdS核壳量子点的制备采用液相反应法[14]制备CdSe/CdS核壳量子点ꎮ向三颈烧瓶中通氮气30min后ꎬ分别加入一定量的单质Se㊁NaBH4和10mL超纯水ꎬ剧烈搅拌后得到无色澄清的NaHSe溶液ꎮ称取一定量的CdCl2溶解于100mL超纯水中ꎬ然后加入一定体积的TGAꎬ再加入1mol/L的NaOH溶液调节pH为11ꎬ再通入氮气30min以排除氧气ꎮ将配制好的NaHSe溶液快速转移至CdCl2混合溶液中ꎬ边通氮气边剧烈搅拌ꎬ升温至80ħ加热回流30minꎬ得到CdSe溶液ꎮ待其冷却至室温后ꎬ按照CdSe和CdS物质的量比为1ʒ1配制一定量的CdCl2和Na2S溶液ꎬ在剧烈搅拌下逐滴加入CdSe溶液中ꎬ将反应体系升温至80ħ并回流30min后制备得到CdSe/CdS核壳结构的量子点ꎮ使用无水乙醇洗涤量子点ꎬ离心3次后重新分散于超纯水中待用ꎮ1.4㊀量子点检测Cu2+的浓度将300μL的CdSe/CdS量子点溶液㊁2.4mL的Tris ̄HCl缓冲液(浓度为10mmol/LꎬpH为9.0)㊁300μL的Cu2+溶液混合后静置10minꎬ再采用397nm波长近紫外光激发ꎬ检测其发射的荧光强度ꎮ2㊀结果与讨论2.1㊀量子点的表征测试得到CdSe和CdSe/CdS量子点的XRD图谱ꎬ如图1所示ꎮ图1㊀CdSe和CdSe/CdS量子点的XRD图26沈㊀阳㊀理㊀工㊀大㊀学㊀学㊀报㊀㊀第42卷㊀㊀由图1可见ꎬCdSe/CdS量子点的XRD谱线在衍射角25.8ʎ㊁43.2ʎ和50.5ʎ三个位置出现清晰的衍射峰ꎬ峰位介于立方CdSe和CdS的(111)㊁(220)和(311)晶面的特征峰之间ꎬ说明CdSe的内核与CdS包层之间存在相互作用力ꎬ使晶格参数发生变化ꎬ从而使其衍射峰位产生偏移ꎮ在CdSe外延生长CdS的纳米颗粒中也观察到类似的衍射峰[15]ꎮ此外ꎬ与CdS和CdSe晶体相比ꎬ这些衍射峰出现明显宽化的现象ꎬ反映出所制备CdSe/CdS样品的量子点特征ꎮ采用透射电子显微镜/能谱仪(TEM/EDS)对CdSe/CdS量子点进行分析ꎬ结果如图2所示ꎮ图2㊀CdSe/CdS量子点的TEM/EDS分析㊀㊀由图2(a)可见ꎬCdSe/CdS量子点显示出良好的分散性ꎬ单个粒子接近球形ꎮ根据量子点统计数据(图2(a)中粒径分布插图)可知ꎬ量子点的平均粒径约为2.4nmꎮ图2(b)中晶格条纹清晰ꎬ晶面间距为0.218nmꎬ对应CdSe的(220)晶面ꎬ证明产物中存在CdSeꎻ在量子点晶格内部及边缘ꎬ没有观察到明显的晶格畸变ꎬ说明CdS与CdSe具有很好的晶格匹配性ꎬCdSe表面可能外延生长出CdS层ꎮ由图2(c)可视区域内个别较大量子点的能谱分析结果可以观察到ꎬCd㊁S㊁Se元素分布较为均匀ꎬS元素分布于量子点团聚体的整个投影区域ꎬ而Se元素倾向于分布在投影区域的内部ꎬ分布面积明显小于S元素ꎬ表明合成物质为CdSe/CdS核壳结构的量子点ꎮCdSe和CdSe/CdS的吸收光谱与荧光光谱如图3所示ꎮ图3㊀CdSe与CdSe/CdS量子点吸收光谱和荧光光谱㊀㊀由图3可以看出ꎬCdSe/CdS的吸收峰相较于CdSe有少许蓝移ꎬ相同的现象也发生于其荧光光谱中ꎮ这是由于在CdSe表面外延生长形成CdS壳层所致ꎮ此外ꎬ图3(b)中CdSe/CdS的荧光强度远远高于CdSe的强度ꎬ这是由于CdS壳层对CdSe核粒子的表面缺陷进行了修饰ꎬ减少了CdSe禁带结构中的缺陷能级数量ꎬ提高了CdSe36第1期㊀㊀㊀汪登鹏等:CdSe/CdS量子点荧光探针检测Cu2+激子复合发光的强度[15]ꎮ2.2㊀荧光检测条件的优化按1.4中实验方法ꎬ采用CdSe/CdS量子点检测Cu2+浓度ꎬ改变静置反应时间ꎬ测得不同反应时间下CdSe/CdS量子点的荧光强度及Cu2+诱使CdSe/CdS量子点的荧光淬灭ꎬ结果如图4所示ꎮ图中纵坐标为荧光强度比I/I0ꎬI表示添加Cu2+时量子点的荧光强度ꎬI0表示不添加Cu2+时量子点的荧光强度ꎮ图4㊀反应时间对荧光强度的影响㊀㊀由图4可见ꎬCdSe/CdS量子点的荧光强度随时间变化不明显ꎬ说明其荧光稳定性较好ꎮ加入Cu2+后ꎬCdSe/CdS量子点的荧光淬灭反应迅速ꎬ5min后荧光强度保持稳定ꎬ说明5min后Cu2+与CdSe/CdS量子点的反应基本完全ꎬ荧光淬灭效果接近最大值ꎮ故适宜的静置反应时间为5minꎮ溶液的pH不同可能会影响量子点的荧光强度ꎬ也可能会影响检测物质的灵敏度和选择性[16]ꎮTGA封端的CdSe/CdS量子点在pH较低的缓冲液中荧光几乎完全猝灭ꎬ并形成沉淀[17]ꎮ如果pH过高ꎬCu2+会与溶液中的OH-发生化学反应ꎬ形成沉淀ꎬ进而影响检测的灵敏度ꎮ因此ꎬ本文考察溶液pH在5.5~10.7的范围内变化时对实验结果的影响ꎮ测得不同pH下的CdSe/CdS量子点荧光强度及Cu2+诱使CdSe/CdS量子点的荧光淬灭ꎬ结果如图5所示ꎮ由图5可以看出:当溶液的pH较小时ꎬ由于量子点表面的硫醇基团不太稳定ꎬ不能保持较高的荧光强度ꎻ随着pH增大ꎬCdSe/CdS量子点的荧光强度逐渐增大并趋于稳定ꎬ当pH为8.0时ꎬ荧光强度接近最大值ꎬ此时Cu2+诱使量子点荧光淬灭效率基本达到最高ꎮ故选择适宜的pH为8.0ꎮ图5㊀pH对荧光强度的影响2.3㊀CdSe/CdS量子点对Cu2+的荧光响应特性㊀㊀CdSe/CdS量子点对Cu2+具有灵敏的荧光响应特性ꎬ测得不同Cu2+浓度下的荧光光谱及荧光淬灭率(1-I/I046沈㊀阳㊀理㊀工㊀大㊀学㊀学㊀报㊀㊀第42卷图6㊀Cu2+对CdSe/CdS量子点的荧光淬灭效应㊀㊀由图6(a)可见ꎬ随着Cu2+浓度的增加ꎬCdSe/CdS量子点的荧光强度逐渐下降ꎮ在Cu2+浓度为60μmol/L的情况下ꎬ荧光猝灭率达到92.7%ꎮ由图6(b)可知ꎬCu2+浓度对CdSe/CdS量子点荧光强度的影响可以由两段线性关系表示ꎬ分别如图6(c)和图6(d)所示ꎮ由图6(c)的拟合结果可知ꎬCu2+浓度(C(Cu2+))在0.5~7μmol/L范围内时ꎬ(1-I/I0)与C(Cu2+)的线性关系为1-I/I0=0.00882+0.07943C(Cu2+)(1)线性相关系数R2=0.969ꎮ由图6(d)的拟合结果可知ꎬC(Cu2+)在7~60μmol/L范围内时ꎬ(1-I/I0)与C(Cu2+)的线性关系为1-I/I0=0.45637+0.00762C(Cu2+)(2)线性相关系数R2=0.989ꎮ浓度检测限(LimitofDetectionꎬLOD)计算公式为[18]LOD=3δ/K(3)式中:δ为空白样11次检测值的标准偏差ꎻK为标准曲线的斜率ꎮ根据式(3)计算得到体系对Cu2+浓度的检测限为0.06μmol/Lꎬ本方法的检测限低于文献[19-21]的研究结果ꎮ采用不同配体的量子点检测Cu2+浓度的方法比较如表1所示ꎮ表1㊀使用量子点测量Cu2+浓度的方法比较量子点材料配体浓度检测限/(μmol L-1)CdS[19]甘油三酯0.1CdS[20]肽0.5CdS[21]半胱氨酸1.5CdSe/CdS(本文)TGA0.062.4㊀荧光检测Cu2+的选择性采用CdSe/CdS荧光探针在最佳条件下对Cu2+进行荧光检测ꎬ通过与其他11种金属离子(即K+㊁Na+㊁Mg2+㊁Ba2+㊁Al3+㊁Mn2+㊁Fe3+㊁Ca2+㊁Pb2+㊁Cd2+㊁Zn2+)相比较ꎬ评估CdSe/CdS量子点体系对Cu2+的选择性ꎮ其中ꎬ添加Cu2+的浓度为50μmol/Lꎬ其他离子浓度取为Cu2+浓度的10倍ꎮ各种离子对CdSe/CdS荧光探针荧光强度的影响如图7所示ꎮ图7㊀各种离子对CdSe/CdS荧光探针荧光强度的影响㊀㊀由图7可以看出ꎬ除Cu2+以外的其他金属离子对CdSe/CdS量子点的荧光强度影响不大ꎬ说明CdSe/CdS量子点对Cu2+的检测具有高选择性ꎮ2.5㊀荧光淬灭机理分析物与荧光探针之间发生荧光淬灭反应的机理主要有静态淬灭和动态淬灭两种[22]ꎮ静态淬灭认为分析物与荧光探针的基态荧光分子发生反应形成非荧光体ꎻ动态淬灭认为荧光淬灭与扩散过程有关ꎬ是分析物与处于激发态的荧光分子之间发生碰撞ꎬ释放热能ꎬ使得荧光体无辐射跃迁至基态ꎬ从而导致荧光淬灭ꎮ静态荧光淬灭过程会形成非荧光体ꎬ因此其反应前后的紫外-可见吸收光谱会发生改变ꎬ但反应前后的荧光寿命不发生改变ꎻ动态荧光淬灭与静态荧光淬灭特征相反ꎬ其反应前后紫外-可见吸收光谱不变ꎬ但荧光寿命会发生变化ꎮ不同Cu2+浓度下CdSe/CdS量子点的紫外-可见吸收光谱如图8所示ꎮ添加Cu2+和不添加Cu2+时CdSe/CdS量子点的荧光寿命谱图如图9所示ꎮ由图8可见ꎬ添加不同浓度Cu2+后CdSe/CdS量子点的紫外-可见吸收光谱没有明显变化ꎮ由图9可见ꎬ添加Cu2+后ꎬ量子点的寿命明56第1期㊀㊀㊀汪登鹏等:CdSe/CdS量子点荧光探针检测Cu2+显减小ꎮ因此ꎬCu2+导致CdSe/CdS量子点荧光淬灭的机理为动态淬灭ꎮ图8㊀不同Cu2+浓度下CdSe/CdS量子点的紫外-可见吸收光谱图9㊀添加和不添加Cu2+时CdSe/CdS量子点的荧光寿命谱图2.6㊀实际水样中Cu2+浓度的检测为评估CdSe/CdS量子点荧光探针对检测Cu2+的实用性与可靠性ꎬ采用实际水样(自来水)进行检测实验ꎮ选取三种不同Cu2+浓度水平(10㊁20㊁30μmol/L)的自来水样品ꎬ每个样品检测三次取平均值ꎬ检测结果如表2所示ꎮ表中回收率为Cu2+浓度的检测值与实际值之比ꎬ相对标准偏差为标准偏差与平均值之比ꎬ反映Cu2+检测的精度ꎮ表2㊀自来水样品中实际Cu2+浓度与检测值的比较样品实际浓度/(μmol L-1)检测值/(μmol L-1)回收率/%相对标准偏差/%54.8897.62.8自来水1010.45104.52.52020.32101.63.8㊀㊀由表2可看出ꎬ各样品的回收率均接近100%ꎮ自来水中可能存在多种阳离子ꎬ如Na+㊁Ca2+㊁Mg2+㊁Mn2+等ꎬ本文实际水样测定结果表明ꎬ这些金属离子的存在不会干扰Cu2+的检测ꎬ再次证明了CdSe/CdS量子点荧光探针对检测Cu2+的实用性与可靠性ꎮ3㊀结论(1)采用溶液反应法成功合成了CdSe/CdS核壳结构量子点荧光探针ꎮ基于Turn ̄off模式利用CdSe/CdS量子点检测水介质中的Cu2+ꎬ在Cu2+浓度为60μmol/L的情况下ꎬ荧光猝灭率达到92.7%ꎮ(2)确定最优检测条件为:反应时间5minꎬ溶液pH为8.0ꎮ确定了荧光淬灭率与Cu2+浓度间的分段线性关系ꎮ(3)紫外-可见吸收光谱和荧光寿命测试结果表明ꎬCdSe/CdS量子点对Cu2+的荧光淬灭为动态淬灭机制ꎮ(4)对自来水样品中Cu2+浓度的检测值与实际浓度的相对标准偏差不超过4%ꎬ且回收率较高ꎮCdSe/CdS量子点对Cu2+的检测具有高选择性ꎬ干扰离子的存在几乎不影响CdSe/CdS量子点对Cu2+荧光响应的灵敏度ꎮ参考文献:[1]ZHANGXYꎬZHANGMꎬLIUHꎬetal.Environmentalsustainability:apressingchallengetobiologicalsewagetreatmentprocesses[J].CurrentOpinioninEnviron ̄mentalScience&Healthꎬ2019ꎬ12:1-5.[2]SMICHOWSKIPꎬLONDONIOA.Theroleofanalyti ̄caltechniquesinthedeterminationofmetalsandmet ̄alloidsindietarysupplements:areview[J].Micro ̄chemicalJournalꎬ2018ꎬ136:113-120.[3]HARIBALAꎬHUBTꎬWANGCGꎬetal.AssessmentofradioactivematerialsandheavymetalsinthesurfacesoilarounduraniumminingareaofTongliaoꎬChina[J].EcotoxicologyandEnvironmentalSafetyꎬ2016ꎬ130:185-192.[4]LEEWꎬKIMHꎬKANGYꎬetal.Abiosensorplatformformetaldetectionbasedonenhancedgreenfluores ̄centprotein[J].Sensorsꎬ2019ꎬ19(8):1846.66沈㊀阳㊀理㊀工㊀大㊀学㊀学㊀报㊀㊀第42卷[5]BIANWꎬWANGFꎬZHANGHꎬetal.FluorescentprobefordetectionofCu2+usingcore ̄shellCdTe/ZnSquantumdots[J].Luminescenceꎬ2015ꎬ30(7):1064-1070.[6]PARKSHꎬKWONNꎬLEEJHꎬetal.Syntheticratio ̄metricfluorescentprobesfordetectionofions[J].ChemicalSocietyReviewsꎬ2020ꎬ49(1):143-179. [7]蔡朝霞ꎬ阮晓娟ꎬ石宝琴ꎬ等.水溶性CdSe量子点的合成及其作为荧光探针对大肠杆菌的快速检测[J].分析试验室ꎬ2011ꎬ30(3):107-110. [8]孙雪花ꎬ张锦婷ꎬ郝都婷ꎬ等.基于Ag+修饰氮掺杂碳量子点用于组氨酸的荧光开启检测[J].分析试验室ꎬ2021ꎬ40(4):399-403.[9]ALDEWACHIHꎬCHALATITꎬWOODROOFEMNꎬetal.Goldnanoparticle ̄basedcolorimetricbiosensors[J].Nanoscaleꎬ2017ꎬ10(1):18-33.[10]李亚楠ꎬ王俊平.基于双发射免标记核酸探针的比率型荧光传感器用于银的检测[J].分析试验室ꎬ2020ꎬ39(1):12-16.[11]WANGJꎬJIANGCXꎬWANGXQꎬetal.Fabricationofan"ion ̄imprinting"dual ̄emissionquantumdotna ̄nohybridforselectivefluorescenceturn ̄onandratio ̄metricdetectionofcadmiumions[J].Analystꎬ2016ꎬ141(20):5886-5892.[12]吕俊杰ꎬ董小绮ꎬ孟鑫ꎬ等.Mn掺杂ZnS/ZnS核壳量子点磷光猝灭法测定铜离子[J].分析试验室ꎬ2019ꎬ38(3):321-325.[13]CAOYWꎬWANGCꎬZHUBHꎬetal.Afacilemeth ̄odtosynthesishigh ̄qualityCdSequantumdotsforlargeandtunablenonlinearabsorption[J].OptMaterꎬ2017ꎬ66:59-64.[14]张梦亚ꎬ高兵ꎬ柳翠ꎬ等.L ̄半胱氨酸修饰CdTe与CdTe/CdS量子点的水相合成与表征[J].稀有金属材料与工程ꎬ2016ꎬ45(S1):554-559.[15]沈嘉林ꎬ李玲ꎬ沈水发.CdSe@CdS核-壳结构量子点的微乳水热法制备[J].功能材料与器件学报ꎬ2019ꎬ25(2):82-87.[16]BIANWꎬWANGFꎬZHANGHꎬetal.FluorescentprobefordetectionofCu2+usingcore ̄shellCdTe/ZnSquantumdots[J].Luminescenceꎬ2015ꎬ30(7):1064-1070.[17]XUHꎬMIAORꎬFANGZꎬetal.Quantumdot ̄based"turn ̄on"fluorescentprobefordetectionofzincandcadmiumionsinaqueousmedia[J].AnalyticaChimi ̄caActaꎬ2010ꎬ687(1):82-88.[18]MANJUBAASHININꎬTHANGADURAITDꎬBHARATHIGꎬetal.Rhodaminecappedgoldnanopar ̄ticlesforthedetectionofCr3+ioninlivingcellsandwatersamples[J].JournalofLuminescenceꎬ2018ꎬ202:282-288.[19]CHENYFꎬROSENZWEIGZ.LuminescentCdSquantumdotsasselectiveionprobes[J].AnalChemꎬ2002ꎬ74(19):5132-5138.[20]GATTÁS ̄ASFURAKMꎬLEBLANCRM.Peptide ̄coatedCdSquantumdotsfortheopticaldetectionofcopper(II)andsilver(I)[J].ChemCommunꎬ2003(21):2684-2685.[21]BOONMECꎬNOIPATꎬTUNTULANITꎬetal.Cys ̄teaminecappedCdSquantumdotsasafluorescencesensorforthedeterminationofcopperionexploitingfluorescenceenhancementandlong ̄wavespectralshifts[J].SpectrochimicaActaPartA:MolecularandBiomolecularSpectroscopyꎬ2016ꎬ169:161-168. [22]甘晓娟ꎬ刘绍璞ꎬ刘忠芳ꎬ等.某些芳香族氨基酸作探针荧光猝灭法测定安乃近及其代谢产物[J].化学学报ꎬ2012ꎬ70(1):58-64.(责任编辑:宋颖韬)76第1期㊀㊀㊀汪登鹏等:CdSe/CdS量子点荧光探针检测Cu2+。
稀土元素在生物医用材料中的应用研究分析

稀土元素在生物医用材料中的应用研究分析在当今生物医学领域,材料科学的不断发展为医疗技术的进步提供了强大的支撑。
其中,稀土元素因其独特的物理、化学和生物学性质,逐渐成为生物医用材料研究的热点之一。
稀土元素在生物医用材料中的应用为疾病的诊断、治疗和组织修复等方面带来了新的机遇和突破。
稀土元素是指元素周期表中镧系元素以及钪和钇共 17 种元素。
它们具有独特的电子结构和光学、磁学等特性。
例如,稀土元素的发光性能优异,在特定条件下能够发出明亮且稳定的荧光,这使得它们在生物成像和检测中具有重要的应用价值。
在生物检测方面,稀土元素被广泛应用于免疫分析、核酸检测等领域。
以免疫分析为例,通过将稀土元素标记在抗体上,可以实现对目标抗原的高灵敏度检测。
由于稀土元素的荧光寿命长,能够有效避免生物体内自发荧光的干扰,从而大大提高检测的准确性和特异性。
此外,稀土元素还可以用于时间分辨荧光免疫分析,通过时间延迟测量荧光信号,进一步降低背景干扰,提高检测的信噪比。
在医学成像领域,稀土元素也发挥着重要作用。
例如,钆是一种常用的磁共振成像(MRI)造影剂。
钆离子能够影响周围水分子的弛豫时间,从而改变组织的信号强度,使病变组织在成像中更加清晰可见。
与传统的造影剂相比,基于稀土元素的造影剂具有更高的弛豫率和更好的成像效果。
除了在检测和成像中的应用,稀土元素在生物治疗方面也展现出了巨大的潜力。
一些稀土化合物具有抗肿瘤活性,可以通过抑制肿瘤细胞的增殖、诱导细胞凋亡等途径发挥抗癌作用。
同时,稀土元素还可以用于药物载体的设计。
利用稀土元素的磁性,将药物负载在磁性纳米粒子上,通过外部磁场的引导,实现药物在体内的靶向输送,提高药物的治疗效果,减少副作用。
在组织工程中,稀土元素同样有着不可忽视的应用。
将稀土元素掺入生物材料中,可以改善材料的力学性能、生物相容性和生物活性。
例如,在骨组织工程中,含有稀土元素的羟基磷灰石具有更好的成骨诱导能力,能够促进骨组织的再生和修复。
分析化学进展

相似文献(10条) 1.学位论文 程玉红 催化荧光动力学分析法的研究与进展和稀土离子荧光探针的应用研究 2004
催化荧光动力学分析法是利用荧光法来检测催化反应速率的一种动力学分析方法。该方法结合了动力学分析和荧光检测的优点,具有灵敏度高、选择 性好的优点。检测限一般可达到ng或pg级,是解决痕量和超痕量分析的有效方法。本论文将催化荧光动力学分析法运用于环境样品的分析,提出了一些新 的分析方法。 荧光探针技术最大的特点是具有高度的灵敏性和极宽的动态响应范围,已被广泛用于生物医药领域。稀土离子因为与某些有荧光或无荧光的有机化合 物配位后,发射稀土离子的特征荧光,产生稀土敏化荧光。这种敏化荧光具有Stocks位移大、光谱线窄、激发态寿命长、稳定、背景干扰小等优良性能 ,因此,得到广泛的应用。据此可以以稀土离子为探针来进行元素分析或测量某些药物和生物分子。 本论文由两部分组成,第一章为催化动力学荧光分析法的研究进展及应用,第二章为稀土离子荧光探针的研究与应用。每章又分为三小节,具体内容 如下: 第一章:催化荧光动力学分析法的研究进展及应用。 第一节:概括论述了整个催化动力学荧光分析法的应用研究现状及进展情况。 第二节:基于磷酸盐缓冲溶液中苯胺对高碘酸钾氧化荧光素的反应有阻抑作用,建立了测量痕量苯胺的新方法。方法灵敏度高、操作简便,应用于自 来水和城市河水中苯胺含量的测定,结果令人满意。 第三节:磷酸盐缓冲溶液中,痕量氰根离子对H2O2氧化丁基罗丹明B的反应有催化作用,使氧化反应速度明显加快。掘此,提出子催化动力学荧光法 测量痕量氰化物的新方法。方法灵敏度高,重现性好,用于环境水样中氰化物的测量,得到满意结果。 第二章:稀土离子荧光探针的进展与应用 第一节:概述了稀土离子荧光探针在元素分析以及医药和生物领域中的应用研究,对稀土离子作为荧光探针的发展作了展望。 第二节:在pH为7.3的六次甲基四胺-HCl缓冲溶液条件下磺基水杨酸可以与铽(Ⅲ)形成二元配合物,磺基水杨酸作为配体向中心离子铽(Ⅲ)发生能量 转移,发射铽(Ⅲ)的特征荧光。本文据此提出以铽离子荧光探针来测量磺基水杨酸的新方法。 第三节:在pH为6.6的缓冲溶液中,铽(Ⅲ)可以和多巴胺形成配合物,发生分子内能量转移,使铽(Ⅲ)的特征荧光辐射明显增强,在铽(Ⅲ)的最大发 射波长545nm处测量其荧光强度。据此提出了测量痕量铽的新方法。
流动注射- 化学发光法测定药物制剂及生物流体中盐酸多巴胺
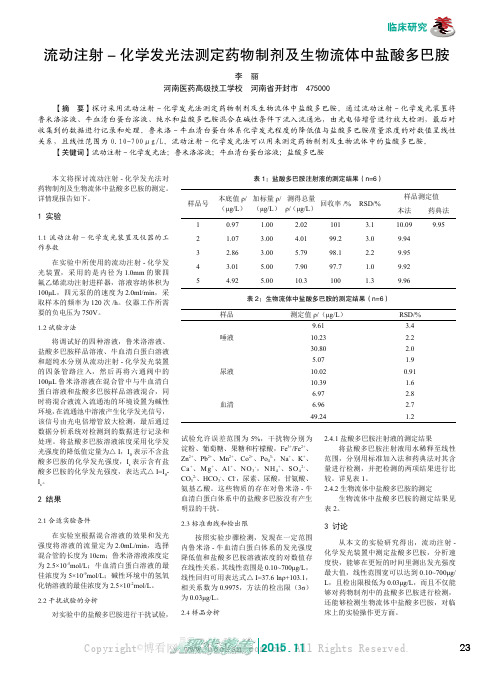
对实验中的盐酸多巴胺进行干扰试验, 2.4 样品分析
3 讨论
从本文的实验研究得出,流动注射 化学发光装置中测定盐酸多巴胺,分析速 度快,能够在更短的时间里测出发光强度 最大值,线性范围宽可以达到 0.10~700μg/ L,且检出限极低为 0.03μg/L,而且不仅能 够对药物制剂中的盐酸多巴胺进行检测, 还能够检测生物流体中盐酸多巴胺,对临 床上的实验操作更方面。
临床研究
流动注射 - 化学发光法测定药物制剂及生物流体中盐酸多巴胺
李 丽 河南医药高级技工学校 河南省开封市 475000
【摘 要】探讨采用流动注射 - 化学发光法测定药物制剂及生物流体中盐酸多巴胺。通过流动注射 - 化学发光装置将 鲁米洛溶液、牛血清白蛋白溶液、纯水和盐酸多巴胺混合在碱性条件下流入流通池,由光电倍增管进行放大检测,最后对 收集到的数据进行记录和处理。鲁米洛 - 牛血清白蛋白体系化学发光程度的降低值与盐酸多巴胺质量浓度的对数值呈线性 关系,且线性范围为 0.10-700μg/L。流动注射 - 化学发光法可以用来测定药物制剂及生物流体中的盐酸多巴胺。
血清白蛋白体系中的盐酸多巴胺没有产生
明显的干扰。
2.4.1 盐酸多巴胺注射液的测定结果 将盐酸多巴胺注射液用水稀释至线性
范围,分别用标准加入法和药典法对其含 量进行检测,并把检测的两项结果进行比 较。详见表 1。 2.4.2 生物流体中盐酸多巴胺的测定
生物流体中盐酸多巴胺的测定结果见 表 2。
2.1 合适实验条件
2.3 标准曲线和检出限
在实验室根据混合溶液的效果和发光 强度将溶液的流量定为 2.0mL/min,选择 混合管的长度为 10cm;鲁米洛溶液浓度定 为 2.5×10-5mol/L;牛血清白蛋白溶液的最 佳浓度为 5×10-9mol/L;碱性环境中的氢氧 化钠溶液的最佳浓度为 2.5×10-2mol/L。
时间分辨荧光微球免疫层析法定量检测克伦特罗

时间分辨荧光微球免疫层析法定量检测克伦特罗赖科洋;陈媛【摘要】建立了一种定量检测克伦特罗的时间分辨荧光微球免疫层析法.对抗体标记量、微孔中克伦特罗抗体-时间分辨荧光微球探针的体积以及检测线上抗原浓度进行了优化.通过时间分辨荧光微球试纸条检测仪读取试纸条上检测线和质控线的信号强度,以克伦特罗标准品的浓度为横坐标,以检测线和质控线信号强度的比值为纵坐标建立标准曲线.结果表明:该方法定量检测范围为0.01~0.81μg/L,检测限为0.004μg/L,半抑制率为0.06μg/L.本检测方法具有简便、灵敏度高、快速和可定量等特点,适合于大批量样品的现场筛查.【期刊名称】《江西科学》【年(卷),期】2018(036)002【总页数】4页(P244-247)【关键词】时间分辨荧光微球;克伦特罗;检测;免疫层析【作者】赖科洋;陈媛【作者单位】南昌市第三中学,330029,南昌;南昌大学食品科学与技术国家重点实验室,330047,南昌【正文语种】中文【中图分类】O657.30 引言克伦特罗(Clenbuterol,CLE)是一种β-肾上腺素受体激动剂,最初作为一种饲料添加剂用于畜牧业养殖,能够显著地提高动物瘦肉率,俗称“瘦肉精”[1]。
人食用残留有CLE的肉制品后会引起如心悸、头晕、心跳加快等中毒症状[2],对人的身体健康造成危害。
因此,我国明文禁止CLE用于饲料添加剂,规定在动物性食品中不得检出CLE[3]。
目前,分析CLE残留常用的方法有气相色谱串联质谱法[4]、液相色谱串联质谱法[5-6]、高效液相色谱法[7]、酶联免疫吸附法[8-9]和胶体金免疫层析法(Colloidal gold lateral flow assay,CGLFA)[10-11]等。
前4种方法具有灵敏度高、准确性好、特异性强的优点,不过检测时间长、操作复杂、费用高,不适合大量样本的现场筛查。
CGLFA具有快速、简便和费用低等优点[12],但该检测方法灵敏度较差,一般只用于定性分析。
常用荧光探针小结

-
11
DAPI (magenta) bound to the minor groove of DNA (green and blue).
DAPI can be used for fixed cell staining, the concentration of DAPI needed for live cell staining is generally very high and rarely used for live cells. Though it was not shown to have mutagenicity to E. coli, it is labelled as a known mutagen in manufacturer information. As it is a DNA binding compound it is likely to have some low level mutagenic properties and care should be taken in its handling and disposal.
-
1
Exitation λmax: 495 nm; Emission λmax: 519 nm; Solvent pH:8.00
-
2
Immunocytochemistry/Immunofluorescence-alpha Tubulin antibody [DM1A] (FITC) (ab64503)
ac413230010rb200也称丽丝胺罗丹明b无定形褐红色粉末不溶于水易溶于酒精和丙酮性质稳定可长期保存最大吸收光谱为570nm呈明亮的橙色荧光因与fitc的黄绿色有明显区别故被广泛用于对比染色或用于两种不同颜色的荧光抗体的双重染色
一种基于罗丹明b衍生物的多通道荧光探针及制备方法与应用

一种基于罗丹明b衍生物的多通道荧光探针及制备方法与应用嘿,朋友们!今天我要给你们讲个超酷的东西——基于罗丹明b衍生物的多通道荧光探针。
这玩意儿就像是荧光世界里的超级特工,有着各种神奇的本领。
先来说说这罗丹明b衍生物,它就像是荧光界的魔法原料。
制备这个多通道荧光探针的时候啊,就像是在做一道超级复杂又超级有趣的魔法料理。
首先呢,得把各种原料准备好,那些原料就像是一群小士兵,在反应容器这个战场上准备大干一场。
制备方法有点像一场精心编排的舞蹈。
各种化学试剂要按照特定的顺序和比例加入,就像舞蹈演员要按照编排好的舞步依次登场。
比如说,要在合适的温度下进行反应,这个温度啊,就像是指挥这场化学舞蹈的指挥家手中的指挥棒,稍微偏差一点,整个舞蹈就乱套啦。
这多通道荧光探针一旦制备成功,那可不得了,就像孙悟空有了火眼金睛一样。
它可以在不同的环境下,像在酸性环境里,就像是一个敏锐的酸侦探,荧光颜色会发生特定的变化。
在金属离子的环境中呢,又像是金属离子的追踪小能手,能准确地捕捉到它们的存在并且通过荧光信号告诉我们,就好像是在和金属离子玩捉迷藏,它总能一下子就把对方找到。
它的应用那更是广泛得不像话。
在生物检测领域,它就像是一个小小的生物间谍,悄无声息地潜入细胞内部,探测细胞内的各种信息。
不管是检测细胞内的酸碱度变化,还是发现那些隐藏起来的有害物质,它都能轻松搞定。
就像一个无所不能的小侦探,在微观世界里穿梭自如。
在环境检测方面,这个多通道荧光探针就像是一个环境卫士。
如果有污染物质像小偷一样偷偷潜入环境中,它立马就能通过荧光信号发出警报。
无论是水里的重金属污染,还是空气中的有害气体,它都能像嗅探犬一样敏锐地察觉到。
而且啊,这个探针的多通道特性就像是拥有好几把不同的钥匙,可以打开不同的检测之门。
每一个通道都像是一个独特的信号通道,就像收音机的不同频道一样,各自传递着独特的信息。
它的稳定性也是杠杠的,就像一个坚强的小战士,不管是在复杂的化学环境还是物理环境中,都能坚守岗位,稳定地发挥自己的荧光探测功能。
三种席夫碱类荧光探针的合成及应用研究

三种席夫碱类荧光探针的合成及应用研究
席夫碱(Xylenol orange)是一种具有荧光性质的化合物,可以作为荧光探针用于生物体内离子检测和分析。
以下列举了三种常见的席夫碱类荧光探针的合成方法及其应用研究。
1. 席夫碱偶氮盐类探针的合成及应用研究:
这类探针是通过将席夫碱与偶氮盐反应得到的,具有良好的荧光性能和选择性。
合成方法包括将席夫碱与亚硝酸钠在酸性条件下反应得到席夫碱偶氮盐。
应用研究中,这类探针常用于检测和测定金属离子(如钴、铁、锰等)的浓度及其分布状态。
2. 席夫碱丙烯酸盐类探针的合成及应用研究:
这类探针是通过将席夫碱与丙烯酸发生酯化反应得到的,具有良好的水溶性和细胞渗透性。
合成方法包括利用化学反应将席夫碱与丙烯酸反应而得。
应用研究中,这类探针常用于细胞内钙离子(Ca2+)的荧光探测和成像。
3. 席夫碱葡萄糖酮类探针的合成及应用研究:
这类探针是通过将席夫碱与葡萄糖酮反应得到的,具有较好的选择性和灵敏度。
合成方法包括将席夫碱与葡萄糖酮在碱性条件下进行加热反应而得。
应用研究中,这类探针常用于检测和测定生物体内葡萄糖的浓度及其分布状态。
总之,席夫碱类荧光探针的合成及应用研究是一个活跃且具有潜力的领域,不仅可以用于生物分析和成像,还可以应用于生物传感器、药物控释等方面的研究。
随着技术的进一步发展,席夫碱类荧光探针在生物医学领域的应用前景将更加广阔。
