氯吡格雷的代谢途径NEJM2009
氯吡格雷与普拉格雷的代谢机制

1
问题的提出
分析1991~2000年18个药物ADR报告,发现发生 率最高的27个药物中(包括Carbamazepine, fluoxetine, Ibuprofen, Imipramine, Isoniazid, Naproxen, Rifampin, Teophylline, Phenytoin, Verapamil , Warfarin等),有16个(57%)药物的ADR发生至少与一 种药酶基因多态性(主要与poor metabolism)有关;反 之,随机抽查药物中,也有7~12%的药物与基因相关,提 示我们,如依据患者个体的基因多态性给药即可大大 减少ADR的发生!
7
FDA1945~2005要求121个药品标明 药物基因组生物标记物相关信息
8
Pharmacotherapy 2008;28(8):992–998
药物基因学的临床应用
Enzyme/Disease
Gene
• Glucose-6-PhosphateDehydrogenase
G6PD
Deficiency (G6PD Def)
• N-Acetylation & Tuberculosis
NAT2
•Cytochrome P450 Enzyme ━Drug Metabolism
CYP2D6
• Warfarin & Coagulation
CYP2C9
VKORC1
•Thiopurine S-Methyltransferase
TPMT
4
20世纪:千人一药一量!
One drug fits all ! One dose fits all !
5
21世纪:一人一药一量
16.氯吡格雷

氯吡格雷的药效之谜——从一篇Meta分析说起今天我们要讨论的药物是氯吡格雷,商品名是波利维。
它是制药巨头赛诺菲安万特十多年前开发的一款抗血小板药物,用于冠心病、动脉粥样硬化等多种心血管疾病,也常用血管支架术的抗凝药。
不同于以前的药物,氯吡格雷的靶点是血小板表面上的ADP受体,而ADP正是激活血小板引起凝血反应的主要源头之一。
由于氯吡格雷药效明确,毒副作用小,很快就获得市场的好评,销量节节攀升。
然而,氯吡格雷也并非十全十美,也常有氯吡格雷用药无效的案例报告,这是什么原因呢?尽管药物有个体化差异,这一点临床医生和药师很早就知道,但氯吡格雷无效的报告还是引起了临床科学家的重视。
氯吡格雷是一个“前药”,它真正发挥作用需要经过肝脏药物代谢酶的活化,后来发现CYP2C19参与了大部分反应。
也有其他的研究组,通过全基因组关联分析的方法找到CYP2C19相关的等位基因。
[1]关于这个问题的探索,这几年一直是临床研究的热门话题。
有研究支持:CYP2C19基因的功能缺失与不良的心血管预后相关。
也有研究提出不同意见,说是没有关系。
一时间,一线的临床工作者有些无所适从。
在这样的背景下,来自Brigham and Women’ Hospital 的Jessica Mega 和Marc Sabatine 2010年主持了一项Meta分析。
[2] Brigham and Women’ Hospital 坐落美国波士顿,距离著名的麻省总医院很近。
它被评为2010年度美国最佳医院之一。
肿瘤、心血管和妇科是它的特色专科。
Jessica Mega 和Marc Sabatine 都来自于心血管科,都擅长介入治疗,这样他们用到氯吡格雷的几率是非常大的,也就有可能及早关注到氯吡格雷用药无效的情况。
难能可贵的是,Marc Sabatine 除了是一位出色的大夫,他还对基因组学和蛋白质组学等新的领域也很有兴趣。
也许是基于这个原因,二人在参与的一个大型临床研究项目中(TRITON–TIMI)打算将与氯吡格雷代谢有关的基因信息也考虑进去。
质子泵抑制剂-氯吡格雷高炜

– 氯吡格雷与阿司匹林预防缺血事件比较(CAPRIE) 研究中,二者严重消化道出血发生率分别为0.52% 和0.72%
– Lanas等研究显示,氯吡格雷与阿司匹林消化道出 血风险相似
抗血小板治疗与消化道出血
GRACE研究显示:ACS患者合并大出血的发 生率为2.3%~4.8%,最常见的出血部位为消 化道,占所有出血部位的31.5%
0
-10
观察时间 7日
PRI Variation (%)
-20
Omeprazole (n=64)
-30
Placebo (n=60)
-40
-32.6
-50
-43.3
p<0.0001
Gilard et al. J Am Coll Cardiol 2008;51:256-60.
FDA早期通报推荐: 继续使用氯吡格雷,谨慎评估PPI的使用
Available online at The Lancet on September 1, 2009
TITAN
随机试验
COGENT Trial
ASA
N ~ 3500
氯吡格雷 (75mg QD)
氯吡格雷 / 奥美拉唑 (75mg QD / 20mg QD)
survival probability
9
6.2
3.6
2.5
0
早期停用抗血小板药物 肾功能衰竭 分叉病变 糖尿病 LVEF降低
Iakovou I, et al. JAMA, 2005, 293: 2126-2130.
术后长期联合抗血小板治疗
阿司匹林 ➢ 无阿司匹林抵抗、过敏或出血危险的患者,应给予阿 司匹林325 mg/d,1-6个月,此后75162 mg/d, 长期口服
NEJM:王拥军教授发现“双抗”显著降低卒中再发风险(CHANCE研究)

由首都医科大学附属北京天坛医院王拥军教授主持进行的氯吡格雷联合阿司匹林与阿司匹林单独治疗急性非致残性脑血管事件高危人群研究(colopidogrel in high-risk patients with acute non-disabling cerebrovascular events,简称CHANCE研究)该研究已被世界权威医学期刊《新英格兰医学杂志》(NEJM)接受,将于今天在新英格兰杂志发表。
此项研究在今年2月份美国夏威夷举行的2013年国际卒中大会(ISC)上公布后,引起广泛反响,在今天的天坛会正式发布。
这是目前为止,全球最大多中心、随机、双盲、双模拟、平行对照小卒中和TIA临床研究。
CHANCE研究结果显示,在短暂性脑缺血发作(TIA)或小卒中后相对短期应用阿司匹林及氯吡格雷联合治疗在降低卒中复发风险方面优于阿司匹林单独治疗,且并不伴有严重出血并发症风险的显著增加。
这项仅在中国进行的CHANCE研究领先于另一项在美国招募和进行的类似研究,即TIA和卒中血小板定向抑制(POINT)研究。
该研究纳入了5170例患者40岁及以上的TIA或小卒中的患者。
其发病时间在24小时内,被随机分配到两组:阿司匹林(首日负荷剂量为75-300mg,随后75mg/天)加安慰剂治疗组,或相同的阿司匹林剂量加氯吡格雷(首日负荷剂量为300mg,随后75mg/天)治疗组。
双抗治疗组的患者还需要经过21天之后停用阿司匹林,因为与其他亚组人群类似,中国的患者具有相对较高的出血风险。
研究结果表明,同时接受阿司匹林和氯吡格雷双抗治疗的患者卒中复发率更低。
90天随访时,双抗治疗组患者无卒中(包括缺血性和出血性卒中)生存的风险比(HR)为0.68(95%CI,0.57 - 0.81,P <0.001)。
对于联合次要终点事件(卒中,心肌梗死,血管性死亡),HR为0.69(95%CI,0.58 - 0.82,P <0.001)。
每日医药——氯吡格雷

每日医药——氯吡格雷
【其他名称】波立维。
【性状】常用其二硫酸盐,为白色粉末,不溶于水,但于ph1的水中易溶。
易溶于甲醇。
【药理及应用】是血小板聚集抑制剂,选择性的抑制ADP与血小板受体的结合及抑制ADP介导的糖蛋白GPⅡb/Ⅲa复合物的活化,而抑制血小板聚集。
也可抑制非ADP引起的血小板聚集。
对血小板ADP受体的作用是不可逆的。
口服吸收迅速,血浆中蛋白结合率为98%,在肝脏代谢,主要代谢产物无抗血小板聚集作用。
用于预防和治疗因血小板高聚集引起的心、脑及其他动脉循环障碍疾病,如近期发作的脑卒中、心肌梗死和确诊的外周动脉疾病。
【用法】每日一次,每次75mg。
【注意】(1)常见的不良反应为消化道出血、中性粒细胞减少、腹痛、食欲减退、胃炎、便秘、皮疹等。
偶见血小板减少性紫癜。
(2)对本品过敏者禁用。
(3)溃疡病患者及颅内出血患者禁用。
(4)肝、肾功能损害者慎用。
【制剂】片剂:每片25mg;75mg。
同为急性冠脉综合征的一线用药,替格瑞洛与氯吡格雷有哪些区别?

同为急性冠脉综合征的一线用药,替格瑞洛与氯吡格雷有哪些区别?
对于急性冠脉综合征和PCI术后的患者来说,双抗药物治疗是抗栓治疗的基础。
其中,阿司匹林联合一种P2Y12受体抑制剂临床比较常用。
P2Y12受体抑制剂用的比较多的是氯吡格雷和替格瑞洛。
那么,作为一线P2Y12受体拮抗剂,二者有哪些区别呢?今天,一文说清。
一、与血小板结合方式不同
氯吡格雷与血小板以不可逆的方式进行结合,用药期间会降低血小板的数量,出血时需要输血补充血小板。
而替格瑞洛与血小板以可逆的方式结合,这也就意味着停药后,血小板会得到恢复。
二、起效时间不同
众所周知,氯吡格雷为前体药物,需要在肝药酶CYP2C19的作用下,方可转化为活性代谢产物。
而替格瑞洛及其主要代谢产物均具有活性,因此,替格瑞洛起效时间更快。
三、抗血小板强度
替格瑞洛的抗血小板作用强于氯吡格雷。
至少在急性冠脉综合征发病后最初12个月内,替格瑞洛的疗效由于氯吡格雷,而在患者不能耐受替格瑞洛的治疗中,方可选用氯吡格雷。
四、代谢酶亚型不同
氯吡格雷为前体药物,主要经由肝药酶CYP2C19的代谢。
而替格瑞洛主要经由CYP3A4代谢,少部分由CYP3A5代谢。
五、出血风险
氯吡格雷和替格瑞洛同为抗血小板药物,二者均有引起出血的风险。
有研究表明,长期使用替格瑞洛的出血风险要高于氯吡格雷,但短期使用的情况下,二者出血风险相似。
氯吡格雷的使用需要注意4点
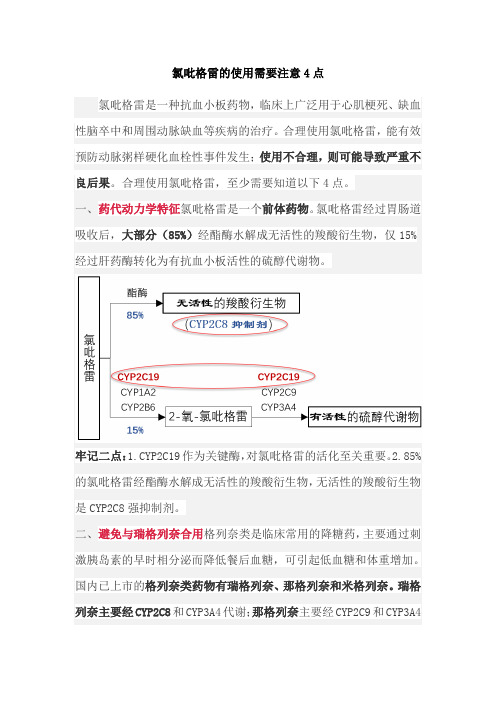
氯吡格雷的使用需要注意4点氯吡格雷是一种抗血小板药物,临床上广泛用于心肌梗死、缺血性脑卒中和周围动脉缺血等疾病的治疗。
合理使用氯吡格雷,能有效预防动脉粥样硬化血栓性事件发生;使用不合理,则可能导致严重不良后果。
合理使用氯吡格雷,至少需要知道以下4点。
一、药代动力学特征氯吡格雷是一个前体药物。
氯吡格雷经过胃肠道吸收后,大部分(85%)经酯酶水解成无活性的羧酸衍生物,仅15%经过肝药酶转化为有抗血小板活性的硫醇代谢物。
牢记二点:1.CYP2C19作为关键酶,对氯吡格雷的活化至关重要。
2.85%的氯吡格雷经酯酶水解成无活性的羧酸衍生物,无活性的羧酸衍生物是CYP2C8强抑制剂。
二、避免与瑞格列奈合用格列奈类是临床常用的降糖药,主要通过刺激胰岛素的早时相分泌而降低餐后血糖,可引起低血糖和体重增加。
国内已上市的格列奈类药物有瑞格列奈、那格列奈和米格列奈。
瑞格列奈主要经CYP2C8和CYP3A4代谢;那格列奈主要经CYP2C9和CYP3A4代谢;米格列奈主要通过与葡萄糖醛酸结合排泄,极少量经CYP2C9代谢。
因为,85%的氯吡格雷经酯酶水解成无活性的羧酸衍生物,无活性的羧酸衍生物可显著抑制CYP2C8。
若氯吡格雷与瑞格列奈合用,可抑制瑞格列奈的体内代谢,使瑞格列奈血药浓度升高3.9~5.1倍,增加低血糖风险,因此氯吡格雷应避免与瑞格列奈合用。
三、能与哪些质子泵抑制剂合用?氯吡格雷可增加胃肠道出血风险。
为了预防氯吡格雷引起的胃肠道损害事件,临床广泛合用质子泵抑制剂。
氯吡格雷是前体药物,在体内经CYP2C19转化后,才能成为能抑制血小板聚集的活性物质。
奥美拉唑、埃索美拉唑能和氯吡格雷竞争CYP2C19,导致氯吡格雷活性过程受阻,可能影响其抗血小板活性。
如果必须合用质子泵抑制剂,可选择兰索拉唑、泮托拉唑、雷贝拉唑和艾普拉唑等。
氯吡格雷(原研药)药品说明书:质子泵抑制剂药品说明书:四、餐前服还是餐后服?氯吡格雷的常规用法用量为:每次75mg,每日一次,与或不与食物同服。
CYP2C19基因多态性与氯吡格雷抵抗的相关性

CYP2C19基因多态性与氯吡格雷抵抗的相关性引言:氯吡格雷是一种广泛用于预防心血管疾病的药物,它能有效抑制血小板聚集,从而预防血栓形成。
一些患者对氯吡格雷的治疗效果不佳,即出现抵抗。
研究表明,CYP2C19基因多态性与氯吡格雷抵抗之间存在一定的相关性。
本文将探讨CYP2C19基因多态性对氯吡格雷抵抗所起的影响,以及如何通过基因检测来指导氯吡格雷的治疗。
CYP2C19基因:CYP2C19基因编码的酶在体内主要参与药物的代谢和清除过程。
CYP2C19基因存在多态性,包括正常代谢型(EM)、慢代谢型(PM)、中间代谢型(IM)等。
这些不同类型的基因多态性会导致个体对于氯吡格雷的代谢速度和血药浓度产生差异,从而影响氯吡格雷的治疗效果。
CYP2C19多态性与氯吡格雷代谢:研究发现,CYP2C19基因的不同多态性对氯吡格雷的代谢速度有着显著影响。
慢代谢型患者(PM)的CYP2C19酶活性较低,代谢氯吡格雷的速度慢,血药浓度升高,因此需要更低的剂量来达到相同的治疗效果;而正常代谢型患者(EM)的CYP2C19酶活性正常,对氯吡格雷的代谢速度和血药浓度处于正常范围。
PM型患者在接受标准剂量的氯吡格雷治疗时,可能无法达到足够的抗血小板聚集效果,从而出现抵抗现象。
CYP2C19基因多态性与氯吡格雷抵抗的相关性:大量临床研究已证实,CYP2C19基因多态性与氯吡格雷抵抗之间存在着密切的相关性。
一项发布于《新英格兰医学杂志》的研究发现,患者中每多携带一个PM型基因,就会增加22%的心血管事件风险。
另一项发表于《心脏杂志》的研究显示,PM型患者在接受氯吡格雷治疗后的血小板抑制效果明显低于EM 型患者。
这些研究结果表明,CYP2C19基因多态性与氯吡格雷抵抗之间确实存在显著的相关性。
基因检测在氯吡格雷治疗中的应用:考虑到CYP2C19基因多态性对氯吡格雷治疗效果的影响,基因检测已被提出用来指导氯吡格雷的治疗。
通过基因检测可以快速准确地确定患者的CYP2C19基因型,进而根据其代谢能力来调整氯吡格雷的剂量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氯吡格雷的代谢 途径
氯吡格雷是药物前体,只有通过CYP450同功酶CYP2C19等代谢水 解成有活性的硫醇衍生物,从而抑制血小板聚集。因此,CYP2C19
的活性对氯吡格雷的抗血小板效应起决定性作用
2021/5/10 NEJM 2009;360:363-75 Pariet
10
CYP2C19:PPI与氯吡格雷共同代谢途径
ADP诱导的血小板聚集(AU*min)
350
300
250
220
200
150
100
50
n=732
0
Control
295.50 *
226
209
n=162
奥美拉埃索美拉唑
*与对照组相比P<0.05
Thromb Haemost 2009; 101:714-719
CYP2C19 PM削弱氯吡格雷的活化
Ho PM et al. JAMA 2009;301:937-944
4
PPI与氯吡格雷联合应用风险:事件初始
2009年1月28日,《加拿大医学会杂志》在线发表了 一项大型研究显示,氯吡格雷联用PPI增加患者再梗 危险(n=13,636)。
该研究同时发现患者服用omeprazole(奥美拉唑) ,lansoprazole(兰索拉唑),或rabeprazole(雷 贝拉唑)等质子泵抑制剂,会显著增加心脏病的复 发率。但没有发现pantoprazole(泮托拉唑)或H2 受体拮抗剂等抑酸药有如此副作用。
在接受氯吡格雷治疗的人群中,携带功能降低的CYP2C19等位 基因者的活性代谢产物水平显著降低,血小板抑制作用显著减小,
并且主要不良心血管事件发生率较高。
13
MEDCO研究: PPI对于氯吡格雷的影响具有类效应
MACE rates by PPI
PPI
MACE rate (%)
Hazard ratio
ACCF/ACG/AHA 2008 专家共识
抗血小板治疗的适应症
评估消化道出血风险
推荐急性心梗后进行抗血小板治疗的患者同时服用PPI
检测Hp, 如阳 性则给与治疗
溃疡并发症病史 溃疡疾病史(非出血性)
胃肠道出血 双重抗血小板治疗
联合抗凝治疗
缓解患者胃灼热等消化道不适,预防抗血小板治疗可能引起的消化
肝脏主要代谢酶:
细胞色素P450 (CYP3A4, CYP2C19)
细胞色素P450 (CYP2C19):氯吡格雷 与PPI的共同代谢途径,
PPI可竞争性抑制 CYP2C19活性
降低活性氯吡格雷血药 浓度
ADP receptor (P2RY12)
降低血小板聚集抑制率
缺血性事件率可能上升
不同PPI对氯吡格雷抗血小板作用的影响
中华内科杂志 2009年7月第48卷第7期 607·610
2
抗血小板治疗与消化道损伤
对既往无溃疡的患者
阿司匹林: 局部损伤+全身损伤,
促进溃疡形成
对已存在溃疡的患者
阿司匹林
肯定延缓愈合
直接刺激消化道粘膜
破坏胃黏膜的疏水保护屏障
抑制环氧酶,减少前列腺素 的合成,从而减少胃黏膜血 流量,不利于胃黏膜修复
PPI降低氯吡格雷的益处?
2008年10月,美国心脏学会(AHA)、美国心脏病学基金 会(ACCF)、美国胃肠病学会(ACG)联合发表共识意见 ,推荐急性心梗后服用阿司匹林的患者同时服用PPI,实 际上其中许多患者也会同时服用氯吡格雷 。
根据上述研究结果,FDA在今年1月建议,当患者服用氯吡 格雷时,临床医师应重新评价应用PPI的必要性。
PPI在防治抗血小板药物消化道损害中的 地位:争论尚未平息
刘健 北京大学人民医院心脏中心
抗血小板药物消化道损伤的预防和治疗中国专家共识
大量循证医学证据显示了抗血小板治疗对血栓栓塞性疾病一级和二级预防的益处。 目前小剂量阿司匹林(75~325 mg)广泛用于冠状动脉粥样硬化性心脏病(冠心病)、脑血 管疾病和外周动脉疾病的治疗 对急性冠状动脉综合征(ACS)和植入药物洗脱支架(DES)的患者更加强调双重抗血小板 治疗(阿司匹林+氯吡格雷)的重要性。
中华内科杂志 2009年7月第48卷第7期 607·610
1
抗血小板药物是一柄“双刃剑”
阿司匹林通过抑制环氧化酶(cox),一方面能抑制血小板活化和血栓形 成,另一方面损伤消化道黏膜,导致溃疡形成和出血,极严重时可致患 者死亡
其他抗血小板药物如氯吡格雷也能加重消化道损伤,联合用药时损伤更 为严重。
氯吡格雷较少损伤
氯吡格雷
…可能延缓愈合
抑制血小板聚集,可能抑 制内皮生长因子,影响溃 疡的愈合
PPI与氯吡格雷联合应用风险:事件初始
急性冠脉综合征患者在合并使用波立维和PPI的 不良转归风险
结论:急性冠脉综合征(ACS)患者在接受氯吡格雷抗血 小板的同时,服用PPI会增加因ACS再次入院的危险。
道出血风险。
1项以上的危险因素 年龄》65岁
使用糖皮质激素 消化不良或
胃食管反流症状
Circulation 2008;118;1894-1909
2021/5/10
Pariet
8
氯吡格雷的作用机制
氯吡格雷通过抑制血小板膜上的ADP(二磷酸腺苷)受体发挥抗血小板作 用
CMAJ 2006;174:1715–1722 9
2009年1月FDA早期通报推荐: 继续使用波立维,谨慎评估PPI的使用
波立维
在取得进一步信息之前,FDA推荐如下: 鉴于氯吡格雷预防血栓所致心脏事件或卒中的已证实的获益,卫生保健人员应继续 处方氯吡格雷,患者应持续应用氯吡格雷。 对于正在接受氯吡格雷治疗的患者,医务人员应谨慎评估启用或继续使用PPI(包 括OTC奥美拉唑)治疗的必要性。 接受氯吡格雷治疗的患者如果目前正在使用或考虑使用PPI(包括OTC奥美拉唑), 应向其卫生保健人员咨询。
p
奥美拉唑
25.1
1.39
<0.0001
埃索美拉唑
24.9
1.57
<0.0001
泮托拉唑
29.2
1.61
<0.0001
兰索拉唑
24.3
1.39
<0.0004
Erick J Stanek,(SCAI) 2009 Scientific Sessions.
奥美拉唑为什么使氯吡格雷减效?
氯吡格雷为一前体药物,须经CYP2C19代谢为有活性的产物才能抑制血小板的聚集。氯吡格雷有 15%主要经CYP2C19代谢为有活性的产物,才能发挥抗血小板作用,这说明该药在较低浓度即可发挥拮 抗血小板的作用,也就意谓着血药浓度的微小变化(增高或降低)就能影响其疗效的强弱。
