泮托拉唑钠肠溶片申报资料
泮托拉唑钠肠溶片与莫沙必利治疗功能性消化不良的临床效果观察

泮托拉唑钠肠溶片与莫沙必利治疗功能性消化不 良的临床效果观察
李丽秋
1 . 3 . 1 对照 组 仅 给予莫 沙 必利 治疗 。每 天 3次 ,每次 5 m g 干三 餐
【 摘要 】 目的 对 比不 同给药方案对功能性消化不 良 ( F D)患者的疗效。
方 法 比较观 察组和 对 照组 4周后 疗效 、复发 率与副 反应情 况。结果 两组用 药 4周后 总有效 率依 次为 8 3 7 8 %、9 6 0 0 %,对照 组远不及观 察 组 效果理想 ( P< ( ) 0 5) 。结 论 给 予 F D 患 者 采 用 泮托 拉 唑 钠 肠 溶 片联 合 莫 沙 必 利 治 疗 ,治 疗 效 果理 想 且远 期 观 察 复 发 率较 低 。
d ys p e p s i a f F D)p a t i e n t s .M e t h o ds Co mpa r i s o n b e t we e n t h e e x p e r i me n t a l
g r o u p a n d t he c o n t r o l g r o u p a f t e r 4 we e k s o f e ic f a c y a nd s i d e e f f e c t s ,
r e c u r r e nc e r a t e .Re s u l t s Th e t wo g r o u p s a te f r 4 we e k s of t r e a t me n t t h e t o t a l e f f e c t i v e r a t e we r e 8 3 . 7 8 % .9 6 % .f a r l e s s t h a n t h e c o n t r o l g r o u p t h e
销售培训PPT-仿制药项目进展及发展规划

11
Confidential ©2013 HEC
国内利好政策密集出台
FDA
SFDA
开展仿制药一致性评价,严格要求仿制药与被仿制药的一致性 国内GMP与WHO cGMP接轨:“软件硬件并重” 鼓励药品生产向优势企业集中(文号流转) 鼓励优势企业尽快通过认证(国际化企业优先审评/直接) 充分发挥价格杠杆作用(5%的定价优势) 集中采购优惠政策(招标采购“排他、优先”)
12 Confidential ©2013 HEC
“一报一批”——更快捷的“优先审评”
临床备案制
• 对优先审评的仿制药,探索实行生物等效性试验方案备案; • 生物等效性试验方案通过备案后,临床试验机构即可以开展试验。
一报一批
• 鼓励国内企业开展境外注册,对于国内企业在境内外同步开展研发和注 册的,接受其提交的境外试验资料。
19
2013年原料药项目计划
预计可完成注册批>20个
1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 阿齐沙坦酯钾 阿立哌唑 厄洛替尼 普瑞巴林 伊马替尼 特拉匹韦 利伐沙班 西格列汀 舒尼替尼 吉非替尼 索拉非尼 阿法替尼 阿瑞吡坦 替加环素 利拉利汀 瑞格菲尼 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. 30. 31. 32. 喹硫平 奥美沙坦酯 坎地沙坦酯 替格瑞洛 度洛西汀 右兰索拉唑 泮托拉唑钠 贝西沙星 Ponatinib 福沙吡坦 Cabozantinib 托法替尼 替诺福韦酯 阿利克仑 非布索坦 恩替卡韦
申报9个(已预约申
报时间)
22
© 2012 HEC R&D Center
处方点评与合理用药ppt课件

患者,男,53岁,诊断:滑囊炎 Rp:头孢克洛缓释片0.375*6片 1盒 1片
bid 口服 滑囊炎是关节腔的无菌性炎症,应使用非甾
体类抗炎药,使用抗生素不适宜。
15
患者,男,61岁, 诊断:膝关节痛,痛风性关节炎 Rp:NS500ml+克林霉素0.9 静滴+地塞米松
NS100ml+奥美拉唑40mg 静滴 qd
20
质子泵抑制剂使用指征不明
患者,男,47岁,诊断:中暑病 Rp: NS100ml+泮托拉唑60mg 静滴 st;GNS
500ml+Vitc2.0+VitB6 0.2静滴 st; 甲氧氯普安针10mg 肌注 st
21
给药途径不适宜
患者,男,34岁,诊断:巩膜炎 Rp: 左氧氟沙星滴眼液5ml*1支 0.1ml q2h 滴眼; 头孢克洛分散片0.125g*18片 2片 tid 口服 由于血眼屏障的存在,口服抗生素巩膜局部
处方超过3日用量,慢性病、老年病或特殊情 况下需要适当延长处方用量未注明理由的;
8
诊断不规范
发热、腹痛、腰痛、呕吐病 关节炎、肢痛、外科病、创伤病
9
不规范处方 用药不适宜处方 超常处方
10
适宜性审核内容包括:
– 规定必须做皮试的药品,处方医师是否注明过敏试 验及结果的判定;
– 处方用药与临床诊断的相符性; – 剂量、用法的正确性; – 选用剂型与给药途径的合理性; – 是否有重复给药现象; – 是否有潜在临床意义的药物相互作用和配伍禁忌; – 其它用药不适宜情况。
其血药浓度很难到达,局部使用滴眼液即可。
22
用法、用量不适宜的;
泮托拉唑钠肠溶片溶出度测定方法学验证

泮托拉唑钠肠溶片溶出度测定方法学验证赵嘉兰;王悦敏;秦凌浩【期刊名称】《广东化工》【年(卷),期】2018(45)3【摘要】目的对自制泮托拉唑钠肠溶片溶出度测定进行方法学验证,同时与市售产品进行对比研究.方法参考美国药典中泮托拉唑钠肠溶片溶出度测定方法,采用紫外分光光度法测定样品中药物吸光度,并对该方法进行了方法学验证.结果应用紫外分光光度法测定样品吸光度,溶出介质、辅料和滤膜吸附对测定无干扰,药物浓度在1~25 μg/mL范围内线性关系良好,回收率在95 %~101 %内,精密度RSD<2 %,样品在四小时内稳定性良好.结论该方法能够准确测定自制泮托拉唑钠肠溶片的溶出度,泮托拉唑钠肠溶片的耐酸力和溶出度均符合要求,与已上市参比制剂的释放行为相似.%Objective To methodologically validate a dissolution method for pantoprazole sodium enteric tablets. The self-made pantoprazole sodium enteric tablets was compared with reference listed drug. Methods The detection was carried out following the procedure described in the second method in United States Pharmacopoeia. The solubility of pantoprazole sodium enteric tablets was detected with ultraviolet spectrophotometry. We methodologically validated the dissolution method. Results The dissolution media, excipients and membrane adsorption did not interferer the determination of pantoprazole sodium in samples by UV. It showed good linearity in drug concentration from 1 μg/mL to 25 μg/mL. The recoveries ranged from 95 % to 102 %. The RSD of precision were less than2 % and the sample was stable in 4 hours. Conclusions The UV method is reliable .The drug release rate of self-made pantoprazole sodium enteric tablets is similar to reference listed drug.【总页数】2页(P10-11)【作者】赵嘉兰;王悦敏;秦凌浩【作者单位】广东药科大学药剂系,广东广州 510006;广东药科大学药剂系,广东广州 510006;广东药科大学药剂系,广东广州 510006【正文语种】中文【中图分类】TQ【相关文献】1.缬沙坦胶囊溶出度测定方法学验证 [J], 王巍2.酒石酸氢可酮片溶出度测定的方法学验证 [J], 杜敏3.茜草双酯片溶出度测定的方法学验证 [J], 彭刚;杨伟权;曾芳;康志英4.青蒿琥脂片溶出度测定的方法学验证 [J], 岳莉5.枳术宽中胶囊辅助泮托拉唑钠肠溶片治疗胃食管反流的疗效及对Gerd Q评分的影响 [J], 宋彬彬因版权原因,仅展示原文概要,查看原文内容请购买。
泮托拉唑钠肠溶片处方及工艺改进研究

泮托拉唑钠肠溶片处方及工艺改进研究肖俊峰;李冬;陈强;吴新荣【期刊名称】《中国药业》【年(卷),期】2016(25)1【摘要】目的:制备性质稳定的泮托拉唑钠肠溶片。
方法用单因素试验设计法对处方和工艺进行筛选。
结果与结论所制备的泮托拉唑钠肠溶片对湿热条件具有更好的稳定性,改进后的处方和工艺能明显提高泮托拉唑钠肠溶片成品的稳定性。
%To prepare a more stable formulation of Pantoprazole Sodium Enteric Tablets. Methods The prescription and process of Pan-toprazole Sodium Enteric Tablets were selected using single-factor design. Results Pantoprazole Sodium Enteric Tablets was obtained by the innovation of prescription and process has a better stability and appearance. Conclusion The quality of innovated Pantoprazole Sodium Enteric Tablets can be obviously improved.【总页数】3页(P17-19)【作者】肖俊峰;李冬;陈强;吴新荣【作者单位】中国人民解放军广州军区总医院药剂科药学部,广东广州 510000;中国人民解放军广州军区总医院药剂科药学部,广东广州 510000;中国人民解放军广州军区总医院药剂科药学部,广东广州 510000;中国人民解放军广州军区总医院药剂科药学部,广东广州 510000【正文语种】中文【中图分类】R460.6;R975+.6【相关文献】1.基于工艺改进的痛经宝颗粒处方精简研究 [J], 陈彦;张振海;王丽静;王绪颖;贾晓斌2.泮托拉唑钠肠溶胶囊的处方以及细微工艺改进措施研究 [J], 尹美艳;高蓉3.泮托拉唑钠肠溶片工艺改进研究 [J], 佟健4.泮托拉唑钠肠溶片的处方工艺研究 [J], 刘登5.硝酸钾牙用膜实训教学的处方工艺改进 [J], 许志罡因版权原因,仅展示原文概要,查看原文内容请购买。
泮托拉唑钠肠溶片治疗老年浅表性胃炎的临床效果观察
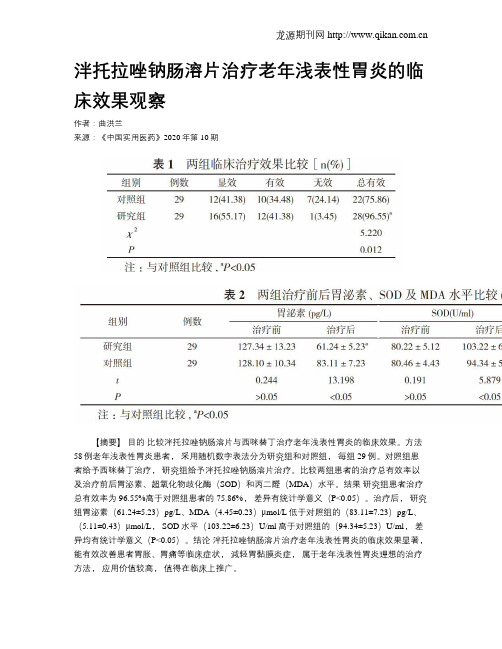
龙源期刊网 http://www.qikan.com.cn 泮托拉唑钠肠溶片治疗老年浅表性胃炎的临床效果观察 作者:曲洪兰 来源:《中国实用医药》2020年第10期
【摘要】 目的 比较泮托拉唑钠肠溶片与西咪替丁治疗老年浅表性胃炎的临床效果。方法 58例老年浅表性胃炎患者, 采用随机数字表法分为研究组和对照组, 每组29例。对照组患者给予西咪替丁治疗, 研究组给予泮托拉唑钠肠溶片治疗。比较两组患者的治疗总有效率以及治疗前后胃泌素、超氧化物歧化酶(SOD)和丙二醛(MDA)水平。结果 研究组患者治疗总有效率为96.55%高于对照组患者的75.86%, 差异有统计学意义(P<0.05)。治疗后, 研究组胃泌素(61.24±5.23)pg/L、MDA(4.45±0.23)μmol/L低于对照组的(83.11±7.23)pg/L、(5.11±0.43)μmol/L, SOD水平(103.22±6.23)U/ml高于对照组的(94.34±5.23)U/ml, 差异均有统计学意义(P<0.05)。结论 泮托拉唑钠肠溶片治疗老年浅表性胃炎的临床效果显著, 能有效改善患者胃胀、胃痛等临床症状, 減轻胃黏膜炎症, 属于老年浅表性胃炎理想的治疗方法, 应用价值较高, 值得在临床上推广。 龙源期刊网 http://www.qikan.com.cn 【关键词】 泮托拉唑钠肠溶片;浅表性胃炎;西咪替丁 DOI:10.14163/j.cnki.11-5547/r.2020.10.055 浅表性胃炎是一种随着人类饮食习惯改变而出现的消化系统疾病, 是胃黏膜呈慢性浅表性炎症的疾病, 为消化系统常见病, 属慢性胃炎中的一种[1]。可因嗜酒、喝浓咖啡、胆汁反流或因幽门螺杆菌感染等引起。患者可有不同程度的消化不良症状, 如进食后上腹部不适、隐痛, 伴嗳气、恶心、泛酸, 偶有呕吐[2]。中老年人有着较高的发病率, 好发于长期酗烟酗酒、不良饮食习惯等人群, 临床上经常表现为恶心、食欲不振、反酸等[3]。老年浅表性胃炎会降低其肠胃吸收营养功能, 大大影响其营养吸收, 不利于身心健康, 且还会导致一系列的并发症, 降低其生活质量。对于该疾病的治疗, 常采取药物的方式来进行, 如西咪替丁、泮托拉唑钠肠溶片等都是常见的药物[4, 5]。本研究选取本院在2018年7月~2019年7月收治的老年浅表性胃炎患者58例, 为两组老年浅表性胃炎患者分别实施西咪替丁治疗以及泮托拉唑钠肠溶片治疗, 分析其治疗效果, 择出疗效显著的方法, 积极改善患者的症状, 为临床治疗老年浅表性胃炎提供有效参考, 现总结如下。
泮托拉唑钠肠溶片在健康中国人体内的药动学研究及生物等效性评价(英文)
泮托拉唑钠肠溶片在健康中国人体内的药动学研究及生物等效性评价(英文)徐海燕;张鹏;王学娅;申涛;赵怀清【期刊名称】《中国药学:英文版》【年(卷),期】2007(16)3【摘要】目的评价健康受试者单剂量口服两种泮托拉唑钠肠溶片的人体药动学与生物等效性。
方法采用两种制剂两周期随机交叉试验设计,HPLC-UV法测定20名男性健康受试者单剂量口服40mg国产泮托拉唑钠肠溶片和进口泮托拉唑钠肠溶片后泮托拉唑的血药浓度。
采用非室模型计算药动学参数。
AUC,C_(max)对数转换后进行方差分析并计算90%可信区间。
结果国产和进口泮托拉唑钠肠溶片的药动学参数分别为:C_(max)(3610±956),(3466±1209)ng.mL^(–1),t_(max)(3.00±0.40),(3.00±0.46)h,AUC0–t(8140±5065),(8390±5474)ng.h.mL^(–1),AUC_(0–∞)(8293±5094),(8625±5606)ng.h.mL^(–1)。
t1/2(1.61±0.28),(1.85±0.27)h。
结论国产和进口泮托拉唑钠肠溶片具有生物等效性。
【总页数】6页(P170-175)【关键词】泮托拉唑;HPLC-UV;药动学;生物等效性【作者】徐海燕;张鹏;王学娅;申涛;赵怀清【作者单位】沈阳药科大学药学院;辽宁中医药大学职业技术学院【正文语种】中文【中图分类】R969.1【相关文献】1.盐酸甲氧氯普胺片在健康人体内药动学及生物等效性评价 [J], 周伊;朱运贵2.青霉素V钾胶囊在健康人体内的药动学与生物等效性评价 [J], 黄璞;刘亚妮;苏玉永;郑思维;马林;于捷飞3.西洛他唑片在健康人体内的药动学及生物等效性研究 [J], 符策浩4.泮托拉唑钠肠溶片在中国男性健康志愿者体内的药动学和相对生物利用度研究(英文) [J], 师少军;李忠芳;陈华庭;曾繁典因版权原因,仅展示原文概要,查看原文内容请购买。
泮托拉唑钠肠溶片不合理用药现状分析
泮托拉唑钠肠溶片不合理用药现状分析
王育惠
【期刊名称】《临床合理用药杂志》
【年(卷),期】2024(17)7
【摘要】目的分析医院泮托拉唑钠肠溶片的不合理用药现状。
方法抽取2020年1—3月漳州市第二医院门诊开具的含有泮托拉唑钠肠溶片的处方450份,收集处方中患者的性别、年龄、主诊断、次诊断和用药情况,分析泮托拉唑钠肠溶片用药目的、处方合理率、不合理用药分布状况。
结果使用泮托拉唑钠肠溶片的患者在各年龄段的男女比例差异不显著,使用年龄以>65岁为主,占比63.56%。
泮托拉唑钠肠溶片的用药目的中,排名前三的是预防抗血小板药物引起的胃黏膜损伤(占41.56%)、胃食管反流病(占21.56%)和消化性溃疡(占14.00%)。
泮托拉唑钠肠溶片的处方合理率为93.78%,不合格率为6.22%。
不合理用药类型主要为无适应证用药(占75.00%)和无预防性用药指征用药(占25.00%)。
结论泮托拉唑钠肠溶片不合理用药类型主要为无适应证用药和无预防性用药指征用药。
【总页数】4页(P130-133)
【作者】王育惠
【作者单位】福建省漳州市第二医院药剂科
【正文语种】中文
【中图分类】R47
【相关文献】
1.我国静脉用药调配中心不合理医嘱现状的文献计量学分析
2.我院中药饮片处方不合理用药现状分析及干预措施
3.某院儿科门诊抗菌药物用药现状及不合理用药原因分析
4.宫颈癌患者的不合理用药医嘱现状分析
5.耳鼻咽喉头颈外科不合理用药现状与分析
因版权原因,仅展示原文概要,查看原文内容请购买。
安徽省物价局关于部分药品价格不予审批的函-皖价医函[2010]126号
安徽省物价局关于部分药品价格不予审批的函正文:---------------------------------------------------------------------------------------------------------------------------------------------------- 安徽省物价局关于部分药品价格不予审批的函(皖价医函〔2010〕126号)有关药品生产经营企业:根据《国家发展改革委药品定价目录》、《安徽省药品定价目录》、《药品差比价规则》和《国家发展改革委关于调整〈国家发展改革委定价药品目录〉等有关问题的通知》(发改价格〔2010〕429号)等有关规定,我局对6月份申请办理政府定价药品最高零售价格的报告进行了审核。
对不符合政府定价要求的,不予审批。
现公布不予审批的品种及原因(见附件)。
今后在办理药品价格审批前,请仔细阅读我局网站上的《公告》。
二〇一〇年七月二十三日附件1:窗口受理药品价格不能审批表金额单位:元序号受理号药品名称剂型规格单位申报价格不能审批的原因生产厂家15104214甲钴胺胶囊0.5mg×20粒盒40不属省定价范围河北海鸿医药25104214甲钴胺胶囊0.5mg×30粒盒56不属省定价范围河北海鸿医药35104229断血流糖衣片0.3g×70片瓶58安庆乘风制药45104229断血流薄膜衣片0.35g×24片盒35.82009医保国家定价安庆乘风制药55104229断血流薄膜衣片0.35g×48片盒52.82009医保国家定价安庆乘风制药65104229断血流薄膜衣片0.35g×60片盒62.8安庆乘风制药75104246垂盆草片剂0.32g×36片盒不属政府定价甘肃佛仁制药85104246垂盆草片剂0.32g×60片盒不属政府定价甘肃佛仁制药95104248活血止痛膏膏剂7×10×2片盒12已公布价格湖北舒尔迈康药业105104249硫酸庆大霉素滴眼液8ml:4万单位/支*8ml/支*1支/盒支7.8提供资料不全长春迪瑞制药115104252精蛋白重组人胰岛素注射剂3ml:300国际单位(笔芯)支73.12009医保国家定价珠海联邦制药125104253复方银翘氨敏胶囊复方24粒粒22.5提供资料不全新疆全安药业135104253复方银翘氨敏胶囊复方36粒粒33.4提供资料不全新疆全安药业145104272兰索拉唑口崩片15mg×10片盒87.1不属于省定价天津武田155104272兰索拉唑口崩片30mg×10片盒148不属于省定价天津武田165104255氯化钾氯化钠注射剂100ml:氯化钾0.11g:氯化钠0.9g瓶6新药暂执行市场价四川奇力制药175104255氯化钾氯化钠注射剂100ml:氯化钾0.22g:氯化钠0.9g 瓶7新药暂执行市场价四川奇力制药185104255氯化钾氯化钠注射剂100ml:氯化钾0.30g:氯化钠0.9g 瓶8新药暂执行市场价四川奇力制药195104256氨金黄敏颗粒剂9袋盒15提供资料不全四川百利药业205104256氨金黄敏颗粒剂12袋盒19.8提供资料不全四川百利药业215104256氨金黄敏颗粒剂18袋盒29.3提供资料不全四川百利药业225104261酒石酸罗格列酮胶囊4mg×7粒盒66新药暂执行市场价辅仁药业集团23510427750/50混合重组人胰岛素注射液300IU:3ml支682009医保国家定价通化东宝药业245104287重组人绒促性素注射剂250μg支2602009医保国家定价默克雪兰诺公司255104292安他唑啉片剂100mg*6片/板*2板盒60不属省定价范围安阳玉威制药有限公司265104293非洛地平缓释片(Ⅱ)缓释片5mg*7片盒23.1新药暂执行市场价合肥立方制药有限公司275104293非洛地平缓释片(Ⅱ)缓释片5mg*14片盒45.05新药暂执行市场价合肥立方制药有限公司285104293非洛地平(Ⅱ)缓释片5mg*10片盒32.57新药暂执行市场价合肥立方制药有限公司295104293非洛地平(Ⅱ)缓释片5mg*20片盒63.52新药暂执行市场价合肥立方制药有限公司305104294喷托维林氯化铵片剂复方×12片盒28.5与喷托维林相比差别太大,需专家论证西南药业股份315104294喷托维林氯化铵片剂复方,24片盒55.6同上西南药业股份325104295单硝酸异山梨酯注射液5ml:20mg/支盒36.5已公布价格南京臣功制药335104295单硝酸异山梨酯缓释片60mg×10片盒32已公布价格南京臣功制药345104295硝酸咪康唑栓剂0.2g×7枚盒13.8已公布价格南京臣功制药355104296阿莫西林克拉维酸钾(7:1)干混悬剂228.5mg×8包盒17.5已公布价格南京臣功制药365104297胶囊剂0.36g*24粒盒39.82009医保国家定价浙江维康药业有限公司375104297骨刺胶囊胶囊剂0.36g*36粒盒592009医保国家定价浙江维康药业有限公司385104299布洛芬软胶囊0.1g×12盒14.8国家基本药物不符合差比价规则石药集团恩必普药业395104299布洛芬软胶囊盒28.9国家基本药物不符合差比价规则石药集团恩必普药业405104299布洛芬软胶囊0.2g×12盒25.2国家基本药物不符合差比价规则石药集团恩必普药业415104300左氧氟沙星注射液2ml:0.2g支3.7已公布价格宁波市天衡制药425104300左氧氟沙星注射液支5.1已公布价格宁波市天衡制药435104311阿米卡星洗剂100ml:250mg 瓶72.6不属于省定价四川方向药业445104314盐酸氮卓斯汀滴眼剂0.05%*6ml瓶48不属于省定价广东众生药业455104316双氯芬酸钠肠溶胶囊50mg*10粒盒15.8不属于省定价范围永信药品工业(昆山)465104316双氯芬酸钠肠溶胶囊50mg*20粒盒30.8不属于省定价范围永信药品工业(昆山)475104318脂溶性维生素(I)冻干粉针(配专用溶媒)复方制剂,每支含维生素A棕榈酸酯(相当于维生素A)0.23万单位;维生素D2 10μg;维生素E 6.4mg;维生素K1 0.2mg 支66属成本监审延期马鞍山丰原制药485104318脂溶性维生素(I)冻干粉针(预充式)复方制剂,每支含维生素A棕榈酸酯(相当于维生素A)0.23万单位;维生素D2 10μg;维生素E 6.4mg;维生素K1 0.2mg 支66属成本监审延期马鞍山丰原制药495104319丹参滴注液注射液250ml:16g瓶38属成本监审延期安徽天洋药业505104319丹参滴注液注射液250ml:12g瓶30.5属成本监审延期安徽天洋药业515104550小儿咽扁颗粒剂8g*10袋盒基药补充品种暂执行原来价格贵州神奇药业525104279酒石酸溴莫尼定滴眼剂0.15%,5ml瓶96.2提供资料不全上海永裕医药535104281银黄咀嚼片0.92g盒13属成本监审延期安徽联谊药业545104728鼻窦炎口服液10ml*6支盒17已有价格,不予提价太极集团5104746碳酸钙D3片片剂30片瓶34.42009医保国家定价惠氏制药565104746碳酸钙D3片片剂60片瓶67.62009医保国家定价惠氏制药附件2:电子邮件受理药品价格不能审批表西药部分序号药品名称剂型规格单位申报价格不能审批的原因生产厂家联系人备注1阿莫西林克拉维酸钾片剂0.2285g×8片盒已公布价格哈药集团制药总厂苏雷158****39912阿莫西林胶囊剂0.25g×50粒盒15已公布价格山西兰花七佛山制药有限公司毕长征************3阿莫西林胶囊剂0.25g×20粒6.2已公布价格山西兰花七佛山制药有限公司毕长征************4阿莫西林胶囊剂0.25g×24粒盒7.4已公布价格山西兰花七佛山制药有限公司毕长征************5阿司匹林肠溶片25mg×30片×2板盒4.5已公布价格亚宝药业大同制药有限公司丁锐138****98486氨酚羟考酮胶囊剂盐酸羟考酮5mg对乙酰氨基酚500mg×10粒61.3不符合差比价计算北京勃然制药有限公司汪雍蓉138****56527氨咖黄敏胶囊复方12粒盒8.6已公布价格多多药业有限公司宋磊133****47778奥美拉唑冻干粉针(配溶媒)40mg支143已公布价格阿斯利康制药有限公司赵永春158****99339奥美拉唑40mg支143已公布价格阿斯利康制药有限公司赵永春158****993310奥美拉唑肠溶片20mg×14片盒215已公布价格阿斯利康制药有限公司赵永春158****993311丙泊酚注射剂50ml:0.5g支284已公布价格阿斯利康制药有限公司赵永春158****993312布洛芬10ml×6支盒20不属于差比价神威药业有限公司王瑞宾133****918813长春瑞宾软胶囊剂20mg×2粒盒401不符合差比价江苏豪森药业股份有限公司钮金梅139****452514单硝酸异山梨酯注射液5ml:20mg×6支盒36.5已公布价格南京臣功制药张迷139****604915单硝酸异山梨酯注射液250ml:20mg袋42已公布价格山东鲁抗辰欣药业有限公司胡美洋133****666716丁酸氢化可的松乳膏剂10g:10mg支15.60已公布价格上海新亚药业闵行有限公司17多潘立酮片剂10mg盒20.1规格不全西安博华制药有限责任公司李原************18复方氨酚烷胺胶囊剂0.4g×12粒盒11.28已公布价格贵州正鑫药业有限公司钟利春************19复方胃蛋白酶复方颗粒10g×12袋盒12已公布价格成都蓉药集团四川长威制药有限公司陈锦梅************20腹膜透析液(乳酸盐)(低钙)注射剂2000ml×1.5%袋33.28已公布价格天津天安药业股份有限公司杭苏强136****487821腹膜透析液(乳酸盐)(低钙)注射剂2000ml×2.5%袋33.28已公布价格天津天安药业股份有限公司杭苏强136****487822腹膜透析液(乳酸盐)(低钙)注射剂2000ml×4.0%袋33.28已公布价格天津天安药业股份有限公司杭苏强136****487823甘油果糖注射液250ml:25g(软袋、双阀)袋56.9不符合差比价提供注册批件山东鲁抗辰欣药业有限公司胡美洋133****666724红霉素肠溶片0.125g×100s×240瓶瓶19已公布价格安徽金太阳生化药业有限公司徐杰139****867325琥乙红霉素颗粒剂0.1g×12袋盒3.4已公布价格上海中瀚投资集团宁国国安邦宁药业有限公司曹逸隆138****454526肌苷氯化钠注射液100ml:0.6g:0.9g塑瓶23.5已公布价格福州海王福药制药有限公司王英*************27肌苷氯化钠注射液100ml:0.5g(软袋、双阀)袋24.1不符合差比价提供注册批件山东鲁抗辰欣药业有限公司胡美洋133****666728甲磺酸罗哌卡因注射剂20ml:178.8mg支74.8已公布价格山东鲁抗辰欣药业有限公司胡美洋133****666729抗感片片剂0.6g×36片盒43不属于政府定价成都蓉药集团四川长威制药陈锦梅************30克林霉素冻干粉针剂1.2g冻干粉瓶45.7已公布价格江苏吴中医药集团有限公司苏州第六制药厂范宝运139****444931克霉唑乳膏10g:0.3g支2.3已公布价格重庆科瑞制药32克霉唑乳膏10g:100mg支1.2已公布价格天津药业集团33口服葡萄糖散剂500g包7.16不符合差比价成都蓉药集团四川长威制药陈锦梅************34老年咳喘片剂12片×3板盒20不属于政府定价成都蓉药集团四川长威制药陈锦梅************35铝碳酸镁咀嚼片0.5g×30粒盒22.9不符合差比价南通久和药业有限公司张小平139****508036门冬氨酸钾镁冻干粉1g支11.5已公布价格山西普德药业有限公司居玉宇133****857737门冬氨酸钾镁冻干粉2g支19.5已公布价格山西普德药业有限公司居玉宇133****857738门冬氨酸洛美沙星葡萄糖注射剂100ml:0.2g:5g瓶28已公布价格海南长安国际制药有限公司董静文139****377639门冬氨酸洛美沙星葡萄糖注射剂100ml:0.2g瓶22.6已公布价格青州尧王制药有限公司杨广峰186****152140萘普生缓释片250mg×12片盒17.1有文件41柠檬烯胶囊75mg(柠檬烯油)×45粒盒51.1不属于政府定价成都蓉药集团四川长威制药陈锦梅************42柠檬烯胶囊75mg(柠檬烯油)×60粒盒67.4不属于政府定价成都蓉药集团四川长威制药陈锦梅************43柠檬烯胶囊75mg(柠檬烯油)×100粒盒83.6不属于政府定价成都蓉药集团四川长威制药陈锦梅************44诺氟沙星胶囊0.1g×12粒×5板盒9.7已公布价格亚宝药业大同制药有限公司丁锐138****984845诺氟沙星胶囊剂0.1g×50片盒7.3已公布价格山西兰花七佛山制药有限公司毕长征************46泮托拉唑冻干粉针剂60mg支98.6已公布价格哈药集团三精加滨药业有限公司宋彦峰189****606847葡萄糖氯化钠注射剂50ml:2.5g:0.45g袋9.3已公布价格湖南康源制药有限公司唐静娴*************48葡萄糖氯化钠注射剂100ml:5g:0.9g袋9.6已公布价格湖南康源制药有限公司唐静娴*************49葡萄糖氯化钠注射剂250ml:12.5g:2.25g袋10.3已公布价格湖南康源制药有限公司唐静娴*************50葡萄糖氯化钠(软袋,双阀)注射液100ml:5g:0.9g袋已公布价格山东齐都药业有限公司张玮***********51葡萄糖氯化钠(软袋,双阀)注射液250ml:12.5g:2.25g袋9.8不符合差比价提供注册批件山东齐都药业有限公司张玮***********52青霉素V钾胶囊剂0.236g×24粒盒10.6重复四川制药制剂有限公司53青霉素V钾胶囊剂0.236g×48粒盒重复四川制药制剂有限公司54曲安奈德益康唑乳膏剂复方0.1%曲安奈德和1%硝酸益康唑盒15规格不全上海朝晖药业有限公司贾俊139****926755曲安奈德益康唑乳膏剂15g支17.5规格不全沈阳圣元药业有限公司卢秀娟************56去痛片(索米痛)片剂复方2000片80.8已公布价格多多药业有限公司宋磊133****477757乳酸左氧氟沙星分散片剂0.2g×6片盒12.4已公布价格海口奇力制药股份有限公司张转意6683083158乳酸左氧氟沙星分散片剂0.2g×18片盒35.9已公布价格海口奇力制药股份有限公司张转意6683083159乳酸左氧氟沙星分散片剂0.2g×24片盒47.3已公布价格海口奇力制药股份有限公司张转意6683083160双氯芬酸钠肠溶片25mg×24片板2.8已公布价格吉林省银河制药厂赵晓旭*************61双氯芬酸钠肠溶胶囊(微丸型)50mg×10粒盒15.8已公布价格永信药品工业(昆山)有限公司62双氯芬酸钠肠溶胶囊(微丸型)50mg×20粒盒30.8已公布价格永信药品工业(昆山)有限公司63缩宫素注射剂10单位瓶24.5已公布价格南京新百药业有限公司梅巍158****051264酮康唑乳膏10g:0.2g支9.2已公布价格重庆科瑞制药头孢哌酮钠舒巴坦钠粉针剂0.75g支21.0已公布价格山东润泽制药有限公司吴丽芳************66头孢哌酮钠舒巴坦钠粉针剂2.25g支40.04已公布价格山东润泽制药有限公司吴丽芳************67头孢哌酮钠舒巴坦钠(2:1)注射剂1.5g(配一次性使用预充注射式溶药器(带针))(2:1)支29.6已公布价格汕头金石粉针剂有限公司李洁*************头孢哌酮钠舒巴坦钠(2:1)注射剂3.0g(配一次性使用预充注射式溶药器(带针))(2:1)支50.3已公布价格汕头金石粉针剂有限公司李洁*************69头孢曲松钠注射剂0.5g(配一次性使用预充注射式溶药器(带针))支4.12已公布价格汕头金石粉针剂有限公司李洁*************70头孢他啶溶媒结晶粉针剂0.75g支14.4已公布价格深圳致君制药有限公司朱阳阳*************71头孢他啶(含精氨酸)注射剂0.75g(配一次性使用预充注射式溶药器(带针))支17.1已公布价格汕头金石粉针剂有限公司李洁*************72头孢他啶(精氨酸)溶媒结晶粉针剂0.75g支已公布价格哈药集团制药总厂苏雷158****399173维生素C丸剂(糖丸)0.1g×100丸瓶3.5已公布价格吉林市鹿王制药股份有限公司董波*************74维生素C丸剂(糖丸)0.05g×100丸瓶2.1已公布价格吉林市鹿王制药股份有限公司董波*************75西替利嗪口服溶液100ml×100mg瓶22.4已公布价格北京韩美药品有限公司胡新国139****876776仙灵脾颗粒10g×12袋盒18规格不全成都蓉药集团四川长威制药陈锦梅************77盐酸洛美沙星滴眼剂8ml瓶19.9规格不全沈阳圣元药业有限公司卢秀娟************78盐酸洛美沙星滴眼剂8ml:24mg支12.9重复江苏汉晨药业有限公司张敏138****215879盐酸洛美沙星滴眼剂10ml:30mg支15.3重复江苏汉晨药业有限公司张敏138****215880盐酸诺美沙星滴眼剂10ml:30mg盒22.6重复武汉诺安药业有限公司聂万民************81盐酸诺美沙星滴耳液5ml:15mg盒10.9重复武汉诺安药业有限公司聂万民************82盐酸诺美沙星滴耳液8ml:24mg盒15.8重复武汉诺安药业有限公司聂万民************83盐酸诺美沙星滴耳液10ml:30mg盒18重复武汉诺安药业有限公司聂万民************84盐酸诺美沙星滴眼剂8ml:24mg盒14.8重复武汉诺安药业有限公司聂万民************85盐酸羟甲唑啉滴眼液10mg×10片瓶33.3剂型与规格不符成都恒瑞制药有限公司汪林133****201386盐酸左氧氟沙星胶囊0.1g(以左氧氟沙星计)×18粒盒21.6已公布价格安徽三精万森制药有限公司周文妹138****380587盐酸左氧氟沙星胶囊0.1g(以左氧氟沙星计)×10粒盒12.8已公布价格安徽三精万森制药有限公司周文妹138****380588盐酸左氧氟沙星胶囊0.1g(以左氧氟沙星计)×20粒盒25.2已公布价格安徽三精万森制药有限公司周文妹138****380589盐酸左氧氟沙星胶囊0.1g(以左氧氟沙星计)×12粒盒15.6已公布价格安徽三精万森制药有限公司周文妹138****380590盐酸左氧氟沙星胶囊0.1g(以左氧氟沙星计)×24粒盒30.06已公布价格。
销售培训-仿制药项目进展及发展规划
22
© 2012 HEC R&D Center
2013制剂中国项目
2013年计划申报25个项目
常规项目15个 1. 注射用泮托拉唑钠 2. 罗氟司特/班布特罗片 3. 西替利嗪颗粒 4. 奥氮平片 5. 克拉霉素缓释片 6. 厄贝沙坦片 7. 盐酸莫西沙星片 8. 苯磺酸氨氯地平片 9. 他克莫司乳膏 10. 瑞苏伐他汀钙片 11. 氯吡格雷片 12. 苯丙哌林干混悬剂 13. 匹伐他汀钙片 14. 克拉霉素干混悬剂 15. 琥珀酸美托洛尔缓释片
料药疗
部三工分三法法三
部包器
部艺析部规规部
材械
硕士
三三
部部
57%
部部
博士
2%
4
Confidential ©2013 HEC
仿药所专家:
Rajiv 博士 印度专家
张绪穆教授 知名化学家
李守峰 博士 制剂专家
波曼 博士
辛格 博士
前Ranbaxy资深专家 资深法规专家
勇特 博士 前拜耳资深科学家
梁晓忠 博士 分析科学家
上 市
项目调研
立项
成立项目组 项目计划书
项目开发
技术转移
DQA
8
© 2012 HEC R&D Center
ARC(分析技术&法规协调会议)
ARC/PRC
原料药 分析
制剂 分析
基地 QC
国内 法规
国外 法规
ATS
项目组
仿药质量一体化
9
Confidential ©2013 HEC
公司仿制药面临的历史机遇
部 三部 三部 三部 三部 三部 S 部* 包装* 器械*
100
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
资料1、药品名称一、药品名称通用名:泮托拉唑钠肠溶片英文名:Pantoprazole Sodium Enteric-Coated Tablets汉语拼音:Pantuolazuona Changrongpian本品主要成分为5-二氟甲氧基-2-{[(3,4-二甲氧基-2-吡啶基)-甲基]亚硫酰基}-1H-苯骈咪唑钠盐-水合物。
其化学名称为:泮托拉唑钠。
其化学结构式为:分子式:C16H14F2N3NaO4S•H2O分子量:423.38二、命名依据参考国家食品药品监督管理局国家药品标准标准,标准号:WS1-(X-120)-2003Z泮托拉唑钠肠溶片标准,并参照《中国药品通用名称》的命名原则,将本品命名为:泮托拉唑钠肠溶片。
资料2、证明性文件1、*************有限公司《营业执照》复印件。
2、*************有限公司《药品生产许可证》复印件。
3、*************有限公司《药品生产质量管理规范》证书复印件。
4、保证书。
5、直接接触药品的包装材料和容器的《药品包装材料和容器注册证》复印件。
保证书我们申请注册的泮托拉唑钠肠溶片,属已有国家药品标准产品,药物的处方、工艺,对他人的专利不构成侵权。
对可能的侵权,申请人承担由此造成的一切法律责任。
申请人:*************有限公司资料3、立题目的与依据一、立题目的与依据应激性溃疡出血是急性脑出血早期的严重并发症之一,其死亡率达87.9%,应激性溃疡一旦形成,患者的预后相当严重,因此尽快有效的控制应激性溃疡出血,可以降低患者的病死率。
应激性溃疡伴有胃酸高度的分泌,受神经、体液调节。
急性脑出血使患者的颅内压急剧升高,可导致脑干出血或受压,丘脑植物神经中枢受损或直接刺激迷走神经核引起胃酸的分泌,在胃酸的作用下胃粘膜发生溃疡,形成溃疡出血。
因此治疗的关键是抑制胃酸的分泌。
消化性溃疡和急性胃粘膜病变出血也都是酸相关性疾病,制酸能有效促进血液的凝固和溃疡的愈合。
泮托拉唑钠是一种新型的质子泵抑制剂,已被明确证明是分子水平的药物。
泮托拉唑钠为质子泵抑制剂。
通过作用于胃腺壁细胞,抑制H+、K+-ATP酶的活性,使壁细胞内的H+不能运转到胃中,从而抑制了胃酸的分泌。
本品还能减少胃液分泌量并抑制胃蛋白酶的分泌及其活性。
泮托拉唑钠在中性和弱酸性条件下相对稳定,在强酸性条件下迅速活化,其pH依赖的活化特性,使其对H+、K+-ATP酶的作用具有更好的选择性。
本品能特异性地抑制壁细胞顶端膜构成的分泌性微管和胞浆内的管状泡上的H+、K+-ATP酶,引起该酶不可逆性的抑制,从而有效地抑制胃酸的分泌。
由于H+、K+-ATP酶是壁细胞泌酸的最后一个过程,故本品抑酸能力强大。
它不仅能非竞争性抑制促胃液素、组胺、胆碱引起的胃酸分泌,而且能抑制不受胆碱或受体阻断剂影响的部分基础胃酸分泌。
H2泮托拉唑钠肠溶片口服吸收不规则,滞后时间达 2.46h,T为 3.35h,血浆半衰期为max1.18h,血浆蛋白结合率为92%,其体内过程符合一级吸收双室模型。
其生物利用度在75%以上,主要在肝脏代谢,但与细胞色素P450很少相互作用;经肾脏消除,大约80%以代谢产物的形式经尿排泄,血浆清除率为11L/h。
[1]泮托拉唑钠通过肝细胞内的细胞色素P450酶系的第I系统进行代谢,同时也可以通过第II系统进行代谢。
当与其它通过P450酶系代谢的药物伍用时,本品的代谢途径可以通过第II 酶系统进行,从而不易发生药物代谢酶系的竞争性作用,减少体内药物间的相互作用。
泮托拉唑钠主要用于:(1)活动性消化性溃疡(胃、十二指肠溃疡);(2)反流性食管炎;(3)卓-艾氏综合征。
十二指肠溃疡、胃溃疡和反流性食管炎,每日早晨口服一片。
十二指肠溃疡疗程通常为2~4周,胃溃疡和反流性食管炎疗程通常为4~8周。
泮托拉唑钠不良反应较少,偶见头晕、失眠、嗜睡、恶心、腹泻、便秘、皮疹和肌肉疼痛等症状。
综上所述,为保证药物疗效,满足临床患者的用药需要,改善临床用药顺应性,增加临床医师的用药选择,我们研制了泮托拉唑钠肠溶片。
二、国内研发现状目前,国内已有的泮托拉唑钠生产厂家有:泮托拉唑钠肠溶胶囊:湖南省岳阳市制药三厂40mg、杭州中美华东制药有限公司。
泮托拉唑钠:湖南省岳阳市制药三厂、杭州中美华东制药有限公司、沈阳东宇药业有限公司、锦州九泰药业有限责任公司。
注射用泮托拉唑钠:南京长澳制药有限公司、杭州中美华东制药有限公司。
泮托拉唑钠肠溶片:锦州九泰药液有限责任公司、沈阳东宇药业有限公司。
三、分类依据根据目前泮托拉唑钠肠溶片国内已上市销售药品的规格为40mg,考虑用药方便和准确性,我们研制的泮托拉唑钠肠溶片的规格定为40mg(以C16H15F2N3O4S计)。
根据《药品注册管理办法》(试行)附件二:化学药品注册分类及申报资料要求:一、注册分类(6)已有国家药品标准的原料药或者制剂,本品应为化学药品注册6类药。
资料4、主要研究结果的总结和评价根据《药品注册管理办法》(试行)规定化学药品第6类(已有国家药品标准的制剂)的各项申报资料的要求,我们现已完成了泮托拉唑钠肠溶片报临床研究工作,现就研究结果作如下总结:一、制剂处方及工艺1、素片规格及处方规格40mg(以C16H15F2N3O4S计)处方解析:2、隔离层包衣液处方:3%羟丙甲纤维素水溶液。
3、肠溶层包衣液采用卡乐康公司93O92157型水性肠溶包衣粉。
4、制备工艺及控制要点:A 制备工艺(1)、将原辅料分别过100目筛。
(2)、称取处方量的原辅料过100目筛混合均匀。
加入纯净水混合制成软材,用24目筛制粒;35℃干燥。
(3)、过24目筛整粒。
(4)、加入滑石粉混合均匀(5)、中间品检测含量,确定片重,选择Φ6.5mm浅凹冲模压片。
(6)、按处方配制隔离层包衣液,包隔离衣层。
雾化压力0.25Mpa,40℃干燥后包肠溶衣。
(7)、肠溶型薄膜包衣液,包肠溶型薄膜衣,连续喷雾包衣,于40℃以下干燥。
(8)包装。
(9)全检,入库。
B 工艺控制要点:(1)原辅料必须过100目筛并充分混匀。
(2)素片包隔离衣开始时应将包衣机间歇启动,直至片面形成一层明显衣膜后,再进行连续包衣。
(3)全过程干燥温度低于45℃。
由上述试验可见,本公司研制的泮托拉唑钠肠溶片处方合理,工艺简单,所采用的辅料,来源易得,价格低廉,适合于工业生产。
二、质量研究及质量标准的总结根据国家药品标准泮托拉唑钠肠溶片质量标准WS1-(X-120)-2003Z进行质量研究,并制定质量标准。
1、含量限度本品为泮托拉唑钠与适量辅料制成的片剂。
采用分光光度法测定本品含量,根据各批样品测定及稳定性试验考察结果,将本品含量限度规定为:含泮托拉唑钠以泮托拉唑(C16H15 F2N 3O4S)计,应为标示量的90.0%~110.0%。
订入质量标准(草案)2、性状根据原辅料来源可能不同及药品贮存条件、稳定性考察结果,将本品性状定为:本品为肠溶衣片,除去包衣后显白色或类白色。
订入质量标准(草案)3、鉴别(1)化学鉴别法,参照泮托拉唑钠肠溶片WS1-(X-120)-2003Z质量标准项下方法,取本品,除去薄膜衣,研细,取细粉适量(约相当于泮托拉唑钠10mg),加水20ml,振摇使泮托拉唑钠溶解,滤过,取滤液2ml,加稀盐酸5滴,滴加硅钨酸试液,各批样品均产生白色絮状沉淀。
另经本品辅料的干扰试验,结果表明本品的辅料不干扰本试验的测定,将此项订入质量标准(草案)中。
(2)采用分光光度法,以最大和最小吸收波长作为本品的鉴别依据,方法灵敏,专属性强。
将此项订入质量标准(草案)中。
4、检查(1)有关物质采用高效液相色谱法。
经试验,确定用十八烷基硅烷键合硅胶为填充剂;以磷酸盐缓冲液(取磷酸氢二钠1.12g与磷酸二氢钠0.18g,加水溶解并稀释至1000ml)-乙腈(62:38)为流动相,检测波长为288nm。
系统适用性试验和破坏性试验表明该色谱条件能成功分离主峰与各杂质峰。
经试验,本品空白辅料无干扰、供试品溶液在5小时内稳定、本法精密度好。
根据各批样品测定结果及稳定性试验考察结果,将本品有关物质限度订为1.5%。
(2)释放度经试验确定检查方法为:照释放度测定法(中国药典2000年版二部附录Ⅹ D 第二法),以0.1mol/L盐酸溶液900ml为溶剂,转速为每分钟100转,依法操作,经30分钟取样测定。
线性关系试验、回收率试验、稳定性和精密度试验等证明:采用紫外分光光度法测定,方法可行;重现性试验、工艺稳定性考察试验结果表明本品工艺稳定。
根据样品测定结果及稳定性试验考察结果将限度规定为75%。
(3)耐酸力泮托拉唑钠肠溶片为肠溶制剂,不但模拟药物在肠道能定位释放,而且还要保证药物的胃液中不释放或不崩解,因此我们采用以0.1mol/L盐酸溶液900ml为溶剂,转速为每分钟100转,依法操作,经2小时,供试品片均不得有裂缝或崩解现象,以更好的模拟肠溶片在胃液环境中耐酸情况。
另经线性、及重现性方法验证,本方法可用于泮托拉钠肠溶片耐酸力的测定。
(4)微生物限度照中国药典2000年版二部附录Ⅺ J检查,本品各批样品均符合规定。
将此项订入质量标准(草案)中。
5、含量测定采用分光光度法测定本品含量。
经线性关系试验、回收率试验、精密度和稳定性试验,结果均比较满意。
泮托拉唑钠溶液在10.92~18.72μg/ml浓度范围内其浓度与吸收值呈良好的线性关系。
回收率试验中平均回收率为99.9%,RSD=0.41%(n=9),表明本法准确度好;精密度试验中RSD=0.30%(n=6),表明本法精密度好;供试品溶液5小时稳定性试验中RSD=0.25%,表明供试品溶液在5小时内稳定。
经检测,各批样品均符合规定。
6、类别本品属消化系统用药。
7、规格根据本品用法用量制订。
8、贮藏根据本品稳定性试验结果制订。
9、有效期根据本品稳定性试验结果,暂定为二年。
质量研究结果表明,本公司制定的质量标准可较好控制泮托拉唑钠质量,所采用的检测方法简单、准确,重复性好,可行性强。
三、稳定性研究总结和评价根据中国药典2000年版二部附录ⅪⅩ C 药物稳定性试验指导原则,取本品中试样品进行影响因素试验、加速试验和长期试验。
影响因素试验结果表明:本品经影响因素考察10天,有关物质略有增大,但均在0.5%以下。
其他各项指标均无明显变化,说明本品处方合理,质量稳定。
本品在高湿条件下吸湿明显,故本品应遮光,密封保存。
加速试验结果表明:本品按市售包装,在温度40±2℃,相对湿度75%±5%的条件下经6个月考察,有关物质略有增加,含量略有下降,其他各项指标均无明显变化。
试验表明本品在上述条件下基本稳定。
长期试验结果表明:本品按市售包装,在温度25±2℃,相对湿度60%±10%的条件下经12个月考察,各项指标均无明显变化。
