第七章醇、硫醇、酚
第七章醇酚醚

[教学目的] 通过本章的学习,使学生掌握醇、 酚、醚的性质。 [教学重点] 本章的重点是醇的化学性质,包括 取代反应和消除反应等,可以和上一章 卤烃的化学性质相比较。 [教学难点] 醇脱水反应历程
第七章 醇酚醚—教学要求
[教学基本要求] 一、醇酚醚的结构和命名 二、醉酚醚的物理性质 三、醇的化学性质 1、醇金属的生成 2、卤烃的生成,酸的催化作用 3、与无机酸作用 4、脱水反应 5、氧化与脱氢反应
酸性:醇小于水——醇比水反应缓和。 碱性:烷氧负离子大于氢氧负离子 ——醇钠可以水解
第七章 醇酚醚—化学性质(似水性)
醇的反应活性:
解释:电子效应:烷基(+I)
第七章 醇酚醚—化学性质(似水性)
(2)生成yang盐
+ ROH +
H2O
HCl HCl
H3O
+
+ +
Cl- ( 水 合 氢离 子 ) Cl- ( 佯 离 子)
(4)对甲苯磺酰氯
(ROTs)
第七章 醇酚醚—化学性质(与酸作用)
(5)羧酸、
(6)酰卤 ROH+R`COX R`COOR+HX
第七章 醇酚醚—化学性质(脱水) 5;1°
第七章 醇酚醚—化学性质(脱水)
第七章 醇酚醚—化学性质(脱水) (2)分子间脱水
第七章 醇酚醚—化学性质(与HX作用) 机理:亲核取代 伯醇SN2 :
叔醇SN1:
第七章 醇酚醚—化学性质(与HX作用)
烯丙醇、苄醇及仲醇可能也是SN1。 有些反应有重排:
第七章 醇酚醚—化学性质(与HX作用)
H迁移
第七章 醇酚醚—化学性质(与HX作用)
有机化学 - 第七章 - 醇和硫醇,醚和硫醚
OH O
C rO 3 2 C 5H 5N O O
O
O
1 醇
o
2 醇
o
3 醇
o
C r O 3 -H 2 S O 4
无 反 应 ( 3 o醇 )
橙 色 变 为 蓝 绿 色 ( 1 o、 2 o醇 )
6. 邻二醇的特有反应 1)高碘酸或四醋酸铅氧化
CH2 OH CH OH CH OH CH2 OH 3 H IO 4 2H C H O + 2 H C O O H
HCl
CH3 C H 3 C -C H C H 3 -H 2O H OH2
+
CH3 C H 3 C -C H C H 3 H Cl CH3 C H 3 C -C H C H 3 H Cl
-
CH3
重排
+
C H 3 C -C H 2 C H 3
+
Cl CH3
-
C H 3 C -C H 2 C H 3 Cl
2)与 PX3 、SOCl2(二氯亚砜) 反应生成RX
3 (C H 3 ) 2 C H C H 2 O H R C H 2O H + B r Br
-
P B r3
3 (C H 3 ) 2 C H C H 2 B r + H 3 P O 3 R C H 2O P B r2 + H B r SN2 R C H 2B r +
+
CH3 CHOH
CH
+
CH3
CH3 CH3
CH3 CHOCH CH3
CH3
CH3
制混合醚 ( 3o 与1o醇)
(C H 3 ) 3 C O H H
+ +
第七章 醇 酚 醚

第一节
醇
醇可以看成是烃分子中的氢原子被羟基(OH)取代后 生成的衍生物(R-OH)。
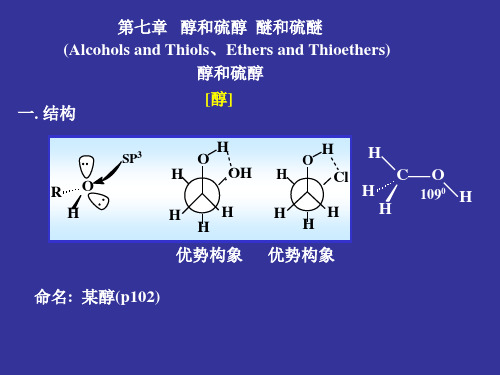
一、醇的结构、分类和命名
1 、醇的结构
2、醇的分类 a. 根据羟基所连碳原子种类分为: 一级醇(伯醇)、二级醇(仲醇)、三级醇(叔醇)。 b. 根据分子中烃基的类别分为: 脂肪醇、脂环醇和芳香醇(芳环侧链有羟基的化合物)。
2、与氢卤酸反应(制卤代烃的重要方法)
1) 反应速度与氢卤酸的活性和醇的结构有关。 HX的反应活性: HI > HBr > HCl 醇的活性次序: 烯丙式醇 > 叔醇 > 仲醇 > 伯醇 > CH3OH
醇与卢卡斯(Lucas)试剂(浓盐酸和无水氯化锌)的反应:
Lucas试剂可用于区别伯、仲、叔醇,但一般仅适用于3-6个 碳原子的醇。原因: 1-2个碳的产物(卤代烷)的沸点低,易挥
高级醇的硫酸酯是常用的合成洗涤剂之一。如 C12H25OSO2ONa (十二烷基磺酸钠)。
(2)与有机酸反应
5、脱水反应 醇与催化剂共热即发生脱水反应,随反应条件而异可发生 分子内或分子间的脱水反应。
醇的脱水反应活性: 3o R-OH > 2o R-OH > 1o R-OH
醇脱水反应的特点:
a. 主要生成札依采夫烯,例如:
β位上有支链的伯醇、仲醇与HX的反应常有重排产物生成。
这是因为空间位阻较大,不利于按SN2历程进行反应。若按 SN1历程进行反应,虽然生成的中间体是稳定性很小的伯碳正离 子,反应速率较慢,但因伯碳正离子可重排为稳定的叔碳正离子, 故得到的是重排产物。
3、与卤化磷和亚硫酰氯反应
4. 与酸反应(成酯反应) (1)与无机酸反应 醇与含氧无机酸硫酸、硝酸、磷酸反应生成无机酸酯。
有机化学——第7章醇酚醚

25
6、氧化脱氢反应
在有机化合物的分子中加入氧或脱去氢的反应都叫做氧化反应。
1) 伯醇氧化生成醛,醛进一步氧化生成酸。
CH3 CH2 CH2OH
K2CrO7-H2SO4
CH3 CH2CHO
[O]
CH3 CH2 COOH
2) 仲醇氧化生成酮,酮不易被继续氧化 。
H3 C CH OH CH3 [O] CH3 C O CH3
烯丙位 苯甲位 一级醇
}
醛
弱碱,反应条件温和, 不饱和键不受影响。
琼斯试剂 CrO3+稀H2SO4
费慈纳-莫法特试剂
醛(产率不高, 不用。)
醛(产率很高)
稀酸,反应条件温和, 不饱和键不受影响。 酸性 (H3PO4) , 其它基团不受影响。 碱性,可逆,分子内 双键不受影响。 28
反应机理 1oROH (SN2)
SN2
SN2
BrCH2CH3 +
2oROH , 3oROH (SN1)
SN2
SN1
(CH3)3C+ + HOPBr2
Br -
(CH3)3CBr
18
ROH + SOCl2
b.p. 79oC
RCl + SO2 + HCl
该反应的特点是:反应条件温 和,反应速率快,产率高,没 有副产物。
13
2、与氢卤酸反应
发生亲核取代反应,生成卤代烃和水,是制取卤代烃的重要方法。
R OH + HX
R X + H2O
氢卤酸的活性次序:HI > HBr > HCl; 醇的活性次序:烯丙式醇,苄基醇 > 3º 醇 > 2º 醇 > 1º 醇。 烯丙醇、叔醇、大多数仲醇及空间位阻大的伯醇,反应是按SN1
硫醇、硫酚、硫醚的PPT课件

SH 2-巯基丙醇
.
4
二、硫醚
• 硫醚可看成是醚分子中的氧原子被硫原子 取代生成的化合物。硫醚的通式为
(Ar)R-S-R(Ar), C-S-C称为硫醚键,是硫醚 的官能团。
.
5
(一)硫醚的命名
• 硫醚的命名与醚相似,只需在醚字之前加 一个硫字。例如:
CH3CH2SCH2CH3 乙硫醚
CH3CH2SCH2CH2CH3 乙丙硫醚
?硫醇的通式为rsh硫酚的通式为ash?硫酚的通式为arsh?其中的sh称为巯基?是硫醇和硫酚的官能团一硫醇和硫酚的命名硫醇和硫酚的命名方法分别与醇和酚的命名方法相似只需在醇和酚字前加一硫字
硫醇、硫酚、硫醚的命名
.
1
一、硫醇和硫酚
• 硫醇和硫酚可分别看成是醇和酚分子中的 氧原子被硫原子取代生成的化合物。
.
6
• 比较复杂的硫醚命名时,选择“较优”烃 基作为母体,把烷硫基作为取代基。例如: CH3CHCH2CH2CH3
|
SCH3 2-甲硫基戊烷
.
7
• 硫醇的通式为R-SH • 硫酚的通式为Ar-SH • 其中的-SH称为巯基 • 是硫醇和硫酚的官能团
.
2
(一)硫醇和硫酚的命名
硫醇和硫酚的命名方法分别与醇和酚的命名 方法相似,只需在醇和酚字前加一硫字。 例如:
CH3CH2CH2SH 丙硫醇
苯硫酚
.ቤተ መጻሕፍቲ ባይዱ
3
• 比较复杂的硫醇命名时,选择“较优”烃 基作为母体,以巯基作为取代基。例如: CH3CHCH2OH
醇、硫醇、酚

CH CH CHO
• 欧芬脑尔(Oppenauer)氧化法:在异 丙醇铝或叔丁醇铝存在下,将仲醇和丙 酮一起反应,醇被氧化成酮,丙酮被还 原成异丙醇的反应。
O R2C HO H+ C H3C C H 3 Al[O C H (C H 3)2]3 O RC R + OH C H3C HC H 3
•在实际工作中,三卤化磷常用红磷与溴或 碘作用产生。如:
CH3CH2OH
P + I2
CH3CH2I
• 醇与PX5也可发生类似的反应,但与PX5 反应时,副产物较多,所以,这不是制 备卤代烃的好方法。
ROH + PCl5 ROH + POCl3 RCl + POCl3 + HCl (RO)3PO + 3HCl 磷酸酯
OH Na2Cr2O7 H2SO 4/
CH3 KMnO4/H H3C C OH CH3
O KMnO4/H CH2CH2COOH CH2CH2COOH
C H3C CH2 KMnO4/H C H C O + CO + H O 3 2 2 CH3 CH
3
(2)用温和的氧化剂氧化(选择性氧化):
沙瑞特(Sarrett)试剂:CrO3/C5H5N 琼斯(Jones)试剂: CrO3/稀H2SO4 活性二氧化锰。
(二)二元醇的反应
1、脱水反应 邻二醇分子内脱水:生成不稳定的烯醇, 再重排成醛或酮 分子间脱水:共轭二烯烃、环醚
2、pinacol重排
CH3 CH3 H3C C C CH3 H2SO4 CH3 H3C C C CH3
OH OH
CH3 O
H+
有机化学课件——Chapter 07 醇、酚、醚
有机化学课件
32
第七章 醇、酚、醚
3. 醇的脱水反应
在浓硫酸催化下,醇通常发生脱水反应得到烯烃或醚. 反应涉及碳正离子中间体. 如果产物为烯烃则遵从Saytzeff规则. 较低温度下反应主要发生分子间脱水成醚, 通常低于140oC . 较高温度下主要发生分子内脱水成烯烃的反应, 通常高于 180oC.
有机化学课件 26 第七章 醇、酚、醚
醇和氢卤酸反应的局限性在于: 所期待的卤代烃不是总能 高收率地得到, 具体表现为四个方面. ① 大多数醇不能和HI反应得到碘代烷烃; ② 1o和2o醇制备氯代烷收率很低; ③ 总是有消除反应产物(烯烃)生成; ④ 碳正离子中间体经常发生重排,得到重排产物.
有机化学课件
OH CH2CH2CH2COOH
有机化学课件 5 第七章 醇、酚、醚
三、醇的物理性质
Unusually high boiling points due to hydrogen bonding between molecules. Small alcohols are miscible in water, but solubility decreases as the size of the alkyl group increases.
有机化学课件
17
第七章 醇、酚、醚
1º, 2º, 3º碳的氧化还原程度
氧化: 分子中C-H 变成C-O. 还原: 分子中C-O 变成C-H.
有机化学课件
18
第七章 醇、酚、醚
1) 仲醇的氧化
许多氧化剂都可以将2o醇氧化为酮. 常用氧化剂如: Na2Cr2O7/H2SO4 H2CrO4 可能是氧化反应的活性物种. 氧化反应伴随明显的颜色变化: 反应溶液由橙色(Cr6+) 变为深蓝色(Cr3+).
有机化学——07醇酚醚
H C C C H 2O H 2-丙 炔 -1-醇
多元醇的命名:应选择连有羟基最多的碳链为主 链。羟基的位次与数目写在“醇”的前面
C | H2 C | HCH3 OH OH
1,2-丙 二 醇
C | H2 C | HC | H2 OH OH OH
丙 三 醇
CH2 CH3
|
C | H2 CHC | HC | H2 OH OHOH
·
C ·
C · C
· C
· ··
·C C
O H
二、酚的分类和命名
(一)酚的分类
根据芳基的不同,可分为苯酚和萘酚等,其中萘酚因羟基
位置不同,有α-萘酚和β-萘酚之分
根据芳环上羟基数目不同,分为一元酚、二元酚和三元
酚等
含有两个以上酚羟基的酚统称为多元酚
— OH
O H
O H
O H
O H
O H
苯 酚
α-萘 酚
四、醇的化学性质
醇的化学性质主要由官能团羟基(-OH)所决定
(一)与活泼金属的反应
由于烷基的给电子诱导效应,醇中氧原子上电子云密 度比较大,所以醇的酸性比水弱
HOH + Na
1 NaOH+2H2
ROH + Na
C2H5OH+ Na 2ROH+M g I2
R 醇 ON 钠 a +1 2H2 C2H5ONa +H2
伯醇 RCH2OH;仲醇 R2CHOH;叔醇 R3COH
3.根据所含羟基数目的多少,醇可分为一元醇、二元醇和三元 醇等
CH3 CH2 OH
乙 醇 ( 一 元 醇 )
CH2 OH CH2 OH
乙 二 醇 ( 二 元 醇 )
第七章 醇、酚、醚
第七章 醇、酚、醚 Ⅰ 学习要求 1. 掌握醇、酚、醚的结构特点及主要化学性质,以及运用这些性质的异同点进行鉴别。
2. 熟练掌握醇、酚、醚各类化合物的系统命名法。 3. 了解沸点、溶解度与分子结构的关系。 4. 熟练掌握乙醇、乙醚、苯酚等几个典型化合物的结构、理化性质及用途。
Ⅱ 内容提要 一. 醇的结构 醇可以看作是水分子中的氢原子被烃基取代的衍生物,羟基是醇的官能团。根据醇分子中烃基的不同,可以分为饱和醇、不饱和醇、脂环醇、芳香醇等。 二. 醇的性质 1. 似水性:醇的酸性比水弱,不能与碱的水溶液作用,只能与碱金属或碱土金属作用放出氢气,并形成醇化物。
醇的反应活性:甲醇>伯醇>仲醇>叔醇 醇化物遇水分解成醇和碱。
醇还有极弱的碱性,可溶于浓酸中。 2. 亲核取代反应(与HX的反应):
HOH+Na22NaOH+H22
ROH2+Na22 RONa
+H
2
ROH2+Mg(RO)2Mg+H
2
醇钠
醇镁
RONa+HOHROH+NaOH
H2O+HClH3O++Cl -ROH+HClRO+H
2+
Cl
-
羊钅盐 HX的活性:HI>HBr>HCl 醇的活性:烯丙醇(苄醇)>叔醇>仲醇>伯醇(按SN1机理进行) 该反应可用于鉴别C6以下的醇,通常使用Lucas试剂(浓HCl + 无水ZnCl2) 3. 酯化反应:醇与酸(包括无机酸和有机酸)作用,失水后所得产物称为酯
4. 脱水反应:反应温度不同,产物不同。
5. 氧化或脱氢:伯醇和仲醇用KMnO4、K2Cr2O7等氧化剂氧化或催化脱氢能得到醛或酮。氧化伯醇得到醛,进一步氧化得到羧酸,氧化仲醇得到酮,叔醇一般不易被氧化。
三. 酚的结构 羟基直接与芳香环相连的化合物叫做酚。由于酚羟基中的氧与芳环有较强的p–π共轭作用,因此酚和醇在性质上有很大的不同。苯酚更容易发生亲电取代反应,酚羟基不容易被取代,但酚的酸性强于醇。 四. 酚的性质
ROH+HXRX+H2O+ROHHONO2RONO2ROH+HOSO2OHROSO2OHROH+HOO2SORROSO2ORROH+HOCOR'R'COOR+ H2O
(2012)有机化学 第七章 醇、酚、醚
酚羟基是一个强的邻、对位定位基,活化了苯 环,使其易于发生亲电取代反应。比较苯、苯 酚分别与溴水、硝酸反应的条件及其产物。有 关反应式:
1.卤代:
2.硝化: 3.磺化:
(三)与FeCl3的显色反应
凡具有酚羟基结构和烯醇式(—C=C—OH)结构 的化合物都能与与FeCl3的显色反应。
OH 、 OH
CH OH
CH OH
C H 2OH
2 H IO 4
C
O
O
C OH
H
O
C H
H
H
四、硫醇
硫醇(thio-alcohol) 的官能团是巯基 (-SH)。硫醇可看作醇分子中的氧原 子被硫原子取代的产物。
(一)硫醇的命名
按相应的醇命名,在醇字前加“硫”字。
C H 3C H 2S H
C H 2S H
乙硫醇
第七章
醇、酚、醚
(alcohols、phenols、ethers)
醇:脂肪烃基或芳香烃的侧链与羟基 相连形成的化合物。 酚:羟基与芳香烃的苯环直接相连形 成的化合物。 醚:醇或酚中羟基上的氢被烃基(脂 肪烃基或芳香烃基)取代后形成的产 物。
R OH
Ar OH
R
O R'
醇
酚
醚
C HO H OH HO H H OH H OH C H2O H
2. 氧化反应
硫醇的氧化表现在巯基上,实质是脱氢反应。
-2 2
[H ] R S S R
R SH
+ 2 [H ]
二、结构
δ O δ
-
OH δ
-
