新课标三年高考化学试题分类解析——化学反应速率与化学平衡
全国高考化学化学反应速率与化学平衡的综合高考模拟和真题分类汇总附答案解析
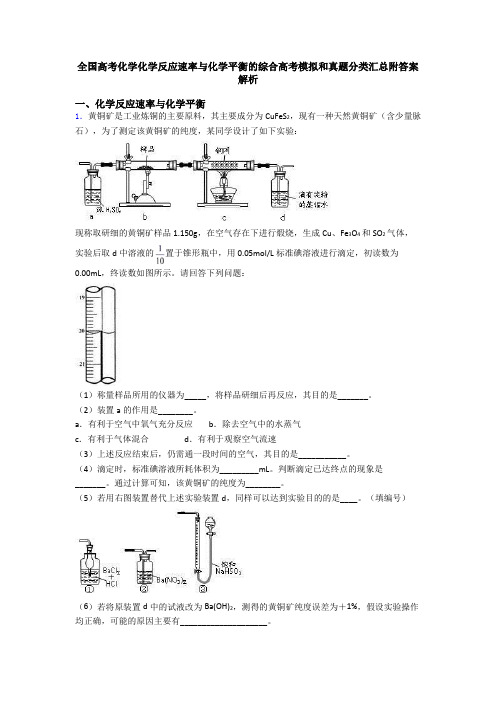
全国高考化学化学反应速率与化学平衡的综合高考模拟和真题分类汇总附答案解析一、化学反应速率与化学平衡1.黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量脉石),为了测定该黄铜矿的纯度,某同学设计了如下实验:现称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,初读数为0.00mL,终读数如图所示。
请回答下列问题:(1)称量样品所用的仪器为_____,将样品研细后再反应,其目的是_______。
(2)装置a的作用是________。
a.有利于空气中氧气充分反应 b.除去空气中的水蒸气c.有利于气体混合 d.有利于观察空气流速(3)上述反应结束后,仍需通一段时间的空气,其目的是___________。
(4)滴定时,标准碘溶液所耗体积为_________mL。
判断滴定已达终点的现象是_______。
通过计算可知,该黄铜矿的纯度为________。
(5)若用右图装置替代上述实验装置d,同样可以达到实验目的的是____。
(填编号)(6)若将原装置d中的试液改为Ba(OH)2,测得的黄铜矿纯度误差为+1%,假设实验操作均正确,可能的原因主要有____________________。
【答案】电子天平使原料充分反应、加快反应速率 b、d 使反应生成的SO2全部进入d 装置中,使结果精确 20.10mL 溶液恰好由无色变成浅蓝色,且半分钟内不褪色 80.4% ②空气中的CO2与Ba(OH)2反应生成BaCO3沉淀;BaSO3被氧化成BaSO4【解析】【分析】(1)根据称量黄铜矿样品1.150g,选择精确度较高的仪器;将样品研细,增大了接触面积;(2)浓硫酸可以将水除去,还可以根据冒出气泡的速率来调节空气流速;(3)反应产生的二氧化硫应该尽可能的被d装置吸收;(4)根据滴定管的读数方法读出消耗碘溶液的体积,根据反应结束时的颜色变化判断滴定终点;先找出黄铜矿和二氧化硫及碘单质的关系式CuFeS2~2SO2~2I2,再根据题中数据进行计算;(5)图2中的②中通入二氧化硫,反应生成了硫酸钡沉淀,可以根据硫酸钡的质量计算二氧化硫的量;(6)Ba(OH)2溶液能吸收空气的CO2,另外BaSO3易被空气中氧气氧化,这些原因均能引起测定误差。
全国高考化学化学反应速率与化学平衡的综合高考真题汇总附详细答案

全国高考化学化学反应速率与化学平衡的综合高考真题汇总附详细答案一、化学反应速率与化学平衡1.某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色先慢后快,即反应速率由小变大。
小组成员为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种,并为此设计实验进行探究验证。
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;猜想Ⅱ:……。
(实验目的)探究草酸与高锰酸钾反应的速率变化“异常”原因(实验用品)仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等。
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容。
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是(3)猜想Ⅱ可是:___________________要设计实验验证猜想Ⅱ,进行该实验还要补充一种试剂及一种仪器,分别是(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容。
【答案】(1)5H2C2O4+2MnO42—+6H+=10CO2↑+2Mn2++8H2O(2)温度计(3)生成的Mn2+对该反应有催化作用,加快反应速率;MnSO4(s)和秒表(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容。
(加入试剂时只要A试管与B试管所加的0.1mol/L H2C2O4溶液、0.05mol/L 酸性KMnO4体积相等即给分。
)【解析】试题分析:猜想II:影响反应速率的因素有浓度、压强、温度和催化剂,而草酸与高锰酸钾溶液发生反应:5H2C2O4+2MnO4-+6H+=10CO2↑+2 Mn2++8H2O,溶液褪色先慢后快,即反应速率由小变大,反应物是溶液,无气体,故不能是反应物的浓度和压强对反应速率产生的影响,则只能是生成的产物又做了此反应的催化剂,加快了反应速率,故答案为生成的Mn2+在反应中起到催化剂的作用,加快了反应速率;(1)草酸中的碳元素被在酸性条件下能被高锰酸钾溶液氧化为CO2,高锰酸根能被还原为Mn2+,根据得失电子数守恒来配平可得离子方程式为:5H2C2O4+2MnO4-+6H+=10CO2↑+2 Mn2++8H2O;(2)由于猜想I是认为可能是由于反应放热导致体系温度升高而加快了反应速率,故应测量反应前和反应开始后一段时间的温度变化,则还缺少温度计;(3)猜想II是认为生成的Mn2+在反应中起到催化剂的作用,由于Cl-也能使高锰酸钾溶液褪色,故为了避免Cl-的干扰,故应补充MnSO4固体,通过测量溶液褪色的时间的长短来验证猜想,则还需的仪器是秒表;(4)要通过对比实验来验证猜想Ⅱ,则实验B和实验A的试剂的选择应除了MnSO4固体不同,其他均应相同,故试管B内加入的试剂是在试管A试剂的基础上多加了MnSO4(s),由于结论是猜想II成立,则试管B的褪色时间应该比试管A的更快,故答案为2.连二亚硫酸钠(Na2S2O4)俗称保险粉,是工业上重要的还原性漂白剂,也是重要的食品抗氧化剂。
高考化学复习专题课件化学反应速率化学平衡课件

a
(mol ·L -1 )
转化
b
x
(mol ·L -1 )
1 s 时
a-x b-
则:v(A)= mol·L-1·s-1,
1
v(B)= mol·L-1·s-1,
1
v(C)= mol·L-1·s-1,
1
v(D)= mol·L-1·s-1。
1
0
(mol ·L -1 )
②根据反应速率方程式可知在p(CH4)一定时,生成速率随p(CO2)的
升高而降低,所以pc(CO2)>pb(CO2)>pa(CO2)。
1
【答案】(1)+247 A 3
(2)①劣于 相对于催化剂X,催化剂Y积碳反应的活化能大,积碳
反应的速率小;而消碳反应活化能相对小,消碳反应速率大 AD
②pc(CO2)、pb(CO2)、pa(CO2)
化能大,积碳反应的速率小;而消碳反应活化能相对小,消碳反应速
率大,所以催化剂X劣于Y。积碳反应、消碳反应均是吸热反应,升
高温度,平衡向正反应方向移动,因此K积、K消均增加,A正确,C错误;
升高温度,反应速率均增大,B错误;积碳量到达最大值以后再升高
温度,积碳量降低,这说明v消增加的倍数比v积增加的倍数大,D正确。
平衡的线,作出判断
6.化学反应方向的判据
【典例】(202X·全国2,27)CH4-CO2催化重整不仅可以得到合成
气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)CH4-CO2催化重整反应为CH4(g)+CO2(g) === 2CO(g)+2H2(g)。
高三化学高考备考一轮复习专题10化学反应速率和化学平衡1_1.讲解部分课件

恒温恒压时:充入无关气体→总体积增大,各反应物浓度减小→反应速率 减小。 ③温度:升高温度,反应速率增大,反之减小,与反应吸热还是放热无关。 ④催化剂:使用催化剂,一般可加快反应速率。 解释:升温、使用催化剂时,体系中活化分子百分数增加,有效碰撞次数增 加,化学反应速率增大。 ⑤其他因素:如反应物的接触面积增大,反应速率增大;构成原电池,反应 速率增大。
平衡 平衡
总压强、总体积、总物质的量一定
不一定平衡
正、逆反应速 在单位时间内消耗了m mol A的同时生成了m mol A,即v正=v逆
率的关系
在单位时间内消耗了n mol B的同时消耗了p mol C
v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q
在单位时间内生成了n mol B,同时消耗了q mol D
应。假设反应A2+B A2B是由两个基元反应组成的:
第一步 A2 2A·
慢反应
第二步 2A·+B A2B
快反应
解析 (1)第一步反应较快,说明其活化能较小,反应较容易。
(2)假设反应前总物质的量为2 mol,则:
2NO(g) + O2(g)
起始(mol)
1
2NO2(g)
1
0
平衡时总物质的量为0.5 mol+0.75 mol+0.5 mol=1.75 mol。恒容容器中, 由于反应前后气体分子数不相等,故反应前后压强发生变化,恒温恒容时
压强
恒容时压强不再变化,当m+n≠p+q时
恒容时压强不再变化,当m+n=p+q时
混合气体的平 M r 一定,当m+n≠p+q时
均相对分子 质量
高考化学 化学反应速率与化学平衡 综合题附答案

高考化学化学反应速率与化学平衡综合题附答案一、化学反应速率与化学平衡1.用H2O2、KI和洗洁精可完成“大象牙膏”实验(短时间内产生大量泡沫),某同学依据文献资料对该实验进行探究。
(1)资料1:KI在该反应中的作用:H2O2+I-=H2O+IO-;H2O2+IO-=H2O+O2↑+I-。
总反应的化学方程式是________________。
(2)资料2:H2O2分解反应过程中能量变化如图所示,其中①有KI加入,②无KI加入。
下列判断正确的是___________(填字母)。
a. 加入KI后改变了反应的路径b. 加入KI后改变了总反应的能量变化c. H2O2+I-=H2O+IO-是放热反应(3)实验中发现,H2O2与KI溶液混合后,产生大量气泡,溶液颜色变黄。
再加入CCl4,振荡、静置,气泡明显减少。
资料3:I2也可催化H2O2的分解反应。
①加CCl4并振荡、静置后还可观察到___________,说明有I2生成。
②气泡明显减少的原因可能是:i. H2O2浓度降低;ii. ________。
以下对照实验说明i不是主要原因:向H2O2溶液中加入KI溶液,待溶液变黄后,分成两等份于A、B两试管中。
A试管加入CCl4,B试管不加CCl4,分别振荡、静置。
观察到的现象是_____________。
(4)资料4:I-(aq)+I2(aq)ƒI3-(aq) K=640。
为了探究体系中含碘微粒的存在形式,进行实验:向20 mL一定浓度的H2O2溶液中加入10mL 0.10mol·L-1 KI溶液,达平衡后,相关微粒浓度如下:微粒I-I2I3-浓度/(mol·L-1) 2.5×10-3a 4.0×10-3①a=__________。
②该平衡体系中除了含有I-,I2,I3-外,一定还含有其他含碘微粒,理由是________________。
【答案】2H2O2KI2H2O+O2↑ a 下层溶液呈紫红色在水溶液中I2的浓度降低 A试管中产生气泡明显变少;B 试管中产生气泡速率没有明显减小 32.510-⨯ 2c (I 2)+c (I-)+3c (I 3-)<0.033mol ·L -1【解析】 【分析】(1)H 2O 2+I -=H 2O +IO -,H 2O 2+IO -=H 2O +O 2↑+I -,把两式加和,即可得到总反应的化学方程式。
高三化学化学反应速率和化学平衡专题高考题14道答案详解要点提示知识点分析
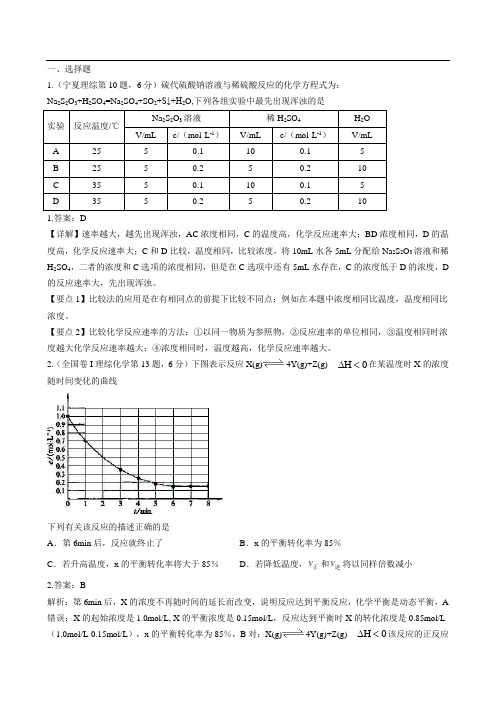
一、选择题1.(宁夏理综第10题,6分)硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na 2S 2O 3+H 2SO 4=Na 2SO 4+SO 2+S↓+H 2O,下列各组实验中最先出现浑浊的是 实验 反应温度/℃ Na 2S 2O 3溶液 稀H 2SO 4H 2O V/mL c/(mol·L -1)V/mL c/(mol·L -1)V/mL A 25 5 0.1 10 0.1 5 B 25 5 0.2 5 0.2 10 C 35 5 0.1 10 0.1 5 D 3550.250.2101.答案:D【详解】速率越大,越先出现浑浊,AC 浓度相同,C 的温度高,化学反应速率大;BD 浓度相同,D 的温度高,化学反应速率大;C 和D 比较,温度相同,比较浓度,将10mL 水各5mL 分配给Na 2S 2O 3溶液和稀H 2SO 4,二者的浓度和C 选项的浓度相同,但是在C 选项中还有5mL 水存在,C 的浓度低于D 的浓度,D 的反应速率大,先出现浑浊。
【要点1】比较法的应用是在有相同点的前提下比较不同点;例如在本题中浓度相同比温度,温度相同比浓度。
【要点2】比较化学反应速率的方法:①以同一物质为参照物,②反应速率的单位相同,③温度相同时浓度越大化学反应速率越大;④浓度相同时,温度越高,化学反应速率越大。
2.(全国卷I 理综化学第13题,6分)下图表示反应X(g)4Y(g)+Z(g) 0H <∆在某温度时X 的浓度随时间变化的曲线下列有关该反应的描述正确的是 A .第6min 后,反应就终止了B .x 的平衡转化率为85%C .若升高温度,x 的平衡转化率将大于85%D .若降低温度,v 正和v 逆将以同样倍数减小2.答案:B解析:第6min 后,X 的浓度不再随时间的延长而改变,说明反应达到平衡反应,化学平衡是动态平衡,A 错误;X 的起始浓度是1.0mol/L, X 的平衡浓度是0.15mol/L ,反应达到平衡时X 的转化浓度是0.85mol/L (1.0mol/L-0.15mol/L ),x 的平衡转化率为85%,B 对;X(g)4Y(g)+Z(g) 0H <∆该反应的正反应是放热反应,逆反应时吸热反应,升高温度平衡向吸热反应方向移动,x 是反应物,x 的平衡转化率将小于85%,C 错;若降低温度,化学反应速率都降低,v 正(放热反应速率)降低的倍数小,v 逆(吸热反应速率)降低的倍数大,化学平衡向正反应方向移动。
化学高考一轮总复习化学反应速率与化学平衡解析
化学高考一轮总复习化学反应速率与化学平衡解析一、引言近年来,随着社会的不断发展,化学作为一门基础学科,在高考中的地位日益重要。
而化学反应速率与化学平衡是化学学科的基础概念,对于理解化学反应和平衡态具有重要意义。
本文将从反应速率的定义、影响因素、反应动力学等多个方面进行解析,帮助高中化学学生对化学反应速率与化学平衡有更深刻的理解。
二、反应速率的定义与测量反应速率使用反应物的浓度变化来定义,通常表示为反应物浓度随时间的变化率。
反应速率可以通过实验测量,并且有几种常见的测量方法,如体积法、质量法和光度法等。
三、影响反应速率的因素1.浓度影响:反应速率随着反应物浓度的增加而增加,这是因为浓度增加会增加反应物的有效碰撞概率。
2.温度影响:温度的增加会提高反应物分子的平均动能,增加反应分子的活动性,从而促进反应速率的增加。
3.催化剂的存在:催化剂可以通过改变反应物分子之间的反应路径,降低活化能,从而提高反应速率。
4.密度影响:在多分子反应中,反应物分子之间的碰撞频率和反应速率与密度有关。
四、反应速率与反应动力学反应速率的研究需要借助反应动力学理论。
反应动力学研究反应速率在不同条件下的变化规律,通过建立反应动力学方程可以揭示反应速率与反应物浓度的关系。
五、化学平衡的概念与条件化学平衡是指在封闭系统中,反应物和生成物浓度达到一定比例后,反应速率保持不变的状态。
达到化学平衡的条件包括:反应物和生成物之间的浓度达到一定比例、反应速率为零、系统处于封闭状态等。
六、平衡常数与化学平衡的平衡方向平衡常数是指在给定温度下,反应物和生成物之间的浓度比值的平衡值,可以通过反应方程式的系数进行计算。
化学平衡的平衡方向可以通过平衡常数的大小来判断,平衡常数大于1则反应向生成物方向进行,小于1则反应向反应物方向进行。
七、化学平衡与反应的移动根据利用Le Châtelier原理,当外界条件改变时,如温度、压力或浓度变化时,反应体系会向能消除或减小改变的方向进行移动,以重新建立平衡状态。
高考化学复习专题02化学反应速率、化学平衡(3年高考)高考化学大题狂做系列(第02期)(解析版).docx
高中化学学习材料唐玲出品1.(2013海南卷)(9分)反应A(g) B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。
温度T1和T2下A 的浓度与时间关系如图所示。
回答下列问题:(1)上述反应的温度T1 T2,平衡常数K(T1) K(T2)。
(填“大于”、“小于”或“等于”)(2)若温度T2时,5min后反应达到平衡,A的转化率为70%,则:①平衡时体系总的物质的量为。
②反应的平衡常数K= 。
③反应在0~5min区间的平均反应速率v(A)= 。
【答案】(1)小于小于(2)①0.085mol ②0.082mol/L ③0.007mol/(L·min)【解析】考点:本题考查化学反应速率和化学平衡。
2.(2013山东卷)(15分)化学反应原理在科研和生产中有广泛应用(1)利用“化学蒸气转移法”制备TaS 2晶体,发生如下反应 TaS 2(s)+2I 2(g)TaI 4(g)+S 2(g) △H ﹥0 (I )反应(I )的平衡常数表达式K= ,若K=1,向某恒容密闭容器中加入1mol I 2(g )和足量TaS 2(s ),I 2(g )的平衡转化率为 ,(2)如图所示,反应(I )在石英真空管中进行,先在温度为T 2的一端放入未提纯的TaS 2粉末和少量I 2(g ),一段时间后,在温度为T 1的一端得到了纯净的TaS 2晶体,则温度T 1 T 2(填“﹥”“﹤”或“=”)。
上述反应体系中循环使用的物质是 。
(3)利用I 2的氧化性可测定钢铁中硫的含量。
做法是将钢样中的硫转化为 H 2SO 3,然后用一定浓度的I 2溶液进行滴定,所用指示剂为 ,滴定反应的离子方程式为 , (4)25℃时,H 2SO 3HSO 3-+H +的电离常数K a=1×10-2mol/L ,则该温度下NaHSO 3的水解平衡常数K h =mol/L ,若向NaHSO 3溶液中加入少量的I 2,则溶液中c(H 2SO 3)c(HSO -3 ) 将 (填“增大”“减小”或“不变”)。
化学反应速率图象-2023年高考化学热点专项导航与精练(新高考专用)解析版)
第四篇化学反应速率与化学平衡化学反应速率图象图象类试题的特征是以图象的形式将一些相关量给出,把题目中的化学原理抽象为数学问题,旨在考查从图象中获得数据、处理应用数据的能力以及对曲线的数学意义和化学意义之间对应关系的运用能力。
近年来高考,化学反应速率图像题多在非选择题中以填空的形式出现。
试题主要是结合图像中的数据及物质的变化趋势进行分析、判断与计算。
常见速率—时间图像(vt图像)类型如下:由图像变化分析外界条件对其影响,已知反应为mA(g)+nB(g)pC(g)+qD(g)ΔH=Q kJ·mol-1。
(1)“渐变”类vt图像图像分析结论t1时v′正突然增大,v′逆逐渐增大;v′正>v′逆,平衡向正反应方向移动t1时其他条件不变,增大反应物的浓度t1时v′正突然减小,v′逆逐渐减小;v′逆>v′正,平衡向逆反应方向移动t1时其他条件不变,减小反应物的浓度t1时v′逆突然增大,v′正逐渐增大;v′逆>v′正,平衡向逆反应方向移动t1时其他条件不变,增大生成物的浓度t1时v′逆突然减小,v′正逐渐减小;v′正>v′逆,平衡向正反应方向移动t1时其他条件不变,减小生成物的浓度图像分析结论t1时v′正、v′逆均突然增大,且v′正>v′逆;平衡向正反应方向进行t1时其他条件不变,增大反应体系的压强且m+n>p+q(正反应为体积减小的反应)t1时其他条件不变,升高温度且Q>0(吸热反应)t1时v′正、v′逆均突然增大,且v′逆>v′正;平衡向逆反应方向进行 t 1时其他条件不变,增大反应体系的压强且m +n <p +q(正反应为体积增大的反应)t 1时其他条件不变,升高温度且Q <0(放热反应)t 1时v′正、v′逆均突然减小,且v′正>v′逆;平衡向正反应方向进行 t 1时其他条件不变,减小反应体系的压强且m +n <p +q(正反应为体积增大的反应) t 1时其他条件不变,降低温度且Q <0(放热反应)t 1时v′逆、v′正均突然减小,且v′逆>v′正;平衡向逆反应方向进行 t 1时其他条件不变,减小反应体系的压强且m +n >p +q(正反应为体积减小的反应) t 1时其他条件不变,降低温度且Q >0(吸热反应)图像 分析 结论t 1时v′正、v′逆均突然增大且v′正=v′逆,平衡不移动 t 1时其他条件不变使用催化剂t 1时其他条件不变增大反应体系的压强且m +n=p +q(反应前后气体体积无变化)t 1时v′正、v′逆均突然减小且v′正=v′逆,平衡不移动 t 1时其他条件不变,减小反应体系的压强且m +n=p +q(反应前后气体体积无变化)1.(2022•北京卷)CO 2捕获和转化可减少CO 2排放并实现资源利用,原理如图1所示。
2019高考化学试题分类解析汇编--化学反应速率和化学平衡(可编辑修改word版)
2019 高考化学试题分类解析汇编--化学反应速率和化学平衡1.[2018·江苏化学卷 10]以下有关说法正确的选项是A.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈C.N2(g)+3H2(g)2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2)和氢气的平衡转化率均增大D.水的离子积常数 Kw 随着温度的升高而增大,说明水的电离是放热反应B 解析:此题是化学反应与热效应、电化学等的简单综合题,着力考查学生对熵变、焓变,水解反应、原电池电解池、化学反应速率的影响因素等方面的能力。
A.分解反应一般是常识吸热反应,熵变、焓变都大于零,仅在高温下自发。
内容来源于《选修四》P34-P36 中化学方向的判断。
B.铁比铜活泼,组成的原电池中铁为负极,更易被氧化。
C.据平衡移动原理,升高温度平衡向逆反应方向移动,平衡转化率减小。
D.水的离子积常数 Kw 随着温度的升高而增大,说明水的电离是吸热反应,越热越电离,水的离子积常数 Kw 随着温度的升高而增大。
2.[2018·江苏化学卷 14]温度为 T 时,向 2.0L 恒容密闭容器中充入 1.0molPCl5,反应PCl5(g)PCl3(g)+Cl2(g)经一段时间后达到平衡。
反应过程中测定的部分数据见下表:t/s 0 50 150 250 350以下说法正确的选项是n(PCl3)/mol0 0.160.190.20.2A.反应在前 50s 的平均速率为v(PCl3)=0.0032mol·L-1·s-1B.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11mol·L-1,那么反应的△H<0C.相同温度下,起始时向容器中充入 1.0molPCl5、0.20molPCl3 和 0.20molCl2,达到平衡前v(正)>v(逆)D.相同温度下,起始时向容器中充入 2.0molPCl3、2.0molCl2,达到平衡时,PCl3 的转化率小于 80%C 解析:此题素材似乎来源于《选修四》课本第 32 页习题的第 8 题,属于基本理论中化学平衡问题,主要考查学生对速率概念理解与计算,平衡常数概念与计算,平衡移动等有关内容理解和掌握程度。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
新课标三年高考化学试题分类解析——化学反应速率与化学平衡 1.(07年宁夏理综·13)一定条件下,合成氨气反应达到平衡时,测得混合气体中氨气的体积分数为20.0% ,与反应前...的体积相比,反应后体积缩小的百分率是 A.16.7% B.20.0% C.80.0% D.83.3% 答案:A 解析:设达到平衡后混合气体的体积为1L,则其中生成的氨气的体积为1L×20.0%=0.2L。则根据反应的方程式有: N2+3H22NH3 △V 1 3 2 2 0.2L 0.2L 所以平衡前混合气体的体积为1L+0.2L=1.2L,因此反应后气体体积缩小率为
%1002.12.0L
L16.7%。
2.(07年广东化学·16)灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知: ①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1
②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2
③Sn(s、灰)Sn(s、白) △H3=+2.1kJ·mol-1
下列说法正确的是 A.△H1>△H2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应 D.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏 答案:D 解析:②-①可得③,△H2-△H1>0,故△H2>△H1 ,A错,根据③,在常温下,灰锡会向白锡转化故常温下以白锡状态存在,正反应为吸热反应,故B、C错,当锡制器皿长期处于低于13.2℃的环境中会转化为灰锡,灰锡以粉末状存在,故会自行毁坏。 3.(07年广东理基·26)把铝条放入盛有过量稀盐酸的试管中,不影响...氢气产生速率的因素
是 A.盐酸的浓度 B.铝条的表面积 C.溶液的温度 D.加少量Na2SO4 答案:D 解析:铝与盐酸反应的实质是2Al+6H+=2Al3++3H2↑,因此盐酸的溶度、铝条的表面积和
溶液的温度均会影响反应的速率,而加少量Na2SO4对溶液中的各物质的浓度没有影响,不会影响反应速率。
4.(07年广东化学·18)下述实验能达到预期目的的是 编号 实验内容 实验目的 A 将SO2通入酸性KMnO4溶液中 证明SO2具有氧化性
B 将Cl2通入NaBr溶液中 比较氯与溴的氧化性强弱
C 将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 研究温度对化学平衡的影响
D 分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2 研究催化剂对H2O2分解速率的影响
答案:BC 解析:本题是一道实验题。A选项中SO2通入酸性KMnO4溶液中,KMnO4做氧化剂,说明SO2具有还原性。B选项中将Cl2通入NaBr溶液中发生Cl2+2NaBr=2NaCl+Br2反应,根据氧化还原反应规律可知Cl2的氧化性大于Br2。C中发生的反应为Cu+4HNO3=Cu(NO3)2+2NO2+2H2O、2NO2(g)N2O4;△H<0,升温气体颜色变深,降温气体颜色变浅,D选项中H2O2溶液的浓度不同,故不能单纯判断催化剂对分解速率的影响。 5.(08年宁夏理综·12)将固体NH4I置于密闭容器中,在一定温度下发生下列反应: ①NH4I(s)NH3(g)+HI(g);②2HI(g)H2(g)+I2(g) 达到平衡时,c(H2)=0.5mol·L-1,c(HI)=4mol·L-1,则此温度下反应①的平衡常数为 A.9 B.16 C.20 D.25 答案:C 解析:求①的平衡常数的关键是求氨气的平衡浓度,若碘化氢不分解时,NH3(g)和HI(g) 的平衡浓度是相等的,因此2c(H2) 与容器中平衡浓度c(HI)之和即为氨气的平衡浓度5 mol·L-1,故此温度下反应①的平衡常数为20。 6.(08年广东化学·8)将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g) 2HBr(g)△H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是A A.a>b B.a=b C.a<b D.无法确定 答案:A 解析:正反应为放热反应,前者恒温,后者相对前者,温度升高。使平衡向左移动,从而使Br2的转化率降低。所以b
7.(08年广东化学·15)碘钨灯比白炽灯使用寿命长。灯管内封存的少量碘与使用过程中沉
积在管壁上的钨可以发生反应:W(s)+I2(g)WI2(g) ΔH<0(温度T1<T2)。下列说法正确的是AD A.灯管工作时,扩散到灯丝附近高温区的WI2(g)会分解出W1W重新沉积到灯丝上 B.灯丝附近温度越高,WI2(g)的转化率越低
C.该反应的平衡常数表达式是)WI()I()W(22cccK D.利用该反应原理可以提纯钨 答案:AD
T1 T2 解析:该反应的正反应为放热反应,温度升高,化学平衡向左移动。所以灯丝附近温度越高,WI2的转化率越高,B错。平衡常数,应为生成物除以反应物: K=c(WI2)/c(W)·c(I2)利用该反应,可往钨矿石中,加如I2单质,使其反应生成WI2
富集,再通过高温加热WI2生成钨,从而提纯W,D正确。
8.(08年广东理基·36)对于反应2SO2(g)+O2(g)2SO3(g)能增大正反应速率的措施是
A.通入大量O2 B.增大容器容积 C.移去部分SO3 D.降低体系温度 答案:A 解析:A. 通入大量O2,反应物浓度增大,正反应速率增大; B. 增大容积,反应物、生成物浓度均减小,正、逆反应速率均下降; C. 移去部分SO3会减小生成物浓度,刚开始正反应速率不变,而后下降; D. 该反应为放热反应,但是降低体系温度正、逆反应速率均减小;同理若增大体 系问题,正、逆反应速率增大; 9.(08年海南化学·10)X、Y、Z三种气体,取X和Y按1︰1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3︰2,则Y的转化率最接近于D A.33% B.40% C.50% D.66% 答案:D 解析:由可知: X+2Y2Z 起始: 1 1 0 转化: a 2a 2a 平衡: 1-a 1-2a 2a
根据题意有:2-3a2a = 32,a=13,Y的转化率最接近65%。
10.(08年山东理综·14)高温下,某反应达到平衡,平衡常数)H()CO()OH()CO(222ccccK。恒容时,温度升高,H2浓度减小。下列说法正确的是A A.该反应的焓变为正值 B.恒温恒容下,增大压强,H2浓度一定减小 C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2OCO2+H2 答案:A 解析:由平衡常数的表达式可得,该反应化学方程式应为CO2+H2CO+H2O,故D错;由题意知,温度升高,平衡向正反应移动,说明正反应为吸热反应,故该反应的焓变为正值,A正确;恒温恒容下,增大压强,H2浓度一定增大而不会减小,故B错;C项,升高温度,正逆反应速率都会 增大,故C错。
11.(09年安徽理综·11)汽车尾气净化中的一个反应如下:NO(g)+CO(g)12N2(g)+CO2(g) △H=-373.4kJ·mol-1。在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意
图正确的是:
催化剂 高温 答案:C 解析:该反应为气体计量数减小的放热反应,升高温度,平衡逆向移动,生成物浓度减小,反应物浓度增大,平衡常数减小,A选项错误;同理,升高温度,平衡逆向移动,CO的转化率减小,B选项错误;平衡常数只与热效应有关,与物质的量无关,C选项正确;增加氮气的物质的量,平衡逆向移动,NO的转化率减小,D选项错误。
12.(09年福建理综·12)某探究小组利用丙酮的溴代反应(CH3COCH3+Br
2
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率v(Br2)通过测定溴
的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
实验 序号 初始浓度c/mol·L-1 溴颜色消失 所需时间t/s CH3COCH3 HCl Br2
① 0.80 0.20 0.0010 290 ② 1.60 0.20 0.0010 145 ③ 0.80 0.40 0.0010 145 ④ 0.80 0.20 0.0020 580 分析实验数据所得出的结论不正确...的是 A.增大c(CH3COCH3), v(Br2)增大 B.实验②和③的v(Br2)相等 C.增大c(HCl), v(Br2)增大 D.增大c(Br2),v(Br2)增大 答案:D 解析:从表中数据看,①④中CH3COCH3,HCl的浓度是相同的,而④中Br2比①中的大,所以结果,时间变长,即速率变慢了,D项错。其他选项依次找出表中两组相同的数据,看一变量对另一变量的影响即可。 13.(09年广东化学·7)难挥发性二硫化钽(TaS2 )可采用如下装置提纯。将不纯的TaS2 粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下:
TaS2 (s)+2I2 (g) TaI4 (g)+S2 (g) 下列说法正确的是 A.在不同温度区域,TaI4 的量保持不变 B.在提纯过程中,I2 的量不断减少 C.在提纯过程中,I2 的作用是将TaS2 从高温区转移到低温区 D.该反应的平衡常数与TaI4 和S2 的浓度乘积成反比 答案:C 解析:高温区TaS2反应生成TaI4气体至低温区,从而在低温区重新生成TaS2,一段时
1123K 1023K
HCl
