华中科技大学有机化学第三篇烯烃
第三章 烯烃
CH2 CHC CH3 CH3
CH2
CH3CH
CH2
C CH3 CH3 2-甲基-2-丁烯
CH3CH2CH
CHCH3
3-甲基-1-丁烯
2. 顺反异构:由于双键旋转受阻,构造相同的分子中的 原子在空间排列方式的不同所造成的异构现象。
CH3 C H C CH3 H
顺-2-丁烯,bp:3.5℃,mp: -139.3℃,r:0.6213
(2).顺反异构体的命名 对于取代基不同的烯烃,很难用顺或反来表示,则 用Z,E表示。
a C b (Z) C d b (E) c a C C c c>d d a>b
优先基团选择规律 a. 原子量大的原子优先 Br>Cl>S>P>Si>F>O>N>C>B>Li>H b. 若取代基游离价所在的原子的原子序数和原子量相同而 无法决定其次序时,应用外推法即顺次比较第一个、第二 个…… (CH3)3C->(CH3)2CH->CH3CH2->CH3c. 确定不饱和基团的次序时,应把不饱和键的成键原子看 做是以单键分别和相同的原子相接。 例如: C O C 当作 C C C O 当作
CH3 C H C CH3 H
CH3 H
C C
H CH3
(Z)-2-丁烯
(E)-2-丁烯
较优先基团在双键同侧的构型为Z,在异侧的构型为E。 例如:
CH3 C C CH3CH2 CH(CH3)2 CH2CH2CH3
CH3 C C CH3CH2
CH(CH3)2 >
CH(CH3)2 CH2CH2CH3
CH2CH2CH3
在酸催化剂存在时,烯烃可与羧酸、醇加成生成羧酸酯和醚:
有机化学--第三章 不饱和烃:烯烃和炔烃

碳碳双键不能绕键轴自由旋转。因此,当两个双键碳 原子各连有两个不同的原子或基团时,可能产生两种不同 的空间排列方式。
一些烯烃的物理性质
构型:(I)和(Ⅱ)的分子式相同,构造亦相同,但分子中的原子在空间 排列不同。分子中原子在空间的排列形式称为构型。 构型异构体:(I)和(Ⅱ)是由于构型不同而产生的异构体,称为构型异 构体(configurational isomers)。构型异构体具有不同的物理性质。
3.1.1 碳原子轨道的sp2杂化
H
H
CC
H
Hale Waihona Puke H1/3s +2/3p
3.1.2 碳碳双键的组成
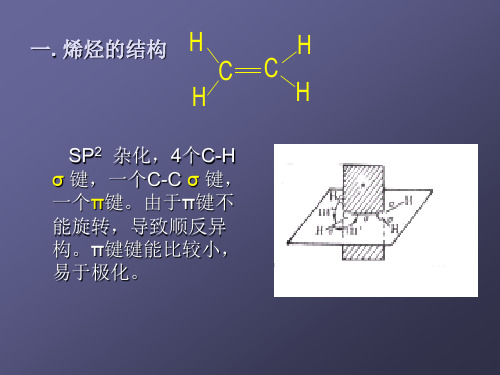
在乙烯中,成键的两碳原子各以一个sp2杂化轨道彼 此交盖形成一个C—C σ键,并各以两个sp2杂化轨道分 别与两个氢原子的1s轨道形成两个C—H σ键,这样形成 的五个σ键其对称轴都在同一平面内。
由于每个碳原子上余下的p轨道的对称轴垂直于同一 平面,且彼此平行,这样两个p轨道就从侧面相互平行交 盖成键,组成新的轨道,称为π轨道。处于π轨道的电子称 为π电子,这样构成的共价键称为π键。
含一个碳碳三键者称为炔烃(alkynes),通式为CnH2n-2, 碳碳三键(一C≡C一)是炔烃的官能团。分子中既含有碳碳 双键,又含有碳碳三键者称为烯炔。
3.1 烯烃和炔烃的结构
碳碳双键是由两对共用电子构成,通常用两条短线表 示:C=C。碳碳三键由三对共用电子构成,通常用三条 短线表示:C≡C。但实验事实表明,它们都不是由两个 或三个σ键加合而成:
与烷基相似,一个不饱和烃从形式上去掉两个氢原 子也构成亚基。最常见的不饱和亚基有—CH=CH—, 称为1,2-亚乙烯基。
有机化学 第三章 烯烃全

KOH
Br
C2H5OH
+ HBr
17
3-4 烯烃的物理性质
物质状态 C2~C4 气体,C5~C18液体 ,C19~固体
沸点、熔点和相对密度 均随相对分子量的增加而上升;直链烯烃的沸 点略高于支链烯烃;末端烯烃(α-烯烃)的沸点 略低于双键位于碳链中间的异构体。
溶解性 不溶于水,易溶于有机溶剂。
HCl CF3CH2CH2 Cl
Cl
CF3CH2CH2
(主)
HCl CF3CHCH3
Cl
Cl
CF3CHCH3
35
烯烃的亲电加成反应
HX反应活性 HI > HBr > HCl > HF
H2C CH2
HBr HAc
CH2 Br
CH2 H
HCl H2C CH2 AlCl3
H2C CH3 Cl
36
与硫酸的加成 ——间接水合
H3C C
H
CH3 C
H
H C
H3C
CH3 C
H
顺式
反式
7
3-2 烯烃的异构和命名
系统命名法
选主链:选择含双键的最长碳链作主链, 称 “某烯”, 若碳原子数大于10, 则称为“某碳 烯”;
编号:从靠近双键的一端开始编号,确定双键 (两双键碳原子中编号小的数字)及其它取代 基的位次;
其它同烷烃的命名。
18
顺 反 异 构 体 的 差 异
极性较大, b.p. 较高 极性较小, b.p. 较低
对称性较差,m.p. 较低
对称性较好,m.p. 较高19
3-5 烯烃的化学性质(重点)
• 反应:加成、氧化、卤代
α HCCC
有机化学第03章 烯炔烃

~
。
具有下列构型的烯烃均有顺反异构: 具有下列构型的烯烃均有顺反异构:
a b
C
a C b
a b
C
C
a d
a b
C
C
d e
注意:任何一个双键C上有相同基团,则无顺反异构。 注意:任何一个双键C上有相同基团,则无顺反异构。
⑵ 命名 顺反命名: ①顺反命名:
若取代基的第一个原子相同,则要外推比较。 ③若取代基的第一个原子相同,则要外推比较。 例: 比较大小: —CH2OH , —CH2CH3 原子序数: ﹥ 原子序数:O﹥C ∴前者为较优基团 比较大小: 比较大小: —C(CH3)3 ; C(C,C,C) ) —CH(CH3)2 ; C(C,C,H) —CH2CH3 ; C(C,H,H)化轨道 sp杂化的C原子, 杂化的 杂化轨道的电负性。 的电负性大于sp2杂化轨道的电负性。 从而使叁键比双键键短;叁键中π 从而使叁键比双键键短;叁键中π键P 轨道之间重叠程度及核对π 轨道之间重叠程度及核对π电子的束缚 力均大于烯烃。 力均大于烯烃。 炔烃π键的断裂和极化较烯烃困难。 ∴炔烃π键的断裂和极化较烯烃困难。
a
b
例题1 例题1
C
C
CH3 H
d
e
C
若 a >b , 若 a >b ,
C CH3 H
d>e d> d< d <e
C
则:(Z)(Z)(E)则:(E)C H CH3
CH3 H
(Z)-2-丁烯 ) 丁烯
(E)-2-丁烯 ) 丁烯
例题2 例题2
CH3 C2H5
C
CH3 C H
CH3 C2H5
有机化学 第三章 烯烃

在次卤酸中,氧原子的电负性(3.5) 较氯原子(3.0)和溴 原子(2.8)强,使分子极化成HO X。加成仍符合马氏规律。 在实际生产过程中,通常用氯和水代替次卤酸,结果生成 氯乙醇和,1,2-二氯乙烷。
CH2=CH2
Cl2/H2O
δ- δ+
CH2CH2 + CH 2CH2 Cl OH Cl Cl
– 反应机理
– 顺反异构体的命名
• 顺/反标记法 相同基团在双键同侧为“顺(cis)” ,反之,为“反(trans)”。 • Z/E标记法 依照“次序规则”,比较双键碳上连接的两个基团, 较优基团在双键同侧为“Z” ,反之,为“E”。
CH3 H C C CH3 CH3 H
H
C
C
CH3 CH2CH3
CH3CH2 H
有 机 化 学 ORGANIC CHEMISTRY
第三章 烯烃
CHAPTER 3 ALKENES
第三章 烯 烃 3 ALKENES
分类
开链烯烃 如:(CH3)2C=CH2
按碳的连 接方式分
环烯烃
如:
单烯烃 按双键 数目分 多烯烃
如:H2C=CH2
如:
第一节 烯烃的结构、异构和命名 3.1 Structure,Isomerism and nomenclature
• 加卤化氢 如:
一卤代烷
AlCl3 130~ 250℃
CH2=CH2 + HCl
CH3CH2Cl
分子不对称的烯烃加HX时,可得两种加成产物:
CH3CH=CH2 + HX CH 3CH2CH2X + CH 3CHCH3 X
马氏(Markovnikov)规律:不对称烯烃发生亲电加成时, 酸中带正电荷的质子H+总是加到含氢较多的双键碳原子 上,而负性基团加到含氢较少的双键碳原子上。如:
大学有机化学第三章 烯烃和炔烃

CH3 → CH=CH2 + HX
CH3CH—CH3 X
马代规则是 不对称试剂与双键发生亲电性加成时, 试剂中正电性部分主要加到能形成较稳定正碳离子 的那个双键碳原子上。 + CH3CHCH3 δ+ δ-
CH3—CH=CH2 + H+
HX分子中的氢以H+ 质子形式发生反应,因此称为亲电试剂
CH3CH2CH2
CH3
顺反异构命名与Z .E命名规则不相同,不能混为一 谈,两者之间没有固定的关系
例如:
Cl Cl C=C CH3 H (Z)-1 , 2-二氯丙烯 顺-1 , 2-二氯丙烯 H C H ‖ C H H 大 Br
Cl
C=C
CH3
Cl 大
Cl C COOH ‖ C Br Cl
(E)-1 , 2-二氯-1-溴丙烯 顺--1 , 2-二氯-1-溴丙烯 CH3 C H ‖ C H H
次产物
因此 1.1.1-三氟-3-氯丙烷是主要产物
2. 加硫酸
R-CH=CH2 + HOSO2OH H3PO4 300℃ 7Mpa R-CHCH3 H2O RCH-CH3 OSO2OH OH (间接水化法制备醇) CH3CH2OH
CH2=CH2 + H2O
3. 加卤素
CH2 = CH2 + X2
CH2 = CH2 + Br2/CCl4 Br2/H2O CH2—CH2 X X CH2-CH2 Br Br
如遇到含多个双键化合物而主链编号有选择时,则编号应从 顺型双键的一端开始 4 1 如 3 2 CH3 H 6 5 CH2 C=C 7 C=C H H H CH3 顺· 反-2.5-庚二烯
四、物理性质 五. 化学性质
有机化学 第03章 单烯烃

例
H2C CH OCH3 H2C CH Cl H2C CH CH2 NH2
甲基乙烯基醚
乙烯基氯
烯丙基胺
烯烃的化学性质
1. 双键的结构与性质分析
C
C
C
C
键能: s 键 ~347 kJ / mol p 键 ~263 kJ / mol p 键活性比 s 键大 不饱和,可加成至饱和
p 电子结合较松散, 易参与反应。是电子 供体,有亲核性。 与亲电试剂结合 与氧化剂反应
邻二卤代烷
OH X R CH CH2 X2 H2O
硫酸氢酯
H2O R CH CH2 H HOR' H
OH R CH CH3
b-卤代醇
醇
O R CH CH2
H
R'COOH
OR'
R
OCOR' R CH CH3 酯
CH CH3
取代环氧乙烷
醚
5. 亲电加成反应机理 (I)—— 经碳正离子的加成机理
① 与HX的加成机理
亲电加成中的重排现象及解释
CH3 HCl CH2 CH3 H3C C CH CH2 H Cl H
加成机理对Markovnikov规则的解释
HBr CH CH2 CH3CH2 CH Br CH2 H + 4:1 CH3CH2 CH H CH2 Br
例: CH3CH2
机理:
CH3CH2 CH CH2 H Br
2o 正碳离子 较稳定
1o 正碳离子 较不稳定
CH3CH2 CH Br
CH2 H
+
CH3CH2 CH H
1
CH CH2 与 CH2CH2CH3
CH CH2
有机化学第3章课后习题答案

有机化学第3章课后习题答案work Information Technology Company.2020YEAR第三章 烯烃二、写出下列各基团或化合物的结构式:① 乙烯基 CH 2=CH- ② 丙烯基 CH 3CH=CH- ③ 烯丙基 CH 2=CHCH 2-CH 3C=CH 2C=C CH 3CH CH 3CH 3H CH 3CH 2CH 3CH 3C CCH 2CH 3CH 3CH 2C=C CH 3CH(CH 3)2CH 2CH 2CH 3三、命名下列化合物,如有顺反异构现象,写出顺反(或)Z-E 名称:1.CH 3CH 2CH 2C=CH 2CH 3CH 22.CH 3CH 22CH 3C=C CH2CH 3CH 33.Cl C=CCH 3CH 2CH 3CH 3CH CH 34.ClBr5.6.C=C CH 3CH 2CH 3C 2H 5CH 3HHH 7.nPr i PrC=CMeCH38MeC=C n BtEtMe五、2,4-庚二烯有否顺反异构现象,如有,写出它们的所有顺反异构体,并以顺反和Z,E 两种命名法命名之。
解:CH3C=CHH2CH33HC=CCHCH3HCH32CH3CH3H2CH3HH六、3-甲基-2的主要产物:CH 3CH=CCH 2CH 3CH 3H 2/Pd -CCH 33CH 22CH 33CH CCH 2CH 3Br CH 33CHCCH 2CH 3CH 3Cl Cl3CH CCH 2CH 3CH 3OHOH 3CHO+CH 3CCH 2CH 3O3CH CHCH 2CH 3CH 33CHCH 32CH 3Br七、乙烯、丙烯、异丁烯在酸催化下与水加成生成的活性中间体分别为: 稳定性顺序 及反应速度顺序是CH 3CH 2+CH 3CH +CH 3CH 3CH 33+CH 3CH 2+CH 3CH +CH 3CH 3CH 33+<<八、试以反应历程解释下列反应结果:(CH 3)3CCH=CH 2+H 2O H +(CH 3)3CCHCH 3OH +(CH 3)2CCH(CH 3)2OH(CH 3)3CCH=CH 2+H +CH 3CCH 3CH 3CH +CH 3CH 3CH 33CH +CH 3+H 2OCH 3CCH 3CH 3CH CH 3CH 3CCH 3CH 3CH CH 3OH 2+H+CH 3CCH3CH 3CHCH 3+CH 3C 2CH 3CH 33CH 3C CH 3CH 3CHCH 3H 2O+OH九、试给出经臭氧化,锌纷水解后生成下列产物的烯烃的结构:1.CH 3CH 2CHOHCHO CH 3CH 2CH=CH 22.CH 3CH 2CCH 3CH 3CHOOCH 3CH 2CH 333.CH 3CHO,CH 3CH 3C O,CH2CHOCH 3CH=CH -CH 2CH 3-CH=CCH 3十列化合物:CH 2OCHClCH 2Ca(OH)OHCH 2ClCH ClCH 2HOClClCH 2CH=CH 2Cl 2+CH 3CH=CH 2nCN[CH ]-CH 2CH 2=CHCNC470NH 3+CH 3CH=CH 2Cl Cl CH 2CHCH 2Cl ClCH 2CH=CH 2C500Cl 2+CH 3CH=CH 2CH 3CH 2CH 2OHB 2H 6+CH 3CH=CH 2CH 3CHCH 3H +H 2O +CH 3CH=CH 2CH 3CH 2CH 2BrROOR HBr +CH 3CH=CH 2BrCH 3CHCH 3HBr+CH 3CH=CH 2NaOH,H O十一、某烯烃催化加氢得2-甲基丁烷,加氯化氢可得2-甲基-2-氯丁烷,如果经臭氧化并在锌粉存在下水解只得丙酮和乙醛,写出给烯烃的结构式以及各步反应式:CH 3C CH 3=CHCH 3CH 3C CH 3=CHCH 3CH 3C CH 3=CHCH 3+H 2CH 3CH 32CH 3+HClCH 3CHCH 2CH 3CH 3Cl +O 3CH 3CH 3C O CHCH 3OOZn/CH 3COOH/H 2OCH 3C CH 3+CH 3CHO十二、某化合物分子式为C 8H 16,它可以使溴水褪色,也可以溶于浓硫酸,经臭氧化,锌粉存在下水解只得一种产物丁酮,写出该烯烃可能的结构式。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
二、烯烃的命名
简单的烯经可以用普通命名法命名。复杂的烯烃用系统命名法命名。 1. 构造异构体 烯烃的构造异构体的系统命名法的要点为: (1)选择含碳碳双键的最长碳链作为主链,并按主链上碳原子的数目称 为某烯。碳原子数在十以上用汉字数字表示,称为某碳烯,如十二碳烯。 (2)从主链上靠近双键的一端开始编号,使双键碳原子的编号最小。 (பைடு நூலகம்)在烯烃名称之前,用阿拉伯数字标出双键的位置。取代基的名称和 位置的表示方法与烷烃相同。例如:
乙烯分子中的碳原子轨道为sp2杂化,碳上的3个sp2轨道处于 同一平面,角度120。碳原子上还有一个和该平面垂直的P轨道。
H
H
H
H
碳碳双键是由一个σ键和一个键组成。 σ键的轨道呈轴对称, 而 键的轨道呈平面对称。
碳原子的二个sp2分别与两个氢原子的1s轨道生成两个σ键,一
个sp2与另一个碳的sp2 轨道生成一个σ键; 所有σ键都在同一平面 上, 键角120。两个pz轨道互相平行从侧面重叠生成键。碳碳双键 和单键不同,它不能旋转,因为旋转就要破坏p轨道与p轨道的重叠, 也就破坏了键。
卤化氢与不对称烯烃加成时理论上可以生成两种加成产物:
卤化氢与不对称烯烃加成所生成的主要产物是氢原子加在含氢较 多的双键碳原子上。这一区域选择性规律被称为马科夫尼可夫规律。
卤化氢与烯烃的加成反应是分步进行的离子型反应。卤化氢分子中带 部分正电荷(δ+)的氢原子接近烯键的电子云时,H-X发生异裂,同时质子 接受一对电子( 键破裂)生成碳正离子(carbocation),这是整个反应的 速度决定步骤(rate-determining step)。
键角:碳碳双键与相邻键夹角120左右 乙烯分子中,HCH: 117.2 HCC: 121.4
• 乙烯的模型
3.2 烯烃的同分异构和命名
一、烯烃的异构 1.构造异构
丁烯有三种构造异构体: 1-丁烯和异丁烯是碳链结构不同的碳 链异构体。1-丁烯和2-丁烯是双键的位置不同而产生的异构体, 叫做官能团位置异构。因此,烯烃的构造异构比烷烃复杂。
烯烃去掉一个氢原子的一价基称为某烯基,烯基的编号应从游 离价所在的碳原子开始。
在同一碳原子上有两个游离价的称为亚基:
2. 顺反异构体 (1)顺-反法
在烯烃的系统名称前冠以“顺”或“反”表示烯烃的构型。例如:
在两个双键碳原子上没有共同的原子或取代基时,用顺-反法表 示构型有困难,则采用Z-E法来标记烯烃的构型。
(2) Z-E法 根 据 系 统 命 名 法 , 顺 反 异 构 体 的 构 型 用 Z( 德 文 Zugammen,
同侧)和E(德文Entgegen,异侧)来表示。
构型是Z或E要用“次序规则”(sequence rule)来决定。一 般情况下可用基团的大小来确定,大基团在双键同侧的构型为Z, 在异侧的构型为E。
3.4 烯烃的化学性质
碳碳双键的键键能比σ键小,因而容易在双键碳原子上加两个原 子或原子团而转变成两个更强的σ键,这样的反应叫做加成反应 (reaction of addition)。
一、亲电加成反应 1.加卤化氢
烯烃与卤化氢起加成反应生成一卤代烷.
烯烃与卤化氢的加成反应一般在极性有机溶剂中进行。HX对烯烃 的加成活性顺序与它们的酸性强度一致:HI>HBr>HCl。
进攻试剂实际上是带正电荷的质子,它从 键接受一对电子,与双 键的碳原子形成σ键,这种试剂叫做亲电试剂(eIectrophile)。由亲电试 剂的进攻引起的反应叫做亲电反应。因此烯烃与卤化氢的加成反应是亲 电加成反应(electrophilic addition)。
碳正离子非常活泼,在一般的有机反应条件下,其存在时间很短(1010-10-6 s)。1962年,美国化学家欧拉(Olah)把(CH3)3CF溶于过量的超 强酸SbF5中,然后用核磁共振检测证实了叔丁基碳正离子(CH3)C+SbF6的存在。
第三章 烯 烃
烯烃是含有碳碳双键的不饱和烃。
自然界存在许多烯烃类化合物。许多热带植物的叶子可以产生 乙烯。乙烯有催熟作用,它还可以加速树叶死亡与脱落。
自然界中还有许多结构复杂的烯类化合物,如萜类与甾族中的 某些化合物。
天然橡胶就是其中重要的一种,具有如下结构:
CH3 H2CCCHCH2 n
3.1 烯烃的结构
顺-反法和Z-E法是表示烯烃构型的两种不同的命名方法。顺-和
(Z)、反-和(E)没有对应关系,即顺式不一定是(Z)-构型,反式也不一定 是(E)-构型。
3.3 烯烃的物理性质 烯烃的物理性质和烷烃很相似。 在室温下含二个到四个碳原子的烯烃为气体, 含五个至十八个碳原子的为液体, 含十九个碳原子以上的为固体。
例如:2-丁烯分子中,与双键相连的两个甲基或两个氢原子在空间 有两种排列方式,即在双键平面的同侧(顺式,cis)或异侧(反式, trans)。
顺式和反式异构体在常温下不能彼此互变,是构型不同的两个化 合物,它们的物理性质完全不同,可以用物理方法分离。
烯烃分子中双键的两个碳原子各带有不同的原子或取代基时 都会有顺反异构体
两个p轨道侧面重叠比头碰头重叠程度小, 键的键能比σ键小。
C-C 键: 263.6kJ/mol C-C σ键 347.3kJ/mol C=C键: 610.9kJ/mol
同时, 电子云分布在σ键的上方和下方, 离原子核较远,容易发生极化。
键没有σ键牢固,化学活泼性较大。
键长:双键比单键短 C-C单键: 154pm C=C双键:134pm
一些烯烃分子具有较小的极性,例如:
碳原子的电负性随杂化轨道的s成分的增加而增大。 因此电负性大小次序为;C(sp)>C(sp2)>C(sp3)。
顺式异构体的沸点较高, 因为偶极吸引力大。 反式异构体熔点较高, 因为具有较好的对称性。 顺反异构体的偶极矩、沸点、熔点的差异对于确定顺 反构型是有用的。
烯烃的构造异构体可以从相应的烷烃出发,变动双键的位置导出。 例如,戊烯有五种构造异构体,两种可以从戊烷导出:
2. 顺反异构
烯烃的顺反异构现象(cis-trans isomerism)是由于碳碳双键旋转 受阻而产生的。
顺反异构体分子中的原子互相连接的次序和方式相同即构造式相同, 但分子中的原子在空间排列方式不同即构型(configuration)不同。
