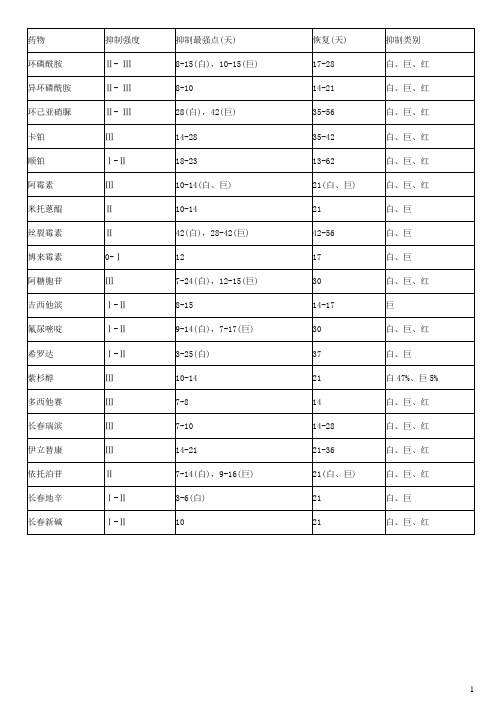
化疗后骨髓抑制分度
(完整版)化疗诱发骨髓抑制的分级和处理

(完整版)化疗诱发骨髓抑制的分级和处理简介化疗是一种常见的治疗癌症的方法。
然而,一些化疗药物可能导致骨髓抑制,这是一种破坏骨髓造血功能的副作用。
由于药物的不同和患者的个体差异,骨髓抑制的严重程度也会有所差异。
因此,对化疗诱发的骨髓抑制进行分级和适当处理非常重要。
分级1. 无骨髓抑制当患者在化疗过程中没有出现骨髓抑制的症状时,可被分级为无骨髓抑制。
2. 轻度骨髓抑制轻度骨髓抑制是指患者可能会出现一些轻微的造血功能损害,但没有明显症状的情况。
一般来说,血细胞计数在正常参考范围的下限附近。
3. 中度骨髓抑制中度骨髓抑制是指患者出现较为明显的造血功能损害,可能会导致贫血、血小板减少以及白细胞减少。
需要密切观察患者的症状并进行相应的处理。
4. 重度骨髓抑制重度骨髓抑制是最严重的分级,患者的造血功能受到严重破坏,可能会出现严重的贫血、出血倾向以及免疫功能低下。
这种情况需要及时采取紧急措施进行处理。
处理化疗诱发的骨髓抑制的处理应根据不同分级采取不同的策略。
1. 无骨髓抑制对于无骨髓抑制的患者,需密切监测血细胞计数,并定期进行化疗进展评估。
如果患者保持稳定状态,可继续进行正常的化疗计划。
2. 轻度骨髓抑制对于轻度骨髓抑制的患者,需要密切监测血细胞计数,并酌情调整化疗剂量或延长化疗间隔时间。
如果患者的骨髓功能恢复良好,可继续化疗。
3. 中度骨髓抑制对于中度骨髓抑制的患者,应及时采取措施进行治疗。
这包括鼓励患者适当休息、提供生活上的支持,以及应用支持性治疗如输血、使用生长因子等。
此外,可能需要调整化疗计划或暂停化疗,直到骨髓功能恢复。
4. 重度骨髓抑制对于重度骨髓抑制的患者,需要立即采取紧急措施进行处理。
这可能包括立即停止化疗、输血、使用生长因子、抗感染治疗等。
骨髓移植可能是一个选择性治疗方法。
总结化疗诱发的骨髓抑制需要进行分级和适当处理。
通过对患者的骨髓抑制程度进行分级,可以帮助医生确定相应的处理策略。
及时监测血细胞计数,并根据不同分级调整化疗剂量和计划,可以最大程度地减少骨髓抑制给患者带来的负面影响。
化疗后骨髓抑制的分度和处理
贫血不仅使患者的组织乏氧导致一般状况差,而且还可能降低放疗或化疗的效果。
对粒系抑制而言,中性粒细胞绝对值比白细胞总数更为重要。
注意两个关键节点:一是中性粒细胞绝对值低于1×109/L,二是血小板计数低于50×109/L。
它们分别是3度粒细胞减少和3度血小板减少的临界点,是容易出现并发症的信号,也是需要给予干预的指征。
II度以上骨髓抑制:停止化疗。
粒细胞的减少通常开始于化疗停药后一周,至停药10-14日达到最低点,在低水平维持2~3天后缓慢回升,至第21~28天恢复正常,呈U型。
血小板降低比粒细胞降低出现稍晚,也在两周左右下降到最低值,其下降迅速,在谷底停留时间较短即迅速回升,呈V型。
红细胞下降出现的时间更晚。
正常血细胞半数生存期: WBC 6-8小时,PLT 5-7天,RBC 120天;因而化疗后WBC↓出现早且重;PLT↓出现晚且相对轻;RBC↓少见。
白细胞下降呈“U”型,血小板下降呈“V”曲线。
化疗后骨髓抑制的规律具有以下意义:(1)它限定化疗疗程的间隔时间。
理论上,化疗应该在最短时间内施以最强剂量,以迅速抑制或杀灭肿瘤细胞。
但化疗后骨髓抑制的恢复需要时间,故很多化疗是3~4周进行一次;(2)涉及对2度骨髓抑制的处理。
对于3度和4度骨髓抑制必须给予干预已经成为共识,但对于2度骨髓抑制,何时必须干预,何时可以短暂观察则较为困惑。
利用上述规律,有助于决策(后述)烷化剂(环磷酰胺、氮芥等)和鬼臼毒素(VP16)的骨髓抑制作用较强。
在铂类药物中,卡铂的肾脏毒性小于顺铂,但其骨髓抑制的作用强于后者。
紫杉醇类药物的主要副作用是过敏反应和周围神经炎,骨髓抑制作用尚不及烷化剂,但多烯紫杉醇(泰索蒂)的骨髓抑制作用较强。
拓泊替康的骨髓抑制作用很强关于输入浓缩红细胞:输入浓缩红细胞的优点是能迅速提高贫血患者的携氧能力,缺点是存在输血相关的风险。
当血红蛋白达到70~80g/L时,绝大多数患者的携氧能力正常。
(详细版)化疗导致骨髓抑制的分级和处理

(详细版)化疗导致骨髓抑制的分级和处理
引言
该文档旨在介绍化疗导致骨髓抑制的分级和处理方法。
骨髓抑制是化疗中常见的不良反应之一,对患者的健康状况和治疗结果有重要影响。
因此,正确地分级和处理骨髓抑制是至关重要的。
分级骨髓抑制
根据血液学检查结果,骨髓抑制可分为三个等级:轻度、中度和重度。
以下是每个等级的定义和特征:
1. 轻度骨髓抑制:血小板计数稍低但仍在正常范围,中性粒细胞计数正常。
2. 中度骨髓抑制:血小板计数明显降低,中性粒细胞计数较低但仍在正常范围。
3. 重度骨髓抑制:血小板计数极低,中性粒细胞计数明显降低或完全缺失。
处理骨髓抑制
处理骨髓抑制的方法取决于其严重程度:
1. 轻度骨髓抑制:通常不需要特殊处理,但需要密切监测患者的血液学指标。
2. 中度骨髓抑制:可能需要采取以下措施:
- 减少化疗剂量或延长化疗周期,以给骨髓更多时间恢复。
- 给予增加血小板计数的药物,如血小板生成素。
- 接受输血以增加血小板计数。
- 减少感染风险,避免接触感染源。
3. 重度骨髓抑制:需要紧急处理,可能需要以下措施:
- 停止或暂停化疗,直到骨髓指标得到恢复。
- 接受输血或血小板输注,以增加血液元素。
- 接受抗生素治疗以预防或治疗感染。
结论
化疗导致的骨髓抑制严重程度的准确分级和及时处理对患者的健康至关重要。
医护人员应密切监测患者的血液学指标,并根据不同等级的骨髓抑制采取适当的处理措施。
早期介入和合理处理可以最大限度地减少并发症和提高治疗效果。
化疗导致的骨髓抑制及其处理]
![化疗导致的骨髓抑制及其处理]](https://img.taocdn.com/s3/m/b1e7dc015f0e7cd185253609.png)
无反应滴度
递增剂量维持疗效
应当调整每位患者的剂 量,以维持足以避免红 细胞输注的最低血红蛋 白水平。 如果Hb达到避免输血 所需的水平或在任何2 周时间内增加> 1 g/dL ,对于阿法依泊汀,降 低25%的剂量,对于阿 法贝泊汀,降低40%的 剂量。
•
增加阿法贝泊汀至300 mcg固定剂量, 每2周1次,皮下注射6 增加阿法贝泊汀至500 mcg固定剂量, 每3周1次,皮下注射
骨髓抑制作用突出的常用化疗药物
烷化剂(环磷酰胺、氮芥等)和鬼臼毒素(VP16)的骨髓抑制 作用较强。 在铂类药物中,卡铂的肾脏毒性小于顺铂,但其骨髓抑制的作 用强于后者。 紫杉醇类药物的主要副作用是过敏反应和周围神经炎,骨髓抑 制作用尚不及烷化剂,但多烯紫杉醇(泰索蒂)的骨髓抑制作 用较强。 拓泊替康的骨髓抑制作用很强,曾与卡铂联合用于大剂量化疗 加外周血造血干细胞移植时骨髓动员前的抑制药物。
化疗后血小板减少的处理
• 对因处理: 暂停化疗或化疗减量
• 刺激造血:IL-11、TPO
• 预防出血:输注血小板、减少创伤性出血机会
IL-11的使用及其不良反应
• 预防性应用:上程化疗出现III/IV度血小板下降,于化疗 后24-48小时开始。 • 治疗性应用:血小板减少时。 • 剂量:IL-11 50μg/kg sc qd。 • 停药指针:应用7-14天,或血小板计数恢复正常时及时停 药。 不良反应 • 心慌、心悸。有心衰、房颤、房扑病史的患者慎用。 • 血管渗漏综合征:结膜充血,胸腹腔积液、下肢浮肿、体 重增加。
癌症患者输注红细胞的适应证 ( NCCN指南2011 )
目标:预防或治疗携氧能力不足 无症状性 • 血流动力学稳定的慢性贫血,无急性冠脉综合征 输血目标是维持血红蛋白在7 – 9 g/dL 症状性 • 有血流动力学不稳定或氧运输能力不足证据的急性出血: 输血目标是纠正血流动力学不稳定和保持充足的氧运输 • 症状性(包括心动过速、呼吸急促、体位性低血压)贫血( 血红蛋白<10 g/dL): 输血目标是根据需要,维持血红蛋白在8 – 10 g/dL,以预防 症状 • 急性冠脉综合征或急性心肌梗死背景中的贫血: 输血目标是维持血红蛋白≥10 g/dL
化疗后判断骨髓抑制的标准和阶段
骨髓抑制就是指骨髓中的血细胞前体的活性下降,主要就是表现为血象中的白细胞和血小板数量下降,大多数的化疗药物都会出现不同程度的骨髓抑制,比如卡铂、异环磷酰胺、长春碱类、阿霉素等。
骨髓抑制往往是影响化疗的一个关键因素,一方面骨髓抑制会影响化疗的效果,另一方面会使病人出现致命性的感染和出血。
因此,化疗期间的检查,每2-3天的血常规是必不可少的。
出现骨髓一直,情况严重的可能会中途停止化疗,这样治疗的效果大大降低,如何配合服用人参皂苷rh2,在一定程度上能够降低骨髓抑制的发生率。
骨髓抑制的程度
其中白细胞是支撑机体免疫力,如果白细胞下降,人体免疫力就下降,而且会引起粒细胞减少症,而粒细胞减少的结果就是感染,包括消化道、呼吸道和皮肤黏膜都会出现感染。
血红蛋白减少,会使血液的运氧能力下降,患者会出现贫血的症状。
血小板则主要起着凝血的作用,如果数量减少,就可能出现出血的情况,包括鼻出血、牙龈出血、消化道出血,最严重的就是脑出血。
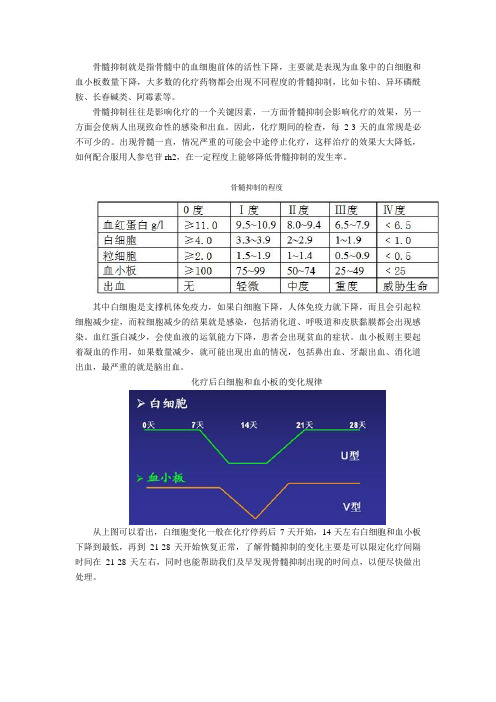
化疗后白细胞和血小板的变化规律
从上图可以看出,白细胞变化一般在化疗停药后7天开始,14天左右白细胞和血小板下降到最低,再到21-28天开始恢复正常,了解骨髓抑制的变化主要是可以限定化疗间隔时间在21-28天左右,同时也能帮助我们及早发现骨髓抑制出现的时间点,以便尽快做出处理。
化疗致骨髓抑制的分级和处理

化疗致骨髓抑制的分级和处理一、定义骨髓抑制是指骨髓中的血细胞前体的活性下降。
血流里的红细胞和白细胞都源于骨髓中的干细胞。
血流里的血细胞寿命短,常常需要不断补充。
为了达到及时补充的目的,作为血细胞前体的干细胞必须快速分裂。
化学治疗(Chemotherapy)和放射治疗(radiation)、以及许多其它抗肿瘤治疗方法,都是针对快速分裂的细胞,因而常常导致正常骨髓细胞受抑。
骨髓抑制是多数化疗药的常见毒性反应。
化疗是恶性肿瘤的主要治疗方法之一,骨髓抑制是其主要的副作用。
骨髓抑制不仅延缓化疗的进行而影响治疗效果,而且可能导致并发症而危及患者生命。
一些恶性肿瘤患者或许不会很快死于疾病本身,却可能由于骨髓抑制致命。
因此,及时发现骨髓抑制并给予相应处理是化疗的重要环节。
二、诊断与鉴别诊断骨髓抑制通常发生在化疗后。
因粒细胞平均生存时间最短,约为6-8小时,因此骨髓抑制常最先表现为白细胞下降;血小板平均生存时间约为5-7天,其下降出现较晚较轻;而红细胞平均生存时间为120天,受化疗影响较小,下降通常不明显。
多数化疗药物所致的骨髓抑制,通常见于化疗后1-3周,约持续2-4周逐渐恢复,并以白细胞下降为主,可有伴血小板下降,少数药如健择、卡铂、丝裂霉素等则以血小板下降为主。
所以在化疗后可检测白细胞和血小板的数量来判断是否发生了骨髓抑制。
三、骨髓抑制的分度目前化疗后骨髓抑制的分度采用的是世界卫生组织抗癌药物急性及亚急性毒性反应分度标准(表1)。
以前对红系抑制的关注较少,原因在于贫血的处理相对简单而且见效迅速,输血或输入浓缩红细胞均可。
但实际上贫血不仅使患者的组织乏氧导致一般状况差,而且还可能降低放疗或化疗的效果。
对粒系抑制而言,中性粒细胞绝对值比白细胞总数更为重要。
注意两个关键节点:一是中性粒细胞绝对值低于1×109/L,二是血小板计数低于50×109/L 。
它们分别是3度粒细胞减少和3度血小板减少的临界点,是容易出现并发症的信号,也是需要给予干预的指征。
骨髓抑制程度分级标准
骨髓抑制程度分级标准一、目的本标准规定了骨髓抑制程度分级的方法和标准,为临床治疗和评估提供依据。
二、适用范围本标准适用于对恶性肿瘤化疗后骨髓抑制程度进行评估。
三、定义骨髓抑制是指恶性肿瘤化疗后,由于化疗药物的毒性作用,导致骨髓造血功能受到抑制,表现为外周血白细胞、红细胞、血小板等指标下降。
四、分级标准根据外周血白细胞、红细胞、血小板等指标的变化,骨髓抑制程度可分为0-Ⅳ度。
1. 白细胞减少分级* Ⅰ度:白细胞计数≥3.0×10^9/L,中性粒细胞计数≥1.5×10^9/L;* Ⅱ度:白细胞计数2.0-3.0×10^9/L,中性粒细胞计数1.0-1.5×10^9/L;* Ⅲ度:白细胞计数1.0-2.0×10^9/L,中性粒细胞计数0.5-1.0×10^9/L;* Ⅳ度:白细胞计数<1.0×10^9/L,中性粒细胞计数<0.5×10^9/L。
2. 红细胞减少分级* Ⅰ度:血红蛋白≥110g/L;* Ⅱ度:血红蛋白90-110g/L;* Ⅲ度:血红蛋白60-90g/L;* Ⅳ度:血红蛋白<60g/L。
3. 血小板减少分级* Ⅰ度:血小板计数≥75×10^9/L;* Ⅱ度:血小板计数50-74×10^9/L;* Ⅲ度:血小板计数25-49×10^9/L;* Ⅳ度:血小板计数<25×10^9/L。
五、处理原则根据骨髓抑制程度分级,采取相应的治疗措施,包括药物治疗、输血、成分输血等。
同时,需密切监测患者病情变化,及时调整治疗方案。
六、注意事项本标准仅供参考,具体治疗方案应根据患者病情和医生建议制定。
在使用化疗药物治疗时,应充分考虑患者的病情、年龄、身体状况等因素,谨慎选择药物和剂量。
化疗不良反应分度
化疗就是恶性肿瘤得主要治疗方法之一•髓抑制就是其主要得副作用。
计髓抑制不仅延缓化疗得进行而影响治疗效果,而且可能导致并发症而危及患者生命。
一些恶性肿瘤患者或许不会很快死于疾病本身,却可能由于丹腌抑制致命。
因此,及时发现卄髓抑制并给予相应处理就是化疗得重要环节。
一、化疗后竹軸抑制得分度:目前化疗后骨髄抑制得分度采用得就是世界卫生组织抗癌药物急性及亚急性毒性反应分度标准(表1 )0以前对红系抑制得关注较少,原因在于贫血得处理相对简单而且见效迅速, 输血或输入浓缩红细胞均可。
但实际上贫血不仅使患者得组织乏氧导致一般状况差,而且还可能降低放疗或化疗得效果。
对粒系抑制而言,中性粒细胞绝对值比白细胞总数更为重要。
注意两个关键节点:一就是中性粒细胞绝对值低于1 X109/L,二就是血小板il•数低于50 X 109/L。
它们分别就是3度粒细胞减少与3度血小板减少得临界点,就是容易出现并发症得信号,也就是需要给予干预得指征。
01234血红蛋白(g/L)Mil 0109-959 4-8079-6 5<65白细胞(1 0 9/L)M 4、03、9一3、02、92 01、9-1. 0<1> 0粒细胞(109/L)^2.01、9-1.51. 4-1. 00 . 9-0.5<0、5血小板(109/L)2 10099-7 574-5 04 9-25<25一般认为,粒细胞得减少通常开始于化疗停药后一周,至停药10-14日达到最低点,在低水平维持2~3天后缓慢回升,至第21-28天恢复正常,呈U型。
血小板降低比粒细胞降低出现稍晚,也在两周左右下降到最低值,其下降迅速,在谷底停留时间较短即迅速回升,呈V型。
红细胞下降岀现得时间更晚。
化疗后计僦抑制得规律具有以下意义:(1)它限左化疗疗程得间隔时间。
理论上,化疗应该在最短时间内施以最强剂量,以迅速抑制或杀火肿瘤细胞。
但化疗后悄•髓抑制得恢复需要时间, 故很多化疗就是3~4周进行一次;(2)涉及对2度秤髓抑制得处理。
(全面版)化疗引发骨髓抑制的分级和处理
(全面版)化疗引发骨髓抑制的分级和处理概述化疗是一种常见的治疗癌症的方法,但它可能会引发骨髓抑制,这是一种严重的副作用。
本文档将介绍骨髓抑制的分级和处理方法。
分级根据骨髓抑制的严重程度,通常将其分为以下三个级别:级别一:轻度骨髓抑制轻度骨髓抑制是指患者的血象指标基本维持在正常范围内,但可能会出现以下可逆的症状:- 乏力- 疲劳- 无力- 轻微的贫血级别二:中度骨髓抑制中度骨髓抑制是指患者的血象指标明显下降,可能出现以下症状:- 明显的乏力和疲劳- 贫血- 血小板减少- 白细胞减少在此级别下,患者需要密切监测其血液指标,并采取相应的处理措施。
级别三:重度骨髓抑制重度骨髓抑制是指患者的血象指标显著下降,可能造成以下严重的并发症:- 严重的贫血- 严重的血小板减少,易引发出血- 严重的白细胞减少,易引发感染患者在此级别下需要进行紧急处理和救治,以避免进一步的并发症发生。
处理针对不同级别的骨髓抑制,可以采取以下处理方法:级别一处理- 给予患者足够的休息和良好的营养- 鼓励患者进行适量的运动和体力活动- 监测血象指标,以确保没有进一步的恶化- 如有需要,可以考虑给予患者一些血液增强剂或支持治疗级别二处理- 密切监测血象指标,确保及时发现任何恶化- 如果血象指标持续下降,需要考虑调整化疗方案或减少剂量- 采取必要的感染防控措施,以避免继发感染- 如有需要,可以考虑输血或使用造血生长因子来帮助恢复造血功能级别三处理- 紧急采取救治措施,包括输血、抗感染治疗等- 考虑暂停或中止化疗,直到患者的血象指标恢复到安全水平- 评估患者的病情和化疗方案,重新制定治疗计划- 如有需要,进行骨髓移植等进一步治疗结论骨髓抑制是化疗的常见副作用之一,需要根据其严重程度进行分级和处理。
医务人员应密切关注患者的血象指标,并采取相应的处理措施,以确保患者的安全和康复。
同时还需要根据患者的病情和化疗方案进行调整,以提高治疗效果。
化疗致骨髓抑制的分级和处理
创作编号:GB8878185555334563BT9125XW创作者:凤呜大王*化疗致骨髓抑制的分级和处理一、定义骨髓抑制是指骨髓中的血细胞前体的活性下降。
血流里的红细胞和白细胞都源于骨髓中的干细胞。
血流里的血细胞寿命短,常常需要不断补充。
为了达到及时补充的目的,作为血细胞前体的干细胞必须快速分裂。
化学治疗(Chemotherapy)和放射治疗(radiation)、以及许多其它抗肿瘤治疗方法,都是针对快速分裂的细胞,因而常常导致正常骨髓细胞受抑。
骨髓抑制是多数化疗药的常见毒性反应。
化疗是恶性肿瘤的主要治疗方法之一,骨髓抑制是其主要的副作用。
骨髓抑制不仅延缓化疗的进行而影响治疗效果,而且可能导致并发症而危及患者生命。
一些恶性肿瘤患者或许不会很快死于疾病本身,却可能由于骨髓抑制致命。
因此,及时发现骨髓抑制并给予相应处理是化疗的重要环节。
二、诊断与鉴别诊断骨髓抑制通常发生在化疗后。
因粒细胞平均生存时间最短,约为6-8小时,因此骨髓抑制常最先表现为白细胞下降;血小板平均生存时间约为5-7天,其下降出现较晚较轻;而红细胞平均生存时间为120天,受化疗影响较小,下降通常不明显。
多数化疗药物所致的骨髓抑制,通常见于化疗后1-3周,约持续2-4周逐渐恢复,并以白细胞下降为主,可有伴血小板下降,少数药如健择、卡铂、丝裂霉素等则以血小板下降为主。
所以在化疗后可检测白细胞和血小板的数量来判断是否发生了骨髓抑制。
三、骨髓抑制的分度目前化疗后骨髓抑制的分度采用的是世界卫生组织抗癌药物急性及亚急性毒性反应分度标准(表1)。
以前对红系抑制的关注较少,原因在于贫血的处理相对简单而且见效迅速,输血或输入浓缩红细胞均可。
但实际上贫血不仅使患者的组织乏氧导致一般状况差,而且还可能降低放疗或化疗的效果。
对粒系抑制而言,中性粒细胞绝对值比白细胞总数更为重要。
注意两个关键节点:一是中性粒细胞绝对值低于1×109/L,二是血小板计数低于50×109/L 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化疗是恶性肿瘤的主要治疗方法之一,骨髓抑制是其主要的副作用。
骨髓抑制不仅延缓化疗的进行而影响治疗效果,而且可能导致并发症而危及患者生命。
一些恶性肿瘤患者或许不会很快死于疾病本身,却可能由于骨髓抑制致命。
因此,及时发现骨髓抑制并给予相应处理是化疗的重要环节。
一、化疗后骨髓抑制的分度:
目前化疗后骨髓抑制的分度采用的是世界卫生组织抗癌药物急性及亚急性毒性反应分度标准(表1)。
以前对红系抑制的关注较少,原因在于贫血的处理相对简单而且见效迅速,输血或输入浓缩红细胞均可。
但实际上贫血不仅使患者的组织乏氧导致一般状况差,而且还可能降低放疗或化疗的效果。
对粒系抑制而言,中性粒细胞绝对值比白细胞总数更为重要。
注意两个关键节点:一是中性粒细胞绝对值低于1×109/L,二是血小板计数低于50×109/L 。
它们分别是3度粒细胞减少和3度血小板减少的临界点,是容易出现并发症的信号,也是需要给予干预的指征。
0 1 2 3 4
血红蛋白(g/L)≥110 109-95 94-80 79-65 <65
白细胞(109/L)≥ <
粒细胞(109/L)≥ <
血小板(109/L)≥ 100 99-75 74-50 49-25 <25
一般认为,粒细胞的减少通常开始于化疗停药后一周,至停药10-14日达到最低点,在低水平维持2~3天后缓慢回升,至第21~28天恢复正常,呈U型。
血小板降低比粒细胞降低出现稍晚,也在两周左右下降到最低值,其下降迅速,在谷底停留时间较短即迅速回升,呈V型。
红细胞下降出现的时间更晚。
化疗后骨髓抑制的规律具有以下意义:(1)它限定化疗疗程的间隔时间。
理论上,化疗应该在最短时间内施以最强剂量,以迅速抑制或杀灭肿瘤细胞。
但化疗后骨髓抑制的恢复需要时间,故很多化疗是3~4周进行一次;(2)涉及对2度骨髓抑制的处理。
对于3度和4度骨髓抑制必须给予干预已经成为共识,但对于2度骨髓抑制,何时必须干预,何时可以短暂观察则较为困惑。
利用上述规律,有助于决策(后述);(3)有助于及早发现骨髓抑制。
根据化疗后骨髓抑制的规律后,能及早发现这一问题并行相应处理。
化疗后每两天检查一次血常规即可达到这一目的。
二、骨髓抑制作用突出的常用化疗药物、病理生理及一般处理原则
化疗药物针对的是生长活跃的细胞。
除恶性肿瘤细胞外,骨髓造血干细胞、消化道粘膜、皮肤及其附属器、子宫内膜和卵巢等器官或组织的细胞更新亦较快,这是化疗药物导致相应不良反应的组织学基础。
可以认为,几乎所有化疗药物都具有骨髓抑制作用,差别仅在于程度而已。
在常用化疗药物中,烷化剂(环磷酰胺、氮芥等)和鬼臼毒素(VP16)的骨髓抑制作用较强。
在铂类药物中,卡铂的肾脏毒性小于顺铂,但其骨髓抑制的作用强于后者。
紫杉醇类药物的主要副作用是过敏反应和周围神经炎,骨髓抑制作用尚不及烷化剂,但多烯紫杉醇(泰索蒂)的骨髓抑制作用较强。
拓泊替康的骨髓抑制作用很强,曾与卡铂联合用于大剂量化疗加外周血造血干细胞移植时骨髓动员前的抑制药物。
下列“顺口溜”或许有助记忆:顺铂稍弱卡铂强,鬼臼毒素不谦让,紫杉不若烷剂狠,托泊替康堪称王。
三、化疗后贫血的处理
关于输入浓缩红细胞[4]:输入浓缩红细胞的优点是能迅速提高贫血患者的携氧能力,缺点是存在输血相关的风险。
当血红蛋白达到70~80g/L时,绝大多数患者的携氧能力正常。
对于化疗患者,如果有明显乏力、气短、心动过速等,有输血指征。
如果患者血红蛋白为70g/L,每单位浓缩红细胞可增加10g/L的血红蛋白。
关于重组人促红细胞生成素(促红素,EPO)的应用:EPO是由肝脏和肾脏合成的激素,能调节红细胞的生成。
很多化疗药物都不同程度地影响肾功能(尤
其是铂类药物),从而引起促红素分泌减少。
因此,促红素尤其适用肾功能有损害的患者,或对输血相关风险顾虑过多的患者。
用法为促红素150u/kg 皮下注射,每周三次。
使用的同时应该补充铁剂和维生素B12 、叶酸等。
当血红蛋白高于80g/L或红细胞压积大于40%后应停药。
副作用少见。
四、化疗后感染的预防及粒细胞减少的处理
关于抗生素的使用:(1)何时用?一般认为,对于粒细胞减少伴有发热的患者,均使用抗生素;对于4度骨髓抑制的患者,无论有无发热,均必须预防性使用抗生素。
(2)用什么?理论上抗生素的使用应该以药敏为依据,但实际工作中很难实现,故多为经验性用药。
通常用广谱抗生素,特别是需要涵盖革兰氏阴性菌和厌氧菌,如三代或四代头孢菌素。
(3)何时停?如果患者有发热,应在发热消退至少48小时后停;如果患者为4度粒细胞减少但无发热,待粒细胞上升至正常后可停用。
关于重组人粒细胞集落刺激因子(G-CSF) 的应用:G-CSF的人工合成被认为是恶性肿瘤化疗的重要里程碑,如何使用好这一类药物对于保障化疗的进行非常重要。
(1)何时用?对于3和4度粒细胞减少,必须使用。
对于I度粒细胞减少,原则上不用;对于2度粒细胞减少,是否应用基于两点:查历史,即检查患者是否有3度以上骨髓抑制的历史。
如果有,则需要使用;观现状,即明确患者目前处于化疗后的时间。
如果化疗后很快出现2度骨髓抑制(两周以内),尤其是患者有3度以上粒细胞减少历史,最好使用。
如果患者是在化疗两周以后出现2度粒细胞减少,而此前又没有3度以上骨髓抑制的历史,则可以密切观察,暂时不用。
(2)如何用? A. 治疗性:5~7ug/kg/d,如果按体重平均50kg计算,一般用300ug/d;主要用于3~4度粒细胞减少;B. 预防性:3-5ug/kg/d,一般用150ug/d,主要用于此前有过4度骨髓抑制历史的患者,或者为了保障短疗程高密度化疗(如周疗)的进行。
通常自化疗结束后48小时开始使用。
C “对付性”:如前所述,对于I度粒细胞减少,原则上不用。
但如果患者即将化疗而又顾虑很大,为了安慰患者和规避风险,有时也使用G-CSF 150ug 1~2天。
一般不提倡这
种用法。
(3)何时停?对于治疗性使用,应在中性粒细胞绝对值连续两次大于10*109/L后停药。
然而,临床上很多患者由于反复化疗,两次中性粒细胞绝对值大于上述标准比较困难,故当白细胞总数两次超过10×109/L亦可考虑停药。
对于预防性使用,应在下次化疗前48小时停用。
五、化疗后血小板减少的处理
关于血小板减少患者的护理:对于血小板减少而言,护理与药物同等重要。
应注意以下问题:(1)减少活动,防止受伤,必要时绝对卧床;(2)避免增加腹压的动作,注意通便和镇咳;(3)减少粘膜损伤的机会:进软食,禁止掏鼻挖耳等行为,禁止刷牙,用口腔护理代替。
(4)鼻出血的处理:如果是前鼻腔,可采取压迫止血。
如果是后鼻腔,则需要请耳鼻喉科会诊,进行填塞;(5)颅内出血的观察:注意患者神志、感觉和运动的变化及呼吸节律的改变。
关于单采血小板的使用:输注单采血小板能迅速提升血小板数量,从而防止在血小板最低阶段出血的发生。
如果患者有3度血小板减少而且有出血倾向,则应输注单采血小板;如果患者为4度血小板减少,无论有无出血倾向,均应使用。
一般而言,一单位单采血小板可提高血小板计数1~2万左右。
然而,外源性血小板的寿命通常仅能维持72小时左右,而且反复输入后患者体内会产生抗体。
因此,近年出现了一些新型药物,如重组人促血小板生成素。
关于重组人促血小板生成素(TPO)的应用:TPO为特异性的巨核细胞生长因子,作用于血小板生成阶段的多个环节,能减少单采血小板的输入量和够缩短血小板降低持续的时间。
用法为300 Iu/kg/d,(15000u/d)皮下注射,7天为一疗程。
当血小板计数超过50×109/L可停用。
其不足之处是起效较慢,通常需要连续使用5天以后才有效果,故在有4度血小板减少历史的患者中预防性使用,其效果可能更好,有关的临床试验正在进行之中。
最后,用如下一段话作为骨髓抑制处理的小结:一度观察二考量,三度四度措施上;纠正贫血抗感染,防止出血心不慌;提升粒系有讲究,抗菌药物谱要广;单采救急一根草,创新药物接力棒。
