维生素C的测定(2,6-二氯酚靛酚滴定法
实验三维生素C的定量测定二氯靛酚滴定法

实验三维生素C的定量测定二氯靛酚滴定法This model paper was revised by the Standardization Office on December 10, 2020实验三 维生素C 的定量测定(2,6-二氯靛酚滴定法)一、原理维生素c 又称为抗坏血酸,其还原型能还原染料2,6-二氯靛酚钠盐,本身则氧化成脱氢抗坏血酸。
在酸性溶液中,2,6-二氯靛酚成红色,被还原后变为无色。
因此可用2,6-二氯靛酚滴定样品中含有的维生素C ,当样品中的维生素C 被完全还原后,在滴加过量的2,6-二氯靛酚,溶液变为淡红色,即为终点。
如无其他杂质干扰,则样品液所还原的2,6-二氯靛酚的量与样品中所含有维生素C 的量成正比。
二、 实验仪器新鲜水果、吸管、容量瓶、滴定装置、锥形瓶、研钵、漏斗三、实验试剂1、标准抗坏血酸溶液:准确称取50毫克纯抗坏血酸,溶于1%的草酸溶液中,并稀释至500毫升,即浓度为0.1mg/ml ,贮棕色瓶,冷藏保存,最好临用时配制。
2、2%草酸溶液:草酸2克,溶于100毫升蒸馏水中。
3、1%草酸溶液:1克草酸溶于100毫升的蒸馏水中。
4、0.01% 2,6-二氯酚靛溶液:溶50毫克2,6-二氯酚靛于300毫升含有104毫克 NaHCO 3的热水中,冷却后加水稀释至500毫升,滤去不溶物,贮于棕色瓶内。
(4℃约可保存1周)每次临用时以标准抗坏血酸溶液标定。
四、实验步骤(一)提取水洗净新鲜的蔬菜(水果),用吸水纸吸干表面水分,然后称取5克剪碎加2%的草酸5毫升,置研钵中研成浆,倒入100毫升的容量瓶内,用2%草酸洗涤数次,最后定容至刻度,充分混匀后过滤。
(二)滴定1、标定2,6-二氯酚靛酚溶液的浓度:量取标准抗坏血酸溶液1ml 和9ml 1%草酸于50ml 锥形瓶1中,同时量取10ml 1%草酸加入另一个50ml 锥形瓶2中作空白对照V 2,用已标定的2,6-二氯酚靛酚滴定至粉红色出现,15秒不退色。
实验三 维生素C的定量测定(2,6-二氯靛酚滴定法)

实验三 维生素C 的定量测定(2,6-二氯靛酚滴定法)一、原理维生素c 又称为抗坏血酸,其还原型能还原染料2,6-二氯靛酚钠盐,本身则氧化成脱氢抗坏血酸。
在酸性溶液中,2,6-二氯靛酚成红色,被还原后变为无色。
因此可用2,6-二氯靛酚滴定样品中含有的维生素C ,当样品中的维生素C 被完全还原后,在滴加过量的2,6-二氯靛酚,溶液变为淡红色,即为终点。
如无其他杂质干扰,则样品液所还原的2,6-二氯靛酚的量与样品中所含有维生素C 的量成正比。
二、 实验仪器新鲜水果、吸管、容量瓶、滴定装置、锥形瓶、研钵、漏斗三、实验试剂1、标准抗坏血酸溶液:准确称取50毫克纯抗坏血酸,溶于1%的草酸溶液中,并稀释至500毫升,即浓度为0.1mg/ml ,贮棕色瓶,冷藏保存,最好临用时配制。
2、2%草酸溶液:草酸2克,溶于100毫升蒸馏水中。
3、1%草酸溶液:1克草酸溶于100毫升的蒸馏水中。
4、0.01% 2,6-二氯酚靛溶液:溶50毫克2,6-二氯酚靛于300毫升含有104毫克 NaHCO 3的热水中,冷却后加水稀释至500毫升,滤去不溶物,贮于棕色瓶内。
(4℃约可保存1周)每次临用时以标准抗坏血酸溶液标定。
四、实验步骤(一)提取水洗净新鲜的蔬菜(水果),用吸水纸吸干表面水分,然后称取5克剪碎加2%的草酸5毫升,置研钵中研成浆,倒入100毫升的容量瓶内,用2%草酸洗涤数次,最后定容至刻度,充分混匀后过滤。
(二)滴定1、标定2,6-二氯酚靛酚溶液的浓度:量取标准抗坏血酸溶液1ml 和9ml 1%草酸于50ml 锥形瓶1中,同时量取10ml 1%草酸加入另一个50ml 锥形瓶2中作空白对照V 2,用已标定的2,6-二氯酚靛酚滴定至粉红色出现,15秒不退色。
记录所用的毫升数,计算每毫升2,6-二氯酚靛酚所能氧化抗坏血酸的毫克数(K )。
2、样品的测定:取50ml 锥形瓶2个,分别加入滤液10ml (V 3),用已标定的2,6-二氯酚靛酚溶液滴定至终点,以微红色能保持15秒不退色为止,整个滴定过程宜迅速,不宜超过2min ,记录两次滴定所得的结果,求平均值V 1。
食物中还原型维生素C的测定----2, 6-二氯酚靛酚滴定法

三、实验步骤
样品前处理
1. 2. 3. 4.
蔬菜摘、洗、沥干; 小棵整体取样,大棵对称均分取样; 切条、片、块等状; 白萝卜 若样品颜色较深用白陶土脱色
生样 100g
2%草酸 100g 捣碎,匀浆 分别称5g 1% 草酸定容至50ml 过滤取上清 熟样沥干称重 2%草酸 等量
白 萝 卜
生样 100g 加入煮沸的水中 煮5min
标准维生素C 溶液 标定: 2, 6-二氯酚靛 酚染料
标定: 标准维生素C 溶液
3、用标定后的2, 6-二氯酚靛酚染料滴 定样品,测得其还原型维生素C的浓度
(1)操作
2, 6-二氯酚靛酚染液(0.2mg/ml)
无色变为淡红色
15s内不褪色
滴定
匀浆后的样品(5ml) 空白组为草酸(5ml,1%)
(2)样品中原型维生素C浓度
GB 6195—86 水果、蔬菜维生素C含 量测定法 (2,6-二氯酚靛酚滴定法) 本标准适用于果品、蔬菜及其加工制 品中还原型抗坏血酸的测定(不含二 价铁、二价锡、一价铜、二氧化硫、 亚硫酸盐或硫代硫酸盐),不适用于
深色样品。
总结
• 优点:
简便快速,不需特殊仪器和试剂
• 缺点
• 非Vit C的专一反应,其它还原性物质对测定也有干扰。
举例含量丰富的食物。
蔬菜:辣椒、油菜、卷心菜、 菜花、芥菜; 水果:猕猴桃、酸枣、柑橘、 柠檬、柚子、草莓、沙棘。
结构与性质
抗坏血酸/维生素C
分子式:C6H8O6 相对分子质量:176 结构:
六个碳原子的α-酮基内酯 酸性多羟化合物
手性C 旋光性
CH OH 2 6 H C5 OH O
4 3 2 1
配制保存试剂时应注意的事项
实验十六-维生素C的定量测定(2-6-二氯酚靛酚滴定法)
维生素C的定量测定(2,6-二氯酚靛酚滴定法)一、目的要求:(1)学习并掌握用2,6—二氯酚靛酚滴定法测定植物材料中维生素C含量的原理和方法。
(2)了解蔬菜、水果中维生素C含量情况.(3)熟悉微量滴定法的基本操作过程。
二、实验原理:维生素C是人类营养中最重要的维生素之一,它与体内其它还原剂共同维持细胞正常的氧化还原电势和有关酶系统的活性.维生素C能促进细胞间质的合成,如果人体缺乏维生素C时则会出现坏血病,因而维生素C又称为抗坏血酸.水果和蔬菜是人体抗坏血酸的主要来源.不同栽培条件、不同成熟度和不同的加工贮藏方法,都可以影响水果、蔬菜的抗坏血酸含量。
测定抗坏血酸含量是了解果蔬品质高低及其加工工艺成效的重要指标。
维生素C具有很强的还原性。
它可分为还原性和脱氢型。
金属铜和酶(抗坏血酸氧化酶)可以催化维生素C氧化为脱氢型。
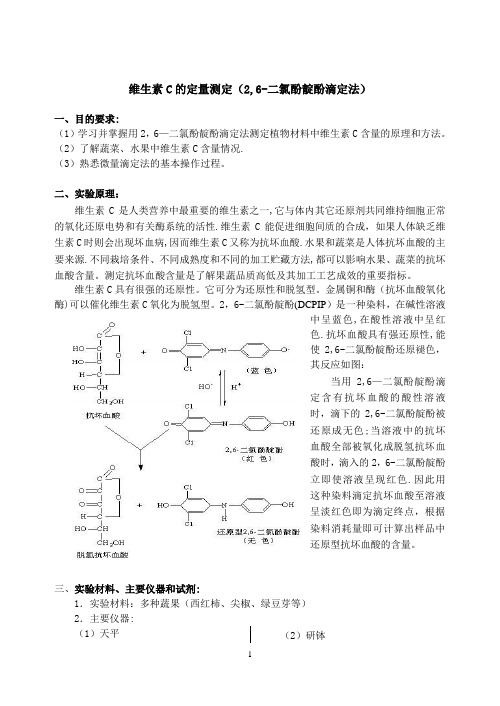
2,6-二氯酚靛酚(DCPIP)是一种染料,在碱性溶液中呈蓝色,在酸性溶液中呈红色.抗坏血酸具有强还原性,能使2,6-二氯酚靛酚还原褪色,其反应如图:当用2,6—二氯酚靛酚滴定含有抗坏血酸的酸性溶液时,滴下的2,6-二氯酚靛酚被还原成无色;当溶液中的抗坏血酸全部被氧化成脱氢抗坏血酸时,滴入的2,6-二氯酚靛酚立即使溶液呈现红色.因此用这种染料滴定抗坏血酸至溶液呈淡红色即为滴定终点,根据染料消耗量即可计算出样品中还原型抗坏血酸的含量。
三、实验材料、主要仪器和试剂:1.实验材料:多种蔬果(西红柿、尖椒、绿豆芽等)2.主要仪器:(1)天平(2)研钵(3)容量瓶(50mL) (4)刻度吸管(5mL,10mL) (5)锥形瓶(100mL)(6)微量滴定管(3mL) (7)漏斗(8)脱脂纱布(9)滤纸3.试剂:(1)2% HCl(2)标准抗坏血酸溶液精确称量抗坏血酸(应为洁白色,如变为黄色则不能用)25mg,溶于25ml 4%HCl中,移入50ml容量瓶中,用蒸馏水稀释至刻度,贮于棕色瓶中,冷藏,最好临用前配制,此溶液每ml 中含抗坏血酸0.5mg,.(3)0.01M 2,6-二氯酚靛酚准确称0。
维生素C的定量测定(2,6-二氯酚靛酚滴定法)

维生素C的定量测定(2,6-二氯酚靛酚滴定法)维生素C的定量测定(2,6-二氯酚靛酚滴定法)一、目的要求:(1)学习并掌握用2,6-二氯酚靛酚滴定法测定植物材料中维生素C含量的原理和方法。
(2)了解蔬菜、水果中维生素C含量情况。
(3)熟悉微量滴定法的基本操作过程。
二、实验原理:维生素C是人类营养中最重要的维生素之一,它与体内其它还原剂共同维持细胞正常的氧化还原电势和有关酶系统的活性。
维生素C能促进细胞间质的合成,如果人体缺乏维生素C时则会出现坏血病,因而维生素C又称为抗坏血酸。
水果和蔬菜是人体抗坏血酸的主要来源。
不同栽培条件、不同成熟度和不同的加工贮藏方法,都可以影响水果、蔬菜的抗坏血酸含量。
测定抗坏血酸含量是了解果蔬品质高低及其加工工艺成效的重要指标。
维生素C具有很强的还原性。
它可分为还原性和脱氢型。
金属铜和酶(抗坏血酸氧化酶)可以催化维生素C氧化为脱氢型。
2,6-二氯酚靛酚(DCPIP)是一种染料,在碱性溶液中呈蓝色,在酸性溶液中呈红色。
抗坏血酸具有强还原性,能使2,6-二氯酚靛酚还原褪色,其反应如图:当用2,6-二氯酚靛酚滴定含有抗坏血酸的酸性溶液时,滴下的2,6-二氯酚靛酚被还原成无色;当溶液中的抗坏血酸全部被氧化成脱氢抗坏血酸时,滴入的2,6-二氯酚靛酚立即使溶液呈现红色。
因此用这种染料滴定抗坏血酸至溶液呈淡红色即为滴定终点,根据染料消耗量即可计算出样品中还原型抗坏血酸的含量。
三、实验材料、主要仪器和试剂:1(实验材料:多种蔬果(西红柿、尖椒、绿豆芽等)2(主要仪器:(1)天平 (2)研钵1(3)容量瓶(50mL) (7)漏斗(4)刻度吸管(5mL,10mL) (8)脱脂纱布(9)滤纸 (5)锥形瓶(100mL)(6)微量滴定管(3mL)3(试剂:(1)2, HCl)标准抗坏血酸溶液精确称量抗坏血酸(应为洁白色,如变为黄色则不能用)(2 25mg,溶于25ml 4,HCl中,移入50ml容量瓶中,用蒸馏水稀释至刻度,贮于棕色瓶中,冷藏,最好临用前配制,此溶液每ml 中含抗坏血酸0.5mg,。
实验三 维生素C的定量测定(2,6-二氯酚靛酚滴定法)

操作
1.提取:称取约10g样品,加1%草酸少许,用研钵磨碎(桌 面放置一块纸板),加20ml 1%草酸,静置5-10分钟,然后 把样品全部过滤(或离心)后转入50ml容量瓶中.加1%草酸 定容到50ml,即可进行滴定。
2.滴定 (1)标准液滴定:准确吸取标准抗坏血酸溶液1.0ml(含 0.1mg抗坏血酸),置50ml 锥形瓶中,加9ml 1%草酸,微 量滴定管以0.1% 2,6-二氯酚靛酚滴定至淡红色,并保持 15秒不消失即为终点。由所用染料的体积计算出1ml染料相 当于多少mg 抗坏血酸。
实验三 蔬菜水果中的维生素 C含量测定(2,6-二氯酚靛酚
滴定法)
基本原理
还原型抗坏血酸能还原染料2,6-二氯酚靛酚 钠盐,本身则氧化成脱氢抗坏血酸。在酸性溶液 中,2,6-二氯酚靛酚呈红色,被还原后呈无色。 且在酸性环境中,干扰物质与染料的反应非常慢, 而抗坏血酸与之反应的特异性有一定程度的提高。 当抗坏血酸全部被氧化后,稍多加一些染料,使 滴定液呈淡红色,即为终点。如无其它干扰物质 存在,样品提取液所还原的标准染料量与样品中 所含的还原型抗坏血酸量成正比。
V=滴定时所用去的染料ml数; T=1ml染料能氧化抗坏血酸mg数; W=10ml定:准确吸取滤液或上清液三份,每份10.0ml 分别放入三个50ml 锥形瓶中,同标准液进行滴定。
说明: 1、滴定速度应迅速,一般不超过2分钟; 2、如样品中Vc含量过高,则取1ml样液加9ml草
酸然后进行滴定,最后计算时W为1ml样液中所含样品的 克数。
计算
V×T/W×100=100g样品中含抗坏血酸mg数;
滴定法测定维生素c
2,6-二氯酚靛酚滴定法定量测定维生素C目的和要求掌握2,6-二氯酚靛酚法测定维生素C的原理和方法。
原理维生素C (Vc)又称抗坏血酸(ascorbic acid)。
最初于1928年从牛的肾上腺皮质中提取出结晶物,证明对治疗和预防坏血病有特殊功效,因此称为抗坏血酸。
氧化型2,6-二氯酚靛酚在酸性溶液中呈粉红色,在中性或碱性溶液中呈蓝色,还原型2,6-二氯酚靛酚无色。
当用此染料滴定含有Vc的酸性溶液时,在Vc 未全部氧化前,滴下的染料立即被还原成无色;一旦溶淀中的Vc全部被氧化时,则滴下的染料立即使溶液显示粉红色,此时即为滴定终点,表示溶液中的Vc刚刚被氧化完全,从滴定时2,6一二氯酚靛酚标准液的消耗量,可以计算出被检物质中Vc的含量。
操作步骤1. 样液制备称取苹果和青椒各5g,分别加少量2%草酸(1%草酸因浓度太低而不能抑制抗坏血酸氧化酶作用)用研钵磨成浆,漏斗(+脱脂药棉)过滤,滤液转入25ml容量瓶后用2%草酸定容。
2. 标准液滴定准确吸取0.1mg/ml的标准抗坏血酸溶液各1.0ml,分置两个100ml锥形瓶中,加入1%草酸9.0ml,用微量滴定管以0.1%的2,6-二氯酚靛酚滴定至淡红色,并保持15s即为终点。
由所用染料的体积计算出T值(平均值),即1ml染料相当于多少mg的Vc。
3. 样液滴定准确吸取已制备的样品滤液各两份,每份10.0ml分别放入两个100ml锥形瓶内,滴定方法同前注意:1. 滴定过程宜迅速,一般不超过2min,因为样品中某些杂质亦能还原二氯酚靛酚,尽管其还原能力较弱且还原速度较Vc更慢。
2. 滴定所用染料宜控制于1~4ml,如果样品含Vc含量过高/低,可酌量增/减样液)。
3. 样品提取液应避免日光直射,否则会加速Vc氧化。
计算m=VT/m0×100式中m:100g样品中含Vc的质量(mg)V:滴定时所用去染料体积(ml)T:每毫升染料能氧化Vc质量数(mg/ml)m0:10ml样液相当于含样品之质量数(g)试剂和器材试剂1. 2%草酸溶液:草酸2g溶于100ml蒸馏水中。
2_6-二氯酚靛酚滴定法定量测定维生素C
2,6-二氯酚靛酚滴定法定量测定维生素C目的和要求掌握2,6-二氯酚靛酚法测定维生素C的原理和方法。
原理维生素C (Vc)又称抗坏血酸(ascorbic acid)。
最初于1928年从牛的肾上腺皮质中提取出结晶物,证明对治疗和预防坏血病有特殊功效。
氧化型2,6-二氯酚靛酚在酸性溶液中呈粉红色,在中性或碱性溶液中呈蓝色,还原型2,6-二氯酚靛酚无色。
当用此染料滴定含有Vc的酸性溶液时,在Vc 未全部氧化前,滴下的染料立即被还原成无色;一旦溶淀中的Vc全部被氧化时,则滴下的染料立即使溶液显示粉红色,此时即为滴定终点,表示溶液中的Vc刚刚被氧化完全,从滴定时2,6一二氯酚靛酚标准液的消耗量,可以计算出被检物质中Vc的含量。
操作步骤1. 样液制备称取苹果和青椒各5g,分别加少量2%草酸(1%草酸因浓度太低而不能抑制抗坏血酸氧化酶作用)用研钵磨成浆,漏斗(+脱脂药棉)过滤,滤液转入25ml容量瓶后用2%草酸定容。
2. 标准液滴定准确吸取0.1mg/ml的标准抗坏血酸溶液各1.0ml,分置两个100ml锥形瓶中,加入1%草酸9.0ml,用微量滴定管以0.1%的2,6-二氯酚靛酚滴定至淡红色,并保持15s即为终点。
由所用染料的体积计算出T值(平均值),即1ml染料相当于多少mg的Vc。
3. 样液滴定准确吸取已制备的样品滤液各两份,每份10.0ml分别放入两个100ml锥形瓶内,滴定方法同前注意:1. 滴定过程宜迅速,一般不超过2min,因为样品中某些杂质亦能还原二氯酚靛酚,尽管其还原能力较弱且还原速度较Vc更慢2. 滴定所用染料宜控制于1~4ml,如果样品含Vc含量过高/低,可酌量增/减样液3. 样品提取液应避免日光直射,否则会加速Vc氧化计算m = VT /m0 × 100式中m:100g样品中含Vc的质量(mg)V:滴定时所用去染料体积(ml)T:每毫升染料能氧化Vc质量数(mg/ml)m0:10ml样液含样品之质量数(g)试剂和器材试剂1. 2%草酸溶液:草酸2g溶于100ml蒸馏水中。
维生素C的定量测定(2,6-二氯酚靛酚滴定法)
维生素C的定量测定(2, 6-二氯酚靛酚滴定法)维生素C的定量测定(2, 6-二氯酚靛酚滴定法)一、目的要求:(1)学习并掌握用2, 6-二氯酚靛酚滴定法测定植物材料中维生素C含量的原理和方法。
(2)了解蔬菜、水果中维生素C含量情况。
(3)熟悉微量滴定法的基本操作过程。
二、实验原理:维生素C是人类营养中最重要的维生素之一,它与体内其它还原剂共同维持细胞正常的氧化还原电势和有关酶系统的活性。
维生素C能促进细胞间质的合成,如果人体缺乏维生素C时则会出现坏血病,因而维生素C乂称为抗坏血酸。
水果和蔬菜是人体抗坏血酸的主要来源。
不同栽培条件、不同成熟度和不同的加工贮藏方法,都可以影响水果、蔬菜的抗坏血酸含量。
测定抗坏血酸含量是了解果蔬品质高低及其加工工艺成效的重要指标。
维生素C具有很强的还原性。
它可分为还原性和脱氢型。
金属铜和酶(抗坏血酸氧化酶)可以催化维生素C氧化为脱氢型。
2, 6-二氯酚靛酚(DCPIP)是一种染料,在碱性溶液中呈蓝色,在酸性溶液中呈 红色。
抗坏血酸具有强还原性, 能使2, 6-二氯酚靛酚还原褪 色,其反应如图:当用2, 6-二氯酚靛酚滴定含有抗坏血酸的酸性溶液时, 滴下的2, 6-二氯酚靛酚被还原 成无色;当溶液中的抗坏血酸 全部被氧化成脱氢抗坏血酸 时,滴入的2, 6-一.氯酚靛酚立抗坏血酸 (蓝色) Cl o HO —CH CH 2O H CF 2.6•二氮(•红色)HO —CHO 一CIH —C脫氢抗坏血酸 还原型2,&二氨酚靛蜀(无色)即使溶液呈现红色。
因此用这种染料滴定抗坏血酸至溶液呈淡红色即为滴定终点,根据染料消耗量即可计算出样品中还原型抗坏血酸的含量。
三、实验材料、主要仪器和试剂:1(实验材料:多种蔬果(西红柿、尖椒、绿豆芽等)2(主要仪器:(1)天平(2)研钵1(3)容量瓶(50mL) (7)漏斗(4)刻度吸管(5mL, 10mL) (8)脱脂纱布(9)滤纸(5)锥形瓶(lOOmL)(6)微量滴定管(3mL)3(试剂:(1)2, HC1)标准抗坏血酸溶液精确称量抗坏血酸(应为洁白色,如变为黃色则不能用)(225mg,溶于25ml 4,HC1中,移入50ml容量瓶中,用蒸憎水稀释至刻度,贮于棕色瓶中,冷藏,最好临用前配制,此溶液每ml中含抗坏血酸O.omg, o(3)0. 01M 2, 6,二氯酚靛酚准确称0. 25g氧化型2, 6,二氯酚靛酚、0. 21g碳酸氢钠溶于250ml热蒸镭水中,稀释至1000ml,充分振摇,装入棕色瓶内,置冰箱内过夜,临用前过滤,用标准Vc标定其浓度。
[精品]2,6-二氯酚靛酚滴定法定量测定维生素C
[精品]2,6-二氯酚靛酚滴定法定量测定维生素C维生素C,也被称为抗坏血酸,是人体所需的一种重要营养物质,具有抗氧化、促进铁吸收等重要作用。
由于人体无法自行合成维生素C,因此需要从食物中摄取。
然而,维生素C很容易被氧化破坏,因此在分析检测过程中需要选择一种敏感、精确、简便的方法对维生素C进行定量分析。
2,6-二氯酚靛酚滴定法是一种广泛应用于维生素C分析的方法之一。
下面将介绍这种方法的原理和操作步骤。
原理:2,6-二氯酚靛酚是一种指示剂,可以在酸性条件下呈现红色,而在还原剂作用下会褪色。
维生素C是一种还原剂,可以将2,6-二氯酚靛酚还原成无色的还原物。
因此,在维生素C存在的条件下,将2,6-二氯酚靛酚逐滴加入已知浓度的维生素C溶液中,当维生素C 耗尽时,2,6-二氯酚靛酚不再被还原,呈现出由红色变为无色的转变。
在此过程中记录2,6-二氯酚靛酚的加入量即可计算维生素C的浓度。
操作步骤:1. 器材准备称取约100mg的2,6-二氯酚靛酚,加入100ml的95%乙醇中,摇匀即可得到表现绿色的溶液。
同时准备0.1mol/L的氢氧化钠溶液、2%的硫酸溶液,以及待测样品。
a. 将待测样品取约2g加入研钵中,加入10ml的2%的硫酸溶液,反复挥发至浓缩,使样品保持在干燥状态。
b. 加入20ml的去离子水,研钵放入热水浴中,加热溶解。
c. 实验设一个平衡水平标志线,定量转移10ml溶液到较大的滴定瓶中,加入几滴2,6-二氯酚靛酚溶液,搅拌均匀。
d. 向滴定瓶中逐滴加入氢氧化钠溶液至溶液呈深黄色,为初始色。
e. 开始滴定,滴定钠氢氧化溶液至溶液呈现红色,即为维生素C耗尽时,记录钠氢氧化溶液的滴定量。
f. 重复操作并求得平均数,计算维生素C浓度。
注意事项:1. 滴定瓶上方要留有足够的空间,以免在滴定时水溅出来。
2. 滴定时要缓慢滴加氢氧化钠溶液,以避免过量反应。
3. 滴定时要注意加入2,6-二氯酚靛酚溶液后,溶液会变为紫色,此时需要加入氢氧化钠溶液搅拌均匀使其还原为黄色,然后再开始滴定。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验一维生素C的测定(2,6-二氯酚靛酚滴定法
一、测定原理
2,6-二氯酚靛酚滴定法用于测定还原型抗坏血酸。
抗坏血酸分子中存在烯醇式结构(HO —C═C—OH),因而具有很强的还原性,还原型抗坏血酸能还原2,6-二氯酚靛酚染料。
2,6—二氯酚靛酚染料在酸性溶液中呈红色,在中性或碱性溶液中呈蓝色。
因此,当用2,6—二氯酚靛酚染料滴定含有抗坏血酸的酸性溶液时,被还原后红色消失成为无色的衍生物,可作为维生素C含量测定的滴定剂和指示剂。
还原型抗坏血酸还原染料后,本身被氧化为脱氢抗坏血酸。
当抗坏血酸全部被氧化时,滴下的2,6—二氯酚靛酚溶液则呈红色。
在测定过程中当溶液从无色转变成微红色时,表示抗坏血酸全部被氧化,此时即为滴定终点。
根据滴定消耗染料标准溶液的体积,可以计算出被测定样品中抗坏血酸的含量。
在没有杂质干扰时,一定量的样品提取液还原标准染料液的量、与样品中所含抗坏血酸的量成正比。
反应式如下:
二、实验仪器与试剂
1.仪器
组织捣碎机;水果刀;
托盘天平;精密天平;称量纸;卷纸;台式离心机;电炉;吸耳球;玻璃棒;
蒸馏水,蒸馏水洗瓶;记号笔、标签纸、定性滤纸;
20cm镊子;5ml、10ml移液管、(微量)酸式滴定管、漏斗;漏斗架;
50ml、250ml、 500ml 、1000ml烧杯;
10ml 、500 ml、1000 ml量筒;100ml具塞量筒(或普通量筒);
100mL、250mL棕色容量瓶;50ml或100ml三角烧瓶。
2.原料及试剂
本实验材料是,用水均为蒸馏水,试剂纯度均为分析纯度。
(1)2%草酸溶液:草酸20g溶于700ml蒸馏水中,稀释至1000ml。
(2)1%草酸溶液:取上述2%草酸溶液450ml,稀释至900ml。
(3)抗坏血酸标准溶液:
称取抗坏血酸20mg,用适量1%草酸溶液溶解后,移入100mL棕色容量瓶中,并以1%草酸溶液定容,振摇混匀,备用。
(4)0.02% 2,6-二氯酚靛酚溶液:
称取碳酸氢钠52.2mg,溶解在200mL沸水中。
再称取2,6-二氯酚靛酚49.2mg,溶于上述碳酸氢钠溶液中。
冷后,过滤于250ml棕色容量瓶中,用水稀释至刻度,摇匀备用。
临用前标定:
取2mL浓度为0.2mg/ml的抗坏血酸标准溶液于三角瓶中,加1%草酸5mL,摇匀,用配制的2,6-二氯酚靛酚染料溶液滴定至微红色,15s不褪色即为终点,并计算如下:每1mL染料溶液相当于抗坏血酸的毫克数=滴定度(T)=C×V1/V2。
式中:C----抗坏血酸的浓度(mg/ml)= 0.2
V1----抗坏血酸的量(ml)=2
V2----消耗染料溶液的量(ml)=31.84
得出T=0.2×2/31.84=1.26×10﹣2
三、实验步骤
1. 取200g新鲜橙子(去皮、去核),置于1000ml烧杯内,称重。
2.将样品倒入组织捣碎机,加入等量2%草酸(W∶V),加盖旋紧,匀浆5min。
3. 取出匀浆物质。
4.称取30g匀浆物质于50ml小烧杯中编号,记录。
5. 用少量1%草酸将称取的匀浆物质倒入100ml容量瓶中,并用1%草酸反复洗涤烧杯(3次),其洗涤液一并移入,并用1%草酸定容到100ml。
6.加塞后将匀浆物质与1%草酸充分混合,静置10min。
7.取上述溶液过滤或离心。
8. 用移液管吸取10ml滤液置于三角烧瓶内,加入10ml 1%草酸(2个平行样品,编号);用
移液管吸取10ml蒸馏水,加入10ml 1%草酸(空白对照)。
9. 加1ml氯仿,将2,6二氯酚靛酚染料滴定至终点(淡粉红色,15s不褪色或观察氯仿层
呈现淡红色。
),记录染料消耗量。
10. 计算每100g样品中维生素C的含量(ml)及平行样品误差范围,公式如下:
维生素C含量(ml/100g)=[(V1-V2)×T/W]×100
式中:V1----滴定样品时耗去的染料溶液的量(ml)
V2----滴定空白时耗去的染料溶液的量(ml)
T ---- 1mL染料溶液相当于抗坏血酸的毫克数
W ----滴定时所取的滤液中,含样品的量(g)
四、实验结果、数据计算与分析
维生素C含量(ml/100g)=[(V1-V2)×T/W]×100=36.13
《食物成分表》(全国平均值)中橙子的VC含量约33mg/100g。
比测定值略小。
五、注意事项及说明
(1) 某些水果、蔬菜(如橘子、西红柿等)浆状物定容时泡沫太多,可加数滴丁醇或辛醇消
泡。
(2)大多数植物组织内含有一种能破坏抗坏血酸的氧化酶,因此,抗坏血酸的测定应采用新
鲜样品并尽快用2%草酸溶液制成匀浆以保存维生素C。
(3) 样品的提取液制备和滴定过程,要避免阳光照射和与铜、铁器具接触,以免抗坏血酸被
破坏。
(4) 整个操作过程要迅速,防止还原型抗坏血酸被氧化。
滴定过程一般不超过2min。
滴定
所用的染料不应小于1ml或多于4ml,如果样品含维生素C太高或太低时,可酌情增减样液用量或改变提取液稀释度。
(5) 本实验必须在酸性条件下进行。
在此条件下,干扰物反应进行得很慢。
2%草酸有抑制抗坏血酸氧化酶的作用。
(6) 干扰滴定因素有:样品中可能有其它杂质还原二氯酚靛酚,但反应速度均较抗坏血酸慢,
因而滴定开始时,染料要迅速加入,而后尽可能一点一点地加入,并要不断地摇动三角瓶,直至呈粉红色,于15s内不消退为终点。
(7) 提取的浆状物如不易过滤,亦可离心,留取上清液进行滴定。
(8)市售2,6-二氯酚靛酚质量不一,以标定0.4mg抗坏血酸消耗2mL左右的染料为宜,可根据标定结果调整染料溶液浓度。
(9)使用酸式滴定管要注意排尽气泡。
实验过程中要保证两个开关不同时开启,且保证漏斗
里必须要有溶液。
