化学年谱(公元1801年~1960年)
化学发展简史大事记汇总
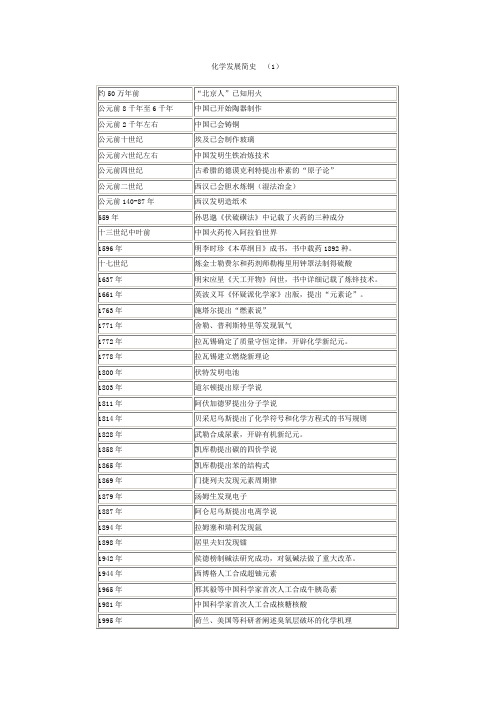
化学发展简史(1)化学发展简史(2)道尔顿的原子论用原子整数比解释了定组成定律和倍比定律,这属于原子间量的关系。
但为什么原子会互相结合和分解?它们结合时遵循什么规律?这些问题似乎应该是无机化学来解决,但处于统治地位的贝采里乌斯的电化二元论过于笼统、不及实质而又十分强大,禁锢了人们的思想。
在有机化学的研究中,许多现象使人们突破了电化二元论,勇敢地探索有机物的分子结构。
这一讲我们将认识维勒、李比希、凯库勒和范霍夫,这些先行者用他们的无畏和智慧,开辟了一条光明之路——通过有机物的分子结构,建立、发展了原子间相互结合的价键理论,并使人们看清了原子在三维空间的排列情况。
维勒初涉“莽林”1800年7月31日维勒出生于德国梅因河畔法兰克福附近的埃希海姆村。
他的祖父是黑森选帝侯的马舍长,他的父亲在马尔堡大学学习兽医和农业,毕业后也曾在选帝侯的王子处任马舍长,1806年在法兰克福附近经营起自己的庄园,1812年迁入法兰克福担任宫廷职务,由于学识渊博能力突出,又热心社会公益事业,不久成了当地名流。
他的母亲是哈瑙一位中学校长的女儿,对幼年维勒施以良好的教育。
维勒七八岁时由父亲启蒙教他读写、绘画,不久入普通小学,又自学了拉丁文、法文、音乐。
1814年入法兰克福的中学受到良师的教导。
农学家的父亲影响他自幼热爱自然,特别是从事理化研究的布赫医生指引这位热心化学试验与采集矿物标本的中学生跟踪前人的工作进行科学的探索:例如他们曾查知一种制硫酸用的矿石中含有硒(这项工作1821年发表在科学杂志上,是维勒发表的第一篇论文),从锌中制得少量镉,以伏打电堆进行电化学试验,以碳还原法制得金属钾,等等,显示出少年维勒对化学的偏爱与才华。
1819年,维勒入马尔堡大学学医,次年转入海得尔堡大学在格曼林教授指导下学习,1823年9月获医学(外科学及产科学)博士学位。
格曼林教授发现维勒的化学实验技能很强,就建议他赴瑞典化学大事贝采里乌斯处进修,专攻化学。
[课外阅读]化 学 年谱4
![[课外阅读]化 学 年谱4](https://img.taocdn.com/s3/m/494e5ea80975f46526d3e125.png)
[课外阅读]化学年谱4发现聚四氟乙烯,开始了含氟聚合物的研究,到五十年代正式投产(美国杜邦公司)。
发现一些简单的磷酸酯对温血动物具有剧毒及强烈的杀虫作用(德国施拉德)。
提出气体在固体表面上的多分子吸附理论(美国布伦瑙尔、埃米特,美籍匈牙利人特勒)。
首次分离得到纯净的维生素B2(德籍奥地利人柯恩)。
1939年人工合成维生素K(美国菲泽)。
1939—1942年,提出联合制碱新法(中国侯德榜等)。
提出多相催化的活性集团假说(苏联柯勃谢夫)。
1899—1939年,分别对非碳四面体元素硅有机物的研究,制得含硅高聚物(英国刻宾,苏联安德利扬诺夫)。
1935—1939年,试用在1873年合成的二氯二苯基三氯乙烷(D.D.T.)于治虫,1942年工业生产(瑞士保·缪勒)。
1940年分别实现用中子和氘轰击铀238,发生衰变以制备超铀元素的方法,制备了93号镎、94号钚,指出超铀元素的性质都相似于镧系稀土元素(美国西博格、艾贝尔森、麦克米伦)。
人工合成元素周期表中另一空位元素85号的砹(美籍意大利人埃·塞格勒)。
提出用六氟化铀,通过热扩散法分离富集铀235(美国艾贝尔森)。
以气体扩散法从铀238中分离铀235(美国尤里)。
分离得到长半衰期放射性同位素碳14,用于生物化学、地质和考古(美籍加拿大人卡门)。
1941年第二次世界大战前后,美国石油开始化学综合利用,用于生产各种有机物、塑料、纤维、橡胶等。
1909—1940年左右,对有机硼化合物进行研究,在高能燃料,耐辐射材料等方面开始获得实际应用(德国斯托克)。
二十世纪四十年代后,发展了离子树脂交换法,对十四个稀土元素进行分离,“稀有金属化学’开始迅速发展(美国斯佩丁)。
1942年应用离子树脂交换法分离得到纯铀二吨,用于制备第一颗原子弹(美国斯佩丁)。
1942—1950年,由于原子反应堆的建立,辐射化学逐步发展成为一门科学。
发展分子结构的立体构象分析理论(挪威哈塞尔,美国巴顿)。
中外化学发展史时间轴

中外化学发展史时间轴一、古代化学(公元前3000年-公元17世纪)公元前3000年左右,古埃及人开始使用化学技术,制造金属器具和染料。
公元前6世纪,古希腊人开始研究火和水等自然现象,奠定了化学研究的基础。
公元2世纪,古罗马人开始研究矿物和药物,并发展了一些实验方法。
二、中世纪化学(公元17世纪-公元18世纪)17世纪,欧洲发生了科学革命,启蒙运动的思想逐渐传播,化学研究开始迅速发展。
1661年,罗伯特·波义耳提出了物质不能被创造或销毁的理论,奠定了现代化学的基础。
18世纪,化学元素的发现和研究成为主要研究领域,安托万·拉瓦锡发现了氧气。
1789年,拉瓦锡提出了化学元素的概念,并建立了现代化学符号和化学方程式。
三、现代化学(19世纪)19世纪初,约翰·道尔顿提出了原子理论,认为所有物质由不可分割的小粒子组成。
1807年,亚历山大·冯·洪堡发现了电解现象,奠定了电化学的基础。
1828年,弗里德里希·维勒首次合成了尿素,证明有机化合物可以由无机物质合成。
1833年,米歇尔·尼克劳斯·塞尔纳克首次提出了化学反应速率的概念,开创了化学动力学的研究领域。
1856年,威廉·普兰克发现了能量量子化的现象,奠定了量子化学的基础。
四、现代有机化学(20世纪)20世纪初,有机化学开始迅速发展,人们对有机物质的结构和性质有了更深入的理解。
1902年,爱尔兰化学家阿瑟·亨利·赖特利首次合成了脂肪酸,开创了有机合成化学的新时代。
1928年,弗里德里希·贝格尔首次合成了橡胶,推动了合成橡胶工业的发展。
20世纪中叶,合成药物的研究取得了重大突破,人们开始广泛使用抗生素等药物。
20世纪末,纳米材料的研究成为热点,人们开始研究纳米粒子的性质和应用。
五、现代无机化学(20世纪)20世纪初,无机化学研究重点转向材料科学和能源领域。
化学年谱(公元1801年 ~ 1899年)

公元1801年~1899年1801年发现化学元素铌(英国哈契脱)。
进行大量能够组成电池的物质对的研究,把化学亲和力归之为电力,指明如何从实验确认元素(英国戴维)。
1802年发现化学元素钽(瑞典爱克伯格)。
发现在O摄氏度时,许多气体的膨胀系数是1/273(法国盖·吕萨克)。
1803年发现化学元素铈(德国克拉普罗兹,瑞典希辛格、柏齐力阿斯)。
发现化学元素钯和铑(英国武拉斯顿)。
提出气体在溶液中溶解度与气压成正比的气体溶解定律(英国威·亨利)。
1804年发现化学元素铱和锇(英国坦能脱)。
1805年提出盐类在水溶液中分成带正负电荷的两部分,通电时正负部分相间排列,连续发生分解和结合,直至两电极,用以解释导电的现象,这是电离学说的萌芽(德国格罗杜斯)。
1806年发现化合物分子的定组成定律,指出一个化合物的组成不因制备方法不同而改变(法国普鲁斯脱)。
首次引入有机化学一词,以区别于无机界的矿物化学,认为有机物只能在生物细胞中受一种“生活力”作用才能产生,人工不能合成(瑞典柏齐力阿斯)。
1807年发现化学元素钾和钠(英国戴维)。
发现倍比定律,即二个元素化合成为多种化合物时,与定量甲素化合的乙元素,其重量成简单整数比,并用氢作为比较标准(英国道尔顿)。
提出原子论(英国道尔顿)。
发现混合气体中,各气体的分压定律(英国道尔顿)。
1808年发现化学元素钙、锶、钡、镁(英国戴维等)。
发现化学元素硼(英国戴维,法国盖·吕萨克、泰那尔德)。
1808—1810年,通过磷和氯的作用,确证氯是一个纯元素,盐酸中不含氧,推翻了拉瓦锡凡酸必含氧的学说,代之以酸中必含氢(英国戴维)。
1808—1827年,《化学哲学的新系统》陆续出版,本书总结了作者的原子论(英国道尔顿)。
发现气体化合时,各气体的体积成简比的定律,并由之认为元素气体在相等体积中的重量应正比于它的原子量,这成为气体密度法测原子量的根据(法国盖·吕萨克,德国洪保德)。
化学发展简史

化学发展简史化学是一门研究物质的组成、性质、结构、转化和应用的科学。
它的发展历史可以追溯到古代的炼金术时期,经过了漫长而丰富多彩的发展过程。
本文将为您详细介绍化学发展的历史,包括重要的里程碑事件和贡献者,以及对人类社会的影响。
1. 古代炼金术时期(公元前3000年-公元17世纪)在古代,人们开始探索物质的性质和转化。
古埃及和古希腊的炼金术士试图将一种物质转变为另一种物质,寻求黄金的创造方法。
然而,炼金术的实践主要基于神奇主义和超自然的信念,缺乏科学的基础。
2. 化学革命时期(17世纪-18世纪)17世纪,化学开始从炼金术的迷信中解脱出来,成为一门独立的科学。
罗伯特·博义和约瑟夫·普里斯特利发现了氧气,揭示了燃烧的本质。
安托万·拉瓦锡提出了化学元素的概念,并系统地整理了化学元素表。
拉瓦锡还提出了化学反应中的质量守恒定律,奠定了化学反应定量研究的基础。
3. 原子理论和化学元素周期表(19世纪)19世纪初,约翰·道尔顿提出了原子理论,认为所有物质都由不可分割的小颗粒组成。
道尔顿的理论为化学提供了一个统一的框架,并解释了化学反应的本质。
随后,德米特里·门捷列夫提出了元素周期表,将化学元素按照其物理和化学性质进行了分类,为化学研究提供了重要的工具。
4. 有机化学和无机化学的发展(19世纪)19世纪,有机化学和无机化学逐渐分离成为两个独立的领域。
弗里德里希·凯库勒首先提出了有机化合物的结构理论,认为有机化合物是由碳原子构成的。
奥古斯特·凯库勒则发现了苯环结构,这个发现对有机化学的发展产生了深远的影响。
同时,无机化学也取得了重要的发展,例如道尔顿提出的化学元素的概念和门捷列夫的元素周期表。
5. 化学工业的兴起(19世纪末-20世纪初)19世纪末,化学工业开始兴起,以满足工业化生产的需求。
弗里茨·哈伯发现了合成氨的方法,开创了工业化学的新时代。
化学发展史简介

化学发展史简介概述化学发展史的五个时期自从有了人类,化学便与人类结下了不解之缘。
钻木取火,用火烧煮食物,烧制陶器,冶炼青铜器和铁器,都是化学技术的应用。
正是这些应用,极大地促进了当时社会生产力的发展,成为人类进步的标志。
今天,化学作为一门基础学科,在科学技术和社会生活的方方面面正起看越来越大的作用。
化学史大致分为:远古的工艺化学时期。
这时人类的制陶、冶金、酿酒、染色等工艺主要是在实践经验的直接启发下经过多少万年摸索而来的,化学知识还没有形成。
这是化学的萌芽时期。
炼丹术和医药化学时期。
从公元前1500年到公元1650年,炼丹术士和炼金木士们,在皇宫、在教堂、在自己的家里、在深山老林的烟熏火燎中,为求得长生不老的仙丹,为求得荣华富责的黄金,开始了最早的化学实验。
记载、总结炼丹术的书藉,在中国、阿拉伯、埃及、希腊都有不少。
这一时期积累了许多物质间的化学变化,为化学的进一步发展准备了丰富的素材。
这是化学史上令我们惊叹的雄浑的一幕。
后来,炼丹术、炼金术几经盛衰,使人们更多地看到了它荒唐的一面。
化学方法转而在医药和冶金方面得到了正当发挥。
在欧洲文艺复兴时期,出版了一些有关化学的书耕,第一次有了“化学”这个名词。
英语的chemistry 起源于alchemy,即炼金术。
chemist至今还保留昔两个相关的含义:化学家和药剂师。
这些可以说是化学脱胎于炼金术和制药业的文化遗迹了。
燃素化学时期。
从1650年到1775年,随着冶金工业和实验室经验的积累,人们总结感性知识,认为可燃物能够燃烧是因为它含有燃素,燃烧的过程是可燃物中燃素放出的过程,可燃物放出燃素后成为灰烬。
定量化学时期,即近代化学时期。
1775年前后,拉瓦锡用定量化学实验阐述了燃烧的氧化学说,开创了定量化学时期。
这一时期建立了不少化学基本定律,提出了原子学说,发现了元素周期律,发展了有机结构理论。
所有这一切都为现代化学的发展奠定了坚实的基础。
科学相互渗透时期,即现代化学时期。
化学发展简史

化学发展简史化学作为一门自然科学,研究物质的组成、性质、结构和变化规律,对人类社会的发展起到了重要的推动作用。
本文将从古代到现代,介绍化学发展的历史,包括重要的科学家和里程碑事件。
古代化学的起源可以追溯到公元前3000年左右的古埃及和古巴比伦文明。
这些古代文明的人们开始研究金属的提炼和合金的制备,同时也发现了一些化学反应,比如酸碱中和反应。
古希腊的哲学家和科学家们也对化学进行了一些探索,比如亚里士多德提出的四元素理论,即地、水、火、气是构成物质的基本要素。
进入中世纪,化学的发展相对缓慢,主要受到宗教和哲学观念的限制。
直到16世纪,化学才开始逐渐从炼金术中分离出来,成为一门独立的科学。
这一时期的重要人物包括瑞士化学家帕拉塞尔苏斯和德国化学家贝克曼。
他们的研究为化学的进一步发展奠定了基础。
17世纪是化学发展的重要时期,英国科学家罗伯特·博义利提出了现代化学的基本概念,包括元素和化合物的概念。
法国科学家拉瓦锡则提出了化学反应的质量守恒定律,即质量在化学反应中是不会凭空消失或增加的。
这些概念和定律为后来的化学研究提供了重要的理论基础。
18世纪是化学发展的黄金时期,被称为“化学革命”的时期。
瑞典化学家卡尔·舍勒提出了化学元素周期表,系统地整理了当时已知的元素。
法国化学家拉瓦锡和他的学生贝尔塔隆则发现了氧气和氮气,为气体化学的研究开辟了新的领域。
英国化学家普里斯特利和德国化学家贝克曼分别独立发现了氧化反应和还原反应,奠定了氧化还原反应的基本理论。
19世纪是化学发展的进一步突破时期。
法国化学家拉瓦锡和德国化学家贝克曼的研究成果为化学定量分析的发展奠定了基础。
英国化学家道尔顿提出了原子理论,认为物质是由不可分割的微小颗粒组成。
瑞典化学家门德莱夫提出了化学反应速率的概念,开创了化学动力学的研究。
德国化学家库尔特·酸根则发现了有机化合物的结构和功能之间的关系,为有机化学的发展做出了重要贡献。
有关金属的化学年谱

有关金属的化学年谱(三)
公元1900年~1960年
1901年法国科学界德马尔塞,发现63号化学元素铕。
1905年美国科学家玻特伍德,从铀矿中铀的衰变指出,铀衰变的最终产物是铅。
首次提出了从铀矿的含铅量及铀的衰变速度来测定地球年龄。
1906年美国科学家波特伍德,在铀的残余物中发现化学性质和钍相同的新放射性物质,这是第一次发现同位素。
1913—1918年镍、铬不锈钢开始获得实际应用(英国哈德费尔德)。
1916年发现加钴的钨钢具有强磁性,开始了新型磁合金的研究,后即制得具有强磁性、耐蚀、耐震、耐温度变化、价廉的铅镍钴磁钢(日本本多光太郎)。
1917年发现化学元素镤(德国哈恩、迈特纳,英国索迪等)。
1925年发现化学元素铼,属周期系中最后一个稳定元素,以后发现的均为放射性元素(德国依·诺台克、瓦·诺台克)。
1930—1932年发现化学元素钫(美国阿立生、麦非)。
1944年
用中子轰击钚和a粒子轰击铀制得95号超铀元素镅,用
粒子轰击钚制得96号超铀元素锔(美国西博格、乔梭)。
1947年发现化学元素钷(美国马林斯基、格兰顿能)。
1950—1953年,用碳和氮轰击镎和铀,制得99号超铀元素锿;用中子轰击钚制得100号超铀元素镄(美国乔梭)。
1953—1955年用粒子轰击锿制得101号超铀元素钔(美国西博格)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学年谱(公元1801年~1960年)公元1900年~1960年1900年美籍俄国科学家冈伯格,从分子量测定首次发现自由基三苯甲烷,自由基是电子出于激发状态的分子或分子碎片,具有自由价,化学性活泼。
法国科学家格林雅尔德,制得金属镁的有机化合物,它是有机合成中的中间体。
德国科学家多恩,证明镭射气是一种新的惰性气体——氡。
法国科学家维尔纳,试制成功人造宝石并投入工业生产。
美国科学家兰米尔,通过氢分子在钨丝上分解,制得氢原子喷灯,可产生近于太阳表面的温度,开始了气体在金属表面上吸附及催化的研究。
英国科学家霍普金,发现蛋白质有两种,一种能维持生命,一种不能维持生命如明胶。
1901年德国科学家奥斯特瓦尔德,提出催化剂是改变化学反应速度的物质,而不出现在最终产物中,认为所有反应都可以进行催化,并指明催化剂在理论和实践中的重要性。
法国科学界德马尔塞,发现63号化学元素铕。
美国科学家吉·路易斯,提出逸度和偏克分子的概念,并统一活度概念,使原来根据理想体系条件求得的热力学关系式仍适用于实际体系。
1902年英国科学家泡帕,用12年时间制得氮、硫、硒、锌等化合物的光学异构体,后也获得不包含不对称原子的、因空间位阻而造成的旋光异构体。
1903年瑞士科学家齐格蒙第,发明观察胶体粒子运动的超显微镜,它也是直接观察平衡涨落的直观仪器。
法国科学家比·居里、英国科学家威·雷姆赛、索迪,居里等观察到镭盐水液有气泡逸出,索迪等证实这是辐射引起的水分解,产生了氢气和氧气,这是辐射化学研究的开端。
1904年德国科学家艾贝格,用五年时间从惰性元素稳定性和元素周期律分为八族出发,首先用电子观点来解释价键。
认为一个原子可以被电子占据的位子数是八;一个元素的最大正负价总和常为八,这即为艾贝格定律,是电价学说的“八偶律”的萌芽。
日本科学家高峰让吉,首次人工合成激素——肾上腺素。
英国科学家哈顿,分解得到非蛋白质小分子“辅酶”,这是酶催化不可缺少的物质。
1905年意大利科学家斯佩西亚,利用温差籽晶生长法制备水井,成为人造水晶技术的基础。
美国科学家科布伦兹,将红外光谱和各类有机分子的结构系统的联系起来,使红外光谱在结构分析上获得广泛应用。
德国科学家塔曼,首先提出玻璃为过冷的液体,对晶体的晶核生长和发展作了系统研究,研究晶核数目及晶核发展速度与过冷度之间的关系。
用热分析法研究合金,为现代金相学奠定基础。
美国科学家玻特伍德,从铀矿中铀的衰变指出,铀衰变的最终产物是铅。
首次提出了从铀矿的含铅量及铀的衰变速度来测定地球年龄。
德国科学家奥斯特瓦尔德,提出胶体是物质多分散聚集状态的观点,把胶体化学发展为表面化学。
1906年英国科学家巴拉克,从X射线的散射和吸收,发现化学元素的特征X辐射。
美国科学家波特伍德,在铀的残余物中发现化学性质和钍相同的新放射性物质,这是第一次发现同位素。
俄国科学家兹维特,发明层析分析法,为分离性质相似的复杂混合物提供了重要方法。
德国科学家博登斯坦,发现链式反应,并提出有关机理。
德国科学家维尔斯坦特,用色层分析法,研究叶绿素的化学结构,从而知道Mg存在于叶绿素中,而铁也以同样形式存在于血红素中。
1907年德国科学家艾·费歇,经过五年研究,证明蛋白质是由简单的氨基酸相连而成,首次人工合成由十八个氨基酸组成的多肽,这是蛋白质结构与合成的开始。
美国科学家吉·卢意思,提出任何物质膨胀系数与压缩系数的热力学关系式,以及他们与热容的关系。
法国科学家乌斑和德国科学家威斯巴克,各自独立发现化学元素镏。
1909年丹麦科学家塞雷森和德国科学家哈伯,引入pH表示酸度,设计一种玻璃电极,用以迅速测定溶液酸碱度。
俄国科学家谢·列别姐夫,首次人工合成橡胶。
德国科学家奥斯特瓦尔德,发明硝酸的工业制法——氨氧化法。
美国科学家兰米尔,在白炽灯中充入惰性气体,改善钨丝在真空中的挥发和氧化,延长了灯泡的使用寿命。
德国科学家华莱赫,对大量重要天然产物,尤其是香料等进行结构测定,发现它们都具有萜的结构,称为异戊二烯规则。
1910年英国科学家索迪,提出同位素假说,后又提出放射元素位移法则,放射化学开始成为独立的学科。
法籍波兰科学家居里夫人,提出高能辐射的初级化学过程全是形成离子的观点。
法国科学家克劳德,利用惰性气体放电,开始生产霓虹灯。
1911年提出电解质离子在半透膜两边平衡的理论,这种平衡是生物化学中的一个重要过程(英国唐纳)。
发现用特种细菌可以合成丙酮、丁醇等化合物,这是微生物合成的早期工作,以后被用到合成配尼西林、维生素B12等 (以色列、英籍俄国人维茨曼)。
推得球形粒子流体力学的粘度公式,即被用于胶体(瑞士、美籍德国人爱因斯坦)。
1912发现硫化锌晶体X射线衍射,证明了X射线的波性,促进了近代结晶化学的发展(德国冯·劳厄等)。
提出范德华力是偶极间引力的学说(德国刻松)。
1911—1913年,确立了有机物的元素碳、氢、硫、氮、磷等几毫克的微量元素分析法(奥地利普雷格尔)。
提出光化当量定律(瑞士、美籍德国人爱因斯坦)。
1913年提出由粒子散射求得的原子核电荷,可能决定该元素在周期表中的位置,后即为摩斯莱所证实(荷兰范德布洛克)。
从X光谱发现原子序数定律,是周期律的一个重要进展,并从而开始建立了X射线光谱学(英国摩斯莱)。
1909—1913年,发明氨的铁催化合成法,投入生产。
并以合金钢代替碳钢,解决了高温高压下钢材脆裂的问题(德国哈伯、波许)。
1913—1918年,开始用示踪原子于无机化学分析,测定了最难溶无机铅盐的溶解度(丹麦籍匈牙利人赫维赛)。
分离出花色素——花青甙,并阐明了花色素因酸、碱条件不同而引起花的颜色的变化(德国威尔斯塔特)。
发现组成可变的金属间化合物——“柏托雷体”(俄国库尔纳可夫)。
发明晶体反射式X射线谱仪,提出X射线反射公式,用于结晶的结构分析。
证实在氯化钠晶体中并没有单个的氯化钠分子,而仅以钠离子和氯离子的形式存在(英国布莱格父子)。
重新精确校定60多种元素的原子量。
从不同矿石中,测得铅原子量不同,支持了同位素理论(美国理查兹)。
发现存在于脂肪中的维生素,从此维生素分为脂溶性和水溶性两大类(美国麦克可仑)。
镍、铬不锈钢开始获得实际应用(英国哈德费尔德)。
发明高压加氢催化法,使重油、煤转化为高辛烷值的燃料、优质润滑油、甲醇等,并实现工业化。
发明裂解木材成简单分子,进而通过化学反应产生醇和糖(德国伯戈斯)。
1914年发展了精确测量X光波长的技术,从而发现每个元素 X光谱,支持了波尔的原子壳层模型(瑞士西格朋)。
1915年1915—1917年,分别制备战争用毒气,如氯气、光气、芥子气等(德国哈伯,英国泡帕)。
1916年发明粉末法照得X射线干涉图来测定晶体结构,后在工业上得到广泛应用(荷兰德拜、谢勒)。
提出经典价键理论的电子学说,以惰性元素外壳电子“八数群”或“八偶律”为基础,指出两原子化合时等或不等地共享电子对,以满足2、8的惰性电子壳层,开始以电子论统一了共价键与离子键(德国柯塞尔,美国吉·路易斯)。
提出气体在固体表面上的吸附理论(美国兰米尔)。
通过对带极性基团烷基同系物表面能的测量,提出表面膜的分子定向说(美国兰米尔)。
发现加钴的钨钢具有强磁性,开始了新型磁合金的研究,后即制得具有强磁性、耐蚀、耐震、耐温度变化、价廉的铅镍钴磁钢(日本本多光太郎)。
1917年发现化学元素镤(德国哈恩、迈特纳,英国索迪等)。
1918年1918—1923年,提出气体反应的碰撞理论(英国沃·路易斯)。
1919年美国美孚石油公司和碳化物碳化学公司从石油裂化气制造异丙醇,是石油化学利用的开端。
提出链反应理论,认为在链式反应中每个反应的活性中心,可以连续地引起许多分子(如一万到百万)的反应,用以解释光化、爆炸,以及后来的加成聚合等许多反应(丹麦约·克里斯琴森,德国能斯脱)。
将共用电子的观念推广到配位化合物(即络合物),指出配位键的两个电子可以来自同一个原子(英国西奇维克)。
引入电子等排物的观念,认为有同数目电子的分子可有基本相同的电子结构,这是分子轨道概念的雏形(美国兰米尔)。
1920年提出高分子长链的概念,认为淀粉和纤维由葡萄糖失水,蛋白质由氨基酸失水缩聚而成,打破长期以来把高分子看成由许多小分子缔合成胶束的观点,促进高分子化学的建立(德国斯托丁格)。
提出范德华力是诱导偶极间引力(荷兰德拜)。
发现乙烯能自行结合成四碳、六碳的化合物,并进而形成具有一定橡胶性质的巨大分子,对支持斯托丁格高分子理论及发展合成橡胶起了重要作用(美籍比利时人诺威兰德)。
1918—1920年,发明极谱分析法,它可以对多种可氧化,还原物质同时进行灵敏的定性定量测定,可应用于水液、非水极性溶剂及熔盐。
于1926年,与志方益三发明自动极谱仪(捷克海洛夫斯基,日本志方益三)。
发现重要香料麝香和香猫酮为16及17元的大环化合物,大环形化合物的环可以不在一个平面上,打破半个世纪前拜耳(1883年)提出的有机物只能形成平面小环的假说(瑞士籍南斯拉夫人拉齐卡)。
二十年代左右,发现非液晶分子溶于液晶物质时,溶质分子会和溶剂分子一样,处于排列成行的状态(德国沙普)。
提出氢键的概念,认为氢键是一种较弱的“键”,用以解释水等物质的性质(美国莱悌默)。
1921年1921—1923年,从研究酸和碱的催化作用,提出共轭酸碱的理论(丹麦勃朗斯台特)。
提出电解质离子平均活度系数的计算法(美国吉·路易斯)。
发现四乙基铅为良好的汽油燃烧抗爆剂,开始了抗爆机制的研究(美国米吉莱)。
1922年提出所有催化过程形成临界络合物,由络合物的形成和分解决定反应的速度,并推得反应方程式(丹麦勃朗斯台特)。
将液晶分为三大类:向列相液晶、胆甾相液晶、近晶相液晶(德国基·费莱德尔)。
1923年提出强电解质溶液的离子互吸理论,认为强电解质在溶液中完全电离,每个离子被带异性电荷的离子氛包围,从而影响了离子的运动及其他性质,由此推出离子的活度系数是离子强度的函数(荷兰德拜,德国休克尔)。
首次确定辅酶的结构,认识到维生素及铜、钴、镁、钼等人体所需的微量金属都是辅酶的部分(瑞典籍德国人欧拉·钱儿宾,英国哈顿)。
用X光分析法,发现化学元素铪(丹麦籍匈牙利人赫维赛,德国考斯特儿)。
开始用放射性铅来跟踪它在植物组织体中的吸附和分布,确立了研究有生命过程的放化分析原则,但因铅有毒未被应用(丹麦籍匈牙利人赫维赛)。
1924年提出原子结构与元素周期律的关系,即波尔—梅因史密司—斯通纳构造原则,使周期律的解释建立在原子结构的基础上(丹麦尼·波尔,美国梅因史密司,英国斯通纳)。
发明超离心法(十万倍于重力),研究胶体粒子和高分子的大小及分布,首次测定了蛋白质的分子量(瑞典斯维特伯格)。
