诺氟沙星合成工艺(改过) PPT课件
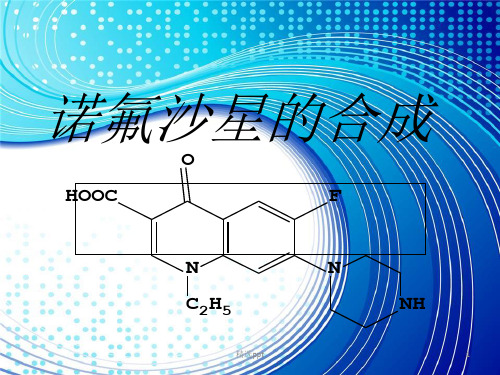
《诺氟沙星的合成》PPT课件
环合剂
环合 冷却 抽滤
蒸出乙醇
丙酮泡洗 甩干
• (环合反应结束,冷却至40℃~50℃或室温,再 离心分离,然后用丙酮洗去环合剂、离心分离, 得到浅褐色晶体。)
• Ⅳ.注意事项:
• 1、反应稳定控制在250℃~260℃,温度过高易 碳化。
• 2、升温要快,否则收率会降低。
• 优点:原料易得,收率较高,成本较低。是我国 目前采用的主要方法
• 缺点:环合反应温度高,哌嗪缩合收率较低,生 成氯哌酸副产物,EMME制备条件苛刻
• ②.3-氯-4-氟苯胺与原甲酸三乙酯反应。
• 优点:避免了使用EMME
• 缺点:有一些副产物,用于合成喹诺酮酸酯收率
较低,质量较差。而且环合时需要250~260℃的
为了更方便和更系统化我们想的是将整个厂房的各种信号集成化实现远程监控为了更节能我们可以在输送电信号的两头安一个光电转化器将电信号转换成光对于诺氟沙星这个比较成熟的生产工艺我们可以选择定值控制系统也就是工艺参数值给定不变比如说某个阀每3小时打开一样这样可提高系统的稳定性和我们的劳动强度
诺氟沙星的合成
O
• 一、环合优化
在经典的诺氟沙星生产工艺中,第一步的环合过程采用
黏度较大的二苯醚做溶剂,反应需要在300℃以上高温下 进行,且后处理工艺繁琐,王敦佳等研究在高温环合时采
用价廉、黏度小的高沸点柴油作为溶剂,并且溶剂可以反 复套用。最终可使前两步反应收率达到95%以上。
第二步环合过程中由于生成物环合定位的不唯一性,在
精选ppt
18
• Ⅲ.工艺流程图
DMSO(回收)
三乙胺
硼螯合物 反应3h
减压蒸馏
加乙醇
年产5亿粒诺氟沙星胶囊的工艺设计

年产5亿粒诺氟沙星胶囊的工艺设计工艺设计说明书年产5亿粒诺氟沙星胶囊的工艺设计名目第一章工艺概述 (3)第二章工艺路线 (10)第三章工艺流程 (13)第四章物料衡算 (18)第五章设备选型 (20)第六章能量衡算 (26)能量平稳表 (27)第七章车间工艺平面布置说明 (28)第八章建厂条件及厂址选择 (32)第九章经济分析 (35)第一章工艺概述1.1 胶囊剂胶囊剂分为硬胶囊、软胶囊(胶丸)、肠溶胶囊、缓释胶囊与控释胶囊。
硬胶囊剂系指将药物,或加辅料制成的粉末、颗粒、速释或缓控释小球,充填于空心胶囊中制成;软胶囊剂系指将一定量的药液包封于球形或椭圆形的软质囊中,可用滴制法或压制法制备;肠溶胶囊剂系指硬胶囊或软胶囊用适宜肠溶材料制备而得,或用肠溶材料包衣的颗粒或小丸充填于胶囊制得,不溶于胃液,但能在肠液中崩解而开释活性成分。
胶囊剂一样供口服用,也可供其他部位如直肠、阴道、植入等使用。
胶囊剂的要紧特点有:①可掩盖药物不良臭味和刺激性,外形整洁、便于识别、携带,使用方便;②药物分散、溶出快,血药浓度达峰时刻比片剂短,有较高的生物利用度;③不稳固的药物,如维生素、抗生素等,装入胶囊后可提高稳固性;④药物能够不同形状装入胶囊,以适应不同性质药物的吸取和使用;⑤可制成速释、缓释、控释、肠溶等多种类型的胶囊剂,以满足各种医疗用途的需要。
但有些药物不能制成胶囊剂,如药物的水溶液或乙醇溶液、易溶性的刺激性药物、易风化的药物、吸湿性药物等。
药品标准规定胶囊剂应整洁,不得有粘结、变形、渗漏或破裂现象,并应无异臭;应按照《中国药典》进行装量差异、崩解时限、微生物限度及其他项目检查,应符合规定。
胶囊剂应密封贮存,存放环境温度不应过高,湿度适宜,以防止发霉、变质。
硬胶囊一样性质量要求(1)硬胶囊内容物的含水量中国药典2000版规定内容物含水量不得超过9.0﹪。
(2)空胶囊的质量依照GB 13731—92,对药用明胶囊的技术要求包括:外观质量、理化性能、微生物检查三大方面。
诺氟沙星的合成

诺氟沙星的合成精心整理诺氟沙星合成工艺的比较1、概述诺氟沙星又称氟哌酸,第三代喹诺酮类抗菌药。
具有抗菌作用强、抗菌谱广、生物利用度高、组织渗透性好及与其他抗菌药无交叉耐药性和副作用小等优点,而且对革兰氏阴性杆菌有强杀菌作用。
已广泛应用于咽喉炎、扁桃体炎、肾盂肾炎及尿道炎等的治疗。
其基本结果如下:分子量:319.34性状:类白色至淡黄色结晶性粉末溶解性:易溶于酸、碱溶液,极微溶于水和醇。
无臭、味微苦。
2、经典合成路线诺氟沙星的合成发展至今,已有数十种合成路线,但有8种经典的诺氟沙星的合成路线。
其余的路线都是通过这8种优化衍生而来的。
按其反应的最后两步关键步骤,可以把这8条路线分为3类:(1)羧基化类,(2)哌嗪化类,(3)成环类。
2.1羧基化类该类反应的最后一步是生成诺氟沙星上的羧基,其包括酯基水解和乙酰基氧化。
按其起始原料可分为以下几类。
优缺点:原料来源困难,操作繁琐,收率也较低。
优缺点:避免使用了EMME 。
缺点是有一些副产物,用于合成喹诺酮酸酯收率较低,且质量较差。
而且环合时需要250-260℃的高温,能量消耗较大。
2.2哌嗪化类该类反应的最后一步是在苯环上发生取代反应,哌嗪取代氯原子使苯环哌嗪化。
优缺点:。
操作简单,原料易得,是各厂家经常使用的方法。
但。
反应温度较高,反应时间较长。
收率偏低,仅为52%左右。
2.3成环类该类反应的倒数第二步的环合,为关键步骤,但该反应只有一种,以2-氯-4-氨基-5-氟-苯甲酸乙酯为原料,最后经PPA 环合而成。
3、工艺改进下面是经硼螯合物生成诺氟沙星的改进工艺。
该工艺原料仍以3.1缩合-环合反应及反环物的控制环合物N H O CH 3FCl OO的生产大多采用由氟氯苯胺与EMME 在150℃左右缩合,再在高温下环合的合成路线,该路线能避免由原甲酸三乙酯/丙二酸二乙酯一锅化路线的边链副产物的产生,但该法存在成环温度高,且有反环物产生的弊端。
该步骤收率能达95%以上。
诺氟沙星的合成工艺路线改进

诺氟沙星的合成工艺路线改进学生姓名梁蕾蕾班级化药903班专业名称化学制药技术系部名称制药工程系指导教师张静提交日期 2011/12/20答辩日期 2011/12/26河北化工医药职业技术学院2011年12月目录摘要 (4)1 前言 (4)1.1喹诺酮类药物 (4)1.1.1喹诺酮简介 (5)1.1.2抗菌作用机制 (5)1.1.3喹诺酮类的共性 (5)1.1.4作用 (6)1.2诺氟沙星概述 (6)1.2.1背景介绍 (6)1.2.2物理性质 (6)1.2.3药理毒理 (6)1.3发展状况 (7)2 制备工艺的优化 (8)2.1环合反应的优化 (8)2.2乙基化反应的优化 (10)2.3哌嗪化反应的优化 (11)3 反应中溶剂的优化 (12)4 反应过程中杂质的检测与定量 (13)5 其他诺氟沙星合成工艺 (14)5.1以 A-(2,4-二氯-5-氟苯甲酰)乙酸乙酯为起始原料 (14)5.2以3-乙氧基-2-(2,4-二氯-5-氟苯甲酰基)丙烯酸乙酯为起始原料 (15)6 总结 (17)参考文献 (18)致谢 (20)摘要诺氟沙星是第3 代喹诺酮类优秀的抗菌药物之一,在医疗领域有着重要的意义。
本文主要对诺氟沙星的合成工艺做了相应的总结,对其中一些典型的合成路线进行了优劣势的分析,并提供了相应的优化方案。
诺氟沙星合成工艺路线大致有两大类型:一、经分子内亲桉取代或Deckmann环余方法先合成喹诺酮环后引入哌嗪基;二、先引入哌嗪基,再逐步形成喹诺酮环。
目前,国内外较多地采用第一类型合成路线:即以3-氯-4-氟苯胺为起始原料,经与EMME (乙氧基亚甲基丙二酸二乙酯)缩合、经烷基化剂乙基化得中间体1-乙基-6-氟-7-氯-1,4-二氢-4-氧-喹啉-3-羧酸乙酯,水解后哌嗪化得诺氟沙星。
本文以 3- 氯- 4- 氟苯胺为起始原料, 经与乙氧基亚甲基丙二酸二乙酯(EMME)缩合、Gould- Jacobs环化、乙基化、硼酸酯络合及与无水哌嗪缩合等五步反应合成了诺氟沙星,总收率为 66.3%。
诺氟沙星制备工艺

诺氟沙星制备工艺《诺氟沙星制备工艺》1. 诺氟沙星的“前世今生”:历史溯源1.1 早期探索的种子其实啊,诺氟沙星的诞生可不是一蹴而就的。
在很久很久以前,人类就一直在和各种细菌感染作斗争。
那时候,一旦感染上细菌,就像被一群小恶魔缠上了一样,人们往往束手无策。
随着科学的发展,科学家们开始探索能够专门对抗细菌的药物。
1.2 诺氟沙星的诞生之旅在20世纪60年代左右,药物研发的大浪潮涌起。
就像探险家在茫茫未知的领域寻找宝藏一样,科学家们在化学物质的海洋里不断筛选、试验。
经过无数次的失败和挫折,诺氟沙星这个神奇的药物终于被发现了。
它就像黑暗中的一盏明灯,给治疗细菌感染带来了新的希望。
刚诞生的时候,人们还不是很清楚它到底有多强大,但是随着研究的深入,它的价值越来越被重视。
2. 诺氟沙星的制作过程:化学魔法秀2.1 原料的聚会诺氟沙星的制作就像是一场原料的盛大聚会。
首先,得有一些特殊的化学原料,比如说某些含氮的化合物和芳香族化合物等。
这些原料就像厨师做菜时的食材一样,是制作诺氟沙星的基础。
打个比方,这就像我们做蛋糕,需要面粉、鸡蛋、糖等原料一样,做诺氟沙星也需要特定的化学原料才能开始。
2.2 反应的奇妙组合有了原料之后,就开始各种奇妙的化学反应啦。
这就像是厨师用不同的烹饪方法把食材变成美味佳肴。
比如说,会有一些缩合反应、环化反应等。
这些反应可不是随随便便发生的,就像一场精心编排的舞蹈,每个步骤都得按照特定的顺序和条件来进行。
比如说温度、酸碱度等条件都得严格控制。
如果把反应条件比作是音乐的节奏,那么一旦节奏乱了,这个化学舞蹈就没法顺利完成,也就做不出合格的诺氟沙星了。
2.3 提纯的“选拔”反应完成后,得到的可不是纯净的诺氟沙星。
里面就像一锅大杂烩,有我们想要的诺氟沙星,还有很多其他的杂质。
这时候就需要提纯了。
提纯就像是一场选拔比赛,要把真正优秀的“选手”(诺氟沙星)从一群“参赛者”(杂质)中挑选出来。
通常会用到一些物理和化学的方法,比如结晶、过滤等。
《诺氟沙星过程简介》PPT课件

优缺点:原料仍可使用3-氯-4-氟苯胺,且前三步与最
后一步完全用方法一的成熟工艺,只在第三步水解反应 产物(1-乙基-6-氟-7-氯-1,4二氢-4-氧代喹啉-3-羧酸)
生成后再与乙酐、醋酸形成一个硼螯合物。实践证明,
这一步的反应很充分,平均收率达98.38 %,并且与哌
嗪的缩合更容易进行,从而使总收率可达到62 %以上。
◆ 反应条件与影响因素
反应温度以250∽260℃为宜,升温要快。常用的热载 体还有二苯乙烷和联苯醚等,但不同的热载体会影响副产 物的生成。
精选PPT
15
1-乙基-7-氯-6-氟-4-氧喹啉-3-甲酸的合成 (第三步)
◆ 工艺原理
精选PPT
16
◆工艺过程
在装有搅拌器、回流冷凝器、温度计、滴液漏斗的250 ml四 颈瓶中,投入环合物、无水碳酸钾、DMF,搅拌加热到70℃,于 70~80℃下,在40—60min内滴加溴乙烷,升温至100~110℃, 保温6—8h,反应完后,减压回收70%~80%的DMF,降温至50℃ 左右,加入200 m1水,析出固体,过滤,水洗,干燥,得粗品, 用乙醇重结晶。
道转移的特性,提高诱导效应, 激活7-氯, 纯化6-氟),可选
择性地提高哌嗪化收率。
精法一:以3-氯4-氟苯胺为原料,与乙氧亚甲基丙二酸二
乙酯反应,经环合、N-乙基化、水解,再与哌嗪缩合而得。 优缺点:方法(1)原料价廉易得,操作简单,是各厂家经 常使用的方法,但缺点是收率偏低,仅为52% 左右。
一、经分子内亲桉取代 或Deckmann环余方法 先合成喹诺酮环后引 入哌嗪基;
二、先引入哌嗪基,再 逐步形成喹诺酮环。
精选PPT
5
目前,国内外较多地采用第一类型合成路线:
诺氟沙星胶囊的制作工艺
诺氟沙星胶囊的制作工艺一、胶囊剂的制备的简要概念1.胶囊剂的概念胶囊剂(capsules )系指将药物装于空心胶囊或有弹性的软质空胶囊中制成的制剂。
胶囊剂可分为硬胶囊剂(hard capsules )和软胶囊剂两种。
硬胶囊剂为将固体或半固体药物加辅料填充于空心胶囊中的制剂。
软胶囊剂(soft gelatin capsules )也称胶丸,为将油类药物或对软质空胶囊无溶解作用的液体药物或混悬液封闭其中形成的制剂。
胶囊剂问世于19世纪中叶,1833年Mothes 提出软胶囊,1848年由Murdock 改进为硬胶囊,随着机械工业的发展和自动胶囊填充机的问世,胶囊剂从理论上和技术上得到了较大的发展。
目前,胶囊剂是临床口服给药最常用的型之一,品种数仅次于注射剂、片剂而居第三位。
本节胶囊剂系指以明胶为囊材。
也有用甲基纤维素、海藻酸钠、变性明胶、聚乙烯醇为囊材。
胶囊剂主要供口服,药物进入胃肠道后,胶囊壳快速溶解。
根据临床需要还可制备供直肠和阴道给药的胶囊剂以及可改变释药特征的缓释、控释胶囊剂及肠溶胶囊剂等。
胶囊剂的特点有:(1) 药物生物利用度较高 胶囊剂的辅料中无粘合剂,空胶囊溶解后药物在胃肠道中分散、溶出,无崩解过程,故吸收速率仅低于散剂,有较高的生物利用度。
(2) 提高药物的稳定性 对光敏感、遇湿热不稳定药物,如维生素、抗生素等,装入空胶囊内后,药物免受光线、空气中水分和氧分子作用,药物稳定性提高。
(3) 药物形态可调适性 药物可以粉末、颗粒的状态,也可以小丸或小片装于胶囊中,还可以以两种状态的混合形式装于胶囊中,以适应临床不同的要求。
液态药物或含油量高的药物难以制成片剂、丸剂时可制成胶囊剂。
剂量小,难溶于水,在消化道中不易吸收的药物,也可将其溶于适当油中制成胶囊剂,有利于吸收。
(4) 延缓药物的释放 将药物制成颗粒或小丸后,用不同性质的高分子材料包衣,使之有不同的释放度,再按不同比例混合装入空胶囊内,可起到缓释、控释,肠溶等作用。
(完整版)年产5亿粒诺氟沙星胶囊的工艺设计
河南中医学院工艺设计说明书年产5亿粒诺氟沙星胶囊的工艺设计目录第一章工艺概述 (3)第二章工艺路线 (10)第三章工艺流程 (13)第四章物料衡算 (18)第五章设备选型 (20)第六章能量衡算 (26)能量平衡表 (27)第七章车间工艺平面布置说明 (28)第八章建厂条件及厂址选择 (32)第九章经济分析 (35)第一章工艺概述1.1 胶囊剂胶囊剂分为硬胶囊、软胶囊(胶丸)、肠溶胶囊、缓释胶囊与控释胶囊。
硬胶囊剂系指将药物,或加辅料制成的粉末、颗粒、速释或缓控释小球,充填于空心胶囊中制成;软胶囊剂系指将一定量的药液包封于球形或椭圆形的软质囊中,可用滴制法或压制法制备;肠溶胶囊剂系指硬胶囊或软胶囊用适宜肠溶材料制备而得,或用肠溶材料包衣的颗粒或小丸充填于胶囊制得,不溶于胃液,但能在肠液中崩解而释放活性成分。
胶囊剂一般供口服用,也可供其他部位如直肠、阴道、植入等使用。
胶囊剂的主要特点有:①可掩盖药物不良臭味和刺激性,外形整洁、便于识别、携带,使用方便;②药物分散、溶出快,血药浓度达峰时间比片剂短,有较高的生物利用度;③不稳定的药物,如维生素、抗生素等,装入胶囊后可提高稳定性;④药物可以不同形态装入胶囊,以适应不同性质药物的吸收和使用;⑤可制成速释、缓释、控释、肠溶等多种类型的胶囊剂,以满足各种医疗用途的需要。
但有些药物不能制成胶囊剂,如药物的水溶液或乙醇溶液、易溶性的刺激性药物、易风化的药物、吸湿性药物等。
药品标准规定胶囊剂应整洁,不得有粘结、变形、渗漏或破裂现象,并应无异臭;应按照《中国药典》进行装量差异、崩解时限、微生物限度及其他项目检查,应符合规定。
胶囊剂应密封贮存,存放环境温度不应过高,湿度适宜,以防止发霉、变质。
硬胶囊一般性质量要求(1)硬胶囊内容物的含水量中国药典2000版规定内容物含水量不得超过9.0﹪。
(2)空胶囊的质量根据GB 13731—92,对药用明胶囊的技术要求包括:外观质量、理化性能、微生物检查三大方面。
诺氟沙星胶囊生产工艺设计之欧阳治创编
专业课程设计题目:年产1亿粒诺氟沙星胶囊生产工艺设计院部:化学化工学院专业:材料化学班级: 1101学号: 201106200126 学生姓名:高首威导师姓名:李谷才完成日期: 2014年6月21日课程设计任务书院部:化学化工学院专业:材料化学班级: 1101姓名:高首威指导教师:李谷才教研室主任:黄先威院教学院长:2014年6月21日目录1 引言12年产1亿粒诺氟沙星胶囊生产工艺设计22.1 诺氟沙星生产工艺设计22.1.1 处方设计22.1.2 工艺流程22.13 产品方案42.2 物料衡算62.2.1 物料衡算依据62.2.2 物料衡算范围62.2.3物料衡算结果72.3 设备的选型72.3.1设备选型的依据72.3.2 生产设备选型82.4车间设计82.4.1 车间布置的依据82.4.2车间的布置要求82.4.3设备的布置92.4.4洁净车间设计103 总结11参考文献121引言诺氟沙星是氟喹诺酮类抗菌药,具广谱抗菌作用,尤其对需氧革兰阴性杆菌的抗菌活性高,对下列细菌在体外具良好抗菌作用:肠杆菌科的大部分细菌,包括枸椽酸杆菌属、阴沟肠杆菌、产气肠杆菌等肠杆菌属、大肠埃希菌、克雷伯菌属、变形菌属、沙门菌属、志贺菌属、弧菌属、耶尔森菌等。
诺氟沙星体外对多重耐药菌亦具抗菌活性。
对青霉素耐药的淋病奈瑟菌、流感嗜血杆菌和卡他莫拉菌亦有良好抗菌作用。
诺氟沙星为杀菌剂,通过作用于细菌DNA螺旋酶的A亚单位,抑制DNA的合成和复制而导致细菌死亡。
肠道病毒属病毒引起的传染病。
临床表现轻者只有倦怠、乏力、低热等,重者可全身感染,脑、脊髓、心、肝等重要器官受损,预后较差,并可遗留后遗症或造成死亡。
本类疾病分布于世界各地,在热带和亚热带全年都有,在温带夏季多见,在温暖潮湿﹑卫生条件差﹑人群拥挤的地区发病率高。
成人和儿童均可发病,儿童较多见。
有些病毒的感染常发生流行,不同年份的流行可由不同种﹑型的病毒引起,有些病毒感染的流行有周期性。
诺氟沙星工艺技术
诺氟沙星工艺技术诺氟沙星是一种广泛应用于抗菌药物领域的药物,具有较广泛的抗菌谱和强效的杀菌作用,特别适用于治疗泌尿系统感染和呼吸道感染等疾病。
下面我将介绍一下诺氟沙星的工艺技术。
诺氟沙星的合成方法主要有两种:一种是将二氟氟醇与氯化醋酸酰胺进行缩合反应,生成二氟氟醇酸酐,再与草酰苯胺进行缩合反应得到诺氟沙星;另一种是采用氟化物和草酰氯反应得到N-取代氟基硅名的中间体,再经过缩合反应生成诺氟沙星。
这两种方法不仅具有较高的产率,而且操作简单,成本较低。
在诺氟沙星的精细化工过程中,主要考虑到环保和安全性。
首先是原料的选择,优选环保无污染的原材料,尽量减少对环境的影响。
在合成过程中,要严格控制反应条件,避免产生有害物质和废气,并对废水废料进行合理的处理和回收利用。
同时,对工作人员进行严格的安全培训和防护,确保操作人员的身体健康和安全。
在诺氟沙星的制剂工艺技术中,主要考虑到制剂的稳定性和有效性。
首先是原料的选择,根据药物的特性选择适合的助溶剂和稳定剂,以提高药物的稳定性和溶解度。
然后是制剂的加工方法,采用合适的工艺条件和设备,确保药物的制剂过程中不会被破坏或受到污染。
最后是包装和储存,采用适当的包装材料和条件,以保持药物的质量和有效性。
诺氟沙星的工艺技术的研究和改进,不仅有助于提高药物的质量和有效性,还可以降低生产成本,提高生产效率。
同时,合理使用并监测工艺技术,可以确保药物的安全性和环保性,避免对环境和人体的危害。
总之,诺氟沙星的工艺技术是一个综合性的过程,需要在合成和制剂过程中考虑到药物的质量、稳定性、有效性、环保性和安全性等因素。
通过合理的研究和改进,可以生产出优质的诺氟沙星药物,并使其更好地服务于医疗事业和患者的健康。
