第四节研究有机化合物的一般步骤和方法说课稿第一课时.doc
《第四节 研究有机化合物的一般步骤和方法》教学设计(安徽省县级优课)

《有机物的分离与提纯》教学设计【教学目标】知识与技能:1、了解怎样研究有机化合物应采取的步骤和方法2、掌握有机化合物分离提纯的常用方法3、掌握蒸馏、重结晶和萃取实验的基本技能过程与方法:通过有机化合物研究方法的学习,了解分离提纯的常见方法情感态度与价值观:通过化学实验激发学生学习化学的兴趣,体验科学研究的艰辛和喜悦,感受化学世界的奇妙与和谐【教学重点】掌握蒸馏、重结晶、萃取的实验操作方法【教学难点】重结晶的原理【教学方法】通过观看网上下载的实验录像、教师演示实验、学生动手操作来学习实验操作,通过多媒体展示教学过程,通过分组实验分组讨论来归纳整理,让学生更直观地学习。
【教学过程】好奇实验:菠菜的颜色是由一种色素构成的吗?小实验现象:3种颜色绿色黄绿色黄色有机物(不纯)——有机物(纯净)——确定实验式——确定分子式——结构式(有哪些官能团)一、蒸馏(1)基本原理:利用混合液体或液-固体系中各组分沸点不同,使低沸点组分蒸发,再冷凝以分离整个组分的操作过程。
【提问】(2)基本条件:①有机物热稳定性较强;②与杂质的沸点相差较大(一般约大于30℃)。
【提问】(3)实验仪器:铁架台、酒精灯、石棉网、蒸馏烧瓶、温度计、冷凝管、牛角管、锥形瓶(4)实验操作:工业酒精的分离【通过网上下载的实验录像《含有杂质的工业乙醇的蒸馏》一起来学习蒸馏的仪器组装,实验过程以及实验注意事项】(5)注意事项:①在蒸馏烧瓶中放少量碎瓷片,防止液体暴沸。
②温度计水银球的位置应与支管底口下缘位于同一水平线上。
③冷凝管中冷却水从下口进,从上口出;先通水后点灯。
【提问】【思考】工业上如何制取无水乙醇?工业乙醇——(蒸馏)——95.6﹪的共沸混合物——(CaO)——99.5﹪以上的无水乙醇【思考与交流】1、如何提取溴水中的溴?2、实验原理是什么?3、用到的实验仪器(玻璃仪器)有哪些?4、如何选取萃取剂?二、萃取(1)基本原理:利用混合物中一种溶质在不同溶剂里的溶解度不同,用一种溶剂把这种溶质从另一种溶剂里提出取出来的方法。
高中化学《研究有机化合物的一般步骤和方法》教案1 新人教选修5
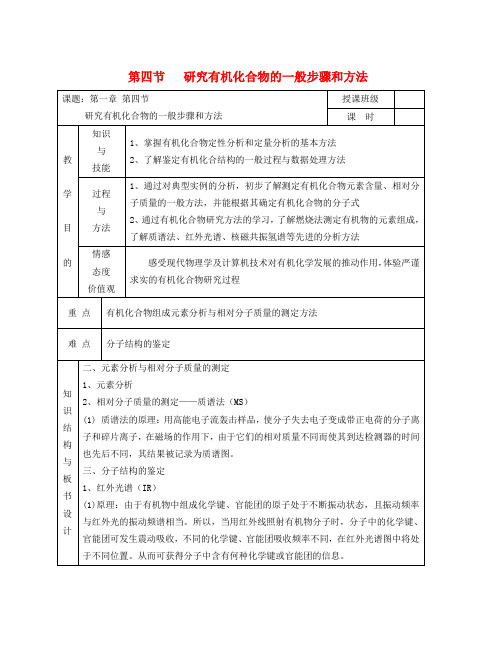
第四节研究有机化合物的一般步骤和方法则该未知物A的实验式为C2H6O讲]实验式和分子式的区别:实验式表示化合物分子所含元素的原[思考与交流]质荷比是什么?如何读谱以确定有机物的相对分子质量?分子离子与碎片离子的相对质量与其电荷的比值。
由于相对质量越大的分子离子的质荷比越大,达到检测器需要的时间越长,因此谱图中的质荷比最大的就是未知物的相对分子质量。
[点击试题]某有机物的结构确定:①测定实验式:某含种元素的有机物,经燃烧分析实验测定其碳的质量分数是相对分子质量为74[讲]从上图所示的乙醇的红外光谱图上,波数在3650cm-1区域附近的吸收峰由O-H键的伸缩振动产生,波数在2960-2870cm-1区域附近的吸收峰由C-H (-CH3、-CH2-)键的伸缩振动产生;在1450-650cm-1区域的吸收峰特别密集(习惯上称为指纹区),主要由C-C、C-O单键的各种振动产生。
要说明的是,某些化学键所对应的频率会受诸多因素的影响而有小的变化。
对称CH3对称CH2C—OANS:(CH3—CH2—O—CH2—CH3)[小结]红外光谱具有高度的特征性,不仅可以用来研究分子的结构和化学键,还可广泛地用于表征和鉴别各种化学物种。
根据红外图1一9二甲醚的核磁共振氢谱[点击试题]一个有机物的分子量为70,红外光谱表征到碳碳双键和C=O的存在,核磁共振氢谱列如下图:①写出该有机物的分子式:C4H6O O②写出该有机物的可能的结构简式: H—C—CH=CHCH3有四类不同信号峰,有机物分子中有四种不同类型的H。
[小结]本节课主要掌握鉴定有机化合物结构的一般过程和方法。
包括测定有机物的元素组成、相对分子质量、分子结构。
了解几种。
研究有机化合物的一般步骤和方法 说课稿 教案

研究有机化合物的一般步骤和方法【教学重点】①蒸馏、重结晶等分离提纯有机物的实验操作②通过具体实例了解某些物理方法如何确定有机化合物的相对分子质量和分子结构③确定有机化合物实验式、相对分子质量、分子式的有关计算【教学难点】确定有机物相对分子质量和鉴定有机物分子结构的物理方法的介绍第二课时三、分子结构的测定1.红外光谱注:该法不需要学生记忆某些官能团对应的波长范围,主要让学生知道通过红外光谱可以知道有机物含有哪些官能团。
2.核磁共振氢谱注:了解通过该谱图确定了(1)某有机物分子结构中有几种不同环境的氢原子(2)有核磁共振氢谱的峰面积之比可以确定不同环境的氢原子的个数比。
有机物分子式的确定1.有机物组成元素的判断一般来说,有机物完全燃烧后,各元素对应产物为:C→CO2,H→H2O,Cl→HCl。
某有机物完全燃烧后若产物只有CO2和H2O,则其组成元素可能为C、H或C、H、O。
欲判定该有机物中是否含氧元素,首先应求出产物CO2中碳元素的质量及H2O中氢元素的质量,然后将碳、氢元素的质量之和与原有机物质量比较,若两者相等,则原有机物的组成中不含氧;否则,原有机物的组成含氧。
2.实验式(最简式)和分子式的区别与联系(1)最简式是表示化合物分子所含各元素的原子数目最简单整数比的式子。
不能确切表明分子中的原子个数。
注意:①最简式是一种表示物质组成的化学用语;②无机物的最简式一般就是化学式;③有机物的元素组成简单,种类繁多,具有同一最简式的物质往往不止一种;④最简式相同的物质,所含各元素的质量分数是相同的,若相对分子质量不同,其分子式就不同。
例如,苯(C6H6)和乙炔(C2H2)的最简式相同,均为CH,故它们所含C、H元素的质量分数是相同的。
(2)分子式是表示化合物分子所含元素的原子种类及数目的式子。
注意:①分子式是表示物质组成的化学用语;②无机物的分子式一般就是化学式;③由于有机物中存在同分异构现象,故分子式相同的有机物,其代表的物质可能有多种;④分子式=(最简式)n。
1.4《研究有机化合物的一般步骤和方法》教案-新人教选修5

第四节研究有机化合物的一般步骤和方法【教学重点】①蒸馏、重结晶等分离提纯有机物的实验操作②通过具体实例了解某些物理方法如何确定有机化合物的相对分子质量和分子结构③确定有机化合物实验式、相对分子质量、分子式的有关计算【教学难点】确定有机物相对分子质量和鉴定有机物分子结构的物理方法的介绍第一课时【引入】从天然资源中提取有机物成分或者是工业生产、实验室合成的有机化合物不可能直接得到纯净物,因此,必须对所得到的产品进行分离提纯,如果要鉴定和研究未知有机物的结构与性质,必须得到更纯净的有机物。
今天我们就来学习研究有机化合物的一般步骤。
【学生】阅读课文【归纳】1(1)分离、提纯(蒸馏、重结晶、升华、色谱分离);(2)元素分析(元素定性分析、元素定量分析)──确定实验式;(3)相对分子质量的测定(质谱法)──确定分子式;(4)分子结构的鉴定(化学法、物理法)。
2一、分离、提纯1.蒸馏完成演示【实验1-1】【实验1-1】注意事项:(1)安装蒸馏仪器时要注意先从蒸馏烧瓶装起,根据加热器的高低确定蒸馏瓶的位置。
然后,再接水冷凝管、尾接管、接受容器(锥形瓶),即“先上后下”“先头后尾”;拆卸蒸馏装置时顺序相反,即“先尾后头”。
(2)若是非磨口仪器,要注意温度计插入蒸馏烧瓶的位置、蒸馏烧瓶接入水冷凝器的位置等。
(3)蒸馏烧瓶装入工业乙醇的量以1/2容积为宜,不能超过2/3。
不要忘记在蒸馏前加入沸石。
如忘记加入沸石应停止加热,并冷却至室温后再加入沸石,千万不可在热的溶液中加入沸石,以免发生暴沸引起事故。
(4)乙醇易燃,实验中应注意安全。
如用酒精灯、煤气灯等有明火的加热设备时,需垫石棉网加热,千万不可直接加热蒸馏烧瓶!物质的提纯的基本原理是利用被提纯物质与杂质的物理性质的差异,选择适当的实验手段将杂质除去。
去除杂质时要求在操作过程中不能引进新杂质,也不能与被提纯物质发生化学反应。
2.重结晶【思考和交流】1.P18“学与问”温度过低,杂质的溶解度也会降低,部分杂质也会析出,达不到提纯苯甲酸的目的;温度极低时,溶剂(水)也会结晶,给实验操作带来麻烦。
化学:1.4《研究有机化合物的一般步骤和方法》课件(新人教版选修5)

即研究有机化合物要经过以下几个步骤: 即研究有机化合物要经过以下几个步骤 粗 产 品 分离 提纯 除 杂 质 每一个操作步骤 是怎样完成的呢? 是怎样完成的呢 实验式或最简式 定性 分析 确定 组成 元素 质 量 分 析 定量分析 测 定 分 子 量 结 构 分 析 结构 式
分子式
一、分离提纯 1、蒸馏:利用混合物中各种成分的沸点不同而使其分离 、蒸馏: 的方法。 的方法。 常用于分离提纯液态有机物; 常用于分离提纯液态有机物; 条件:有机物热稳定性较强、含少量杂质、与杂质沸点 条件:有机物热稳定性较强、含少量杂质、与杂质沸点 相差较大(一般大于30℃ 相差较大(一般大于 ℃) 课本P.17实验 工业乙醇的蒸馏 实验1-1工业乙醇的蒸馏 课本 实验
100%
31
乙醇
相对丰度(R 以图中最强的离子峰(基峰 高为100%, 相对丰度 A)——以图中最强的离子峰 基峰 高为 以图中最强的离子峰 基峰)高为 %, 其它峰的峰高则用相对于基峰的百分数表示。 其它峰的峰高则用相对于基峰的百分数表示。 29 60% + CH3CH2 27 +45 CH CH=OH
[练习 某工厂废液经测定得知主要含有乙醇,其中还溶有丙酮、 练习3]某工厂废液经测定得知主要含有乙醇 其中还溶有丙酮、 练习 某工厂废液经测定得知主要含有乙醇, 乙酸和乙酸乙酯。根据各物质的性质(如下表), ),确定通过下 乙酸和乙酸乙酯。根据各物质的性质(如下表),确定通过下 列步骤回收乙醇和乙酸。 列步骤回收乙醇和乙酸。 物质丙酮乙酸乙酯乙醇乙酸沸点( 物质丙酮乙酸乙酯乙醇乙酸沸点(℃)56.2 77.06 78 117.9 向废液中加入烧碱溶液,调整溶液的pH= ①向废液中加入烧碱溶液,调整溶液的 =10 ②将混和液放入蒸馏器中缓缓加热 收集温度在70~ ℃ ③收集温度在 ~85℃时的馏出物 ④排出蒸馏器中的残液。冷却后向其中加浓硫酸(过量),然 排出蒸馏器中的残液。冷却后向其中加浓硫酸(过量),然 ), 后再放入耐酸蒸馏器进行蒸馏, 后再放入耐酸蒸馏器进行蒸馏,回收馏出物 请回答下列问题: 请回答下列问题: (1)加入烧使溶液的 =10的目的是 使乙酸转变成钠盐 ; )加入烧使溶液的pH= 的目的是 乙醇 (2)在70~85℃时的馏出物的主要成份是 ) ~ ℃ ; 加入过量浓硫酸的目的是( (3)在步骤④中,加入过量浓硫酸的目的是(用化学方程式 )在步骤④ 2CH3COONa+H2SO4=2CH3COOH+Na2SO4 表示) 表示)______________________________________ (4)当最后蒸馏的温度控制在 ~125℃一段时间后,残留 )当最后蒸馏的温度控制在85~ ℃一段时间后, 液中溶质的主要成份是 Na2SO4 H2SO4 。
新人教版高中化学教案-研究有机化合物的一般步骤和方法教案 (1)

第四節研究有機化合物的一般步驟和方法【教學重點】①蒸餾、重結晶等分離提純有機物的實驗操作②通過具體實例瞭解某些物理方法如何確定有機化合物的相對分子品質和分子結構③確定有機化合物實驗式、相對分子品質、分子式的有關計算【教學難點】確定有機物相對分子品質和鑒定有機物分子結構的物理方法的介紹第一課時【引入】從天然資源中提取有機物成分或者是工業生產、實驗室合成的有機化合物不可能直接得到純淨物,因此,必須對所得到的產品進行分離提純,如果要鑒定和研究未知有機物的結構與性質,必須得到更純淨的有機物。
今天我們就來學習研究有機化合物的一般步驟。
【學生】閱讀課文【歸納】1研究有機化合物的一般步驟和方法(1)分離、提純(蒸餾、重結晶、昇華、色譜分離);(2)元素分析(元素定性分析、元素定量分析)──確定實驗式;(3)相對分子品質的測定(質譜法)──確定分子式;(4)分子結構的鑒定(化學法、物理法)。
2有機物的分離、提純實驗一、分離、提純1.蒸餾完成演示【實驗1-1】【實驗1-1】注意事項:(1)安裝蒸餾儀器時要注意先從蒸餾燒瓶裝起,根據加熱器的高低確定蒸餾瓶的位置。
然後,再接水冷凝管、尾接管、接受容器(錐形瓶),即“先上後下”“先頭後尾”;拆卸蒸餾裝置時順序相反,即“先尾後頭”。
(2)若是非磨口儀器,要注意溫度計插入蒸餾燒瓶的位置、蒸餾燒瓶接入水冷凝器的位置等。
(3)蒸餾燒瓶裝入工業乙醇的量以1/2容積為宜,不能超過2/3。
不要忘記在蒸餾前加入沸石。
如忘記加入沸石應停止加熱,並冷卻至室溫後再加入沸石,千萬不可在熱的溶液中加入沸石,以免發生暴沸引起事故。
(4)乙醇易燃,實驗中應注意安全。
如用酒精燈、煤氣燈等有明火的加熱設備時,需墊石棉網加熱,千萬不可直接加熱蒸餾燒瓶!物質的提純的基本原理是利用被提純物質與雜質的物理性質的差異,選擇適當的實驗手段將雜質除去。
去除雜質時要求在操作過程中不能引進新雜質,也不能與被提純物質發生化學反應。
第四节-研究有机化合物的一般步骤和方法说课稿第一课时

第四节研究有机化合物的一般步骤和方法说课稿第一课时设计思想:新课课倡导“从生活走进化学,从化学走向社会。
”“让学生学习有用的化学”。
一、教材分析研究有机化合物的一般步骤和方法在选修5第一章第四节,前面三节已经对有机物的分类、结构特点以及命名有所学习与掌握。
二、学情分析学生在高一必修2中已经学习了有关有机物的分离与提纯,对有机物的分离与提纯的方法已经有所掌握。
又学过最简式等有机知识,有一定的基础,所以容易接受。
三、教学目标及重难点的确定:1.教学目标(三维目标的有机整合):知识与技能:1、了解怎样研究有机化合物应采取的步骤和方法2、掌握有机化合物分离提纯的常用方法3、掌握蒸馏、重结晶和萃取实验的基本技能过程与方法:1. 通过对典型实例的分析,初步了解测定有机化合物元素含量、相对分子质量的一般方法,并能根据其确定有机化合物的分子式。
2. 知道通过化学实验和某些物理方法可以确定有机化合物的结构。
情感态度与价值观:通过化学实验激发学生学习化学的兴趣,体验科学研究的艰辛和喜悦,感受化学世界的奇妙与和谐。
2.教学重点:有机化合物分离提纯的常用方法和分离原理3.教学难点:有机化合物分离提纯的常用方法和分离原理四、教学过程:[引入]我们已经知道,有机化学是研究有机物的组成、结构、性质、制备方法与应用的科学。
那么,该怎样对有机物进行研究呢?一般的步骤和方法是什么?这就是我们这节课将要探讨的问题。
第四节研究有机化合物的一般步骤和方法[讲]从天然资源中提取有机物成分,首先得到的是含有有机物的粗品。
在工厂生产、实验室合成的有机化合物也不可能直接得到纯净物,得到的往往是混有未参加反应的原料,或反应副产物等的粗品。
因此,必须经过分离、提纯才能得到纯品。
如果要鉴定和研究未知有机物的结构与性质,必须得到更纯净的有机物。
下面是研究有机化合物一般要经过的几个基本步骤:[板书][思考与交流]分离、提纯物质的总的原则是什么?1.不引入新杂质;2.不减少提纯物质的量;3.效果相同的情况下可用物理方法的不用化学方法;4.可用低反应条件的不用高反应条件[讲]首先我们结合高一所学的知识了学习第一步——分离和提纯。
第1章第4节 研究有机化合物的一般步骤和方法教案
第一章第4节研究有机化合物的一般步骤和方法课前预习学案一、预习目标预习“研究有机化合物的一般步骤”有哪些,初步认识各步骤的研究方法有哪些及及判断依据。
二、预习内容研究有机化合物的步骤一般有四个,即:、、oyWcelkwU5、。
1.分离与提纯2.元素分析确定实验式一般采用,由燃烧产物计算求得有机物的。
3.M的测定采用,图中最大的代表了该有机物的相对分子质量。
4.分子结构的鉴定:一是光谱,利用或的振动吸收频率不同,从而获得分子中含有何种或的信息。
oyWcelkwU5二是谱,通过观察图谱中峰的和,确定不同环境的氢原子的种类与个数。
oyWcelkwU5课内探究学案一、学习目标1.了解研究有机化合物的一般步骤;2.掌握有机物的分离与提纯方法<蒸馏法、重结晶法、萃取法等);3.了解测定有机化合物元素含量、相对分子质量的一般方法;4.掌握确定有机化合物的分子式;5.理解鉴定有机化合物结构的一般过程和方法。
学习重难点:分离与提纯方法。
二、学习过程<一)、分离与提纯探究:1,研究有机物为什么要先分离与提纯?2,分离与提纯有什么区别?3,有机物除杂原则是什么?⒈蒸馏温度计水银球位于;为什么?加热前加素烧瓷片,目的是;冷凝水进出方向为口进,口出。
oyWcelkwU5探究:什么是共沸溶液?怎样提纯含少量水的乙醇?⒉重结晶:探究:实验1-2中,为了获得更多的苯甲酸晶体,是不是结晶的温度越低越好?⒊萃取:操作:振荡,静置分层,下层液体从口放出,上层液体从口倒出。
例举:其它分离、提纯的方法还有<二)、元素分析与相对分子质量的测定⒈元素分析的目的是。
oyWcelkwU5思考:如何进行元素C、H、O的测定?⒉相对分子质量的测定测定可用质谱法,该法是现代最快速、微量、精确测定相对分子质量的方法,此外还可用:标态密度法、相对密度法等进行求算。
oyWcelkwU5<三)、有机物分子式的确定:由最简式结合相对分子质量求出。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第四节研究有机化合物的一般步骤和方法说课稿第一课时
设计思想:
新课课倡导“从生活走进化学,从化学走向社会。
”“让学生学习有用的化学”。
一、教材分析
研究有机化合物的一般步骤和方法在选修5第一章第四节,前面三节已经对有机物的分类、结构特点以及命名有所学习与掌握。
二、学情分析
学生在高一必修2中已经学习了有关有机物的分离与提纯,对有机物的分离与提纯的方法已经有所掌握。
又学过最简式等有机知识,有一定的基础,所以容易接受。
三、教学目标及重难点的确定:
1.教学目标(三维目标的有机整合):
知识与技能:1、了解怎样研究有机化合物应采取的步骤和方法
2、掌握有机化合物分离提纯的常用方法
3、掌握蒸馏、重结晶和萃取实验的基本技能
过程与方法:1. 通过对典型实例的分析,初步了解测定有机化合物元素含量、相对分子质量的一般方法,并能根据其确定有机化合物的分子式。
2. 知道通过化学实验和某些物理方法可以确定有机化合物的结构。
情感态度与价值观:
通过化学实验激发学生学习化学的兴趣,体验科学研究的艰辛和喜悦,感受化学世界的奇妙与和谐。
2.教学重点:有机化合物分离提纯的常用方法和分离原理
3.教学难点:有机化合物分离提纯的常用方法和分离原理
四、教学过程:
[引入]我们已经知道,有机化学是研究有机物的组成、结构、性质、制备方法与应用的科学。
那么,该怎样对有机物进行研究呢?一般的步骤和方法是什么?这就是我们这节课将
要探讨的问题。
第四节研究有机化合物的一般步骤和方法
[讲]从天然资源中提取有机物成分,首先得到的是含有有机物的粗品。
在工厂生产、实验室合成的有机化合物也不可能直接得到纯净物,得到的往往是混有未参加反应的原料,或反应副产物等的粗品。
因此,必须经过分离、提纯才能得到纯品。
如果要鉴定和研究未知有机物的结构与性质,必须得到更纯净的有机物。
下面是研究有机化合物一般要经过的几个基本步骤:
[板书][思考与交流]分离、提纯物质的总的原则是什么?
1.不引入新杂质;
2.不减少提纯物质的量;
3.效果相同的情况下可用物理方法的不用化学方法;
4.可用低反应条件的不用高反应条件
[讲]首先我们结合高一所学的知识了学习第一步——分离和提纯。
一、分离(separation)、提纯(purification)
[讲]提纯混有杂质的有机物的方法很多,基本方法是利用有机物与杂质物理性质的差异而将它们分离。
接下来我们主要学习三种分离、提纯的方法。
1、蒸馏
[讲]蒸馏是分离、提纯液态有机物的常用方法。
当液态有机物含有少量杂质,而且该有机物热稳定性较强,与杂质的沸点相差较大时(一般约大于30ºC),就可以用蒸馏法提纯此液态有机物。
定义:利用混合液体或液-固体系中各组分沸点不同,使低沸点组分蒸发,再冷凝以分离整个组分的操作过程。
要求:含少量杂质,该有机物具有热稳定性,且与杂质沸点相差较大(大于30℃)。
[投影]演示实验1-1含有杂质的工业乙醇的蒸馏
所用仪器:铁架台(铁圈、铁夹)、酒精灯、石棉网、蒸馏烧瓶、温度计、冷凝管、接受器等。
实验基本过程:含杂质工业乙醇工业乙醇(95.6%)无水乙醇(99.5%)
[强调]特别注意:冷凝管的冷凝水是从下口进上口出。
小结:蒸馏的注意事项
1、注意仪器组装的顺序:“先下后上,由左至右”;
2、不得直接加热蒸馏烧瓶,需垫石棉网;
3、蒸馏烧瓶盛装的液体,最多不超过容积的1/3;不得将全部溶液蒸干;
4、需使用沸石(防止暴沸);
5、冷凝水水流方向应与蒸汽流方向相反(逆流:下进上出);
6、温度计水银球位置应与蒸馏烧瓶支管口齐平,以测量馏出蒸气的温度;
[投影]演示实验1-2 (要求学生认真观察,注意实验步骤)
高温溶解―――趁热过滤――-冷却结晶――称量-溶解-搅拌-加热-趁热过滤-降温、冷却、结晶-过滤-洗涤烘干
2、结晶和重结晶(recrystallization)
(1)定义:重结晶是使固体物质从溶液中以晶体状态析出的过程,是提纯、分离固体物质的重要方法之一。
[投影]重结晶常见的类型
(1)冷却法:将热的饱和溶液慢慢冷却后析出晶体,此法适合于溶解度随温度变化较大的溶液。
(2)蒸发法:此法适合于溶解度随温度变化不大的溶液,如粗盐的提纯。
(3)重结晶:将以知的晶体用蒸馏水溶解,经过滤、蒸发、冷却等步骤,再次析出晶体,得到更纯净的晶体的过程。
[讲]若杂质的溶解度很小,则加热溶解,趁热过滤,冷却结晶;若溶解度很大,则加热溶解,蒸发结晶
[讲]重结晶的首要工作是选择适当的溶剂,要求该溶剂:(1)杂质在此溶剂中的溶解度很小或溶解度很大,易于除去;(2)被提纯的有机物在此溶剂中的溶解度,受温度的影响较大。
(2)溶剂的选择:1 杂质在溶剂中的溶解度很小或很大,易于除去;
2 被提纯的有机物在此溶液中的溶解度,受温度影响较大。
3、萃取
(1)所用仪器:烧杯、漏斗架、分液漏斗。
(2)萃取:利用溶液在互不相溶的溶剂里溶解度的不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来,前者称为萃取剂,一般溶质在萃取剂里的溶解度更大些。
分液:利用互不相溶的液体的密度不同,用分液漏斗将它们一一分离出来。
[投影]基本操作:1.检验分液漏斗活塞和上口的玻璃塞是否漏液;
2.将漏斗上口的玻璃塞打开或使塞上的凹槽或小孔对准漏斗口上的小孔,使漏斗内外空气相通漏斗里液体能够流出
3.使漏斗下端管口紧靠烧怀内壁;及时关闭活塞,不要让上层液体流出
4.分液漏斗中的下层液体从下口放出,上层液体从上口倒出。
[投影]注意事项:
1、萃取剂必须具备两个条件:一是与溶剂互不相溶;二是溶质在萃取剂中的溶解度较大。
2、检查分液漏斗的瓶塞和旋塞是否严密。
3、萃取常在分液漏斗中进行,分液是萃取操作的一个步骤,必须经过充分振荡后再静置分层。
4、分液时,打开分液漏斗的活塞,将下层液体从漏斗颈放出,当下层液体刚好放完时,要立即关闭活塞,上层液体从上口倒出。
学生阅读[科学视野]
[小结]本节课要掌握研究有机化合物的一般步骤和常用方法;有机物的分离和提纯。
包括操作中所需要注意的一些问题。
作业:1、2、3。
