不饱和烃命名
有机化学 第三章 不饱和烃

(2) 炔烃的结构
以乙炔为例。 仪器测得:C2H2中,四个原子共直线:
0.106nm 0.120nm
H CC H
量子化学的计算结果表明,在乙炔分子中的碳原 子是sp杂化:
激发 杂化
杂化
2个sp p轨道
二个sp杂化轨道取最大键角为180°,直线构型:
C
乙炔分子的σ骨架:
HC
CH
每个碳上还有两个剩余的p轨道,相互肩并肩形成2个π键:
第三章 不饱和烃
(一) 烯烃和炔烃的结构 (二) 烯烃和炔烃的同分异构 (三) 烯烃和炔烃的命名 (四) 烯烃的物理性质 (五) 烯烃和炔烃的化学性质 (六) 烯烃和炔烃的工业来源和制法
第三章 不饱和烃
含有碳碳重键(C=C或C≡C)的开链烃称为不饱和烃。 例如:
(一) 烯烃和炔烃的结构
(1) 烯烃的结构 (2) 炔烃的结构
CH=CH2
5-乙烯基-2-辛烯-6-炔
(3) 烯烃的顺反异构体的命名
(甲) 顺反命名法
两个双键碳上相同的原子或原子团在双键的同一侧者, 称为顺式,反之称为反式。例:
2-丁烯: H3C
CH3
C=C
H
H
( I):m.p
。
-132 C
顺-2-丁烯
H3C
H
C=C
H
CH3
(II):m.p -105。C
反-2-丁烯
H C
H
CH3 C
H
丙烯的结构
H C
H
C2H5 C
H
丁烯的结构
小结
π键的特性:
①π键不能自由旋转。 ②π键键能小,不如σ键牢固。
碳 碳 双 键 键 能 为 611KJ/mol, 碳 碳 单 键 键 能 为 347JK/mol,
第三章不饱和烃(UnsaturatedHydrocarbons剖析

顺-2-丁烯
CH3 H
H C H3C
反-2-丁烯
CH3 C H
当双键碳原子上各连有两个不相同的原子或基 团时,由于双键不能自由旋转,在空间就会形成不 同的排列方式,形成顺反异构(也叫几何异构)。
烯烃顺反异构体的命名 顺/反标记法
H3C CH2 C C H H
顺-2-戊烯
CH3
(Z)-1-氯-2-溴丙烯
(Z)-3-甲基-4-异丙基-3-庚烯
H3C C CH3CH2CH2
CH3 CH2 CH2 (CH3)2 CH
CH2CH2CH3 C CH(CH3)2
> CH3 > CH3 CH2 CH2
(Z)-4-甲基-5-异丙基-4-辛烯
(反-4-甲基-5-异丙基-4-辛烯)
3.1.3 烯烃的物理性质
D
顺式加成,定量完成;从位阻小的一面进行。
亲电加成反应
亲电加成反应:
由亲电试剂的作用而引起加 成反应。 亲电试剂: 在反应中,具有亲电性能的 试剂。亲电试剂通常为带正电 的离子(如H+、X+等)或为在 反应中易被极化带正电荷的分 子(如X2)。
加 卤 素 加卤化氢 加 硫 酸 加 水
加次卤酸
C
C
C
C
键能为: 610.9-347.3 =263.6KJ/mol
键能为: 347.3 KJ/mol
π 键只有对称面没有对称轴。所以,双键碳原子之 间不能以两碳核间联线为轴自由旋转
C
C
σ键可绕键轴自由旋转
Байду номын сангаас
π键
σ键
π 键电子云比较分散,有较大的流动性,容易极化 变形,化学反应性较强
第二章不饱和烃

RC H H 2C 3
烯烃的催化加氢反应是定量进行的,因此 可以通过测量氢气体积的方法,来确定烯烃中 双键的数目。
注: 烯烃催化加氢为游离基型加成机理.
(2)加卤素`卤化氢`硫酸`水 _亲电加成反应
烯烃容易给出电子,因而易受到带正电荷或 带部分正电荷的缺电子试剂(称为亲电试剂)的 进攻而发生加成反应,称为亲电加成反应
三、单烯烃的物理性质(自学)
四、单烯烃的化学性质
单烯烃的主要化学反应如下:
R-CH-CH CH-R' H
烯烃的加成反应 烯烃的氧化反应 α - H 的卤代反应
1、加成反应
(1)加氢 烯烃在铂、钯或镍等金属催化剂的存在下, 可以与氢加成而生成相应的烷烃。
RC H C H 2
+
H 2
N i
200 300 C
② 与卤化氢加成
C H H C + 2= 2
H XC H C H X 3 2
卤化氢反应活性顺序为:HI>HBr>HCl 反应历程 烯烃与卤化氢的加成也是亲电加成。
C=C +H X
+ X
慢
C C + H C C H X
+ X
C C + H
快
不对称的烯烃与卤化氢加成时,可能得到两 种不同的产物。
C H HC H X 3 C 2+ H C H HC H 3C 3 X 主 要
+ + + δ δ δ δ δ δ δ
C H C H C H 3 C l 2 2 3 2 1
诱导效应的特点
(1)诱导效应是一种静电诱导作用,其影响
随距离的增加而迅速减弱或消失。诱导效应在沿σ 链传递时,一般认为每经过一个原子,即降低为原 来的三分之一,经过三个原子以后,影响就极弱了, 超过五个原子后便没有了。
烯烃和炔烃结构及命名

一个sp 一个 杂化轨道
二个sp 二个 杂化轨道
未参与杂化的两个p轨道的对称轴互相垂直且都垂直 未参与杂化的两个 轨道的对称轴互相垂直且都垂直 杂化轨道对称轴所在直线。 于sp杂化轨道对称轴所在直线。 杂化轨道对称轴所在直线
乙炔分子的结构: 乙炔分子的结构:
H C C H
乙炔分子的σ键 乙炔分子的 键
一、 烯烃和炔烃的结构
主要指碳碳双键和碳碳三键的结构。 主要指碳碳双键和碳碳三键的结构。
C C
键能 / kJ mol · 键长 / nm
-1
C C
611 0.134
C C
837 0.120
347 0.154
以上数据表明:碳碳双键和碳碳三键都不是由两个或三个 加 以上数据表明:碳碳双键和碳碳三键都不是由两个或三个σ加 和而成的。 和而成的。
烯烃和炔烃
不饱和烃:含有碳碳重键( 不饱和烃:含有碳碳重键(碳碳双键和碳碳三 的烃。 键)的烃。 烯烃:含有碳碳双键的烃。通式:CnH2n。 烯烃:含有碳碳双键的烃。通式: 炔烃:含有碳碳三键的烃。通式: 2n炔烃:含有碳碳三键的烃。通式:CnH2n-2。 烯炔:同时含有碳碳双键和碳碳三键的烃。 烯炔:同时含有碳碳双键和碳碳三键的烃。
二、 烯烃和炔烃的同分异构
含有四个或四个以上碳原子的烯烃和炔烃不仅 存在碳架异构还存在官能团位置异构 碳架异构还存在官能团位置异构。 存在碳架异构还存在官能团位置异构。
CH3CH2CH CH2
1-丁烯 丁烯
CH3
CH3 C CH2
CH3CH CHCH3
2-丁烯 丁烯
2-甲基丙烯 甲基丙烯 (异丙烯 异丙烯) 异丙烯
存在
原子轨道头碰头交盖成; 成键情况 原子轨道头碰头交盖成; 头碰头交盖成 交盖程度大; 交盖程度大; 轨道对键轴呈圆柱形 圆柱形对称 轨道对键轴呈圆柱形对称 分布 性质 键能较大; 键能较大;可沿键轴自由 旋转; 旋转;键的极化性较小
不饱和烃

四、烯烃的化学性质 1、加成反应 (1)加氢 单烯烃在铂、钯或镍等金属催化剂的存在下, 可以与氢加成而生成烷烃。
R CH CH2 + H2
催化剂
R CH2 CH3
(2)亲电加成反应
烯烃容易给出电子,因而易受到正电荷或部 分带正电荷的缺电子试剂(称为亲电试剂)的进 攻而发生反应,称为亲电加成反应。
4.聚合反应
TiCl4 Al(C2H5)3
n CH2
CH2
[ CH2
CH2 ] n
CH3 n CH3CH CH2
TiCl4 Al(C2H5)3
[ CH CH2 ] n
第二节
通式为 CnH2n-2。
炔 烃
炔烃是分子中含有碳碳叁键的烃。
炔烃比相应的烯烃少两个氢原子。
一、炔烃的结构和命名
1. 乙炔的结构 乙炔为最简单的炔烃,分子式为C2H2,构 造式为HC ≡ CH
a C b
(Z)构型
c C d
a C b
(E)构型
d C c
条件:a>b,c>d
例如:
CH3 C H C CH3 CH3 CH2CH3 H C C CH3 CH2CH3
(Z) -3-甲基-2-戊烯
(E) -3-甲基-2-戊烯
三、烯烃的物理性质
烯烃的物理性质与烷烃相似,也是随着碳原 子数的增加而呈规律性变化。在常温下,含2至4 个碳原子的烯烃为气体,含5~18个碳原子的为 液体,19个碳原子以上的为固体。它们的沸点、 熔点和相对密度都随分子质量的增加而上升,但 相对密度都小于1,都是无色物质,不溶于水, 易溶于有机溶剂。
C6H5 C C C6H5
H C C H C C
+
+ H
知识总结——不饱和烃
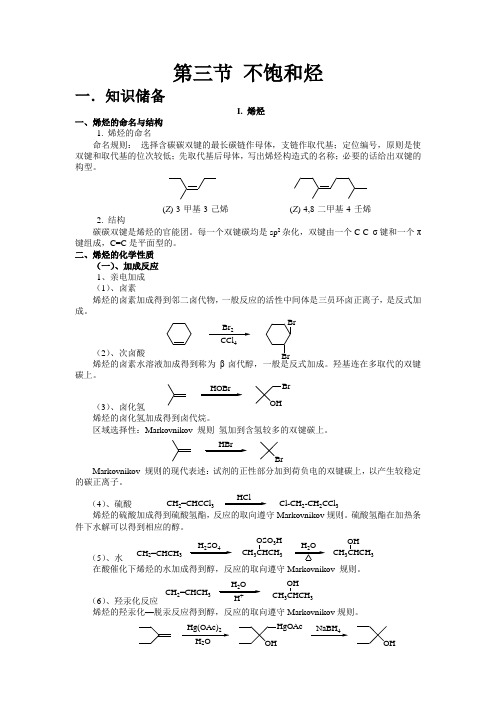
BrBrBr 24HOBrBr OH HBr Br CH 2=CHCCl 3HClCl-CH 2-CH 2CCl 3CH 2=CHCH 3CH 3CHCH 3OSO 3H CH 3CHCH 3OH24CH 2=CHCH 3CH 3CHCH 3OH 222NaBH 4OHHgOAc OH 第三节 不饱和烃一.知识储备I. 烯烃一、烯烃的命名与结构1. 烯烃的命名命名规则: 选择含碳碳双键的最长碳链作母体,支链作取代基;定位编号,原则是使双键和取代基的位次较低;先取代基后母体,写出烯烃构造式的名称;必要的话给出双键的构型。
(Z )-3-甲基-3-己烯 (Z )-4,8-二甲基-4-壬烯2. 结构碳碳双键是烯烃的官能团。
每一个双键碳均是sp 2杂化,双键由一个C-C σ键和一个π键组成,C=C 是平面型的。
二、烯烃的化学性质(一)、加成反应 1、亲电加成 (1)、卤素烯烃的卤素加成得到邻二卤代物,一般反应的活性中间体是三员环卤正离子,是反式加成。
(2)、次卤酸 烯烃的卤素水溶液加成得到称为β-卤代醇,一般是反式加成。
羟基连在多取代的双键碳上。
(3)、卤化氢烯烃的卤化氢加成得到卤代烷。
区域选择性:Markovnikov 规则 氢加到含氢较多的双键碳上。
Markovnikov 规则的现代表述:试剂的正性部分加到荷负电的双键碳上,以产生较稳定的碳正离子。
(4)、硫酸烯烃的硫酸加成得到硫酸氢酯,反应的取向遵守Markovnikov 规则。
硫酸氢酯在加热条件下水解可以得到相应的醇。
(5)、水在酸催化下烯烃的水加成得到醇,反应的取向遵守Markovnikov 规则。
(6)、羟汞化反应烯烃的羟汞化—脱汞反应得到醇,反应的取向遵守Markovnikov 规则。
+21.KM nO 4RR'C=O + CO RR'C=O + R''CO 2RR'C=CH 2RR'C=CHR''+21.KM nO 4H 322B3OH.OH 3.i22-ii HBr Br 2+ ΔH 。
不饱和烃习题解答
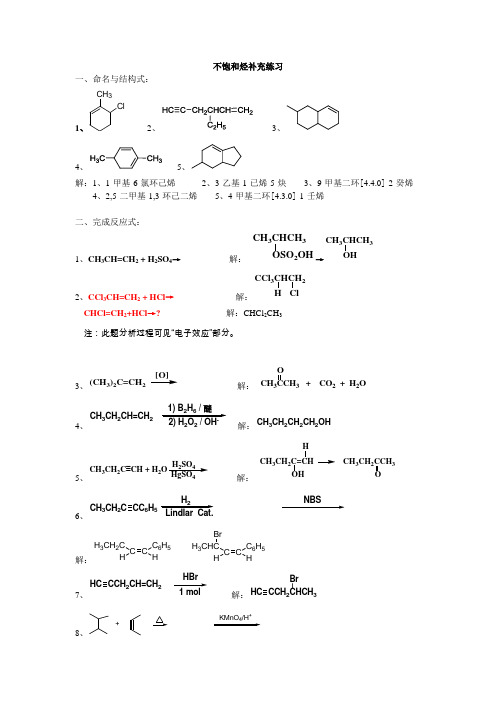
不饱和烃补充练习一、命名与结构式:1、CH3Cl2、3、4、5、解:1、1-甲基-6-氯环己烯2、3-乙基-1-已烯-5-炔3、9-甲基二环[4.4.0]-2-癸烯4、2,5-二甲基-1,3-环己二烯5、4-甲基二环[4.3.0]-1-壬烯二、完成反应式:1、CH3CH=CH2 + H2SO4→解:CH3CHCH3OSO2OH→CH3CHCH3OH2、CCl3CH=CH2 + HCl→解:CCl3CHCH2 CHCl=CH2+HCl→?解:CHCl2CH3注:此题分析过程可见“电子效应”部分。
3、[O](CH3)2C=CH2解:CH3CCH3 + CO2 + H2OO4、CH3CH2CH=CH21) B2H6 / 醚22解:CH3CH2CH2CH2OH5、CH3CH2C≡CH + H2HgSO4H2SO4解:OHHCH3CH2C=CH CH3CH2CCH3O6、NBS CH3CH2C CC6H5H2解:C CC6H5HH3CH2CHC CC6H5HH3CHCHBr7、HC CCH2CH=CH21 mol解:HC CCH23Br8、KMnO/H+ +解:O O9、C 2H 5C CHNaNH 2/NH 3(l)3解:C 2H 5C CNaC 2H 5CC CH 310、HBr 过氧化物CH 2解:CH 2Br三、合成题:(合成有多种路径可完成,不必拘泥于答案)1、由乙炔合成H 3CH 2HHCH 2CH 3解:分析:产物与原料相比,需要在两个端基引入新基团(乙基),故考虑通过炔钠与伯卤代烃(溴乙烷)的反应来实现,增长碳链后再将炔烃还原至反式烯烃:HCCH23C 2H 5C CC 2H 5C 2H 5BrNa 3C 25H HC 2H 52、由1-丁炔合成顺-2-戊烯 HC CCH 2CH 3H 3C C 2H 5解:分析:产物与原料比,端基需引入甲基且需还原为顺式烯烃,故考虑由炔钠合成高级炔烃后经林德拉还原体系得到目标化合物。
不饱和烃-有机化学

147 pm
碳原子均为SP2杂化
H H
C C C
H
C
H
H
大 键的形成
三、共轭效应(conjugative effect)
象1,3 – 丁二烯分子这样具有共轭 键结构的体系称为 共轭体系。 共轭体系的特点: (1) 键长的平均化 (2) 体系能量降低
C C
H H
.......
乙烯的分子球棍模型
乙烯的结构特点:a.平面分子 b.双键不是2个碳碳单键的加合
二. 烯烃的命名(IUPAC)
规则:a. 选主链:选择含双键的最长 碳链作主链,称某烯。 b. 编号:从靠近双键的一端开始编号。 确定取代基、双键的位置 c. 命名:取代基位次+数目+名称+ 双键位次+某烯。 例如:
H2O
BrCH2CH2Br + BrCH2CH2OH BrCH2CH2Br + BrCH2CH2Cl BrCH2CH2Br + BrCH2CH2OCH3
H2O , Cl-
CH3OH
δ Br
–
反应历程:
H3C C H
Br + δ
H C CH 3
–
慢
Br
H3C C H
Br C
H
CH 3
H3C H
Br C H3C H C H
共轭体系的类型:π-π,
p-π, σ-π
在共轭体系中,由于原子间相互影响,使整个分 子的电子云的分布趋于平均化,键长也趋于平均化, 体系能量降低而稳定性增加,这种效应称为共轭效 应。
四、共轭二烯的化学性质
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
不饱和烃命名
不饱和烃是指分子中含有C=C双键或C≡C三键的有机分子,因其
分子内含有不饱和键而具有较强的化学活性,是有机化学中的重要分
子类别之一。
不饱和烃包括烯烃和炔烃两大类。
烯烃是指分子中含有一个或多个C=C双键的有机分子。
烯烃按照
双键数目可以分为单烯、二烯、三烯等。
对于不同种类的烯烃,其分
子结构和性质也各不相同。
单烯是最简单的烯烃,最常见的单烯是乙烯(C2H4),有着较小
的极性和较强的活性,因此在有机合成和化工生产中应用广泛。
二烯
较少见,比较有代表性的是丁二烯(C4H6),通常用于合成丁基橡胶。
三烯非常少见,通常是一些天然化合物的组成部分。
炔烃是指分子中含有一个或多个C≡C三键的有机分子。
炔烃也有
不同的种类,包括单炔、双炔、三炔等。
比较有代表性的炔烃是乙炔(C2H2),其是工业化学中非常重要的原料。
命名不饱和烃时,首先要确定分子的主链,并找出每个双键或三
键的存在。
主链的选取原则是要求主链包含多数碳原子,并使取代基
数目最小。
对于不饱和键,需要在主链上标记,使用体系名称,标记
方法如下:
对于烯烃,可以将双键所在的碳原子编号,并在前面加上ene后缀,如乙烯为ethene,但是对于分子中存在多个双键时,应使用二烯、三烯等前缀,如丁二烯为buta-1,3-diene。
对于炔烃,可以将第一个三键所在的碳原子编号,并在前面加上yne后缀,如乙炔为ethyne,但是对于分子中存在多个三键时,应使
用二炔、三炔等前缀,如丙二炔为prop-1,2-diyne。
此外,对于分子中存在双键和三键的混合物,需要在前缀中同时
包含ene和yne,如苯乙烯为phenylethene,但是对于存在双键和三
键都有的复合烃,可以使用diene、triene、diyne、triyne等前缀表示。
总之,不饱和烃是有机化学中重要的一类分子,它分为烯烃和炔
烃两大类,根据烯烃和炔烃分子中不饱和键的数目,可以分为不同种
类的单烯、二烯、三烯、单炔、双炔、三炔等。
当命名不饱和烃时,
需要确定主链,并将不饱和键标记在主链上,使用ene和yne等后缀
表示。
