免疫球蛋白A(IgA)测定试剂盒(免疫透射比浊法)产品技术要求mairui
免疫球蛋白M测定试剂盒(免疫比浊法)产品技术要求北京世纪沃德生物
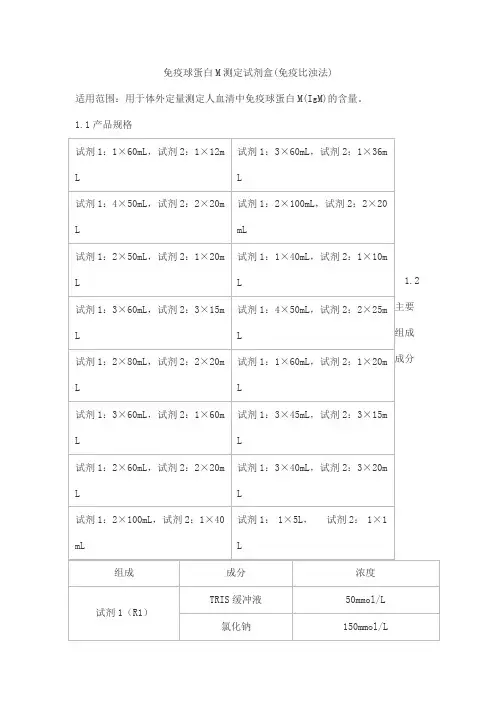
免疫球蛋白M测定试剂盒(免疫比浊法)
适用范围:用于体外定量测定人血清中免疫球蛋白M(IgM)的含量。
1.1产品规格
2.1 外观
试剂1应为无色澄清液体,试剂2应为无色或淡褐色澄清液体。
试剂盒标签标识清晰,外包装完整无损。
2.2 装量
不少于瓶签标示量。
2.3 试剂空白
在340nm处测定试剂空白吸光度,应≤0.5。
2.4 分析灵敏度
测试2.0 g/L的被测物时,吸光度变化值(ΔA)应≥0.1。
2.5 线性
2.5.1 在[0.1,
3.0] g/L区间内,线性相关系数r≥0.990。
2.5.2 在[0.1,1.0) g/L区间内,线性绝对偏差不超过±0.15g/L;在[1.0,
3.0] g/L区间内,线性相对偏差不超过±15%。
2.6 精密度
2.6.1 重复性
测试高、低两个水平浓度样本,其结果的变异系数应不超过5%。
2.6.2 批间差
随机抽取三批试剂盒测试同一份样本,批间相对极差(R)应≤10%。
2.7 准确度
待检系统与比对系统测值的相关系数r≥0.975;在[0.1,1.0) g/L区间内,绝对偏差不超过±0.15g/L;在[1.0,3.0] g/L区间内,相对偏差不超过±15%。
2.8稳定性
该产品在2℃~8℃条件下贮存有效期为12个月,取效期末的产品进行检测,应符合2.1、2.3、2.4、2.5、2.6.1、2.7之规定。
免疫球蛋白(IgA)定量测定试剂盒标准操作程序

*免疫球蛋白(IgA)测定标准操作程序1.摘要本试剂盒适用于体外临床检验,用于测定人血清中免疫球蛋白IgA的含量。
IgA的主要功能是与抗原结合,并进一步触发抗原的分解。
2.适用范围程序适用于AU5811自动生化分析仪检测血清、血浆中IgA的浓度。
3.职责使用AU5811自动生化分析仪进行测定IgA浓度的工作人员要严格按照本 SOP程序进行, 实验室负责人监督管理;本SOP的改动,可由任一使用本SOP的工作人员提出,并报经生化室负责人、科主任签字批准生效。
4.检测方法上海科华生物工程股份有限公司生产的免疫球蛋白(IgA)试剂盒采用的是免疫透射比浊法。
5.原理样本中的IgA与试剂中相应的抗体相遇,立即形成抗原抗体免疫复合物,在特定的缓冲环境中形成浊度,其浊度在合适的抗体浓度存在时与抗原含量成正比,与相同条件下操作的校准品比较,即可求出样本中IgA的含量。
6.仪器AU5811自动生化分析仪7.试剂7.1试剂来源:上海科华生物工程股份有限公司提供7.2试剂瓶内主要成分:磷酸缓冲液(PH7.2)、Tween20、PEG、NaN s、羊抗人IgA抗体。
7.3试剂稳定性:试剂避光保存于 2-8E,若无污染,可稳定至失效期,本试剂有效期为 12个月。
试剂不可冰冻。
R1、R2打开后冷藏于分析仪中可稳定 28天。
7.4试剂准备:试剂为即用式。
8.标准品和质量控制8.1校准程序:使用上海科华生物工程股份有限公司试剂盒内提供的校准品对自动分析仪进行校准。
由a、b、c、d、e五只组成,浓度见瓶签。
校准品可溯源至国际参考物质ERM4708.2质控品:使用罗氏公司提供的生化复合定值质控血清做为室内质控品。
每日在测定前做一次质控,加试剂后做一次质控。
该质控品为干粉包装,在2-8C冰箱可稳定到失效期,使用前用5ml去离子水复溶,待质控物充分溶解(大约 30分钟)后使用。
8.3质控数据管理:按程序对检验后的质控结果进行转换,对质控数据进行分析处理,如出现失控值,应及时分析失控原因,并填写好相关失控记录。
免疫球蛋白M测定试剂盒(免疫比浊法)产品技术要求jiuqiang

免疫球蛋白M测定试剂盒(免疫比浊法)适用范围:用于体外定量测定人血清中免疫球蛋白M的含量。
1.1 包装规格表1 包装规格试剂1:2×50ml、试剂2:2×10ml试剂1:4×50ml、试剂2:2×20ml试剂1:30×4.3ml、试剂2:6×4.3ml试剂1:30×3.8ml、试剂2:6×3.8ml试剂1:1×60ml、试剂2:1×12ml试剂1:1×25ml、试剂2:1×5ml480测试/盒(试剂1:2×50ml、试剂2:2×10ml)600测试/盒(试剂1:2×50ml、试剂2:2×10ml)720测试/盒(试剂1:2×50ml、试剂2:2×10ml)校准品(液体,1水平):1×1ml质控品(液体,水平1):3×1ml;1×1ml质控品(液体,水平2):3×1ml;1×1ml质控品(液体,水平3):3×1ml;1×1ml 1.2 主要组成成分表2 主要组成成分试剂成分浓度试剂1:18.16 mmol/L三羟甲基氨基甲烷缓冲液pH7.6氯化钠聚乙二醇防腐剂123.20 mmol/L试剂2:三羟甲基氨基甲烷缓冲液pH7.6IgM抗体防腐剂18.16mmol/L校准品:人血清基质免疫球蛋白M≥50% 180~300 mg/dl质控品:人血清基质免疫球蛋白M≥50%水平1:40~150 mg/dl 水平2:120~250 mg/dl 水平3:200~400 mg/dl2.1 外观试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂2为无色到淡黄色液体,目测不得有任何沉淀及絮状悬浮物;校准品为无色或浅黄色澄清液体,目测不得有任何沉淀及絮状悬浮物;质控品为无色或浅黄色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂盒标签标识清晰,外包装完整无损。
免疫球蛋白AIgA测定免疫比浊法-检验科免疫室作业指导书

免疫球蛋白AIgA测定免疫比浊法1.原理分析原理是液相免疫沉淀散射比浊终点测定法。
抗血清用缓冲液稀释后加到一份病人血清中,经过孵育后可以测定抗原抗体复合物产生的散射光。
散射光结果和血清中的IgA浓度成正比。
2.标本采集:2.1标本采集前病人准备:受检者空腹2.2标本种类:血清或血浆2.3标本要求:取被检者静脉血2ml,室温放置不超过4小时,分离血清备用。
3.标本储存:待测标本在2-8℃存放不超过24小时,-20℃不超过三个月,-70℃长期保存。
避免反复冻融。
4.标本运输:室温运输5.标本拒收标准:细菌污染、溶血、脂血不能作测定。
6.试剂6.1试剂名称:免疫球蛋白A检测试剂盒6.2试剂生产厂家:芬兰Orion诊断试剂公司6.3包装规格:60Test/kit6.4试剂盒组成:缓冲液30ml空白缓冲液30ml抗血清试剂0.5ml定标液0.5ml磁卡1张7.仪器设备:7.1仪器名称:OrionTurboxRplus特定蛋白分析仪7.2仪器厂家:芬兰Orion集团公司7.3仪器型号:Turboxplus8.操作步骤:8.1试剂配制:8.1.1抗血清应用液准备:吸取500ul抗血清加到反应缓冲液中,轻轻混匀,应用液2-8℃可保存12个星期。
8.1.2空白缓冲液:液体待用。
8.1.3定标液:用0.9%NaCL进行1:51稀释。
定标液根据IFCC提供的材料CRM470进行标定。
收集与处理样品:样品用0.9%Nacl进行1:51稀释。
为每一份样本测定准备一份样品空白,同样,为定标液另外准备一份定标液空白。
准备两份定标液测定(定标完成后,标准曲线数据存储在磁卡内。
下次检测如使用同批试剂,可以不必做定标而直接使用磁卡上的定标信息)。
如下准备各比色管:轻轻摇动混匀,室温18-25℃放置30±5分钟。
仪器测试步骤:参见TurboxR特定蛋白分析仪作业指导书。
9.结果计算:仪器直接计算并打印结果。
10.临床意义:IgA分为血清型和分泌型两种。
免疫球蛋白A测定试剂盒(免疫比浊法)产品技术要求xksm

免疫球蛋白A测定试剂盒(免疫比浊法)
组成:
试剂1(R1)主要成分:Tris缓冲液(pH 6.0~9.0)4mmol/L;
试剂2(R2)主要成分:抗IgA抗血清适量。
适用范围:用于体外定量检测人血清中免疫球蛋白A的浓度。
2.1 外观
外包装完整无破损,标签清晰;试剂1应为无色透明溶液;试剂2应为无色透明溶液。
2.2 净含量
应不低于试剂瓶标示装量。
2.3 试剂空白
在340nm处测定试剂空白吸光度,应≤0.20。
2.4 分析灵敏度
测定浓度为450mg/dl的样品,吸光度变化(ΔA)应不低于0.15。
2.5 线性
2.5.1在[18.0,621.0]mg/dl范围内,线性回归的相关系数应不低于0.990;
2.5.2测试浓度[50.0,621.0]mg/dl的样品,相对偏差应不超过±15%;测试浓度[18.0,50.0)mg/dl的样品,绝对偏差应不超过±7.5mg/dl。
2.6 重复性
2.6.1 批内重复性
变异系数(CV)应不超过5%。
2.6.2 批间差
对同一份样品进行重复测定,相对极差(R)应不超过10%。
2.7 准确度
回收率应在85%~115% 范围内。
2.8空白限
试剂空白限为18mg/dL。
2.9 稳定性
原包装试剂在2℃~8℃条件下有效期为18个月,取到效期后6个月内的试剂盒检测,应符合本技术要求2.1、2.3、2.4、2.5、2.6.1、2.7、2.8之规定。
α1-微球蛋白测定试剂盒(免疫比浊法)产品技术要求jiuzhoutaikang

α1-微球蛋白测定试剂盒(免疫比浊法)适用范围:用于体外定量测定人血清或尿液中α1-微球蛋白的含量。
1.1规格试剂Ⅰ(R1):60ml×3,试剂Ⅱ(R2):60ml×3试剂Ⅰ(R1):60ml×2,试剂Ⅱ(R2):60ml×2试剂Ⅰ(R1):60ml×1,试剂Ⅱ(R2):60ml×1试剂Ⅰ(R1):40ml×2,试剂Ⅱ(R2):20ml×4试剂Ⅰ(R1):40ml×2,试剂Ⅱ(R2):40ml×2试剂Ⅰ(R1):80ml×1,试剂Ⅱ(R2):80ml×1试剂Ⅰ(R1):20ml×2,试剂Ⅱ(R2):20ml×21.2主要组成成分2.1 外观试剂盒外观应整洁,文字符号标识清晰;试剂Ⅰ(R1)为澄清溶液,试剂Ⅱ(R2)为乳白色悬液。
2.2装量用通用量具测量,液体试剂的净含量应不少于标示值。
2.3空白吸光度用纯化水作样本,在波长A570nm,比色光径1cm,反应温度37℃下,试剂空白吸光度测定值,应≤1.50A。
2.4分析灵敏度测试浓度15mg/L的样本时,吸光度变化值≥0.002。
2.5线性在[1,120]mg/L范围内,线性回归的确定系数应不低于0.990;在[1,50)mg/L范围内,线性绝对偏差不超过±5mg/L;在[50,120]mg/L范围内,线性相对偏差不超过±10%。
2.6重复性用低、高二个水平的样本检测,检测结果批内变异系数(CV)应不超过10%。
2.7批间差用三个批号的试剂盒测定同一血清或尿液样本,试剂盒批间相对极差不超过15%。
2.8 准确度使用Fitzgerald公司的纯品,进行回收试验,计算回收率,应介于85%-115%之间。
2.9 稳定性试剂在未开瓶状态下,于2℃~8℃可保存12个月。
有效后两个月内进行测定,检测结果应符合2.3、2.4、2.5、2.6、2.8的要求。
免疫球蛋白(IgG、IgM、IgA)检测试剂盒(免疫比浊法)产品技术要求
医疗器械产品技术要求编号:免疫球蛋白(IgG、IgA、IgM)检测试剂盒(免疫比浊法)1.产品型号/规格及其划分说明序号规格12×200Tests2R1:2×80ml、R2:2×20ml3R1:2×60ml、R2:2×15ml4R1:2×40ml、R2:2×10ml5R1:2×50ml、R2:1×25ml6校准品(选配):1×1ml2.性能指标2.1外观试剂R1溶液应无色、无颗粒、无杂质、无沉淀和悬浮物;试剂R2溶液应呈淡黄色、无颗粒、无杂质、无沉淀和悬浮物;校准品为米白色至浅黄色冻干粉末。
2.2净含量试剂盒各试剂装量应不小于标示值。
2.3试剂空白吸光度应为≤0.4,IgA、用蒸馏水作为样品加入试剂测试,IgG试剂空白吸光度A570nm应为≤0.4。
IgM试剂空白吸光度A340nm2.4分析灵敏度测试IgG:4.85g/L、IgA:0.94g/L、IgM:0.47g/L被测物时,吸光度差值(△A)IgG应不小于0.20、IgA应不小于0.20、IgM应不小于0.05。
2.5线性范围IgG:在(0~35.0)g/L范围内,其线性相关系数r≥0.990;浓度≥5.0g/L 时,相对偏差≤20%;浓度<5.0g/L时,绝对偏差≤1.0g/L。
IgA:在(0~8.0)g/L范围内,其线性相关系数r≥0.990;浓度≥1.3g/L 时,相对偏差≤20%;浓度<1.3g/L时,绝对偏差≤0.4g/L。
IgM:在(0~4.8)g/L范围内,其线性相关系数r≥0.990;浓度≥0.4g/L时,相对偏差≤20%;浓度<0.4g/L时,绝对偏差≤0.2g/L。
2.6测量精密度2.6.1重复性用控制血清重复测试所得结果的重复性(变异系数,CV)应≤6.0%。
2.6.2批间差批间差应≤10.0%。
2.7准确度用参考物质进行测试,其相对偏差应≤20.0%。
免疫球蛋白G测定试剂盒(免疫比浊法)产品技术要求jiuqiang
免疫球蛋白G测定试剂盒(免疫比浊法)适用范围:用于体外定量测定人血清中免疫球蛋白G的含量。
1.1 包装规格表1 包装规格试剂1:2×50ml、试剂2:2×10ml试剂1:4×50ml、试剂2:2×20ml试剂1:4×20ml、试剂2:4×20ml试剂1:30×4.3ml、试剂2:6×4.3ml试剂1:30×3.8ml、试剂2:6×3.8ml试剂1:1×60ml、试剂2:1×12ml试剂1:1×25ml、试剂2:1×5ml480测试/盒(试剂1:2×50ml、试剂2:2×10ml)600测试/盒(试剂1:2×50ml、试剂2:2×10ml)720测试/盒(试剂1:2×50ml、试剂2:2×10ml)校准品(液体,1水平):1×1ml质控品(液体,水平1):3×1ml;1×1ml质控品(液体,水平2):3×1ml;1×1ml质控品(液体,水平3):3×1ml;1×1ml 1.2 主要组成成分表2 主要组成成分试剂成分浓度试剂1:三羟甲基氨基甲烷缓冲液pH7.6 氯化钠聚乙二醇防腐剂18.16 mmol/L 123.20 mmol/L试剂2:三羟甲基氨基甲烷缓冲液pH7.618.16mmol/LIgG抗体防腐剂校准品:人血清基质免疫球蛋白G≥50% 20~30 g/L质控品:人血清基质免疫球蛋白G≥50%水平1:5~10 g/L 水平2:10~18 g/L 水平3:15~28 g/L2.1 外观试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂2为无色到淡黄色液体,目测不得有任何沉淀及絮状悬浮物;校准品为无色或浅黄色澄清液体,目测不得有任何沉淀及絮状悬浮物;质控品为无色或浅黄色澄清液体,目测不得有任何沉淀及絮状悬浮物;试剂盒标签标识清晰,外包装完整无损。
免疫球蛋白G测定试剂盒(免疫比浊法)产品技术要求dimai
免疫球蛋白G测定试剂盒(免疫比浊法)适用范围:本试剂盒用于体外定量测定人血清中免疫球蛋白G浓度。
1、型号规格试剂1:1×30ml;试剂2:1×10ml试剂1:2×30ml;试剂2:1×20ml试剂1:1×60ml;试剂2:1×20ml试剂1:3×80ml;试剂2:4×20ml试剂1:4×60ml;试剂2:4×20ml试剂1:2×60ml;试剂2:2×20ml试剂1:2×30ml;试剂2:2×10ml试剂1:6×60ml;试剂2:2×60ml2.1 外观试剂1、试剂2应澄清、无异物。
2.2 净含量试剂的净含量不少于标称装量。
2.3 试剂空白吸光度用生理盐水作为样本加入试剂测试时,试剂空白吸光度应<0.40A。
2.4 分析灵敏度IgG含量为10g/L时,测定吸光度差值的绝对值应>0.050△A。
2.5 线性区间试剂(盒)线性在[0.1,40.0]g/L区间内:2.5.1 线性相关系数(r)应不小于0.990;2.5.2 [0.1,4.0]g/L区间内,线性绝对偏差不超过±1g/L;(4.0,40.0]g/L区间内,线性相对偏差不超过±10%。
2.6 精密度2.6.1 重复性用相同批号试剂盒测试两个水平的样本,所得结果的变异系数(CV)应<10%。
2.6.2 批间差用3个不同批号试剂盒测试两个水平的样本,试剂(盒)批间相对极差应<10%。
2.7 准确度与已上市的同类产品比对,用40个在[0.1,40.0]g/L区间内不同浓度的人源样本,用线性回归方法计算两组结果的相关系数(r)不小于0.990;[0.1,4.0]g/L 区间内,线性绝对偏差不超过±1g/L;(4.0,40.0]g/L区间内,线性相对偏差不超过±10%。
免疫球蛋白G测定试剂盒(免疫比浊法)产品技术要求lepu
免疫球蛋白G测定试剂盒(免疫比浊法) 适用范围:用于体外定量测定人血清中免疫球蛋白G的浓度。
1.1 规格试剂1:1×60mL,试剂2:1×12mL;试剂1:1×60mL,试剂2:1×15mL;试剂1:1×60mL,试剂2:1×20mL;试剂1:3×40mL,试剂2:3×20mL;试剂1:2×50mL,试剂2:2×10mL;试剂1:1×45mL,试剂2:1×9mL;试剂1:1×5L,试剂2:1×1L;试剂1:2×5L,试剂2:1×2L。
1.2 主要组成成分试剂1主要组分:试剂2主要组分:2.1 净含量应不低于试剂瓶标示装量。
2.2 外观试剂1应为无色或浅色液体,试剂2应为无色或浅色液体。
外包装完好、无破损,标签完好、字迹清晰。
2.3 试剂空白在700nm处测定试剂空白吸光度,应≤1.9。
2.4 分析灵敏度测试10g/L的被测物时,吸光度变化(ΔA)应不低于0.0025。
2.5 准确度在样品中加入一定体积的纯品,计算回收率,应介于90%-110%之间。
2.6 重复性批内变异系数(CV)应不超过10%。
2.7 线性2.7.1在[0.3,25]g/L区间内,线性相关系数r应不低于0.990;2.7.2 在[0.3,3.0)g/L区间内,绝对偏差不超过±0.36g/L;在[3.0,25]g/L 区间内,相对偏差不超过±12%。
2.8 批间差对同一份样品进行重复测定,相对极差≤12%。
2.9 空白限空白限为0.01g/L。
2.10 稳定性取在2℃~8℃条件下贮存达到12个月后的试剂进行检测,应符合本标准2.2、2.3、2.4、2.5、2.6、2.7、2.9之规定。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2性能指标
2.1外观
试剂应为清澈透明的液体,无沉淀、悬浮物和絮状物。
2.2净含量
液体试剂的净含量应不少于标示值。
2.3试剂空白吸光度
试剂以水为空白在37 ℃ 1 ℃,340 nm 波长条件下,吸光度应小于0.3 A。
2.4分析灵敏度
当样本浓度为 2.5 g/L 时,吸光度变化应不小于0.63 A。
2.5线性范围
试剂盒在(0.2~5.6)g/L 范围内:
a)线性相关系数r 应不小于0.9900;
b)当样本浓度不大于2.4 g/L 时,线性绝对偏差应不大于±0.24 g/L;当样本浓度大于
2.4 g/L 时,线性相对偏差应不大于±10.0%。
2.6测量精密度
2.6.1重复性
变异系数:CV 应不大于 4.0%。
2.6.2批间差
相对偏差:R 应不大于 6.0%。
2.7准确度
测定校准品,测定结果与靶值的相对偏差应不大于±10.0%。
2.8分析特异性
血红蛋白浓度在500 mg/dL 内、抗坏血酸浓度在30 mg/dL 内、胆红素浓度在40 mg/dL 内,对试剂检测结果的偏差影响应在±10%以内。
2.9校准品均一性
试剂盒校准品的均一性:CV 应不大于 4.0%。
2.10生物安全性
校准品的HBsAg、HIV抗体、HCV抗体、梅毒螺旋体TP抗体检测应为阴性。
1。
