烷烃的熔点沸点表
甲烷熔沸点

甲烷熔沸点甲烷(CH4)是一种无色、无味的气体,在自然界中广泛存在于天然气和沼气中。
作为最简单的烷烃,甲烷具有许多重要的应用,例如作为燃料和化学原料。
了解甲烷的熔沸点对于理解其性质和应用具有重要意义。
甲烷的熔沸点是指在常温常压条件下,从固态转变为液态的温度称为熔点,从液态转变为气态的温度称为沸点。
对于甲烷而言,其熔点和沸点较低,使得它在常温下处于气态状态。
甲烷的熔点为-182.5摄氏度(-296.5华氏度),沸点为-161.5摄氏度(-258.7华氏度)。
这意味着当甲烷的温度降低到-182.5摄氏度时,它将从气态转变为固态;当温度升高到-161.5摄氏度时,它将从液态转变为气态。
甲烷的低熔沸点主要是由于其分子结构所决定的。
甲烷分子由一个碳原子和四个氢原子组成,碳原子的四个键角都与氢原子形成共价键。
这种简单的分子结构使得甲烷分子之间的相互作用相对较弱,因此需要较低的能量才能使其分子间相互作用减弱,从而实现相态转变。
甲烷的低熔沸点使得它成为理想的燃料。
在常温常压下,甲烷处于气态,便于储存和运输。
而且,由于甲烷分子结构的稳定性,它在燃烧过程中产生的副产品相对较少,对环境的污染较小。
因此,甲烷被广泛应用于家庭供暖、工业生产和交通运输等领域。
甲烷的低熔沸点也为科学研究提供了便利。
在实验室中,研究人员可以通过控制温度,使甲烷在不同的相态之间转变,从而探索其在不同条件下的性质和行为。
例如,在极低温下,甲烷可以形成固态冰,这种冰的结构与常规冰有所不同,对了解宇宙中冰的性质和形成过程具有重要意义。
甲烷是一种具有重要应用的气体化合物,其熔沸点较低,使得它在常温常压下处于气态。
了解甲烷的熔沸点对于理解其性质和应用具有重要意义。
甲烷的低熔沸点使其成为理想的燃料,并为科学研究提供了便利。
希望通过对甲烷熔沸点的了解,可以更好地认识和利用这一重要气体化合物。
烷烃熔沸点高低的判断规律

烷烃熔沸点高低的判断规律1. 前言大家好,今天咱们来聊聊烷烃的熔沸点,听起来有点高大上,对吧?其实这玩意儿跟我们的日常生活息息相关,烷烃就像是化学界的老好人,平常又不张扬,但它的熔沸点可有不少讲究,咱们可得好好研究研究!所以,准备好了吗?让我们一起解锁这个小秘密吧!2. 烷烃的基本概念2.1 什么是烷烃?首先,烷烃其实就是一类饱和碳氢化合物,听上去复杂,其实就是碳和氢的搭档,像个好朋友一样紧紧相拥,构成了一条条长长的链子。
比如,最简单的甲烷(CH₄)就是一个碳原子旁边蹲着四个氢原子,简简单单,清清爽爽。
随着碳链越来越长,熔沸点的变化就像火箭升空一样,速度那是相当快呀。
2.2 为什么熔沸点会变化?要说熔沸点,简单来说,就是物质从固态变成液态,或者从液态变成气态时的温度。
烷烃的熔沸点变化跟它的分子结构有很大关系。
分子越大,链子越长,互相之间的吸引力就越强,就像家里人多了,聚会热闹得很,彼此之间的联系也更加紧密。
反过来,如果链子短,吸引力弱,那熔沸点自然也就低了。
3. 熔沸点高低的规律3.1 碳链长度的影响首先,咱们得从碳链长度说起,越长的烷烃,熔沸点就越高。
这就像是树木,树干粗了,枝叶繁茂,自然抵抗风雨的能力强了。
举个简单的例子,甲烷的沸点是161°C,而辛烷的沸点可是121°C,想想看,这温差就像冬天和夏天的感觉一样,简直让人想不到。
不过,长链的烷烃熔沸点高也有个代价,它们的流动性就差点,像是长途旅行的疲惫感,难免会显得笨重。
3.2 分支结构的作用再来说说分支结构,这个也是个大问题。
你想啊,如果一根长长的链子上长了几个分支,那它的熔沸点又会如何呢?通常,分支越多,熔沸点越低。
为什么呢?因为分支让分子之间的相互作用力弱了,像是多了几个朋友来聚会,热闹了,气氛就散了。
比如,正己烷的沸点比异己烷高,异己烷因为分支多,所以相对“轻松”,所以低温就能变气。
4. 实际应用中的烷烃4.1 生活中的烷烃其实,烷烃不仅仅是课本里的理论,它们在我们的生活中无处不在。
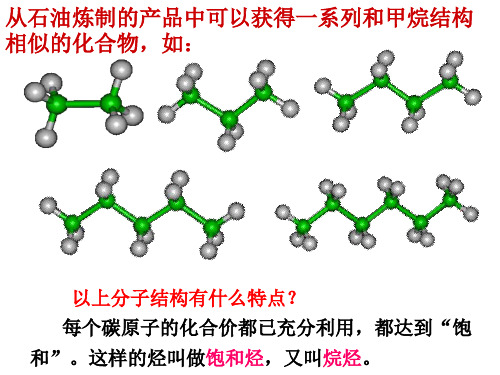
烷烃

有多种等长的最长碳链可供选择时,应选择取代基最多
的碳链为主链。 CH3-CH2-CH—CH-CH2-CH3 3 4 CH3— —CH3 2 CH CH 5 1 CH3 CH3 6
② 编号——从靠近支链的一端开始,编号时应尽可能
使取代基具有最低编号。
两端一样长时,从小取代基一端开始编号。 CH3CH2CHCH2CHCH2CH3 CH3 CH2CH3
C、2mol
D、6mol
3、 写出下列烷烃的分子式:
(1)含有38个碳原子的烷烃的分子式
(2)含有38个氢原子的烷烃的分子式 (3)相对分子量为128的烷烃的分子式
正丁烷
异丁烷
名称 正丁烷 异丁烷
熔点/℃ -138.4 -159.6
沸点/℃ 相对密度 -0.5 0.5788 -11.7 0.557
2、立方烷是一种新合成的烃,其分子 结构为正方体,碳架结构如图所示: (1)立方烷的分子式为? C8H8 (2)该立方烷的二氯代物具有同分异 构体的数目是? 三种
4:
1 互为同位素,___ 2 是同 下列五组物质中___ 素异形体,___ 5 是同分异构体,___ 4 是同 系物,___ 3 是同一物质。
沸点/ ℃
-164 -88.6 -42.1 -0.5 36.1 301.8
相对 密度
0.466 0.572 0.585 0.5788 0.6262 0.7780
水溶性 不溶 不溶 不溶 不溶 不溶 不溶
分析表3-1烷烃的结构简式,写出对应的分子式。相邻
两个烷烃结构和分子组成上有什么联系?
五. 烷烃的命名
1.直链烷烃的命名
与普通命名法基本相同,但不用“正”字。
戊
烷烃的性质数据

化合物英文名分子量熔点(K)Reference CH416.042585.7N/AC2H630.06989.2Timmermans, 1935C3H844.095685.5Streng, 1971C4H1058.1222140. ± 1.00N/AIsobutane58.1222140. ± 1.00N/AC5H1272.1488143.4 ± 0.7N/AButane, 2-methyl-72.1488113. ± 1.N/ANeopentane72.1488255. ± 3.N/AC6H1486.1754178. ± 1N/AButane, 2,3-dimethyl-86.1754143. ± 6N/APentane, 2-methyl-86.1754120. ± 7.N/AButane, 2,2-dimethyl-86.1754173. ± 2N/APentane, 3-methyl-86.1754155.15Hoog, Smittenberg, C7H16 1.Heptane100.2019182.6 ± 0.4N/A2.Hexane, 2-methyl-154.7 ± 0.6N/A3.Pentane, 2,4-dimethyl- 153. ± 3.N/A4.Pentane, 2,2-dimethyl-149. ± 2N/A5.Pentane, 2,3-dimethyl-149.36Anonymous, 19616.Hexane, 3-methyl-153.75Timmermans, 19217.Butane, 2,2,3-trimethyl- 248. ± 1N/A8.Pentane, 3,3-dimethyl-138.1 ± 0.9N/A9.Pentane, 3-ethyl- 154.4 ± 0.2N/AC8H18 1.Pentane, 2,2,4-trimethyl- 114.2285165.77 ± 0.06N/A2.Heptane, 2-methyl- 163. ± 2.N/A3.Heptane, 3-methyl- 152. ± 1N/A4.Pentane, 2,3,4-trimethyl- 163.8 ± 0.4N/A5.Heptane, 4-methyl- 151. ± 3N/A6.Octane216.3 ± 0.3N/A7.Hexane, 2,5-dimethyl-182. ± 2N/A8.Hexane, 2,3-dimethyl-9.Hexane, 2,4-dimethyl-10.Hexane, 3,4-dimethyl-11.Hexane, 2,2-dimethyl- 151.9 ± 0.2N/A12.Hexane, 3,3-dimethyl-147.01 ± 0.06N/A13.Hexane, 3-ethyl-14.Pentane, 3-ethyl-2-methyl-158.1 ± 0.4N/A15.Pentane, 2,2,3-trimethyl-160.5 ± 0.8N/A16.Pentane, 2,3,3-trimethyl-172. ± 1N/A17.Butane, 2,2,3,3-tetramethyl- 374. ± 3N/A18.Pentane, 3-ethyl-3-methyl-182.5 ± 0.8N/AC9H20Nonane128.2551219.5 ± 0.5N/AOctane, 2-methyl-192.75Mears, Fookson, etHexane, 2,2,5-trimethyl-167.2 ± 0.3N/AOctane, 3-methyl-165.15White and Glasgow,Octane, 4-methyl-159.95Slabey and Wise, 19Heptane, 2,4-dimethyl-Heptane, 2,2-dimethyl-160.0 ± 0.2N/APentane, 3,3-diethyl-241. ± 2.N/APentane, 2,2,4,4-tetramethyl-207. ± 1.N/AHexane, 2,3,5-trimethyl-145.25Howard, Mears, et aHexane, 2,2,4-trimethyl-153.15Streiff, Zimmerman,Heptane, 2,3-dimethyl-Heptane, 2,5-dimethyl-Heptane, 2,6-dimethyl-169.55Henne and Chanan, 1Heptane, 3,3-dimethyl-Hexane, 2,2,3-trimethyl-Pentane, 2,2,3,3-tetramethyl-263. ± 1.Heptane, 3-ethyl-Pentane, 2,2,3,4-tetramethyl-150.95Howard, Mears, et aHeptane, 3,4-dimethyl-Heptane, 4-ethyl-Hexane, 2,4,4-trimethyl-159.77Streiff, Murphy, etHexane, 2,3,4-trimethyl-Heptane, 3,5-dimethyl-Heptane, 4,4-dimethyl-Hexane, 2,3,3-trimethyl-156.35Streiff, Zimmerman,Pentane, 2,3,3,4-tetramethyl-171.01Howard, Mears, et aPentane, 3-ethyl-2,4-dimethyl-150.75 ± 0.04N/AHexane, 3,3,4-trimethyl-171.95Streiff, Zimmerman,Pentane, 3-ethyl-2,2-dimethyl-173.62Streiff, Schultz, eHexane, 4-ethyl-2-methyl-Hexane, 3-ethyl-3-methyl-Hexane, 3-ethyl-2-methyl-Hexane, 3-ethyl-4-methyl-Pentane, 3-ethyl-2,3-dimethyl-C10H22Decane142.2817243.3 ± 0.6N/ANonane, 3-methyl-188.49N/ANonane, 2-methyl-201.5Mears, Fookson, etNonane, 4-methyl-174.69Parks, West, et al.Nonane, 5-methyl-186.7Parks, West, et al.Octane, 2,3-dimethyl-Octane, 2,6-dimethyl-Octane, 2,7-dimethyl-220. ± 3N/AOctane, 3,3-dimethyl-Octane, 4-ethyl-4,4-Dimethyl octaneOctane, 3,5-dimethyl-Heptane, 2,4,6-trimethyl-Heptane, 3,3,5-trimethyl-Heptane, 2,2,4-trimethyl-Octane, 2,4-dimethyl-Hexane, 2,2,5,5-tetramethyl-258. ± 1N/AOctane, 2,5-dimethyl-3,4-Diethyl hexaneHexane, 3,3,4,4-tetramethyl-Heptane, 4-propyl-Octane, 4,5-dimethyl-3-Ethyl-3-methylheptaneHexane, 2,2,3,3-tetramethyl-219.15Anonymous, 1960Heptane, 2,2,6-trimethyl-168.15Brooks, Cleaton, etHeptane, 2,3,6-trimethyl-Pentane, 2,2,3,3,4-pentamethyl-236.66Howard, Mears, et aHeptane, 2,5,5-trimethyl-Heptane, 2,4,4-trimethyl-Hexane, 4-ethyl-2,2-dimethyl-Heptane, 2,3,4-trimethyl-Hexane, 2,2,3,5-tetramethyl-Hexane, 2,2,4,5-tetramethyl-Hexane, 2,3,4,4-tetramethyl-Hexane, 2,2,3,4-tetramethyl-Pentane, 2,2,3,4,4-pentamethyl-234.34Howard, Mears, et aHexane, 2,3,4,5-tetramethyl-Hexane, 2,3,3,4-tetramethyl-Hexane, 2,3,3,5-tetramethyl-Pentane, 3-ethyl-2,2,3-trimethyl-230.9Meshcheryakov, Erzyutova, et al., 1952 Pentane, 3-ethyl-2,2,4-trimethylPentane, 2,4-dimethyl-3-(1-methylethyl)-191.4 191.4 K N/A HowardPentane, 3-ethyl-2,3,4-trimethyl-Hexane, 3,3-diethyl-Heptane, 2,3,3-trimethyl-沸点(K)Reference STP生成焓kJ/mol Reference p0p1 111. ± 2Streng, 1971-74.87Chase, 1998184.6 ± 0.6N/A-84. ± 0.4Manion231.1 ± 0.2N/A-104.7 ± 0.50Pittam and Pilcher, 1972262. ± 2.N/A-134.2 ± 0.63Pittam and Pilcher, 1972262. ± 2N/A-134.2 ± 0.63Pittam and Pilcher, 1972309.2 ± 0.2N/A-146.8 ± 0.59Good, 1970301.1 ± 0.2N/A-153.7 ± 0.59Good, 1970282.6 ± 0.5N/A-167.9 ± 0.63Good, 1971341.9 ± 0.3N/A-167.1Good and Smith, 1969331.2 ± 0.2N/A-177.8 ± 1.0Prosen and Rossini, 1945334. ± 1.N/A-174.3 ± 1.0Prosen and Rossini, 1945322.9 ± 0.1N/A-185.6 ± 0.96Prosen and Rossini, 1945336.4 ± 0.4N/A-171.6 ± 0.96Prosen and Rossini, 1945371.5 ± 0.3N/A-187.8 ± 0.79Prosen and Rossini, 1945363.2 ± 0.5N/A-195.0 ± 1.3Prosen and Rossini, 1945353.7 ± 0.3N/A-202.1 ± 0.96Prosen and Rossini, 1945352.3 ± 0.3N/A-206.2 ± 1.3Prosen and Rossini, 1946362.9 ± 0.3N/A-199.2 ± 1.3Prosen and Rossini, 1947365.0 ± 0.3N/A-192.3 ± 1.3Prosen and Rossini, 1948354.1 ± 0.2N/A-204.8 ± 1.1Prosen and Rossini, 1949359.2 ± 0.2N/A-201.5 ± 0.92Prosen and Rossini, 1950366.6 ± 0.2N/A-189.7 ± 1.2Prosen and Rossini, 1951372.4 ± 0.2N/A-224.1 ± 1.3Prosen and Rossini, 1951390.7 ± 0.8N/A-215.5 ± 1.3Prosen and Rossini, 1952392. ± 1N/A-212.6 ± 1.1Prosen and Rossini, 1953386.8 ± 0.3N/A-217.4 ± 1.7Prosen and Rossini, 1954390.9 ± 0.4N/A-212.1 ± 1.2Prosen and Rossini, 1955398.7 ± 0.5N/A-208.7Prosen and Rossini, 1956382.1 ± 0.9N/A-222.6 ± 1.5Prosen and Rossini, 1957389. ± 1.N/A-213.9 ± 1.5Prosen and Rossini, 1958382. ± 2N/A-219.4 ± 1.1Prosen and Rossini, 1959391. ± 1N/A-213.0 ± 1.5Prosen and Rossini, 1960380.0 ± 0.3N/A-224.7 ± 1.0Prosen and Rossini, 1961385.1 ± 0.4N/A-220.1 ± 1.1Prosen and Rossini, 1962391.7 ± 0.2N/A-210.9 ± 1.2Prosen and Rossini, 1963388.8 ± 0.2N/A-211.2 ± 1.3Prosen and Rossini, 1962383.1 ± 0.2N/A-220.1 ± 1.5Prosen and Rossini, 1963387.8 ± 0.3N/A-216.4 ± 1.4Prosen and Rossini, 1964379.6 ± 0.5N/A-225.9 ± 1.9Prosen and Rossini, 1965391.5 ± 0.3N/A-215.0 ± 1.3Prosen and Rossini, 1966423.8 ± 0.3N/A-228.3Good, 1969416.1 ± 0.9N/A397. ± 2.N/A-253.1Good, 1969417. ± 1N/A415. ± 1N/A406. ± 1N/A405. ± 3N/A-246.1Good, 1969419.3 ± 0.4N/A436.52Finke H.L., 1976395.4 ± 0.7N/A-241.5 ± 1.5Fuchs and Peacock, 1979404. ± 2.N/A-242.6Good, 1969399.6 ± 0.4N/A-282.8 ± 1Good, 1969413. ± 2N/A408. ± 2.N/A408. ± 2N/A410. ± 1.N/A406.55Schlesman, 1943-282.7 ± 0.92Good, 1969413.42 ± 0.04-278.3ALS416.75Bazhulin, Ukholin, et al., 1949N/A-277.7Johnson, Prosen, et al., 1947 406.153 ± 0.00413.8Weast and Grasselli, 1989414.35Butler, 1941404. ± 1N/A-280.2 ± 0.92Good, 1969412. ± 1N/A409.15Fenske, Braun, et al., 1947408.4Weast and Grasselli, 1989410.75Cline, 1939-281.1 ± 1.0Good, 1969413. ± 6.N/A-277.9Johnson, Prosen, et al., 1947 409.81Anonymous, 1954-269.7 ± 0.92Good, 1969413.57Pomerantz, Mears, -277.5 ± 0.92Good, 1969406.96-272.7 ± 0.92Good, 1970406.95Fenske, Braun, et al., 1947413.75Fenske, Braun, et al., 1948411.15Fenske, Braun, et al., 1949413.55Fenske, Braun, et al., 1950414.75Kinney and Spliethoff, 1949447.2 ± 0.3N/A-249.7 ± 1.1Prosen and Rossini, 1967 440.9 ± 0.3N/A440Weast and Grassell-260.2Moore, Renquist, et al., 1940 440. ± 3N/A438.3Weast and Grassell-258.6Moore, Renquist, et al., 1942 437.46Mears, Fookson, et al., 1950432. ± 1.N/A433.1 ± 0.8N/A434.35Kinney and Spliethoff, 1949436.51Pomerantz, Fookson, et al., 1954430.7Weast and Grasselli, 1989432. ± 4N/A419Kinney and Spliethoff, 1949428.8Anonymous, 1952419.15Braun, Spooner, et al., 1950429.05Levina, Tantsyreva, et al., 1951410.7Weast and Grassell-285Doering, Roth, et al., 1989 430Shuikin and Cherkashin, 1957430.7Sokolova, 1953443.2Meshcheryakov, Erzyutova, et al., 1952430Challenger and Pantony, 1954436.15Desty and Fidler, 1951437.05Kinney and Spliethoff, 1949431.2Whitmore, Goldsmith, et al., 1950421.15Marschner and Carmody, 1951410.64Anonymous, 1959439.2Howard, Mears, et al., 1947425.95Boord, Greenlee, et al., 1947422.7Petrov, Sushchinskii, et al., 1957420.2Braun, Spooner, et al., 1950429Cherkasova, Bal'yan, et al., 1964422Whitmore, Goldsmith, et al., 1950421.02Howard, Mears, et al., 1947434.75Pomerantz, Mears, et al., 1949432Foehr and Fenske, 1949432.44Howard, Mears, et al., 1947429.15Petrov and Melekhin, 1955437.74Pomerantz, Mears, et al., 1949426Whitmore, Goldsmith, et al., 1950 ryakov, Erzyutova, et al., 1952428.45Pomerantz, Mears, et al., 1949430.19Howard, Mears, et al., 1947442.59Pomerantz, Mears, et al., 1949435.85Kinney and Spliethoff, 1949433.2Cline, 1939p-1p2p-2q2q3q4q5。
烷烃
4—甲基—3—乙基
⑦写名称
取代基在前,“某烷”在后,将两者名写在一起
6 7 8 CH3 CH2 —CH2 —CH3 | | 例: CH3—CH—CH2—CH2—CH—CH2—CH3 |2 1 3 4 5| CH3 CH3
2,2,5—三甲基—5—乙基辛烷
练习:用系统命名法命名下列有机物
CH3—CH2—CH2 | CH2 戊烷 | CH3 CH3 |2 1 5 4 3 CH3—CH2—CH—CH—CH3 | CH3
同分异构现象和同分异构体
[讨论]下面是正丁烷和异丁烷的组成和某些物质性质,试分析有 何异同并探讨其原因。 名 称 分子式 C4H10 相对分子质量 熔 58 点 沸 点 相对密度 0.5788 正丁烷 -138.4 -0.5
CH 3—CH—CH— CH2 —CH 3 2 CH 3 CH 3CHCH2CH 2CH 3
CH 3 或者: CH 3CH(CH3 )CH2CH 2CH 3
它们对应的结构简式:
乙烷: H H | | H-C-C-H | | H H 丙烷: H H H | | | H-C-C-C-H | | | H H H
CH3CHCH3 CH3
3烷烃的名称:
碳原子数 分子式 名称
1 CH4
2 C 2H 6
3 4 5 C3H8 C4H10 C5H12
甲烷 乙烷
丙 烷 丁烷
戊烷
6 7 8 9 10 碳原子数 分子式 C6H14 C7H16 C8H18 C9H20 C10H22 名称
己 烷 庚 烷 辛烷 壬烷 癸 烷
碳原子数大于十时,以汉字数字代表称某烷,
①找起点 主链中离支链最近端作为起点 先简单取代基 再繁取代基 ②编序号 用阿拉伯数字给主链碳原子编号 以确定支链的位置
化合物的物理性质

化合物的物理性质《烷烃的物理性质》一. 物质的状态室温下,C1-C4为气体,C5-C16为液体,C17以上是固体。
二.熔点和沸点烷烃的熔点和沸点都很低,并且熔点和沸点随分子量的增加而升高。
但值得注意的是:(1)对同数碳原子的烷烃来说,结构对称的分子熔点高。
因为结构对称的分子在固体晶格中可紧密排列,分子间的色散力作用较大,因而使之熔融就必须提供较多的能量。
(2)含偶数碳原子的正烷烃比奇数碳原子的熔点高。
这主要取决于晶体中碳链的空间排布情况。
X光证明,固体正烷烃的碳链在晶体中伸长为锯齿形,奇数碳原子的链中两端的甲基处在同一边,而偶数碳原子的链中,两端的甲基处在相反的位置,从而使这种碳链比奇数碳链的烷烃可以彼此更为靠近,于是它们之间的色散力就大些。
烷烃的沸点上升比较有规则,每增加一个CH2基,上升20-30℃,越到高级系列上升越慢。
在相同碳原子数的烷烃中,直链的沸点比带支链的高,这是由于在液态下,直链的烃分子易于相互接近,而有侧链的烃分子空间阻碍较大,不易靠近。
三. 比重、溶解度、折光率(略)环烷烃的物理性质在常温常压下环丙烷及环丁烷为气体,环戊烷为液体,高级环烷烃为固体。
环烷烃的熔点较同数碳原子的直链烷烃高,因为环烷烃比直链烷烃在晶格中排列更紧密。
环烷烃的密度为0.688~0.853g•c m-3 。
环烷烃不溶于水。
一些环烷烃的熔点和沸点见表3-2。
表3.2 环烷烃的熔点、沸点、张力能(kJ·mol-1)和每一个-CH2-单元的燃烧热(kJ·mol-1 )《芳烃的物理性质》苯及其同系物大多为液体,故有特殊的香气,但它们的蒸气有毒。
高浓度的苯蒸气作用于中枢神经,引起急性中毒。
长期接触低浓度的苯蒸气能损害造血器官。
因此,应尽量注意少接触苯。
有时可以用甲苯代替苯作溶剂,因少量甲苯在人体中可以与甘氨酸作用被人体中酶催化形成马尿酸(C6H5CONHCH2CO2H)而排出体外,故甲苯毒性相对较小。
有机化学烷烃知识
引言概述:有机化学烷烃是一类重要的有机化合物,具有简单的化学结构和广泛的应用。
烷烃是碳氢化合物,其分子由碳、氢原子组成。
在本文中,将详细介绍有机化学烷烃的概念、结构、性质以及常见的应用。
正文内容:一、烷烃的概念与分类1.定义及基本结构:烷烃是一类仅由碳和氢原子组成的有机化合物,其分子由碳原子通过单键相连而成。
2.分类:根据碳原子的连接方式,烷烃可分为直链烷烃、支链烷烃和环烷烃三类。
二、烷烃的物理性质1.沸点与熔点:烷烃的沸点和熔点随碳原子数的增加而增加。
直链烷烃的沸点和熔点一般高于相同碳原子数的支链烷烃。
2.密度:烷烃的密度一般较小,随着碳原子数的增加,密度逐渐增加。
3.溶解性:烷烃一般不溶于水,但可以溶于非极性溶剂。
三、烷烃的化学性质1.燃烧性质:烷烃是易燃物质,可以通过燃烧产生大量热能。
2.氧化性质:烷烃可以通过氧化反应得到相应的醇、酮等官能团。
3.卤素取代反应:烷烃可以与卤素发生取代反应,相应的卤代烷烃。
4.加成反应:烷烃可以通过加成反应相应的烯烃或环烷烃。
四、烷烃的应用1.燃料:由于烷烃易于燃烧,因此广泛用作燃料,如汽油、柴油和天然气等。
2.溶剂:烷烃可以作为有机溶剂,常用于涂料、清洁剂等领域。
3.化学原料:烷烃是许多化学合成的重要原料,可制备醇类、酮类、醚类等有机化合物。
4.制冷剂:一些烷烃具有较低的沸点,被用作制冷剂,如氟利昂等。
5.生物医药:部分烷烃可以作为药物的活性部分,如烷烃类抗生素等。
五、烷烃的环境影响和安全性1.燃烧产生的污染物:烷烃的燃烧会产生二氧化碳和氮氧化物等温室气体和大气污染物。
2.化学品的安全性:某些烷烃具有易燃、爆炸性和刺激性等危险特性,需要妥善存储和使用。
总结:有机化学烷烃是碳氢化合物的重要代表,具有简单的结构和广泛的应用。
本文详细介绍了烷烃的概念与分类、物理性质、化学性质以及常见的应用。
同时,也指出了烷烃在环境和安全方面的相关问题。
研究和应用烷烃化合物对于理解有机化学的基本原理和推动现代科技发展具有重要意义。
大学有机化学第二章 链烃-2
△H= +4 kJ· mol-1 △H=-108kJ·mol-1 H= -10kJ· mol
在链增长阶段, 一氯甲烷达到一定浓度时 达到一定浓度时, 在链增长阶段 当一氯甲烷达到一定浓度时 氯原子 除了同甲烷作用外,也可与一氯甲烷作用, 除了同甲烷作用外,也可与一氯甲烷作用,结果生成 二氯甲烷。以同样方式,可生成氯仿 四氯化碳。 氯仿及 二氯甲烷。以同样方式,可生成氯仿及四氯化碳。 Cl· + CH3Cl —> CH2Cl· + HCl CH2Cl· + Cl2 —> CH2Cl2 + Cl· Cl· + CH2Cl2 —> CHCl2· + HCl CHCl2· + Cl2 —> CHCl3 + Cl· Cl· + CHCl3 —> CCl3· + HCl CCl3· + Cl2 —> CCl4 + Cl·
一、烷烃的化学性质 (一) 稳定性 一
烷烃分子中只有牢固的C—Cσ键和 C—Hσ键 , 所以烷烃具有高度的化学稳定 键 室温下烷烃与强酸、 强碱、 性 。 室温下烷烃与强酸 、 强碱 、 强氧化剂 或强还原剂一般都不发生反应。 或强还原剂一般都不发生反应。
上页
下页
首页
(二) 卤代反应 二
有机化合物分子中的氢原子(或其它原子、 有机化合物分子中的氢原子(或其它原子、基 被另一原子或基团取代的反应称为取代反应 取代反应。 团)被另一原子或基团取代的反应称为取代反应。 卤代(halogenation)。 被卤原子取代叫卤代 。 被卤原子取代叫卤代 1. 甲烷的氯代反应
C C
+A B
C C A B
碳原子sp 碳原子sp3 杂化 四面体型结构
c10烷烃沸点
c10烷烃沸点
摘要:
一、烷烃的定义和性质
二、烷烃沸点的影响因素
三、c10烷烃沸点的具体数值
四、c10烷烃沸点在实际应用中的意义
正文:
烷烃是一类碳氢化合物,分子中仅含有单键,其化学性质稳定,不溶于水,易挥发。
烷烃沸点受到多种因素的影响,如分子结构、分子量、分子间作用力等。
c10烷烃,即碳原子数为10的烷烃,是一种具有十个碳原子的直链烷烃。
其沸点受分子量的影响较大,随着分子量的增加,分子间作用力逐渐增强,沸点也逐渐升高。
此外,c10烷烃的沸点还受到分子结构的影响,例如分支、饱和度等。
具体来说,c10烷烃的沸点约为30摄氏度。
这一沸点值对于实际应用具有重要意义。
例如,在工业生产中,c10烷烃可用作溶剂、制冷剂等。
在科学研究中,c10烷烃沸点的研究有助于更深入地了解烷烃的物理性质,为后续研究提供理论支持。
总之,c10烷烃沸点的研究有助于我们更好地理解烷烃的物理性质,为实际应用提供参考。
烷烃环烷烃的物理化学性质详解
过渡态(Transition State)理论
在化学反应中,反应物相互接近,总是先达到一势能最高点 (活化能,相应结构称为过渡态),然后再转变为产物。
例:机理步骤(2)
Cl + H CH3
势能增加
Cl
H CH3
过渡态
势能最高
Cl H + CH3
(3) CH3 + Br Br
CH3 Br + Br
第(2), (3)步反应重复进行
链引发 chain initiation
链转移 (链传递,链增长)
chain propagation
(4) Br + Br (5) Br + CH3 (6) CH3 + CH3
Br Br CH3 Br CH3 CH3
Cl H + CHCl2 CHCl3 + Cl
Cl H + CCl3 CCl4 + Cl
3. 其它烷烃的卤代反应(一卤代)
反应通式 机理通式
hv or R H + X2
hv or
(1) X X
2X
RX + HX 链引发
(2) X + H R
XH + R
(3) R + X X
R X+ X
第(2), (3)步重复进行
接上页
Cl2
Cl
CH3
HCl CH4
.
有效碰撞(产生CH3Cl和Cl ) 自由基消失,反应终止
净结果=0
Cl2
CH3
Cl HCl
CH4 CH3Cl
