化学概念与原理课件
化学课件ppt

熟悉实验室常见的仪器设备,如烧杯、试管、滴 定管、容量瓶等。
分析化学实验技术
化学分析方法
掌握酸碱滴定法、络合滴定法、沉淀滴定法等常见的化学分析方 法。
仪器分析技术
了解色谱法、光谱法、质谱法等仪器分析技术的应用范围和原理 。
分析数据处理
掌握实验数据的处理方法,如误差分析、数据统计和结果分析等 。
反应速率方程
反应速率方程是表示反应速率与反应物浓度的关系,可以用来描述 化学反应进行的快慢和规律。
反应速率常数
反应速率常数是反应速率方程中的常数,表示反应进行的快慢程度 ,与反应的温度有关。
化学反应热力学
反应热
反应热是指在一定条件下,化学反应在单位质量下所释放 出来的热量,通常用焓变(ΔH)来表示。
能量守恒定律
能量守恒定律是指在一个封闭的 系统中,能量既不会凭空产生也 不会凭空消失,它只会从一种形
式转化为另一种形式。
化学基本计算
01
02
03
物质的量
物质的量是衡量物质数量 的单位,通常用摩尔表示 。
摩尔质量
摩尔质量是指单位物质的 量的物质所具有的质量。
阿伏伽德罗常数
阿伏伽德罗常数是指1摩 尔物质所含有的微粒数目 ,通常用NA表示。
化学课件
目录
CONTENTS
• 化学基础知识 • 化学物质与能量变化
• 化学反应与环境 • 化学实验与技术 • 化学应用与案例
• 复习与巩固
01 化学基础知识
CHAPTER
化学基本概念
物质的变化
物质的变化包括物理变化和化学 变化,其中化学变化是指物质在
化学反应中发生的质的变化。
化学反应
化学反应是指两种或两种以上的物 质相互作用,产生新的物质的过程 。
化学ppt课件

化学反应与能量转化
化学反应
化学反应是指分子破裂成原子,原子重新排列组合生成新物质的过程。
能量转化
化学反应中常常伴随着能量的转化,如放热或吸热等。
化学方程式及其计算
化学方程式
化学方程式是用化学符号和式子表示化学反应的式子。
化学方程式的计算
根据化学方程式,可以计算出反应物和生成物的质量比,也 可以计算出反应物和生成物的物质的量之比。
金属与非金属
金属
如铁(Fe)、铜(Cu)、铝(Al)、锌(Zn)等,具有良好的导电性和延 展性。
非金属
如碳(C)、硅(Si)、硫(S)、磷(P)等,一般不具有金属特性。
酸碱盐
• 酸:如盐酸# 人体所需的营养素
03
化学实验
实验室安全与操作规范
实验室安全意识
进入实验室前需要了解实验室的安全规定,遵循正确的操作规程,避免发生意外 事故。
2023
化学ppt课件
目录
• 化学基础知识 • 化学物质 • 化学实验 • 化学与生活 • 化学前沿 • 复习与考试指导
01
化学基础知识
化学的定义与性质
化学是一门研究物质变化的自然科学
化学是研究物质的组成、结构、性质和变化规律的自然科学。
化学性质
化学性质指的是物质在发生化学变化时所表现出来的性质。
3
研究特点
操纵单个原子和分计和制备具有特定化学结构 和功能的新分子和材料。
涉及领域
材料科学、生物学、医学、能 源、环境科学等。
研究热点
高效合成方法、不对称合成、 组合化学等。
06
复习与考试指导
学习方法与策略
制定学习计划
01
根据教学内容和自身情况,制定详细的学习计划,合理安排时
化学实验基础知识PPT课件

表格法
适用于大量数据的整理和表达, 能清晰展示各组数据间的对比关
系。
图形法
直观展示数据间的变化趋势和规 律,便于分析和理解。常用图形 包括柱状图、折线图、散点图等。
文字描述法
对实验结果进行概括性描述和分 析,阐述实验结论和意义。应结 合图表进行解释和说明,增强表
达效果。
THANK YOU
根据实验需求选择合适的搅拌器,如玻璃棒、磁力搅拌器等。
根据实验需求控制搅拌速度,避免产生过多的气泡或溅出。
搅拌、过滤和蒸发操作要点
选择合适的滤纸
根据实验需求选择合适的滤纸,如慢速滤纸、中速滤纸等。
折叠滤纸
将滤纸折叠成合适的形状,放入漏斗中,用水润湿并贴紧 漏斗内壁。
搅拌、过滤和蒸发操作要点
• 过滤操作:将待过滤的液体沿玻璃棒慢慢倒入漏斗中,注 意液面不要超过滤纸边缘。
仪器的准备
标准溶液的配制
按照准确称量的基准物质的质量,配 制一定浓度的标准溶液。
准备好滴定管、容量瓶、移液管等仪 器,并进行校准。
滴定分析法原理及操作过程
待测溶液的取样和处理
准确移取一定体积的待测溶液,并进行必要 的预处理。
终点判断
根据指示剂的颜色变化或电位突跃等信号判 断滴定终点。
滴定操作
将标准溶液逐滴加入待测溶液中,同时搅拌 并观察反应现象。
待测溶液的取样和处理
准确移取一定体积的待测溶液,并进 行必要的预处理。
吸光度或发光强度的测定
将待测溶液置于比色皿中,在分光光 度计上选择合适的波长和测量模式, 测定其吸光度或发光强度。
数据处理
根据标准曲线和待测溶液的吸光度或 发光强度计算待测组分的含量。
06
实验数据处理与结果表 达技巧
初中化学PPT课件

可燃性,氧化剂,用于制造硫酸、 硫化橡胶等。
17
金属与非金属
金属的性质和用途
导电性、导热性、延展性、可塑性等,用于制造电线、电缆、机器零件等。
非金属的性质和用途
大多数非金属具有氧化性,有些非金属还有还原性。用于制造化肥、农药、合 成材料等。
2024/1/26
18
05 化学实验基本操作与技能
分解反应
由一种物质生成两种或两种以上其他物质 的反应,特点是“一变多”。
B
C
置换反应
由一种单质和一种化合物反应,生成另一种 单质和另一种化合物的反应,特点是“单换 单”。
复分解反应
由两种化合物互相交换成分,生成另外两种 化合物的反应,特点是“双交换”。
D
2024/1/26
14
04 常见的化学物质
2024/1/26
化学的发展包括:元素周期表的发现 和完善;化学键理论的建立和发展; 量子化学和计算化学的兴起;绿色化 学和可持续化学的提出和实践。
2024/1/26
6
物质的组成与结构
02
2024/1/26
7
元素与元素周期表
01
元素的概念及分类
介绍元素定义,阐述元素分类方法,如金属元素、非金 属元素等。
2024/1/26
醛、酮
分别含有醛基和酮基的 有机物,可发生氧化、 还原等反应。
羧酸及其衍生物
含有羧基或羧酸衍生物 的有机物,具有酸性、 酯化等反应性质。
2024/1/26
30
有机合成材料及其应用
合成纤维
通过化学方法合成的高分子纤 维,如涤纶、锦纶、腈纶等。
合成塑料
通过化学方法合成的高分子塑 料,如聚乙烯、聚丙烯、聚氯 乙烯等。
大学普通化学-课件

04
化学实验基础
实验安全与操作规范
01
实验安全须知
了解实验中可能存在的危险因素 ,遵守实验室安全规定,确保自 身和他人安全。
02
实验操作规范
03
实验器材使用
掌握实验操作流程,严格按照实 验步骤进行操作,避免因操作不 当引发事故。
正确使用实验器材,了解各类器 材的用途、使用方法和注意事项 。
实验设计与数据处理
有机化合物与高分子材料
01
02
03
04
有机化合物是指含碳元素的化 合物,其种类繁多,性质各异
。
有机化合物在工业、农业、医 药、环保等领域具有广泛的应 用,如塑料、合成纤维、农药
等。
高分子材料是指分子量较大的 有机化合物,其具有优良的力
学性能和化学稳定性。
高分子材料在工业、农业、交 通、通讯等领域具有广泛的应 用,如合成橡胶、合成纤维等
化学在工业生产中的应用
农业
化肥、农药、植物生长调节剂等。
制造业
材料合成、表面处理、电镀等。
能源
石油、天然气、太阳能等的开采和利用。
环保
污水处理、大气治理等。
化学前沿科技与发展趋势
纳米技术
纳米材料、纳米药物等。
绿色化学
环境友好型的合成方法、反应 条件等。
生物技术
基因工程、蛋白质工程等。
新能源
燃料电池、太阳能电池等。
大学普通化学-课件
目录
• 化学基本概念 • 化学反应原理 • 元素与化合物性质 • 化学实验基础 • 化学应用与前沿科技
01
化学基本概念
化学的定义与性质
总结词
理解化学的本质和特性是学习化学的基础。
化学基本概念和原理
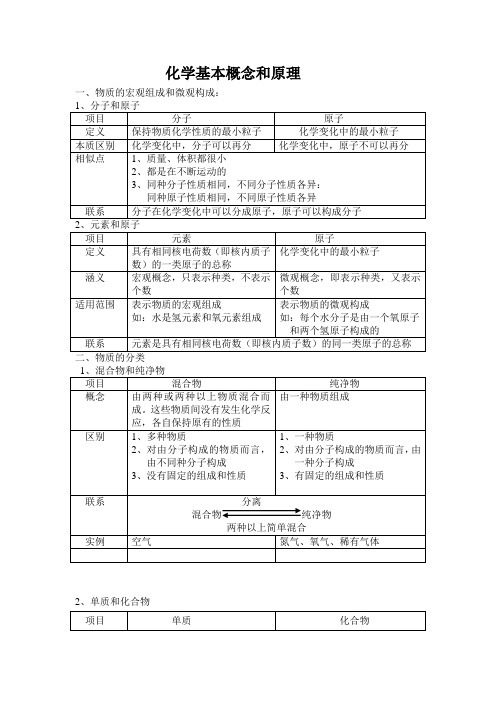
单位
克
是比值,无单位
计算公式
(溶质质量/溶液质量)×100%
水、二氧化碳
三、化学用语
1、化合价和离子符号
项目
价标符号
离子符号
意义
表示某元素或原子团的化合价
表示某种离子所带的电荷数
写法
化合价的正、负在前,数字在后:
写在元素符号或原子团的正上方
数字在前,正、负号在后:写在元素符号或原子团的右上方
举例
+2 –1 +1-2
MgCl2H2O
Mg2+Cl-H+O2-
四、溶液
化学基本概念和原理
一、物质的宏观组成和微观构成:
1、分子和原子
项目
分子
原子
定义
保持物质化学性质的最小粒子
化学变化中的最小粒子
本质区别
化学变化中,分子可以再分
化学变化中,原子不可以再分
相似点
1、质量、体积都很小
2、都是在不断运动的
3、同种分子性质相同,不同分子性质各异:
同种原子性质相同,不同原子性质各异
和两个氢原子构成的
联系
元素是具有相同核电荷数(即核内质子数)的同一类原子的总称
二、物质的分类
1、混合物和纯净物
项目
混合物
纯净物
概念
由两种或两种以上物质混合而成。这些物质间没有发生化学反应,各自保持原有的性质
由一种物质组成
区别
1、多种物质
2、对由分子构成的物质而言,由不同种分子构成
3、没有固定的组成和性质
1、一种物质
2、对由分子构成的物质而言,由一种分子构成
3、有固定的组成和性质
有机化学的基本概念和原理

有机化学的基本概念和原理有机化学是研究有机物和其反应的科学,主要研究含碳的化合物。
有机化学的基本概念和原理是理解和掌握有机化学的关键。
下面将从有机化学的特点、碳的价电子、键的形成以及有机反应机理等方面探讨有机化学的基本概念和原理。
一、有机化学的特点有机化学研究的是含碳的化合物,而无机化学研究的是无机物。
有机化合物的共同特点是含有碳-碳键或碳-氢键。
碳原子的四个价电子能力使其形成复杂的分子结构,为有机化学提供了无限的可能性。
二、碳的价电子碳原子有4个价电子,可形成4个共价键。
其中,三个价电子以单键的形式与其他原子结合,第四个价电子则用于构建碳骨架或与其他原子形成多重键。
而其他非金属元素的价电子数目较少,因此无法像碳一样形成复杂的分子结构。
三、键的形成原理在有机化学中,键的形成原理包括共价键的形成和键的极性。
共价键的形成是指两个原子共享一对电子,通过电子云重叠来实现。
共价键的稳定性取决于电子云的重叠程度和电子云的密度。
而键的极性是指共价键中电子密度不均匀,其中一个原子对电子的吸引力较大。
极性键的特点是由于电子云偏向一个原子,使该原子带有部分正电荷,而另一个原子则带有部分负电荷。
四、有机反应机理有机反应机理是指有机反应的整体过程和细节。
它描述了反应物转化为产物的步骤和中间物的生成消失过程。
有机反应机理可以分为基于键裂解和键生成的机理类型。
键裂解的机理包括自由基反应机理、离子反应机理和共轭体系反应机理。
键生成的机理包括亲电反应机理和核催化反应机理。
结论:有机化学的基本概念和原理是理解和掌握有机化学的基础。
了解有机化学的特点、碳的价电子、键的形成原理和有机反应机理能够帮助我们理解和预测有机化合物的性质和反应方式。
通过不断学习和实践,我们可以进一步深入了解有机化学并应用于生物、医药等领域。
有机化学将继续为人类社会的发展做出贡献。
高中化学ppt课件

03
化学实验基础
实验安全和操作规范
实验安全
确保实验环境安全,遵守实验安 全规定,避免发生意外事故。
操作规范
遵循正确的操作步骤和规范,确 保实验结果的准确性和可靠性。
实验器材和试剂
实验器材
了解和掌握实验所需的器材,如烧杯、试管、滴定管等,并 正确使用。
试剂
熟悉实验所需的试剂,了解其性质和使用方法,注意试剂的 储存和使用期限。
02
化学基础知识
原子结构和元素周期表
总结词
理解元素周期表的规律和元素性质的关系
总结词
掌握原子结构的基本理论
详细描述
元素周期表是化学学科中重要的工具,通过学习元素周期 表的排列规律,可以理解元素性质的变化趋势,如金属性 、非金属性、电负性等。
详细描述
原子结构包括原子核和核外电子,通过学习原子的电子排 布规律,可以理解元素的化学性质和反应机制。
实验设计和数据处理
实验设计
根据实验目的和要求,设计合理的实验方案,确保实验结果的准确性和可靠性 。
数据处理
掌握实验数据的记录、整理和分析方法,正确处理实验数据,得出科学结论。
04
化学在生活中的应用
生活中的化学物质
总结词
了解生活中的化学物质
详细描述
生活中常见的化学物质包括水、食盐、糖、醋酸、酒等,它们在我们的饮食、清 洁和日常用品中都有广泛应用。
05
化学前沿和展望
现代化学的发展趋势
绿色化学
随着环保意识的增强,绿色化学 成为未来化学发展的主要趋势, 旨在减少或消除化学品对人类健
康和环境的负面影响。
计算化学
利用计算机模拟和理论计算方法研 究化学反应过程和分子性质,为新 材料的发现和优化提供有力支持。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(1) 识别分子、原子和离子(包括原子团) [I] (2) 从组成上对物质进行分类,如:混合物和纯净物、单质和化合物、金属与非金属等 [II] (3) 根据物质组成和性质理解酸、碱、盐、氧化物的分类及其相互联系 [II]
化学用语
考查的重点: 化学用语书写
基 本 概 念
2008年:化学式2个;电子式1个;化学方程式3个;离子方程式 (1) 熟记元素并正确书写常见元素的名称与符号,离子符号 [I] 4个;有机方程式1个;结构简式 2个 (2) 根据元素的化合价正确书写化学式 (分子式)或根据化学式判断化合价 [II] 2009 年:化学式 1 个;电子式 1 个;化学方程式 5 个;离子方程式 (3) 能用原子结构示意图、电子式、结构式和结构简式表示物质的组成和结构 [I] 化学计量
盐类
水解平衡 难溶物 溶解平衡
(8)理解盐类水解的原理,掌握影响盐类水解程 度的主要因素和盐类水解应用 [II] (9)在理解离子反应的本质基础上,能从离子角 度分析电解质在水溶液中的反应 [II] (10)了解难溶电解质的溶解平衡及沉淀的转化 的本质 [I]
3个;热化学方程式1个;有机方程式2个;结构简式2个 2010年:化学式3个;电子式1个;化学方程式3个;离子方程式 (4) 利用相对原子质量、相对分子质量进行有关计算 [II] 3 个;热化学方程式 1 个;有机方程式 3 个;结构简式 2 个 (5) 理解质量守恒定律的含义 [II]
(6) 理解物质的量及其单位的含义,能根据物质的量与摩尔质量、气体摩尔体积、物质的 量浓度、阿伏加德罗常数、微粒数目之间的相互关系进行计算 [II] (7) 能用化学方程式、离子方程式表示物质的变化并进行相关计算 [II]
(1)了解元素、核素和同位素的含义 [I] (2)依据原子的结构了解原子序数、核电荷数、 质子数、核外电子数的彼此关系和质子数、中子 数、质量数之间的相互关系 [I] (3)了解原子核外电子排布 [I]
(4)了解元素周期表的结构 [I] (5)通过同一短周期或同一主族元素性质的递变 规律与原子结构的关系,理解元素周期律的实质 [II] [II] (6)通过金属、非金属在元素周期表中的位置及 其性质递变的规律,理解元素的原子结构、元素 在周期表中的位置和元素性质三者之间的相互 关系 [II] (7)通过离子键、共价键(极性键和非极性键)的 形成过程认识化学键 [I]
电 化 学
(7)理解原电池和电解池的工作原理并正确书写电极反应和总反应 方程式 [II] (8)了解原电池和电解池在实际中的应用 [I] (9)能解释金属发生电化学腐蚀的原因 [II] (10)了解金属腐蚀的危害和金属的防护措施 [I]
反应 速率
1) 了解化学反应速率的概念和表示方法 [I] 2) 结合具体实例,理解外界条件对反应速率的影响 [II]
化学 反应 速率 和 化学 平衡
化学 平衡
3)了解化学反应的可逆性和化学平衡建立的过程 [I] 4) 理解化学平衡和化学平衡常数的含义,并进行简单计 算 [II] 5) 结合具体实例,理解外界条件对化学平衡的影响 [II] 6) 认识化学反应速率和化学平衡的调控在社会、生产和 科学研究领域中的重要作用 [I] 7) 通过催化剂实际应用的实例,了解催化剂在社会、生 产和科学研究领域中的重要作用 [I]
化学 反应 与能 量
(1)根据化学反应的特点理解不同类型的化学反应 [II] (2)在分析元素化合价变化的基础上,理解氧化还原反应的本质 [II] (3)根据氧化还原反应的规律研究物质的化学性质以及常见氧化剂 和还原剂之间的反应 [II] (4)通过化学键的断裂和形成,能说明化学反应中能量变化的原因 [I] (5)通过化学能与热能、化学能与电能的相互转化,认识常见的能 量转换形式及其重要性 [I] (6)能正确书写热化学方程式并根据盖斯定律进行有关计算 [II]
弱电解质 电离平衡
(1)了解电解质的概念 [I] (2)根据根据电解质在水溶液中的电离与电解质 溶液的导电性,理解强电解质和弱电解质的概 念,并能正确书写电离方程式 [II] (3)理解弱电解质在水溶液中的电离平衡 [II]
电解质 溶液
(4)了解水的电离及离子积常数 [I] (5)认识溶液的酸碱性、溶液中c(H+)、c(OH-)、 水的电离 PH三者之间的关系,并能进行简单计算 [I] [I] 溶液酸碱性 (6)了解酸碱中和滴定的原理 (7)了解溶液PH的调控在社会、生产和科学研 究中的重要作用 [I]
溶液和胶体
(1) 了解溶液、溶解度、溶质的质量分数的概念 (2) 利用溶解度表或溶解度曲线,获取相关物质溶解性等信息 (3) 理解溶液的组成并能用溶液中溶质的质量分数、物质的量浓度 进行相关计算 (4) 了解溶液与胶体的区别
和元 素周 期律
元素 周期律
