实验四 配合物的生成和性质(免费)
配合物的生成和性质实验报告大一

配合物的⽣成和性质实验报告⼤⼀配合物的⽣成和性质实验报告⼤⼀⼀、实验⽬的:1、了解有关配合物的⽣成与性质。
2、熟悉不稳定常数和稳定常数的意义。
3、了解利⽤配合物的掩蔽效应鉴别离⼦的⽅法。
⼆、实验原理:中⼼原⼦或离⼦与⼀定数⽬的中性分⼦或阴离⼦以配位键结合形成配位个体。
配位个体处于配合物的内界。
若带有电荷就称为配离⼦,带正电荷称为配阳离⼦,带负电荷称为配阴离⼦。
配离⼦与带有相同数⽬的相反电荷的离⼦(外界)组成配位化合物,简称配合物。
简单⾦属离⼦在形成配离⼦后,其颜⾊,酸碱性,溶解性及氧化还原性等往往和原物质有很⼤的差别。
配离⼦之间也可转化,⼀种配离⼦转化为另⼀种稳定的配离⼦。
具有环状结构的配合物称为螯合物,螯合物的稳定性更⼤,且具有特征颜⾊。
利⽤此类鳌合物的形成作为某些⾦属离⼦的特征反应⽽定性、定量地检验⾦属离⼦的存在。
仪器与试剂:H2SO4 (2mol.L-1)三、实验内容:1.配合物的⽣成(1) CuSO4 溶液中滴加NH3 H2O,先产⽣蓝⾊沉淀,继续滴加,蓝⾊沉淀溶解得⼀深蓝⾊溶液:Cu2+ + SO42- + 2NH3 =2NH4++Cu2(OH)2SO4↓Cu2(OH)2SO4 + 8NH3 = 2[Cu(NH3)4]2++ SO42-+2OH- 深蓝⾊溶液[Cu(NH3)4]2+分为四份:A:加碱:产⽣蓝⾊沉淀[Cu(NH3)4]2+ +2OH- = 4NH3 + Cu(OH)2↓再加酸:蓝⾊沉淀溶解Cu(OH)2+4H+ = Cu2+ +4H2OB:滴加BaCl2:产⽣⽩⾊沉淀[Cu(NH3)4]SO4+BaCl2 = BaSO4↓+[Cu(NH3)4]Cl2C: [Cu(NH3)4]SO4中加⼊1mL ⼄醇, 溶液呈浑浊。
D: [Cu(NH3)4]SO4备⽤在FeCl3中滴加NH4F:产⽣⽆⾊溶液Fe3+ + 6F- = [FeF6]3-[FeF6]3- + I- = 不反应(3) 在K3[Fe(CN)6]中滴加KSCN:⽆现象K3[Fe(CN)6] + SCN-⽆变化在NH2Fe(SO4)2,FeCl3中分别滴加KSCN:溶液呈⾎红⾊Fe3+ + n SCN- = [Fe(NCS)n]3-n2.配位平衡的移动(1) 配离⼦之间的转化FeCl3中加⽔稀释:溶液呈⽆⾊Fe3+ + 6H2O = Fe(H2O)63+再滴加KSCN:溶液呈⾎红⾊Fe(H2O)63+ + n SCN- = [Fe(NCS)n]3-n + 6H2O再滴加NH4F:⾎红⾊褪去,溶液呈⽆⾊[Fe(NCS)n]3-n+ 6F-= [FeF6]3- +n SCN-再滴加饱和(NH4)2(C2O4)2溶液出现浅黄⾊[FeF6]3-+ 3(C2O4)22- = [Fe(C2O4)3]3-+6F-(注意:实际中由于饱和(NH4)2(C2O4)2的浓度可能过⼩,常观察不到溶液的浅黄⾊,可使⽤固体(NH4)2(C2O4)2)稳定性:[Fe(C2O4)3]3->[FeF6]3- > [Fe(NCS)n]3-n(2)配位平衡与氧化还原反应① A试管:FeCl3中加少许NH4F(s),溶液的黄⾊褪去,溶液呈⽆⾊,再滴加⼊KI,充分震荡后,加⼊CCl4,CCl4层呈⽆⾊Fe3+ 6F-= [FeF6]3- [FeF6]3-+ I- = 不反应B 试管:FeCl3中滴加⼊KI,充分震荡后,加⼊CCl4,CCl4层呈紫红⾊2Fe3+ 2I- = 2Fe2+-+ I2A试管:HCl中加⼊⼩块Cu⽚:⽆现象Cu + HCl = 不反应B 试管:HCl中加⼊硫脲(s),再加⼊⼩块Cu⽚:产⽣⽓体2Cu + 2HCl + 8CS(NH2)2 = 2{Cu[CS(NH2)2]4}Cl + H2(3)配离⼦稳定性的⽐较① AgNO3中滴加Na2CO3,产⽣棕⾊沉淀2 Ag+ + CO32- →Ag2O ↓(棕) + CO2② a中沉淀离⼼后,加⼊NH3?H2O,沉淀溶解,得⼀⽆⾊溶液Ag2O + 4NH3?H2O → 2[Ag(NH3)2]+ + 2OH- + 3H2O③ b中再滴加NaCl,产⽣⽩⾊沉淀[Ag(NH3)2]+ + Cl- = AgCl ↓(⽩) + 2NH3④ c 中⽩⾊沉淀离⼼后,加⼊NH3?H2O ,沉淀溶解,得⼀⽆⾊溶液AgCl + NH3?H2O → [Ag (NH3)2]+ + Cl-⑤ d 中再滴加KBr ,产⽣淡黄⾊沉淀[Ag(NH3)2]+ + Br- →AgBr↓(淡黄⾊)⑥ e 中淡黄⾊沉淀离⼼后,加⼊Na2S2O3溶液,沉淀溶解,得⼀⽆⾊溶液AgBr +2 S2O32- →[Ag(S 2O3)2]3- + Br-⑦ f 中再滴加KI ,产⽣黄⾊沉淀[Ag(S2O3)2]3- + I- → AgI↓+ 2 S2O32-⑧ g 中黄⾊沉淀离⼼后,加⼊KCN 溶液,沉淀溶解,得⼀⽆⾊溶液AgI +2 CN- →[Ag(CN)2]- + I- (注意KCN 溶液的毒性)⑨ h 中再滴加Na2S ,产⽣⿊⾊沉淀2[Ag(CN)2]- + S2- → Ag 2S ↓+ 4CN-所以: KSP θ: AgCl >AgBr >AgIKf θ:[Ag(CN)2]- > [Ag(S2O3)2]3- > [Ag(NH3)2]+(4) 配位平衡与酸碱度① H3BO3为⼀元弱酸: pH 约为:4~5H3BO3 + H2O = B(OH)4- + OH-H3BO3与多元醇作⽤后,酸性增强:pH :约为3CH 2CH OH CH 2OH OH H 3BO 3+H +H 2O2+OH CH CH 2O CH 2O B O -+酸性增强3. 配合物的某些应⽤(1)鉴定某些离⼦NiSO4中滴加NH3?H2O ,得⼀蓝⾊溶液,再滴加⼆⼄酰⼆肟,析出鲜红⾊沉淀Ni2+CH3CC NOHCH3NOH+CH3CC NOCH3NOH2Ni+2H+(2) 配合物的掩蔽效应Co2++4SCN- → [Co(NCS)4]2- (溶于有机溶剂戊醇,显蓝绿⾊) Fe3+会产⽣⼲扰:Fe3+ + n SCN- = [Fe(NCS)n]3-n(⾎红⾊)Fe3+ 掩蔽⽅法:Fe3+ +6F- → [FeF6]3-四、实验步骤:1.配合物的⽣成(1)在⼀试管中加1mL 1mol/L CuSO4溶液,滴加2mol/L NH3 H2O ⾄产⽣沉淀后,继续滴加⾄溶液变为蓝⾊为⽌。
实验十一-配合物的生成、性质与应用

实验十一-配合物的生成、性质与应用一、实验目的1.了解配合物的形成原理及其相关理论知识;2.掌握配合物的生成、性质和应用;3.学会使用一些化学实验技术,如分离、纯化、结晶等。
二、实验原理1. 配合物的定义配合物是由阳离子、阴离子或分子中心离子(配体)和周围的一个或多个配位体(也称配体)组成的化学物质。
配位体是一种能够向中心离子提供一个或多个共价键(配位键)的化合物或离子。
一般情况下,配位体都是较小的分子,如水分子、氨分子和氯离子等。
2. 配合物的形成原理配合物的形成受到多种因素的影响,主要有以下三方面:1.配位体的性质:配位体通常具有一个或多个孤对电子,可以与中心离子形成配位键。
2.中心离子的性质:中心离子通常具有空的d轨道或f轨道,可以接受来自配位体的电子形成配位键。
3.形成的稳定性:配合物的稳定性取决于配位键的强度、离子的电荷、配位体空间位阻等因素。
3. 配合物的性质配合物具有以下一些特征:1.配合物中心离子的化学性质发生变化。
2.配位体对中心离子的性质有重要影响。
3.配合物常呈现出较强的带电性。
4.配合物的化学性质受配位键性质、离子作用力等因素的影响。
4. 配合物的应用配合物具有广泛的应用,包括:1.工业上用于制造农药、颜料、化学催化剂等。
2.医学上用于治疗疾病,如铁离子配合物用于治疗缺铁性贫血等。
3.生物学上用于研究生物大分子结构和作用机制。
三、实验步骤1. 实验材料和仪器FeCl3·6H2O、KSCN、NaClO、稀盐酸、热水、恒温加热器、移液管、pH试纸、试管等。
2. 实验步骤1.制备混合物:将溶液A(5mL FeCl3·6H2O和4mL稀盐酸)和溶液B(5mL NaClO和4mL稀盐酸)混合,注意不要相互混合,避免产生气体。
2.稀释混合物:将混合溶液加入10mL的水中,形成红褐色混合物。
3.测量pH值:用pH试纸测量溶液的pH值,记录下来。
4.添加配体:加入2滴KSCN溶液,并轻轻摇动管子。
配合物的性质
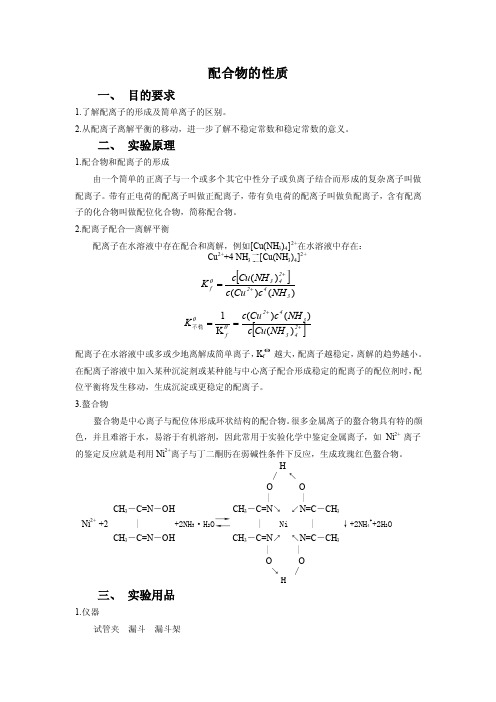
配合物的性质一、 目的要求1.了解配离子的形成及简单离子的区别。
2.从配离子离解平衡的移动,进一步了解不稳定常数和稳定常数的意义。
二、 实验原理1.配合物和配离子的形成由一个简单的正离子与一个或多个其它中性分子或负离子结合而形成的复杂离子叫做配离子。
带有正电荷的配离子叫做正配离子,带有负电荷的配离子叫做负配离子,含有配离子的化合物叫做配位化合物,简称配合物。
2.配离子配合—离解平衡配离子在水溶液中存在配合和离解,例如[Cu(NH 3)4]2+在水溶液中存在:Cu 2++4 NH 3→←[Cu(NH 3)4]2+ [])()()(342243f NH c Cu c NH Cu c K ++=θ []++==243342f NH Cu c NH c Cu c K )()()(K 1θθ不稳 配离子在水溶液中或多或少地离解成简单离子,K f θ越大,配离子越稳定,离解的趋势越小。
在配离子溶液中加入某种沉淀剂或某种能与中心离子配合形成稳定的配离子的配位剂时,配位平衡将发生移动,生成沉淀或更稳定的配离子。
3.螯合物螯合物是中心离子与配位体形成环状结构的配合物。
很多金属离子的螯合物具有特的颜色,并且难溶于水,易溶于有机溶剂,因此常用于实验化学中鉴定金属离子,如Ni 2+ 离子的鉴定反应就是利用Ni 2+离子与丁二酮肟在弱碱性条件下反应,生成玫瑰红色螯合物。
H↚ ↖O O| |CH 3-C=N -OH CH 3-C=N ↘ ↙N=C -CH 3Ni 2+ +2 | +2NH 3·H 2O →← | Ni | ↓+2NH 4++2H 2O CH 3-C=N -OH CH 3-C=N ↗ ↖N=C -CH 3| |O O↘ ↚H 三、 实验用品1.仪器试管夹 漏斗 漏斗架2.药品H2SO4 1mol·L-1,NH3·H2O 2mol·L-1、6mol·L-1,NaOH 0.1mol·L-1、2mol·L-1 ,AgNO3 0.1 mol·L-1,CuSO4 0.1 mol·L-1,HgCl2 0.1mol·L-1,KI 0.1 mol·L-1,K3[Fe(CN)6] 0.1 mol·L-1,KSCN 0.1 mol·L-1,NaF 0.1 mol·L-1,NH4F 4mol·L-1,NaCl 0.1 mol·L-1,FeCl3 0.1 mol·L-1,Na2S2O3 1 mol·L-1、饱和溶液,Ni(NO3) 2 0.1 mol·L-1,Na2S 0.1 mol·L-1,EDTA 0.1 mol·L-1,Na2CO3 0.1 mol·L-1,KBr 0.1 mol·L-1,C2H5OH 95%,CCl4,丁二酮肟试液。
实验六、配合物的生成、性质与应用

实验六、配合物的生成、性质与应用一、实验目的1、了解几种不同类型的配合物的生成,比较配合物与简单化合物和复盐的区别。
2、了解影响配合平衡移动的因素。
3、了解螯和物的形成条件。
4、熟悉过滤和试管的使用等基本操作.二、实验原理由中心离子(或原子)和一定数目的中性分子或阴离子通过形成配位共价键相结合而成的复杂结构单元称配合单元,凡是由配合单元组成的化合物称配位化合物。
在配合物中,中心离子已体现不出其游离存在时的性质。
而在简单化合物或复盐的溶液中,各种离子都能体现出游离离子的性质。
由此,可以区分出有否配合物存在.配合物在水溶液中存在有配合平衡:M n+ + aL—→ Ml a n—a配合物的稳定性可用平衡常数KΘ稳来衡量。
根据化学平衡的知识可知,增加配体或金属离子浓度有利于配合物的形成,而降低配体或金属离子浓度有利于配合物的解离。
因此,弱酸或弱碱作为配体时,溶液酸碱性的改变会导致配合物的解离。
若有沉淀剂能与中心离子形成沉淀反应,则会减少中心离子的浓度,使配合平衡朝解离的方向移动,最终导致配合物的解离。
若另加入一种配体,能与中心离子形成稳定性较好的配合物,则又可能使沉淀溶解。
总之,配合平衡与沉淀平衡的关系是朝着生成更难解离或更难溶解的物质的方向移动。
中心离子与配体结合形成配合物后,由于中心离子的浓度发生了改变,因此电极电势数值也改变,从而改变了中心离子的氧化还原能力。
中心离子与多基配体反应可生成具有环状结构的稳定性很好的螯和物。
很多金属螯和物具有特征颜色,且难溶于水而易溶于有机溶剂。
有些特征反应长用来作为金属例子的鉴定反应。
三、仪器和药品仪器:试管,试管架,离心试管,漏斗,漏斗架,白瓷点滴板,离心机,滤纸药品: 2 mol·L-1H2SO4;2mol·L-1NH3·H2O,6mol·L-1NH3·H2O ,0。
1 mol·L-1NaOH,2mol·L-1NaOH.0.1mol·L—1 CuSO4,0.1mol·L-1HgCl2, 0.1mol·L-1KI,0.1mol·L—1BaCl2,0。
配合物的生成和性质实验报告

配合物的生成和性质实验报告配合物的生成和性质实验报告引言:配合物是由中心金属离子与配体之间形成的化合物。
通过配位键的形成,配合物具有独特的结构和性质。
本实验旨在通过合成不同配合物,探究其生成机制和性质。
实验一:合成铁氰化物配合物材料与方法:1. 氰化钠(NaCN)溶液2. 氯化铁(III)溶液3. 乙醇溶液4. 氢氧化钠(NaOH)溶液5. 过滤纸6. 玻璃棒步骤:1. 取一定量的氰化钠溶液,加入氯化铁(III)溶液中。
2. 搅拌溶液,观察颜色变化。
3. 加入乙醇溶液,继续搅拌。
4. 加入氢氧化钠溶液,观察颜色变化。
5. 过滤得到沉淀。
结果与讨论:实验过程中,我们观察到溶液由无色逐渐变为深蓝色,并最终生成了蓝色的沉淀。
这表明我们成功合成了铁氰化物配合物。
实验二:配合物的溶解性实验材料与方法:1. 合成的铁氰化物配合物2. 氯化铵(NH4Cl)溶液3. 硝酸银(AgNO3)溶液4. 玻璃棒步骤:1. 取一定量的铁氰化物配合物溶液。
2. 分别加入氯化铵溶液和硝酸银溶液。
3. 观察颜色变化和沉淀的生成情况。
结果与讨论:我们发现,加入氯化铵溶液后,配合物的颜色变浅,说明配合物发生了溶解。
而加入硝酸银溶液后,观察到白色沉淀的生成。
这表明铁氰化物配合物可以与氯化铵发生配位置换反应,但无法与硝酸银发生反应。
实验三:配合物的热稳定性实验材料与方法:1. 合成的铁氰化物配合物2. 火焰步骤:1. 将铁氰化物配合物放置在火焰上方。
2. 观察颜色变化和物质的行为。
结果与讨论:我们观察到,铁氰化物配合物在火焰下发生分解,产生橙色火焰。
这表明配合物在高温下不稳定,容易分解。
结论:通过本实验,我们成功合成了铁氰化物配合物,并探究了其性质。
我们发现铁氰化物配合物具有一定的溶解性和热稳定性。
这些实验结果对于进一步研究配合物的生成机制和性质具有重要的参考价值。
附录:实验中所用的化学品均需在实验室中按照安全操作规程进行操作。
配合物的性质的实验报告doc

配合物的性质的实验报告篇一:实验六配位化合物的生成及其性质山东大学西校区实验报告姓名危诚年级班级公共卫生1班实验六配位化合物的生成及其性质实验目的:了解配离子与简单离子的区别;比较配离子的相对稳定性,掌握配位平衡与沉淀、氧化还原反应和溶液酸度的关系;了解螯合物的形成。
实验原理:平衡原理;螯合物反应等。
实验器材:试管,离心试管,试管架,试管刷等。
实验药品:,实验过程:(一)配合物的生成和配合物的组成(1)取一支试管,加入1ml 0.1mol/L的变为深蓝色。
溶液,滴加2mol/L的溶液,溶液等配位化合物的反应;配位离子的稳定标准常数,。
取出1ml溶液于一支试管中,加入1ml无水乙醇,发现产生蓝色沉淀。
说明铜铵配合物在乙醇中溶解度较小。
(2)取一支试管,加4滴0.1mol/L的溶液,滴加0.1mol/L的溶液,观察到有红色沉淀生成。
再滴加过量的溶液,红色沉淀溶解。
;(3)取两支试管A、B,各加1ml 0.2mol/L的的溶液,在B试管中滴加0.1mol/L的;另取一支试管,加2ml的0.2mol/L的溶液,滴加6mol/L的溶液,在A试管中滴加0.1mol/L溶液。
A、B试管中都产生白色沉淀。
溶液,边加边震荡,待生成的沉淀完全溶解后,把溶液分在在两支试管C、D中。
在C试管中滴加0.1mol/L的溶液,在D试管中滴加0.1mol/L的溶液,C试管有白色沉淀生成,D管无明显现象。
;D管中镍离子以生反应。
(4)取一支试管,加10滴0.1mol/L的液变成血红色。
另取一支试管,10滴0.1mol/L的明显现象。
说明(二)配合物的稳定性的比较(1)取两支试管AB,各加4滴0.1mol/L的观察到有浅黄色的溶液和2滴0.1mol/L的,滴加0.1mol/L的L的发溶液,溶溶液,无溶液,溶沉淀生成。
在A试管中滴加0.1mol/L的液,边滴加边震荡,直至沉淀刚好溶解;在B试管中滴加相同体积的0.1mol/L的溶液,观察到沉淀溶解。
4.配合物的生成和性质

1
实验四 配合物的生成和性质
一、 实验目的
1. 加深理解配合物的组成和稳定性,了解配合物形成时的特性。
2. 初步学习利用配位溶解的方法分离常见混合阳离子。
3. 学习电动离心机的使用和固-液分离操作。
二、 实验原理
配位化合物与配位平衡
配位化合物的内、外层之间是靠离子键结合的,在水中是完全解离。
而配位个体在水中是部分的、分步的解离,因此就存在解离平衡。
配合物的标准平衡常数θ
f K ,也被称为稳定平衡常数。
θf K 越大,表明配合物越稳定。
形成配合物时,常伴有溶液颜色、酸碱性、难溶电解质溶解度、中心离子氧化还原性的改变等特征。
利用配位溶解可以分离溶液中的某些离子。
三、实验内容
2
3
4
四、注意事项
1.使用离心机时要注意安全。
2.及时记录实验过程中配合物的特征颜色。
3.节约药品,废液倒入废液缸。
5。
实验三-配合物的生成、性质与应用

实验三-配合物的生成、性质与应用一、实验目的•了解配位化学的基本概念。
•掌握化学配位反应的基本原理和方法。
•观察并比较各种类型的配合物结构和性质。
•熟悉配合物的应用。
二、实验原理1. 配位化学配位化学是指由 Lewis 酸-碱相互作用形成的含有金属离子的化合物体系。
金属离子通过配位原子与配体结合,形成配合物。
在配位化学中,金属离子的性质主要取决于其电荷、电子配对数、配位伸展度等。
2. 配合物的生成配合物的生成通常通过溶液反应来实现。
通常将金属离子在水溶液中与带有反应性基团的有机分子(即配体)进行反应,形成稳定的配合物。
反应机理与物理化学性质有关,因此反应条件及中间产物的性质对于配合物的合成至关重要。
3. 配合物的性质配合物的主要性质包括结构、热力学稳定性、光谱特征、反应机理、磁性等。
其中,X射线晶体结构分析和 NMR 谱等是常见的配合物结构解析技术,热分析和热重分析法则可以评估配合物的热稳定性,磁性法则可以表征配合物的电子结构和顺磁性等。
4. 配合物的应用配合物作为功能性材料受到广泛的应用。
主要包括:光电材料、磁性材料、医药化学、金属有机化学等领域。
光电薄膜、催化剂、液晶显示材料等均是含有配合物的新材料。
三、实验步骤实验器材和试剂•乙酸铝•异辛醇•离心机•烘箱•无水乙醇实验步骤1.称取适量乙酸铝与异辛醇,加入瓶中,振荡混合后置于烘箱中加热,待产物完全形成后取出。
2.将产物加少量无水乙醇,振荡混合后放于离心机内离心分离。
3.将上层液体去除,将沉淀加无水乙醇洗涤,最后在烘箱中加热干燥,得到样品。
4.将样品进行 X 射线衍射分析,测定其晶体结构。
5.用红外光谱测试样品的化学键结构。
四、结果与分析在实验过程中,我们成功合成了一种配合物并进行了晶体结构和化学键结构的分析。
通过 X 射线晶体结构分析,我们发现配合物为五配位的正四面体结构,其中铝离子与四个氧原子配合,异辛醇弯曲成 L 型区域配位于铝离子周围。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验四配合物的生成和性质
1. 简单离子与配离子的区别
铁氰化钾K3[Fe(CN)6]加SCN-无血红色
Fe3+ + nSCN- = [Fe(NCS)n]3-n有血红色
结论:FeCl3为离子型简单化合物,在水中可解离出大量的Fe3+,K3[Fe(CN)6]为配合物,配离子[Fe(CN)6]3-比较稳定,难以解离出大量的Fe3+。
2. 配离子稳定性的比较
(1) Fe3+ + n SCN- = [Fe(NCS)n]3-n(有血红色)
[Fe(NCS)n]3-n+(C2O4)22-→ [Fe(C2O4)3]3-+SCN-
稳定性[Fe(C2O4)3]3->[Fe(NCS)n]3-n
(2)AgNO3+ NaCl →AgCl ↓(白) + NH3 H2O→ [Ag(NH3)2]+
[Ag(NH3)2]++ KBr →AgBr↓(淡黄色),
再滴加Na2S2O3溶液→ 沉淀溶解[Ag(S2O3)2]3-,滴加KI溶液→AgI↓
AgBr + 2S2O32-→[Ag(S2O3)2]3- + Br-; [Ag(S2O3)2]3- + I-→ AgI↓+ 2S2O32-
比较:K SPӨ: AgCl >AgBr >AgI; 稳定性: [Ag(S2O3)2]3-> [Ag(NH3)2]+
(3) I2 + [Fe(CN)6]4- = I- + [Fe(CN)6]3-
EӨ (Fe3+/Fe2+) > EӨ (I2/I-) > EӨ ([Fe(CN)6]3-/[Fe(CN)6]4-)
稳定性[Fe(CN)6]3- >[Fe(CN)6]4-
3. 配位离解平衡的移动
2CuSO4 + 2NH3·H2O → Cu2(OH)2SO4↓+(NH4)2SO4
Cu2(OH)2SO4↓+8NH3·H2O→ [Cu(NH3)4]SO4 + [Cu(NH3)4](OH)2 + 4H2O
(1) 利用酸碱反应破坏[Cu(NH3)4]2+
SO42- + 2[Cu(NH3)4]2+ + 6H+ + 2H2O = Cu2(OH)2SO4↓ + 8NH4+
(2) 利用沉淀反应破坏[Cu(NH 3)4]2+
[Cu(NH 3)4]2+ + S 2- → CuS ↓ + 4NH 3
(3) 利用氧化还原反应破坏[Cu(NH 3)4]2+
[Cu(NH 3)4]2+ + Zn = [Zn(NH 3)4]2+ + Cu
(4) 利用生成更稳定配合物(螯合物)的方法破坏[Cu(NH 3)4]2+
[Cu(NH 3)4]2+ + edta 4- → [Cu(edta)]2- + 4NH 3
4. 配合物的某些应用
(1) 利用生成有色配合物定性鉴定某些离子
pH 控制为5-10:Ni 2+ + NH 3 H 20 +二乙酰二肟 → 鲜红色沉淀
Ni 2+CH 3C C NOH CH 3NOH +CH 3C C NO
CH 3NOH 2Ni +2H +
(2) 利用生成配合物掩蔽干扰离子
Co 2+ + 4SCN - → [Co(NCS)4]2- (溶于有机溶剂戊醇显蓝绿色) 而Fe 3+ + n SCN - = [Fe(NCS)n]3-n (血红色) 会产生干扰 Fe 3+掩蔽方法:Fe 3+ + 6F - → [FeF 6]3- (无色) (3) 硬水软化
N CH 2
CH 2N CH 2COOH CH 2COOH HOOCH 2C
HOOCH 2C
EDTA(简式H 4Y)
问题:为什么加入edta 二钠盐的溶液没有白色悬浮物产生? Ca 2+ + edta 4- = [Ca(edta)]2-
Mg 2+ + edta 4- = [Mg(edta)]2-。
