生产过程微生物监控记录.docx
微生物限度、控制菌检查记录

产品名称
批号
数量
供货单位
取样量
检验日期
温度
湿度
报告日期
检验依据
供试液制备
取供试品(g),加pH7.0无菌氯化钠蛋白胨缓冲液至ml,混匀,作为1:10的供试液;细菌检查:吸取本品1ml至5个平皿,每个平皿0.2ml;霉菌和酵母菌检查:吸取本品1ml至平皿
平皿号
细菌
培养基/批号
营养琼脂培养基/
供试品
阳性对照
阴性对照
结果
□检出□未检出(规定:)
备注
结论
本品按进行检验,结果。
检验人
复核人
2天
3天
3天
4天
4天
5天
5天
5
1天
1天
2天
2天
3天
3天
4天
4天
5天
5天
每组菌落总数
平均数
平均数
结果
(规定:)
结果
(规定:)
备注
结论
本品经按进行检验,结果。
检验人
复核人
控制菌检查记录
检验编号:
产品名称
批号
数量
供货单位
取样量
检验日期
温度
湿度
报告日期
检验依据
一、大肠埃希菌检查
供试品制备:取供试品(g/ml/cm2),加PH7.0无菌氯化钠蛋白胨缓冲液至ml,混匀,作为的供试液。
培养基信息:①营养肉汤培养基配制批号:②四硫磺酸钠亮绿培养基配制批号:
③胆盐硫乳琼脂培养基配制批号:④EMB配制批号:
培养温度:培养时间:培养箱编号:
营养肉汤预增菌(18~24h)
四硫磺酸钠亮绿增菌(18~24h)
生产过程微生物监控记录
填表说明:本表由质检部负责填写,按照企业生产过程微生物监测制度定期检验,填表汇总,存在为题的用红笔填写,并报告质
量负责人(质检部负责人)
ቤተ መጻሕፍቲ ባይዱ
编号:
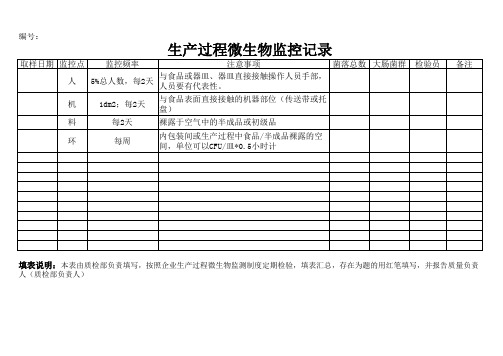
生产过程微生物监控记录
取样日期 监控点 人 机 料 环 监控频率 5%总人数,每2天 1dm2;每2天 每2天 每周 注意事项 与食品或器皿、器皿直接接触操作人员手 部,人员要有代表性。 与食品表面直接接触的机器部位(传送带或 托 盘) 裸露于空气中的半成品或初级品 内包装间或生产过程中食品/半成品裸露的 空 间,单位可以CFU/皿*0.5小时计 菌落总数 大肠菌群 检验员 备注
生产过程微生物监控记录

填表说明:本表由质检部负责填写,按照企业生产过程微生物监测制度定期检验,填表汇总,存在为题的用红笔填写,并报告质
量负责人(质检部负责人)
与食品表面直接接触的机器部位传送带或托盘裸露于空气中的半成品或初级品内包装间ห้องสมุดไป่ตู้生产过程中食品半成品裸露的空间单位可以cfu皿05小时计菌落总数大肠菌群检验员备注填表说明
编号:
生产过程微生物监控记录
取样日期 监控点 人 机 料 环 监控频率 5%总人数,每2天 1dm2;每2天 每2天 每周 注意事项 与食品或器皿、器皿直接接触操作人员手 部,人员要有代表性。 与食品表面直接接触的机器部位(传送带或 托 盘) 裸露于空气中的半成品或初级品 内包装间或生产过程中食品/半成品裸露的 空 间,单位可以CFU/皿*0.5小时计 菌落总数 大肠菌群 检验员 备注
微生物限度检查记录 版

表:微生物限度检查记录(通用)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)微生物限度检查记录(30~35℃,3~5天)20℃~25℃,5~7天)沙氏葡萄糖琼脂培养基(配制批号:)三、控制菌检查(30-35℃)表:胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)(30℃~35℃)胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)五、耐胆盐革兰阴性菌检查胰酪大豆胨液体培养基(配制批号:)、肠道菌增菌液体培养基(配制批号:),紫红胆盐葡萄糖琼脂培养基(配制批号:)表:(含药材原粉的片剂)胰酪大豆胨液体培养基(配制批号: )、麦康凯液体培养基(配制批号: )麦康凯琼脂培养基(配制批号: )(30℃~35℃)胰酪大豆胨液体培养基(配制批号: )、RV 沙门增菌液体培养基(配制批号: ),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号: )、三糖铁琼脂(配制批号: )五、耐胆盐革兰阴性菌检查胰酪大豆胨液体培养基(配制批号: )、肠道菌增菌液体培养基(配制批号: ),紫红胆盐葡萄糖琼脂培养基(配制批号: )表:微生物限度检查记录(蛇胆川贝液)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、RV沙门增菌液体培养基(配制批号:),木糖赖氨酸脱氧胆酸盐琼脂培养基(配制批号:)、三糖铁琼脂(配制批号:)表:微生物限度检查记录(30~35℃,3~5天)20℃~25℃,5~7天)沙氏葡萄糖琼脂培养基(配制批号:)胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)表:微生物限度检查记录(内包材)三、大肠埃希菌检查胰酪大豆胨液体培养基(配制批号:)、麦康凯液体培养基(配制批号:)麦康凯琼脂培养基(配制批号:)。
微生物限度检查记录
阳性对照
检验人
结果
复核人:复核日期:
二、大肠菌群检查(30~35℃)
培养基编号:RDF- MKK-
平皿号:
培养基类别
乳糖胆盐发酵
培养基
麦康凯琼脂
培养基
操作日期培养Leabharlann 编号供试液10-1
供试液
10-2
供试液
10-3
阴性对照
阳性对照
检验人
结果
复核人:复核日期:
24
1
2
48
1
2
72
1
2
96
120
结果
报告值
Cfu/
培养基编号:MGH-
检验人:复核人:
检验日期:复核日期:
控制菌检查记录
检品名称:批号:
检验依据:
一、大肠埃希菌检查(30~35℃)
培养基编号:DRZ- MUG-
DJZ-平皿号:
培养基类别
胆盐乳糖
培养基
MUG
培养基
靛基质
试液
备注
操作日期
培养基编号
供试品
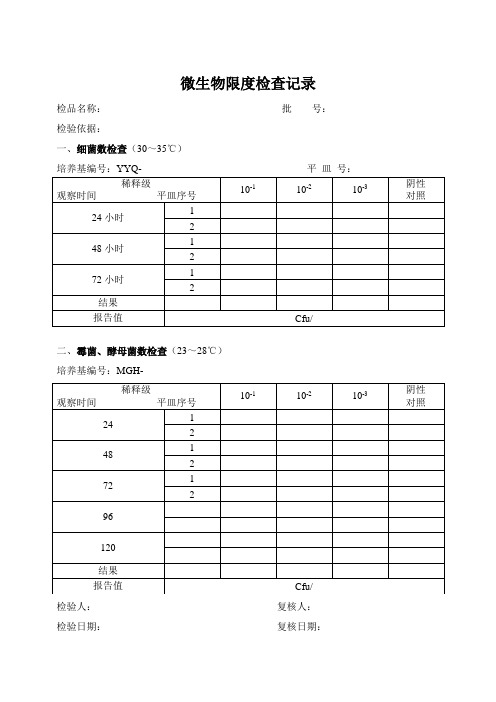
微生物限度检查记录
检品名称:批号:
检验依据:
一、细菌数检查(30~35℃)
培养基编号:YYQ-平皿号:
稀释级
观察时间平皿序号
10-1
10-2
10-3
阴性
对照
24小时
1
2
48小时
1
2
72小时
1
2
结果
报告值
Cfu/
二、霉菌、酵母菌数检查(23~28℃)
稀释级
观察时间平皿序号
10-1
10-2
10-3
阴性
对照
微生物检验原始记录

⑴菌落总数(平板计数琼脂36±1℃、48±2h)
序号
原液(1ml)
1:10稀释液(1ml)
1:100稀释液(1ml)
阴性对照
阳性对照
结果:CFU/mL
1
均值:
2
⑵霉菌、酵母菌计数(孟加拉虎红27±1℃5d)
序号
原液(1ml)
1:10稀释液(1ml)
1:100稀释液(1ml)
微生物检验原始记录
NO:
品名:包装规格:
批号:数量:
生产车间:检品数量:
检验人员:复核人员:
检验依据:检验目的:
检验日期:报告日期:
检验记录与结果:
1.取样:
(1)原液取样
(2)无菌称取样品25g或者25ml,置225ml灭菌的0.85%的生理盐水中,充分混匀,制成1:10稀释液。取1:10稀释液1ml置9ml灭菌的0.9%生理盐水中,制成1:100稀释液。
阴性对照
阳性对照
结果:CFU/mL
1
均值:
2
⑶大肠杆菌(月桂基磺酸盐胰蛋白胨【LST】肉汤,36±1℃、48±2h)
序号
原液(1ml)
1:10稀释液(1ml)
1:10稀释液(10ml)双料
1:100稀释液(1ml)
阴性对照
阳性对照
结果:MPN/mL
1
均值:
2
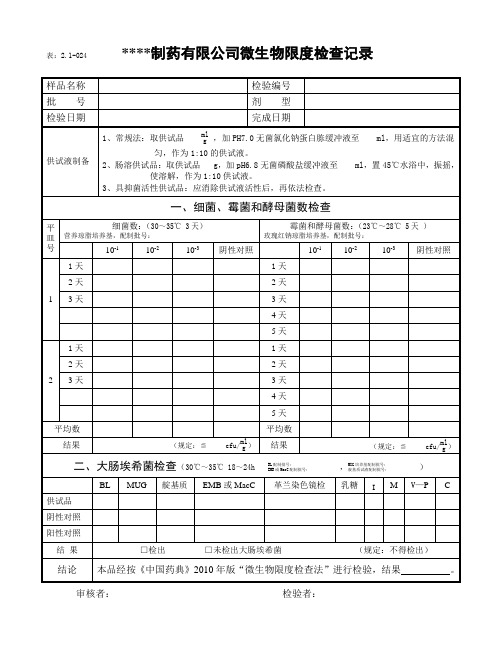
2010年版微生物限度检查记录
样品名称
检验编号
批号
剂型
检验日期
完成日期
供试液制备
1、常规法:取供试品,加PH7.0无菌氯化钠蛋白胨缓冲液至ml,用适宜的方法混
匀,作为1:10的供试液。
2、肠溶供试品:取供试品g,加pH6.8无菌磷酸盐缓冲液至ml,置45℃水浴中,振摇,使溶解,作为1:10供试液。
三糖铁琼脂斜面(18~24h)
供试品
阳Hale Waihona Puke 对照阴性对照结果□检出□未检出沙门菌(规定:不得检出)
结论
本品经按《中国药典》2010年版“微生物限度检查法”进行检验,结果。
审核者:检验者:
表:2.1-024****制药有限公司微生物限度检查记录(大山楂颗粒)
样品名称
检验编号
批号
剂型
检验日期
完成日期
供试液制备
3、具抑菌活性供试品:应消除供试液活性后,再依法检查。
一、细菌、霉菌和酵母菌数检查
平皿号
细菌数:(30~35℃3天)
营养琼脂培养基,配制批号:
霉菌和酵母菌数:(23℃~28℃5天)
玫瑰红钠琼脂培养基,配制批号:
10-1
10-2
10-3
阴性对照
10-1
10-2
10-3
阴性对照
1
1天
1天
2天
2天
3天
3天
4天
5天
2
1天
1天
2天
2天
3天
3天
4天
5天
平均数
平均数
结果
(规定:≦cfu/)
结果
(规定:≦cfu/)
生产过程微生物监控记录
填表说明:本表由质检部负责填写,按照企业生产过程微生物监测制度定期检验,填表汇总,存在为题的用红笔填写,并报告质量负责
人(质检部负责人)
编号:
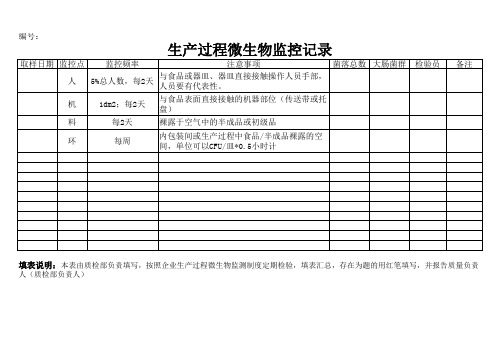
生产过程微生物监控记录
取样日期 监控点 监控频率
注意事项
菌落总数 大肠菌群 检验员
人
5%总人数,每2天
与食品或器皿、器皿直接接触操作人员手部, 人员要有代表性。
备注
机(传送带或托 盘)
料
每2天
裸露于空气中的半成品或初级品
环
每周
内包装间或生产过程中食品/半成品裸露的空 间,单位可以CFU/皿*0.5小时计
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
编号:
生产过程微生物监控记录
取样日期监控点监控频率注意事项菌落总数大肠菌群检验员备注
人5%总人数,每 2天与食品或器皿、器皿直接接触操作人员手部,人员要有代表性。
机1dm2;每 2天与食品表面直接接触的机器部位(传送带或托盘)
料每2天裸露于空气中的半成品或初级品
环每周内包装间或生产过程中食品 / 半成品裸露的空间,单位可以 CFU/皿*0.5 小时计
填表说明:本表由质检部负责填写,按照企业生产过程微生物监测制度定期检验,填表汇总,存在为题的用红笔填写,并报告质量负责人(质检部负责人)。
