结肠癌项目
结肠癌最新化疗方案

结肠癌最新化疗方案结肠癌是一种常见的消化系统恶性肿瘤,其发病率和死亡率在全球范围内均呈上升趋势。
针对结肠癌的治疗手段不断演进,化疗作为结肠癌综合治疗的重要组成部分,也在不断创新和改进。
本文将介绍结肠癌最新的化疗方案,以期提供参考和指导。
一、术前化疗术前化疗是指在结肠癌手术前进行的化疗治疗。
这种治疗方案的目的是通过减小肿瘤体积,缩小肿瘤边缘,达到手术切除的目的。
目前,广泛采用的术前化疗方案是FOLFOX方案,即同时使用氟尿嘧啶、奥沙利铂和亚叶酸钙。
该方案在多项临床试验中表现出较好的疗效和耐受性。
二、术后化疗术后化疗是指在结肠癌手术后进行的辅助化疗治疗。
其主要目的是杀灭和抑制术后微小残留癌细胞,预防癌细胞复发和转移。
常用的术后化疗方案包括CAPOX方案和FOLFOX方案。
前者是指使用氟尿嘧啶、奥沙利铂和卡培他滨进行化疗,后者与术前化疗方案相同。
三、个体化化疗个体化化疗是指根据患者结肠癌的分子特征和药物敏感性,进行个体化针对性的化疗方案。
目前,个体化化疗在结肠癌治疗中越来越受关注。
例如,一些针对KRAS突变阳性患者的药物已得到临床应用,如带铂类药物和EGFR抑制剂的联合应用。
此外,DNA修复缺陷患者也可选用PD-1/PD-L1免疫疗法。
四、靶向治疗靶向治疗是指通过作用于癌细胞特定的分子靶点,抑制肿瘤生长和扩散的治疗手段。
在结肠癌最新的化疗方案中,靶向治疗起到了重要作用。
EGFR抑制剂和血管生成抑制剂是常用的靶向治疗药物。
使用单抗结合化疗药物,可提高化疗的疗效。
五、免疫治疗免疫治疗是近年来结肠癌治疗领域的新进展。
通过激活患者自身免疫系统,增强抗肿瘤免疫应答,进而达到治疗结肠癌的效果。
PD-1/PD-L1免疫检查点抑制剂是目前最常用的免疫治疗药物。
临床试验表明,与传统化疗方案相比,免疫治疗在一些结肠癌患者中表现出更好的疗效和耐受性。
综上所述,结肠癌最新的化疗方案包括术前化疗、术后化疗、个体化化疗、靶向治疗和免疫治疗等多种手段。
结肠癌标准根治术
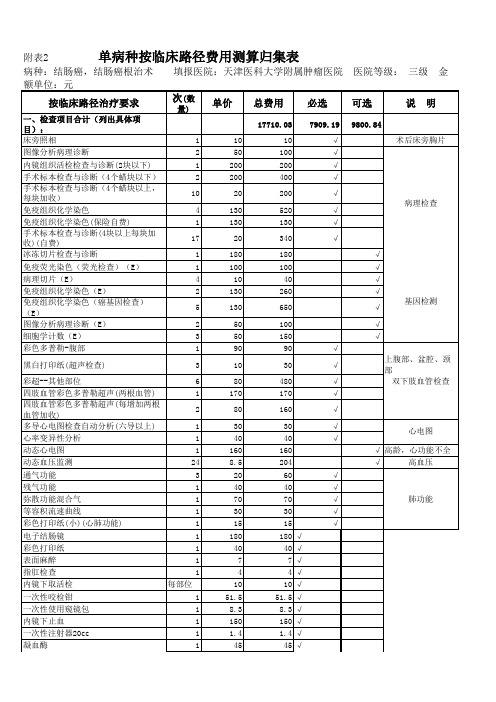
5 5.5 20 30 80 60 5 5 5 5 10 40 30 50 40 30 40 60 120 200 200 240 80 50 7 60 20 45 45 300 220 60 260 60 150 120 30 180 285 1063.5 1063.5
√ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √5 140 1 20 4.2 94.7 20.6 10 9.99 2 1.5 12.4 12.4 700 8.3 8 7 40 0.7 12.4 9.2 0.5 0.7 6 3 0.23 0.5 12.4 10 51.5 150 1.4 45 15 90 10 45 20 360 150 50 9 270 400 900 4586
100 260 150 30 50 20 20 20 20 140 25 10 25 25 2 13 20 80 40 13 12 10 15 10 10 10 25 10 15 80 20 5 4 20 50 10 10 25 40 20 26 23 23 23 4 23 23 50 45
100 260 150 30 50 20 20 20 20 280 75 30 25 25 2 39 60 240 120 39 36 30 45 30 30 30 75 30 45 240 60 15 12 60 150 30 30 75 120 60 78 69 69 69 12 69 69 50 45
√ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √ √
血凝常规
中国结直肠癌诊疗规范(2020年版)

中国结直肠癌诊疗规范(2020年版)中国结直肠癌诊疗规范(2020年版)导语:结直肠癌是世界范围内发病率和死亡率排名前列的恶性肿瘤之一。
随着人口老龄化的趋势和环境及生活方式的改变,结直肠癌在中国的发病率呈增长趋势。
为了规范结直肠癌的诊疗,提高患者的生存率和生活质量,中国肿瘤学会结直肠癌专业委员会制定了《中国结直肠癌诊疗规范(2020年版)》。
一、诊断1. 临床观察:对高危人群进行常规的体格检查和腹部触诊,了解患者病史、症状及体征,重点询问家族史和肠道疾病史。
2. 高危人群筛查:根据年龄、家族史、环境和生活方式等因素对高危人群进行筛查,如粪便DNA检测、结肠镜检查等。
3. 影像学检查:包括盆腔超声、腹部CT、胸部CT以及骨扫描等,以评估肿瘤的分期及转移情况。
4. 病理学检查:通过组织活检或手术标本病理学分级,确定肿瘤的类型、分化程度和淋巴结转移情况。
二、治疗1. 外科治疗:手术切除是结直肠癌的主要治疗方式,根据癌肿的位置和分期选择不同的手术方法,包括肠道吻合术、直肠切除术等。
对于早期癌或无法耐受手术的患者,还可以考虑内镜下黏膜切除术或介入治疗。
2. 化疗:手术后的化疗可减少复发和转移的风险,同时也可以通过新辅助化疗或姑息化疗来缓解症状和控制疾病进展。
3. 放疗:结直肠癌的放疗主要用于术前辅助治疗、术中放疗或姑息治疗,可以通过减少局部复发和控制疾病进展来提高患者生存率。
4. 靶向治疗:EGFR抗体、VEGF抗体等靶向药物的应用可以有效抑制肿瘤生长和进展,提高患者的生存率。
5. 免疫治疗:PD-1抗体、PD-L1抗体等免疫治疗药物的应用在结直肠癌治疗中也显示出一定的效果,可用于晚期或转移性结直肠癌患者。
三、术后辅助治疗1. 化疗:对于高危患者,术后化疗可以减少复发和转移的风险,主要通过氟尿嘧啶联合奥沙利铂等化疗药物。
2. 靶向治疗:EGFR抗体、VEGF抗体等可以用于KRAS野生型患者进行靶向治疗,提高患者的生存率。
结肠癌(乙状结肠癌根治术)临床路径

结肠癌(乙状结肠癌根治术)临床路径一、结肠癌(乙状结肠癌根治术)临床路径标准住院流程(一)适用对象。
1.第一诊断为结肠癌(ICD-10:C18)。
2.行乙状结肠癌根治术(ICD-9-CM-3:45.76008)。
(二)诊断依据。
根据《临床诊疗指南-外科学分册》(中华医学会编著,人民卫生出版社),《临床技术操作规范-外科学分册》(中华医学会编著,人民卫生出版社),《NCCN结肠癌临床实践指南》(中国版,2009年第一版)。
1.腹胀、腹痛、大便习惯改变、便血、贫血等临床表现,体格检查发现腹部肿物。
2.大便隐血试验多呈持续阳性。
3.影像学检查提示并了解有无器官和淋巴结转移。
4.纤维结肠镜检查明确肿瘤情况,取活组织检查作出病理诊断。
5.术前应判断是早期结肠癌还是进展期结肠癌,并根据上述检查结果进行临床分期。
(三)治疗方案的选择。
根据《临床诊疗指南-外科学分册》(中华医学会编著,人民卫生出版社),《临床技术操作规范-外科学分册》(中华医学会编著,人民卫生出版社),《NCCN结肠癌临床实践指南》(中国版,2009年第一版)。
根治手术(乙状结肠癌根治术):进展期结肠癌,无远处转移,肿瘤条件允许或联合脏器切除可以根治的结肠癌患者。
(四)标准住院日为14-21天。
(五)进入路径标准。
1.第一诊断必须符合ICD-10:C18结肠癌疾病编码,拟行乙状结肠癌根治术。
2.术前评估肿瘤切除困难者可先行新辅助化疗后再次评估,符合手术条件者可以进入路径。
3.当患者同时具有其他疾病诊断,但在住院期间不需要特殊处理也不影响第一诊断的临床路径流程实施时,可以进入路径。
(六)术前准备(术前评估)3-5天。
1.所必须的检查项目:(1)血常规、尿常规、大便常规;(2)肝肾功能、电解质、血型、凝血功能、感染性疾病筛查(乙肝、丙肝、艾滋病、梅毒等);(3)胸片、B超、心电图、腹部CT;(4)门诊或入院后完成结肠镜检查;(5)病理学活组织检查与诊断;(6)肿瘤标记物检查。
结直肠癌基因检测项目

结直肠癌基因检测项目结直肠癌是一种常见的恶性肿瘤,也是致死率很高的一种癌症,常常被称为“富贵病”,在欧美国家已成为常规筛查项目。
随着基因检测技术的发展,结直肠癌基因检测日渐普及,成为预防和早期诊断的一种有效手段。
结直肠癌是一种多因素引起的疾病,其中遗传因素是非常重要的。
结直肠癌基因检测是通过分析人体中与结直肠癌相关的基因变异,来评估个体结直肠癌患病风险的一项检测。
目前,结直肠癌基因检测主要包含两个方面:一是检测结直肠癌易感基因,包括APC、MLH1、MSH2、MSH6、PMS2、STK11等。
这些基因的突变会导致某些重要蛋白质的功能失常,从而增加结直肠癌发生的风险。
二是检测结直肠癌遗传易感性的基因多态性,如GSTP1、XRCC3、CYP2C9、UGT1A1等。
结直肠癌基因检测的优点在于早期诊断和预防结直肠癌方面的作用。
随着年龄的增长,患结直肠癌的风险也逐渐增加,这是由于肠黏膜的正常细胞开始发生变异,变异的细胞不受控制增殖而形成肿瘤。
检测结直肠癌易感基因和遗传易感性的基因多态性,能够更早的发现患者的风险,同时提供个性化的预防和治疗方案,从而避免肠道癌前病变的进一步转化成癌症。
但是,结直肠癌基因检测也存在不足之处,如检测结果可能存在误判、假阴性或假阳性等情况,另外费用也较高,这限制了其在一些地区的普及。
总之,结直肠癌基因检测是一种非常重要的检测手段,可以帮助家庭医生、肿瘤科医生更早地发现结直肠癌患者,更好地治疗癌症,最终提高患者的生命质量。
但是,我们也应该注意到该项检测的局限性,以及需要在专业医生的指导下进行检测,以免出现不必要的麻烦和误判。
结肠癌(开腹)临床路径说明

C18.900结肠恶性肿瘤,行45.73005右半结肠根治性切除术/45.75006左半结肠根治性切除术/45.74003横结肠切除术/45.76008乙状结肠切除术临床路径一、C18.900结肠恶性肿瘤,行45.73005右半结肠根治性切除术/45.75006左半结肠根治性切除术/45.74003横结肠切除术/45.76008乙状结肠切除术临床路径标准住院流程(一)适用对象。
1.第一诊断为C18.900结肠恶性肿瘤,行45.73005右半结肠根治性切除术/45.75006左半结肠根治性切除术/45.74003横结肠切除术/45.76008乙状结肠切除术。
2.可RO切除的结肠癌(1期、∏期和部分H1期)。
(二)诊断依据。
根据卫生部《结直肠癌诊疗规范(2010年)》和NCCN《结肠癌临床实践指南中国版(2011年)》等。
1.症状:便血,脓血便,排便习惯改变,腹痛,贫血,腹部肿块等。
2.体格检查:(1)一般情况评价:体力状况评分、是否有贫血、全身浅表淋巴结肿大;(2)腹部检查:是否看到肠型及肠蠕动波、触及肿块、叩及鼓音、听到高调肠鸣音或金属音;(3)直肠指诊:是否有指套血染。
3.实验室检查:粪常规+粪潜血;血清肿瘤标记物。
4.辅助检查:术前肿瘤定性及TNM分期,指导选择正确的术式。
(1)结肠镜取活检,病理检查明确肿瘤组织类型(腺癌、粘液腺癌、印戒细胞癌)和分化程度(高、中、低);排除同时性结直肠多原发癌。
(2)胸部X线检查排除肿瘤肺转移。
全腹部CT,排除其他脏器转移。
5.鉴别诊断:与胃肠道间质瘤(G1ST)、炎性肠疾病、淋巴瘤、肠结核、阑尾炎、寄生虫感染、息肉等常见的结肠疾病,以及腹腔其他脏器疾病累及结肠等鉴别。
(三)治疗方案的选择。
根据卫生部《结直肠癌诊疗规范(2010年)》和NCCN《结肠癌临床实践指南(中国版,2011年)》等。
1.结肠癌根治切除手术。
2.抗菌药物使用按照《抗菌药物临床应用指导原则》(卫医发(2004)285号)执行。
结直肠癌及相关检测项目介绍

盲肠
乙状结肠
直 肠
小肠 大肠
3.1 结直肠组织结构
结直肠模式图
结直肠H&E图 低倍镜
3.2 结直肠癌H&E对比图
固 有 层
粘膜肌层
肌层
正常结直肠H&E图 400倍
结直肠癌H&E图 200倍
四、临床表现
早期常无特殊症状,随病情进展可出现: 1、排便习惯与粪便性状的改变:表现为排
便次数增加、腹泻、便秘、粪便中带血、 脓或粘液; 2、腹痛:多为持续性隐痛,肠梗阻时阵发性绞痛; 3、腹部肿块; 4、肠梗阻症状:为结肠癌的晚期症状,表现 为不完全肠梗阻,腹胀和便秘。腹部胀 痛或阵发性绞痛。左侧结肠癌有时以急 性完全性结肠梗阻为首先出现的症状; 5、全身症状:贫血、消瘦、乏力、低热等。
结直肠癌 及相关检测项目介绍
李耀斌
目录
一、流行病学 二、病因学 三、生理病理 四、临床表现
五、临床诊断 六、治疗 七、检测项目 八、遗传性肠道肿瘤
一、流行病学
1、全球范围内,结直肠癌的男、女性患者,在地区分布上基本一 致,女性发病率、死亡率普遍比男性低;
2、结、直肠癌的发病率在全球范围内一直呈上升趋势,实际上主 要是结肠癌发病增多,尤其在发展中国家,趋势更为明显;
缺失:TS表达↓,敏感性↑,毒性 风险↑
3RG/3RG: 3RG/3RC: 2R/3RG: TS表达↑,敏感性↓,预后较差 2R/2R,3RC/3RC,2R/3RC: TS表达↑,敏感性↓,毒性风险↑
活性↓,敏感性↑
7.2 铂类药物
铂类药物(顺铂、卡铂、奥沙利铂等) 是临床上最常用的化疗药物之一,广泛用 于结直肠癌、非小细胞肺癌等疾病的治疗。
FOLFIRI
诊断肠癌的金标准

诊断肠癌的金标准
目前,诊断肠癌的金标准是组织活检(Tissue Biopsy)并通过病理学检查来确定。
组织活检通常通过内窥镜检查或手术切除肿瘤组织获取,然后送至实验室进行病理学检查。
以下是一些常用的组织活检技术,用于诊断肠癌:
1. 结肠镜活检(Colonoscopy Biopsy):通过结肠镜在结肠或直肠内直接取样。
2. 钳活检(Forceps Biopsy):通过内窥镜引导,使用特殊钳子取样,常用于较小的肿瘤。
3. 切除活检(Excisional Biopsy):通过手术切除整个肿瘤或部分肿瘤,用于大型或深入组织的肿瘤。
4. 针吸活检(Fine Needle Aspiration Biopsy):使用细针抽取肿瘤细胞或液体,常用于肿瘤预测、监测和诊断。
通过对组织样本进行病理学检查,病理学专家会评估肿瘤细胞的形态、细胞特征、组织结构和异常变化等,以确认
是否存在肠癌。
除了组织活检,还可以结合其他检查方法来辅助肠癌的诊断,如:
1. 影像学检查(如CT扫描、MRI和超声检查):用于评估肿瘤的位置、大小、浸润深度和转移情况。
2. 血液检查:包括检测肿瘤标志物,如CEA(癌胚抗原)和CA19-9(糖链抗原19-9),用于辅助诊断和监测治疗反应。
诊断肠癌的完整评估通常需要结合临床病史、体格检查、影像学结果和病理学检查等多种信息。
如果您担心是否患有肠癌,请咨询专业的医生或肿瘤学专家,进行个体化的评估和建议。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
【摘要】Ⅱ期结肠癌辅助化疗的效果一直以来都存在争议。
目前尚无一个随机临床试验证实辅助化疗可给Ⅱ期结肠癌术后患者带来明显的生存获益。
有实验表明,对于有不良预后因素患者应该考虑辅助化疗。
目前的研究热点是对于II期结肠癌的化疗预后及预测因子的研究。
本文就Ⅱ期结肠癌的辅助化疗的若干争论和问题,以及关于化疗优势人群的选择问题做一简单介绍。
【关键词】结肠癌;Ⅱ期;化学治疗;进展
结肠癌是严重危及人类健康的常见恶性肿瘤之一。
根据国内部分地区的统计资料,我国结肠癌的发病率和死亡率均呈上升趋势。
手术切除是结肠癌主要的治疗手段,术后5年生存率大约在70%,有40%~50%患者出现术后复发或转移,其中绝大多数患者失去再治愈的机会。
2010年美国的Cancer Statistics表明:结直肠癌无论在男性还是女性其预计新发病例及死亡病例人数都位于第三位。
因此,除了手术治疗之外,化学治疗在结肠癌的综合治疗中必将成为不可或缺的一部分。
目前,对于Ⅲ期结肠癌患者的辅助治疗已经达成共识,但二期患者的辅助治疗目前仍然存在争论。
一Ⅱ期结肠癌患者是否需要给予辅助化疗
INT-0035研究、IMPACT B2 研究及2002年SEER的数据分析表明:对II期结肠癌进行辅助治疗不能取得明显的生存获益。
Sharlene Gill Pooled Analysis、Japanese Meta-Analysis Group、QUASAR
及2010年NSABP研究相继给出结果:II期大肠癌辅助性化疗,DFS获益仅为5-10%,但沒转换成OS
的明显获益。
今年ASCO的ACCENT最新报道可以看到,单药对II期患者辅助化疗的TTR、TRD(time f rom recurrence to death)和OS是“meaningfully improved”。
QUASAR研究证明II期结肠癌接受辅助化疗的临床获益可能不到5%。
在一篇2010年ASCO的壁报中,W. Gonsalves等分析了II期结肠癌辅助化疗的生存获益情况。
该研究分析了1995-2003年手术后的3628例Ⅱ期结肠癌患者,分别研究诊断时年龄、淋巴结检出数量、病理分级及是否接受辅助化疗对OS的影响。
结果:在3628例2期结肠癌患者中,接受辅助化疗的患者与未接受辅助化疗的患者5年生存率分别是62%和50%(p = 0.0028)。
在亚组分析中,接受辅助化疗ⅡA期结肠癌患者的5年生存率与未接受化疗的相比为70% vs. 54% (HR = 0.627, 95% CI = 0.547-0.718) ,而ⅡB期则为62% vs. 33% (HR = 0.470, 95% CI = 0.350-0.630) 。
所有年龄段接受化疗的患者均获得了生存获;在所有Ⅱ期患者中生存的获益与淋巴结的检出数目和诊断时年龄相关,在ⅡB期患者中分级也与生存相关。
结论:辅助化疗或许能给2期结直肠癌患者提供长期的获益,淋巴结数目和诊断时年龄是提高5年生存有独立的预后因素,组织学分级仅在ⅡB期患者有明显的预后作用。
当然,还需要更多的随机对照研究来验证。
二奥沙利铂在Ⅱ期结肠癌辅助治疗中的地位
MOSAIC试验确立了奥沙利铂在有高危因素(ⅡB期、组织学分级差——3或4级、肿瘤周围淋巴管侵犯、肠梗阻、T3伴有局部穿孔或封闭、切缘不确定或阳性、淋巴结活检数量小于12)的Ⅱ期结肠癌辅
助治疗中的地位。
MOSAIC试验共入组2246 病例,随机分组接受LV5FU2 或FOLFOX4 6 月,主要观查终点为DFS,次要观查终点为OS和安全性。
结果:5年DFS 为73.3% 和67.4% 分别在FOLFO X4 和LV5FU2 组([HR] = 0.80;95% CI,0.68 to 0.93;P = 0.003)。
6年OS 为78.5% 和76. 0% 在FOLFOX4 与LV5FU2 组(HR = 0.84;95% CI,0.71 to 1.00;P = 0.046);其中6年OS 在3期患者为:72.9% and 68.7%,(HR = 0.80;95% CI,0.65 to 0.97;P = 0.023)。
MOSAIC 试验亚组分析的结果显示,随访6年后Ⅱ期患者仍然没有显示出使用FOLFOX的DFS优势(HR=0.84,95%CI 0.62-1.14,P=0.258)。
亚组分析却显示高危Ⅱ期患者使用FOLFOX4具有较长DFS的趋势(HR =0.74,95%CI 0.52-1.06),表明这部分患者可能会从中获益;然而,MOSAIC试验发现低危Ⅱ期患者未能从FOLFOX方案中获益。
在2010年ASCO的一篇壁报上,将MOSAIC试验中的II期患者长期随访结果根据危险因子不同进行了分析,对高危II期辅助化疗仍是认可的,但不推荐用于低危患者。
MOSAIC试验奠定了奥沙利铂在高危Ⅱ期结肠癌辅助治疗中的地位。
但奥沙利铂的外周感觉神经毒性使其在使用过程中受到一定程度的限制。
使用FOLFOX化疗的患者3级外周感觉神经毒性发生率为12.4%,安全性的长期随访结果显示大多数能逐渐缓解。
然而4年后这些患者中仍有15.5%患者存在神经毒性,表明这种由奥沙利铂诱发的神经毒性在某些患者可能是无法完全逆转的。
2010年ASCO在其Education se ssion中发表了《Management of oxaliplatin-induced neurotoxicity》,提醒我们做好奥沙利铂的毒性管理,使患者能够顺利实施治疗,从而使患者最大程度地从含奥沙利铂的联合方案治疗中获益。
三关于II期结肠癌辅助化疗获益人群的选择
鉴于II期结肠癌辅助化疗的绝对临床获益不足5%,如何选择II期结肠癌辅助化疗获益人群将成为今后研究的重点。
在一些回顾性研究中,一个有趣的分子预后因素是错配修复缺失(dMMR)。
一项研究显示,采用免疫组化(IHC)检测的MMR蛋白和聚合酶链反应(PCR)检测的微卫星不稳定性(MSI)可发现结肠癌生物类型的两种表现,即dMMR对应MSI-H,错配修复正常(pMMR)对应低度微卫星不稳定性/微卫星稳定(MSI-L/MSS)。
2003年Christine M. Ribic等进行的一项回顾性研究提示,MSI-H患者并不能从FU的辅助化疗中获益。
2008年D. J. Sargent等进行的一项荟萃分析亦显示,在Ⅱ期患者中,具有dMMR者接受辅助化疗较未经治疗者并无生存优势,5年无病生存(DFS)率反而显著缩短(72%对87%)。
乳腺癌21基因RS给一部分特殊病人治疗带来很好的指导意义。
今年ASCO也发表了类似的对CRC领域的探索,口头陈述的12-gene colon cancer Recurrence Score和poster的ColoPrint都给我们留下了深刻的印象。
目前,反映II期结肠癌高危风险生物标志物是基于回顾性分析发现的,还没有前瞻性的研究来证明它们在个体化治疗选择中的有效性。
目前正在进行的ECOG 5202研究计划入组3610例I I期大肠癌患者,试验分层——是否存在微卫星不稳定性(MSI)以及是否存在18q杂合性缺失(LOH)。
将实验分为高危组和低危组:高危组(MSS和18qLOH)分为A组和B组,A组给予FOLFOX,B组给
予FOLFOX+贝伐单抗;低危组(MSI+或无18q缺失)给予临床观察。
这一研究正在进行中,我们希望它能给我们带来更多有意义的结果。
四结语
鉴于以上的争论和研究结果,以及目前国内的手术和病理检查过程中存在的不确定因素,同时兼顾国内的医疗体制、医疗环境和肿瘤患者的心理因素,对高危患者应考虑给予术后辅助化疗,方案可选用5-F U/LV、卡培他滨或5-FU/LV/奥沙利铂(3种均为2A类);目前并无证据支持伊利替康,单克隆抗体用于II期结肠癌患者的辅助治疗;有关Ⅱ期患者是否需行辅助化疗的临床决策,应该让医生和患者进行个体化讨论,包括对疾病特征的详细解释、疗效的相关证据以及治疗可能引起的毒副作用,最终让患者做出选择。
我们期待更多的临床研究关注这一领域,尤其关于基于生物标志物的治疗有效人群的富集的研究。
我们希望在不久的将来可以对所有II期结肠癌患者真正做到“Tailored Therapy ”!
II期结肠癌患者的辅助治疗一直在争论中前进,必将还有更进一步的争论,但争论的过程本身就是共识产生的过程,相信我们正走在“共识”的大道上!。
