第二章-缩聚中基本概念-线形缩聚动力学..
合集下载
线型缩聚反应动力学讲义

线型缩聚反应动力学
1.不可逆线形缩聚动力学
若将体系中的低分子副产物不断排出,则反应不可逆地向正方向进行。
如聚酯反应采用减压脱水使平衡向产物方向移动,符合不可逆的条件。
若将体系中的低分子副产物不断排出,则反应不可逆地向正方向进行。
如聚酯反应采用减压脱水使平衡向产物方向移动,符合不可逆的条件。
2.可逆平衡线性缩聚动力学
聚酯化反应平衡常数K值较小,小分子副产物若不及时排除,逆反应不能忽视。
令羧基的起始浓度为C0,t时刻的浓度为C,分别考虑水不排除和部分排除(残留水的浓度为nw)两种情况:
缩聚反应大多呈现可逆条件下的动力学,所以要达到高分子量,副产物尽可能除尽,工业上采取高温、高真空的方法。
高分子化学-线型缩聚动力学
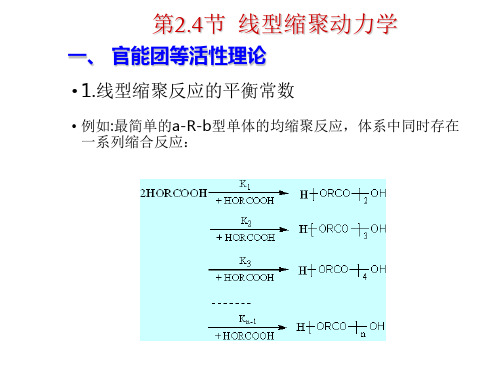
的活性作用减弱,因而官能团活性相近。 2)官能团的活性与基团的碰撞频率有关,不决 定于整个大分子的扩散速率。
Flory对此进行了解释 ,同时指出,官能团等活 性理论是近似的,不是绝对的。
4.4.3 线型缩聚动力学
以二元酸和二元醇的聚酯化反应为例
4
1) 不可逆条件下的线型缩聚反应动力学
缩聚反应不断排出低分子副产物情况下,符合不可逆条件。 酯化或聚酯化是酸催化反应,机理如下: 第一步 羧酸先质子化:
聚合度与单体起始浓度和反应时间 t 是线性关
系,即随反应时间增加而线性增长,由直线的斜
率可以求k′→k
• 有实验数据证明当P(或聚合度)在一定范围内, 1/(1-P)—t的线性关系良好,这也证明了官能 团等活性的假定是正确的。 • 工业生产总是以外加酸作催化剂来加速反应
(2)自催化聚酯化动力学
• 在无外外加酸的情况下,二元酸单体作催化剂。但有机羧酸 电离度较少,特别是随着聚合度的提高,体系将从少量电离 逐步趋向不电离,催化作用减弱,情况比较复杂,分两种情 况分析。
6
k3是最慢的一步反应,由于不可逆, k4暂不考虑,聚酯反应速 率用羧基消失速率来表示:
d[COOH ] Rp - k 3[C (OH )2][OH ] dt
(7-5)
[C+(OH)2]是质子化羧基的浓度,难以确定,设法消去,令
+ - k 1 [ C ( OH ) 2 ][ A ] , K = = k2 [ COOH ][ HA ]
t 时水未排出 C 水部分排出 C
聚酯反应净速率是正、逆反应速率之差 水未排出时速率
dC 2 2 ( ) - = k1 C - k 1 - C -1 dt
(7-19a)
高分子化学-第二章 缩聚和逐步聚合
N0
N0
反应程度与转化率的区别
转化率:参加反应的单体量占起始单体量的分数,是指已 经参加反应的单体的数目
反应程度:则是指已经反应的官能团的数目
例如: 一种缩聚反应,单体间双双反应很快全部变成二聚体,就 单体转化率而言,转化率达100%;而官能团的反应程度 仅50%
反应程度与平均聚合度的关系
聚合度是指高分子中含有的结构单元的数目
聚加成:形式上是加成反应,但反应机理是逐步反应。 如聚氨酯的合成(p17)。
开环反应:部分开环反应为逐步反应,如水、酸引发的己内 酰胺的开环反应。
氧化-偶合:单体与氧气的缩合反应, 如 2,6-二甲基苯酚和氧 气形成聚苯撑氧,也称聚苯醚。
2 逐步聚合反应的特点
官能团间的反应,无特定的活性中心;无所谓的引发、 增长、终止等基元反应;反应逐步进行,每一步的反 应速率和活化能大致相同;
[ H + ][ A- ] KHA =
[ HA ]
[ HA ] [ H + ] [ A- ] = KHA
代入式
-d [ COOH ] = k1k3[ COOH ][OH ][ H+]
dt
k 2KHA
催化用酸HA:可以是二元酸本身,但反应较慢,也可以是 外加酸,如H2SO4,大大加速
自催化缩聚反应
无外加酸,二元酸单体催化剂,[HA] = [COOH]
Flory对此进行了解释:
官能团等活性理论是近似的,不是绝对的,这一理论大大简化了研 究处理,可用同一平衡常数表示,整个缩聚过程可以用两种官 能团之间的反应来表征
COOH + HO
k1
OCO
k1
2. 线型缩聚动力学
不可逆条件下的缩聚动力学
高分子化学与物理第二章

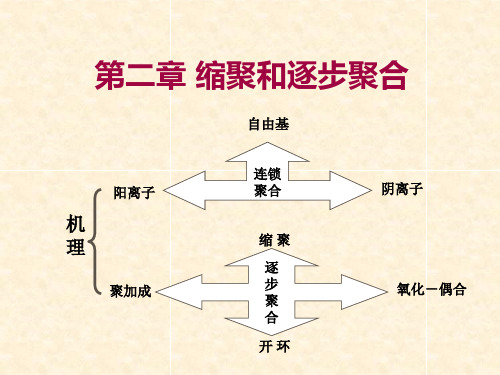
逐步聚合反应的分类:
逐步聚合反应
缩合聚合 逐步加成 开环聚合 氧化偶合 Diels-Alder加成聚合
✓ 缩聚:
✓聚加成:形式上是加成,机理是逐步的。
聚氨基酸酯,简称聚氨酯
✓开环反应:部分为逐步反应。 ✓氧化偶合:单体与氧气的缩合反应。
✓ Diels-Alder加成聚合:单体含一对共轭双键,如:
2.3.2 线形缩聚机理特征:逐步的、可逆平衡 1、逐步性:以二元酸和二元醇为例:
通式为:
缩聚反应的单体转化率、产物聚 合度与反应时间关系示意图
反应程度p: 参加反应的基团数占起始基团数的分率。 N0:起始的基团数
N:反应到 t 时体系中残留的基团数
以等摩尔的二元酸和二元醇缩聚为例: N0:体系中的羧基数或羟基数,等于二元酸与二元醇的分子总数, 也等于反应时间 t 时的二元酸和二元醇的结构单元总数。 N:反应到 t 时体系中残留的羧基数或羟基数 ,等于聚酯的分子数, 因为一个聚酯分子平均带有一个端羧基和1个端羟基。
1)不可逆的缩聚动力学
在及时脱水的条件下,k4=0;k1、k2、k5都比k3大,聚酯化速率 或羧基消失速率由第三步反应控制。
质子化种的浓度[C+(OH)2]难以测定, 引入平衡常数K’消去
考虑到HA的离解平衡
上式中氢离子[H+]可来自羧酸本身,进行自催化,但因为酯 化反应为慢反应,一般采用外加无机酸催化加速。
1-2官能度体系 例:辛醇与邻苯二甲酸酐(官能度为2)反应形成邻苯 二甲酸二辛酯(DOP)。
二元反应体系中若有一原料的官能度为1,则缩合后只能 得到低分子化合物,称为缩合反应。
2-2官能度体系
2官能度体系 2-2或2官能度体系的单体进行缩聚,形成线形缩聚物。
[理学]第二章缩聚
![[理学]第二章缩聚](https://img.taocdn.com/s3/m/576305dadb38376baf1ffc4ffe4733687e21fc4b.png)
本章主要研究以缩聚为主的逐步聚合
7
2.2 缩聚反应
1)定义:官能团间经多次缩合形成聚合物的反应,即缩 合聚合的简称。如己二胺和己二酸合成尼龙-66:
n
n
特点: • 缩聚物有特征结构官能团; • 有低分子副产物; • 缩聚物和单体分子量不成整数倍。
8
2)缩合反应体系 官能度:分子中能参与反应的官能团数 官能团:-OH,-NH2,-COOH,-COOR,-COCl,-(CO)2O,-SO3H
聚酯化反应:二元醇与二元羧酸、二元酯、二元酰氯等反应:
5
聚加成:形式上是加成,机理是逐步的。 含活泼氢功能基的亲核化合物与含亲电不饱和功
能基的亲电化合物之间的聚合。如: 聚氨基酸酯,简称聚氨酯
6
开环反应:部分为逐步反应,如水、酸引发己内酰胺的开 环生成尼龙-6。
氧化偶合:单体与氧气的缩合反应。 如2,6-二甲基苯酚和氧气形成聚苯撑氧,也称聚苯醚(PPO)
17
反应程度p: 参加反应的基团数(N0-N)占起始基团数(N0)的分率。
18
聚 合 度
反应程度
聚合度与反应程度的关系
19
2)可逆平衡 指缩聚过程中生成的产物可被反应中伴生的小分子降
解,单体分子与聚合物分子之间存在可逆平衡的反应。 如聚酯化反应:
20
缩聚反应的平衡常数 多数缩聚反应属可逆平衡反应: 平衡常数: 如聚酯化反应是可逆反应,可用下式表示:
53
1、卡罗瑟思法(Carothers)凝胶点的预测 理论基础:出现凝胶点时数均聚合度为无穷大,此是
时的反应程度p即为凝胶点pc。Carothers方程关联了凝胶 点pc与平均官能度的关系。 1)等基团数 平均官能度 f :单体混合物中每一个分子平均带有的基团数
7
2.2 缩聚反应
1)定义:官能团间经多次缩合形成聚合物的反应,即缩 合聚合的简称。如己二胺和己二酸合成尼龙-66:
n
n
特点: • 缩聚物有特征结构官能团; • 有低分子副产物; • 缩聚物和单体分子量不成整数倍。
8
2)缩合反应体系 官能度:分子中能参与反应的官能团数 官能团:-OH,-NH2,-COOH,-COOR,-COCl,-(CO)2O,-SO3H
聚酯化反应:二元醇与二元羧酸、二元酯、二元酰氯等反应:
5
聚加成:形式上是加成,机理是逐步的。 含活泼氢功能基的亲核化合物与含亲电不饱和功
能基的亲电化合物之间的聚合。如: 聚氨基酸酯,简称聚氨酯
6
开环反应:部分为逐步反应,如水、酸引发己内酰胺的开 环生成尼龙-6。
氧化偶合:单体与氧气的缩合反应。 如2,6-二甲基苯酚和氧气形成聚苯撑氧,也称聚苯醚(PPO)
17
反应程度p: 参加反应的基团数(N0-N)占起始基团数(N0)的分率。
18
聚 合 度
反应程度
聚合度与反应程度的关系
19
2)可逆平衡 指缩聚过程中生成的产物可被反应中伴生的小分子降
解,单体分子与聚合物分子之间存在可逆平衡的反应。 如聚酯化反应:
20
缩聚反应的平衡常数 多数缩聚反应属可逆平衡反应: 平衡常数: 如聚酯化反应是可逆反应,可用下式表示:
53
1、卡罗瑟思法(Carothers)凝胶点的预测 理论基础:出现凝胶点时数均聚合度为无穷大,此是
时的反应程度p即为凝胶点pc。Carothers方程关联了凝胶 点pc与平均官能度的关系。 1)等基团数 平均官能度 f :单体混合物中每一个分子平均带有的基团数
第二章-线形缩聚物线形缩聚中聚合度的因素和控制方法

为避免高温时缩聚产物的氧化降解,常需在惰性气体( N2、CO2)中进行 为获得高分子量产物,聚合后期一般需要减压,甚至在 高真空下进行
反应完成后,聚合物以粘流状态从釜底流出,制带、冷 却、切粒
聚碳酸酯的合成- 酯交换法:
笔记本电脑、 手机、光学
n HO_
媒体
灯具,现代 汽车头灯
光盘基板
H_[O_
CH 3 _C _
X-聚体的分子量 X-聚体的分子数
WX = x M0 Nx = xN 0Px-1(1-P)2
W N0 M0
N0
结构单元数 结构单元 (单体数) 分子量
Wx = xPx-1(1-P)2 x-聚体的重量分布函数
W
2.6 逐步聚合方法掌握定义、典型例子方程式)
熔融缩聚
是单体和聚合产物均处于熔融状态下的聚合反应。 是最简单的缩聚方法。只有单体和少量催化剂存在。 优点:
112
114
结构单元的平均分子量
M0=112
+ 2
114
=
113
则平均聚合度
Xn = 13500-146=118 113
当反应程度P = 0. 994时,求r值:
根据
1+r
q+2
Xn = 1+r-2rP = q+2( 1-P )
118= 1
+
1+r r-2 ×0.994r
己二胺和己二酸的配料比 r = 0.995
产物纯净,分离简单,甚至不用分离 通常以釜式聚合,生产设备简单 是工业上和实验室常用的方法 熔融缩聚在工艺上有以下特点:
反应温度高 一般在200-300 ℃之间,比生成的聚合物的熔点高10 -20 ℃ 一般不适合生产高熔点的聚合物
反应时间长, 一般都在几个小时以上
反应完成后,聚合物以粘流状态从釜底流出,制带、冷 却、切粒
聚碳酸酯的合成- 酯交换法:
笔记本电脑、 手机、光学
n HO_
媒体
灯具,现代 汽车头灯
光盘基板
H_[O_
CH 3 _C _
X-聚体的分子量 X-聚体的分子数
WX = x M0 Nx = xN 0Px-1(1-P)2
W N0 M0
N0
结构单元数 结构单元 (单体数) 分子量
Wx = xPx-1(1-P)2 x-聚体的重量分布函数
W
2.6 逐步聚合方法掌握定义、典型例子方程式)
熔融缩聚
是单体和聚合产物均处于熔融状态下的聚合反应。 是最简单的缩聚方法。只有单体和少量催化剂存在。 优点:
112
114
结构单元的平均分子量
M0=112
+ 2
114
=
113
则平均聚合度
Xn = 13500-146=118 113
当反应程度P = 0. 994时,求r值:
根据
1+r
q+2
Xn = 1+r-2rP = q+2( 1-P )
118= 1
+
1+r r-2 ×0.994r
己二胺和己二酸的配料比 r = 0.995
产物纯净,分离简单,甚至不用分离 通常以釜式聚合,生产设备简单 是工业上和实验室常用的方法 熔融缩聚在工艺上有以下特点:
反应温度高 一般在200-300 ℃之间,比生成的聚合物的熔点高10 -20 ℃ 一般不适合生产高熔点的聚合物
反应时间长, 一般都在几个小时以上
第二章 缩聚中基本概念 线形缩聚动力学

数据处理:对实验数据进行整理、清洗和预处理,包括缺失值处理、 异常值检测与剔除等 数据分析:运用统计分析、机器学习等方法对实验数据进行深入分析, 挖掘数据背后的规律和趋势
结果呈现:将分析结果以图表、报告等形式呈现,便于理解与交流
P线A形R缩T聚6动力学的发展趋势与
展望
动力学模型的发展趋势
复杂系统建模:随着对复杂系统研究的深入,动力学模型将更加精细和复杂,以模拟真实 系统的行为。
动力学参数的确定
动力学方程:描述反应速率与反应物浓度的关系 反应速率常数:表示反应的快慢程度 活化能:表示反应的活化能大小 动力学参数的确定方法:通过实验数据拟合和计算得出
PART 4
线形缩聚动力学模型
模型建立的原则
简化为线性模型 忽略非线性效应 假设系统是线性的 考虑时间演化过程
模型建立的步骤
PART 1
单击添加章节标题
PART 2
线形缩聚动力学的定义
缩聚反应的定义
缩聚反应:由单体通过聚合反 应生成高分子化合物的过程
反应特点:反应过程中不断产 生小分子,如水、醇等
反应类型:加成聚合、缩合聚 合等
影响因素:温度、压力、催化 剂等
线形缩聚反应的特点
反应过程中分子量逐渐增加 反应速率逐渐降低 反应体系粘一种单体进行的聚合反应
共聚反应:由两种或两种以上的单体进行的聚合反应
连锁聚合反应:在引发剂或催化剂的作用下,单体分子中的双键打开,不断加成聚合成 长链高聚物的聚合反应 逐步聚合反应:单体在聚合过程中,逐步由单体双键打开加成到高聚物分子链上,同时 生成水或其他小分子的聚合反应
确定研究问题
求解数学模型
添加标题
添加标题
建立数学模型
添加标题
结果呈现:将分析结果以图表、报告等形式呈现,便于理解与交流
P线A形R缩T聚6动力学的发展趋势与
展望
动力学模型的发展趋势
复杂系统建模:随着对复杂系统研究的深入,动力学模型将更加精细和复杂,以模拟真实 系统的行为。
动力学参数的确定
动力学方程:描述反应速率与反应物浓度的关系 反应速率常数:表示反应的快慢程度 活化能:表示反应的活化能大小 动力学参数的确定方法:通过实验数据拟合和计算得出
PART 4
线形缩聚动力学模型
模型建立的原则
简化为线性模型 忽略非线性效应 假设系统是线性的 考虑时间演化过程
模型建立的步骤
PART 1
单击添加章节标题
PART 2
线形缩聚动力学的定义
缩聚反应的定义
缩聚反应:由单体通过聚合反 应生成高分子化合物的过程
反应特点:反应过程中不断产 生小分子,如水、醇等
反应类型:加成聚合、缩合聚 合等
影响因素:温度、压力、催化 剂等
线形缩聚反应的特点
反应过程中分子量逐渐增加 反应速率逐渐降低 反应体系粘一种单体进行的聚合反应
共聚反应:由两种或两种以上的单体进行的聚合反应
连锁聚合反应:在引发剂或催化剂的作用下,单体分子中的双键打开,不断加成聚合成 长链高聚物的聚合反应 逐步聚合反应:单体在聚合过程中,逐步由单体双键打开加成到高聚物分子链上,同时 生成水或其他小分子的聚合反应
确定研究问题
求解数学模型
添加标题
添加标题
建立数学模型
添加标题
第二章-缩聚中基本概念-线形缩聚动力学

HOOC-R-COO-R'-OOC-R-COO-R'-OH + H2O 四聚体
。 。 。 n HOOC-R-COOH + n HO-R'-OH
。 。 O O 。 HO ( C R C OR'O ) H + (2n-1) H2O n
缩聚基本特征(对比自由基聚合)
(1)功能基反应-聚合反应是通过单体功能基之间的反 应逐步进行的; (2)基元反应-没有明显的几个基元反应,每步反应的 机理相同,因而相应的反应速率和活化能大致相同;
• 需要说明:反应程度与转化率根本不同,转化率: 参加反应的单体量占起始单体量的分数是指已经参 加反应的单体分子的数目。
• 反应程度则是指已经反应的官能团的数目,不涉及具体 单体分子 例如: 一种缩聚反应,单体间双双反应很快全部变成二聚体, 就单体转化率而言,转化率达100%; 而官能团的反应程度仅50%。 • 反应程度与平均聚合度的关系(更为重要),聚合度是 指高分子中含有的结构单元的数目。
*
n
2. 绝大多数加聚反应均是典型的连锁聚合,但有些加聚 反应却属于缩合聚合机理(加聚反应不等于连锁聚合)
O H2C CH2 O
+
H2C CH2 O
D-A Reaction
*
*
* O
*
没有活 性中心
n
+
3.其他逐步聚合反应:
自由基缩聚、氧化偶联缩聚、分解缩聚(聚甲撑)、环 化缩聚、逐步加聚(聚氨酯)逐步开环聚合(环氧树脂)
第二章要点:
1.本章的一些基本概念:如(平均)官能度、凝胶点 2.缩聚反应动力学特点: 逐步 可逆
3.线型缩聚反应平衡及相对分子质量控制方法
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
*
n
2. 绝大多数加聚反应均是典型的连锁聚合,但有些加聚 反应却属于缩合聚合机理(加聚反应不等于连锁聚合)
O H2C CH2 O
+
H2C CH2 O
D-A Reaction
*
*
* O
*
没有活 性中心
n
+
3.其他逐步聚合反应:
自由基缩聚、氧化偶联缩聚、分解缩聚(聚甲撑)、环 化缩聚、逐步加聚(聚氨酯)逐步开环聚合(环氧树脂)
2.2 线形缩聚反应机理特征
1. 线型缩聚的逐步特性
以二元醇和二元酸合成聚酯为例 HOROH + HOOCR`COOH
HOROCOR`COOH + H2O
HOROH
2 四聚体
HOOCR`COOH
HOROCOR`COOROH
三聚体
HOOCR`COOROCOR`COOH
三聚体
二、三、四等多聚体间可相互反应,也可自身反应-含羟基的任何 多聚体和含羧基的任何多聚体都可反应,如此重复。 在反应过程中, 聚合物分子量随时间延长而逐渐增加,显示出逐步的特征,通式如 下:
n HOOC(CH2)4COOH + n HOCH2CH2OH
HO CO(CH 2)4COOCH 2CH 2O
n
H + (2n-1) H2O
线形缩聚-高分子化学
2 官能度体系
同一单体带有两个不同且能相互反应的官能团, 得到线形聚合物,如氨基乙酸、羟基乙酸等
n HORCOOH H ORCO nOH + (n-1) H2O
缩聚过程中的副反应
1. 环化反应
2 HOCH2COOH
H2O
H2O
HOCH2COOCH2COOH
C O
2-2或 2 官能度体系 是线形缩聚的必要条 件,但不是充分条件
CH2 O O C O CH2
环的稳定性与环上取代基或元素有关 八元环不稳定,取代基或元素改变,稳定性增加
CH3 CH3 Si O CH3 Si CH3 O
反 应程 度P
当P=0. 9,Xn = 10; P=0. 95,Xn = 20; P=0. 99,Xn = 100 。 一般高分子的Xn = 100 ~ 200,P要提高到 0. 99 ~ 0. 995 聚合初期和中期反应程度的快速增加并未使聚合度快速升高。反 应后期,反应程度的微小增加即导致聚合度的快速上升。这是缩 聚反应的一大特点。(只有高反应程度才可得聚合物分子)
HOOC(CH2)nCOOH
HOOC(CH2)nH + CO2
重复单元(链 3. 化学降解 节):聚合物中 化学组成相同的 低分子醇酸水可使聚酯、聚酰胺等醇解、酸解、水解 最小单位
H (OROCOR`CO ) m ( OROCOR`CO) n OH
聚合度:高分子 链中重复单元的 醇解 重复次数,聚合 酸解 度是衡量高分子 大小的一个指标。 水解
• 需要说明:反应程度与转化率根本不同,转化率: 参加反应的单体量占起始单体量的分数是指已经参 加反应的单体分子的数目。
• 反应程度则是指已经反应的官能团的数目,不涉及具体 单体分子 例如: 一种缩聚反应,单体间双双反应很快全部变成二聚体, 就单体转化率而言,转化率达100%; 而官能团的反应程度仅50%。 • 反应程度与平均聚合度的关系(更为重要),聚合度是 指高分子中含有的结构单元的数目。
体系中起始二元酸和二元醇的分子总数为N0(结构单 元数),等于起始羧基数或羟基数。
HOH2C CH2OH
C
HOH2C CH2OH
t 时的聚酯分子数为N,等于残留的羧基或羟基数 N0-N N P= =1 - N0 N0
½ N0 二元酸 和½ N0 二元醇反应,则反前官能团酸与醇均为N0,
聚酯分子数为N,则聚酯大分子所带官能团为2 N,而酸与醇官 能团数又是相等的, 所以反应后残留的酸与醇数均为N。
HOOC-R-COO-R'-OOC-R-COO-R'-OH + H2O 四聚体
。 。 。 n HOOC-R-COOH + n HO-R'-OH
。 。 O O 。 HO ( C R C OR'O ) H + (2n-1) H2O n
HOOC-R-COOH + HO-R'-OH
HOOC-R-COOH HOOC-R-COO-R'-OH + HO-R'-OH
HOOC-R-COOH + HO-R'-OH
HOOC-R-COOH HOOC-R-COO-R'-OH + HO-R'-OH
HOOC-R-COO-R'-OH + H2O 二聚体
HOOC-R-COO-R'-OOC-R-COOH + H2O 三聚体 HO-R'-OOC-R-COO-R'-OH + H2O
2 HOOC-R-COO-R'-OH
HOOC-R-COO-R'-OH + H2O 二聚体
HOOC-R-COO-R'-OOC-R-COOH + H2O 三聚体 HO-R'-OOC-R-COO-R'-OH + H2O
2 HOOC-R-COO-R'-OH
HOOC-R-COO-R'-OOC-R-COO-R'-OH + H2O 四聚体
。 。 。 + n HO-R'-OH n HOOC-R-COOH
HOOC-R-COOH + HO-R'-OH
HOOC-R-COOH HOOC-R-COO-R'-OH + HO-R'-OH
HOOC-R-COO-R'-OH + H2O 二聚体
HOOC-R-COO-R'-OOC-R-COOH + H2O 三聚体 HO-R'-OOC-R-COO-R'-OH + H2O
2 HOOC-R-COO-R'-OH
体形缩聚-高分子化学
2-3、2-4官能度体系
如:苯酐和甘油反应 苯酐和季戊四醇反应
a a a a b b b
O
体形缩 聚物
HOH2C
C O C O
CH2OH
C
HOH2C CH2OH
注意:双官能度体系的成环反应
在生成线形缩聚物的同时,常伴随有 成环反应 (副反应),环的稳定性与环大小关系如下: 5, 6 > 7 > 8 ~ 11 > 3, 4 环的稳定性越大,反应中越易成环, 五元环、 六元环最稳定,故易形成环状化合物。
二醇 二酸
结构单元数目 N0 Xn = = 大分子数 N
P=
N0-N N =1 - N0 N0
代入反应程度关系式
N0-N N P= =1 - N0 N0
300 250 200 150 Xn 100 50 0 0.0 0.2 0.4 0.6 0.8 1.0
1 P=1 - Xn 1 Xn = 1 -P
按生成聚合物的结构分类 线形缩聚 体型缩聚 按参加反应的单体种类 均缩聚:只有一种单体进行的缩聚反应,2 体系 混缩聚:两种分别带有相同官能团的单体进行 的缩聚反应,即 2-2体系,也称为杂缩聚
在均缩聚中加入第二种单体进行的缩聚反应
共缩聚 在混缩聚中加入第三或第四种单体进行的缩
聚反应
共缩聚在制备无规和嵌段共聚物方面获得应用: 无规共缩聚可适当降低聚合物的 Tg、Tm 可合成聚氨酯、聚酯型热塑弹性体
K值小, 如聚酯化反应,K 4, 副产物水对分子量影响很大 K值中等,如聚酰胺化反应,K 300~500 水对分子量有所影响 K值很大,在几千以上,如聚碳酸酯、聚砜 可看成不可逆缩聚
缩聚反应分类
按反应热力学的特征分类
指平衡常数小于 103 的缩聚反应 聚酯 K 4;聚酰胺 K 400 不平衡缩聚反应 平衡常数大于 103 采用高活性单体和相应措施 平衡缩聚反应
3. 反应程度
在缩聚反应中,常常选用多官能团单体,反应中一个单 体上的官能团可能不反应、部分反应或全部反应,不宜用 转化率表示反应进行的程度大小,故常用反应程度来描述 反应的深度。 反应程度:是参加反应的官能团数占起始官能团数的分 数,用P表示; 对于等物质量的二元酸和二元醇缩聚反应 (为例),设:
H HOOCR`CO H
OROH OH OH
结构单元:构成大分子 链并决定其结构,以单 体结构为基础的原子 (团)组合
降解反应使分子量降低,在聚合和加工中都可能发生
4.链交换反应
聚酯、聚酰胺、聚硫化物的两个分子可在任何地方 的酯键、酰胺键、硫键处进行链交换反应
H (OROCOR`CO )m ( OROCOR`CO)n OH H (OROCOR`CO )p ( OROCOR`CO)q OH
第二章要点:
1.本章的一些基本概念:如(平均)官能度、凝胶点 2.缩聚反应动力学特点: 逐步 可逆
3.线型缩聚反应平衡及相对分子质量控制方法
4.体型缩聚反应特点、基本条件及凝胶点的计算 5.缩聚实施方法及重要缩聚物如涤纶等的合成反应
2.1 缩聚反应基本概念
1. 缩聚反应ห้องสมุดไป่ตู้
是通过官能团相互作用并且伴有小分子生成而形成聚 合物的过程(多次缩合反应、最重要的逐步聚合) 单体常带有各种官能团: - COOH 、- OH 、- COOR 、- COCl 、- NH2 - NCO 等等, 以二元羧酸与二元醇的聚合反应为例
O O HO ( C R C
。 。 。 ) OR'O
n
H + (2n-1) H2O
(3)体系组成-反应体系始终由单体和分子量递增的一 系列中间产物组成,单体以及任何中间产物两分子间都 能发生反应; (4)分子量形成-聚合产物的分子量是逐步增大的。
n
2. 绝大多数加聚反应均是典型的连锁聚合,但有些加聚 反应却属于缩合聚合机理(加聚反应不等于连锁聚合)
O H2C CH2 O
+
H2C CH2 O
D-A Reaction
*
*
* O
*
没有活 性中心
n
+
3.其他逐步聚合反应:
自由基缩聚、氧化偶联缩聚、分解缩聚(聚甲撑)、环 化缩聚、逐步加聚(聚氨酯)逐步开环聚合(环氧树脂)
2.2 线形缩聚反应机理特征
1. 线型缩聚的逐步特性
以二元醇和二元酸合成聚酯为例 HOROH + HOOCR`COOH
HOROCOR`COOH + H2O
HOROH
2 四聚体
HOOCR`COOH
HOROCOR`COOROH
三聚体
HOOCR`COOROCOR`COOH
三聚体
二、三、四等多聚体间可相互反应,也可自身反应-含羟基的任何 多聚体和含羧基的任何多聚体都可反应,如此重复。 在反应过程中, 聚合物分子量随时间延长而逐渐增加,显示出逐步的特征,通式如 下:
n HOOC(CH2)4COOH + n HOCH2CH2OH
HO CO(CH 2)4COOCH 2CH 2O
n
H + (2n-1) H2O
线形缩聚-高分子化学
2 官能度体系
同一单体带有两个不同且能相互反应的官能团, 得到线形聚合物,如氨基乙酸、羟基乙酸等
n HORCOOH H ORCO nOH + (n-1) H2O
缩聚过程中的副反应
1. 环化反应
2 HOCH2COOH
H2O
H2O
HOCH2COOCH2COOH
C O
2-2或 2 官能度体系 是线形缩聚的必要条 件,但不是充分条件
CH2 O O C O CH2
环的稳定性与环上取代基或元素有关 八元环不稳定,取代基或元素改变,稳定性增加
CH3 CH3 Si O CH3 Si CH3 O
反 应程 度P
当P=0. 9,Xn = 10; P=0. 95,Xn = 20; P=0. 99,Xn = 100 。 一般高分子的Xn = 100 ~ 200,P要提高到 0. 99 ~ 0. 995 聚合初期和中期反应程度的快速增加并未使聚合度快速升高。反 应后期,反应程度的微小增加即导致聚合度的快速上升。这是缩 聚反应的一大特点。(只有高反应程度才可得聚合物分子)
HOOC(CH2)nCOOH
HOOC(CH2)nH + CO2
重复单元(链 3. 化学降解 节):聚合物中 化学组成相同的 低分子醇酸水可使聚酯、聚酰胺等醇解、酸解、水解 最小单位
H (OROCOR`CO ) m ( OROCOR`CO) n OH
聚合度:高分子 链中重复单元的 醇解 重复次数,聚合 酸解 度是衡量高分子 大小的一个指标。 水解
• 需要说明:反应程度与转化率根本不同,转化率: 参加反应的单体量占起始单体量的分数是指已经参 加反应的单体分子的数目。
• 反应程度则是指已经反应的官能团的数目,不涉及具体 单体分子 例如: 一种缩聚反应,单体间双双反应很快全部变成二聚体, 就单体转化率而言,转化率达100%; 而官能团的反应程度仅50%。 • 反应程度与平均聚合度的关系(更为重要),聚合度是 指高分子中含有的结构单元的数目。
体系中起始二元酸和二元醇的分子总数为N0(结构单 元数),等于起始羧基数或羟基数。
HOH2C CH2OH
C
HOH2C CH2OH
t 时的聚酯分子数为N,等于残留的羧基或羟基数 N0-N N P= =1 - N0 N0
½ N0 二元酸 和½ N0 二元醇反应,则反前官能团酸与醇均为N0,
聚酯分子数为N,则聚酯大分子所带官能团为2 N,而酸与醇官 能团数又是相等的, 所以反应后残留的酸与醇数均为N。
HOOC-R-COO-R'-OOC-R-COO-R'-OH + H2O 四聚体
。 。 。 n HOOC-R-COOH + n HO-R'-OH
。 。 O O 。 HO ( C R C OR'O ) H + (2n-1) H2O n
HOOC-R-COOH + HO-R'-OH
HOOC-R-COOH HOOC-R-COO-R'-OH + HO-R'-OH
HOOC-R-COOH + HO-R'-OH
HOOC-R-COOH HOOC-R-COO-R'-OH + HO-R'-OH
HOOC-R-COO-R'-OH + H2O 二聚体
HOOC-R-COO-R'-OOC-R-COOH + H2O 三聚体 HO-R'-OOC-R-COO-R'-OH + H2O
2 HOOC-R-COO-R'-OH
HOOC-R-COO-R'-OH + H2O 二聚体
HOOC-R-COO-R'-OOC-R-COOH + H2O 三聚体 HO-R'-OOC-R-COO-R'-OH + H2O
2 HOOC-R-COO-R'-OH
HOOC-R-COO-R'-OOC-R-COO-R'-OH + H2O 四聚体
。 。 。 + n HO-R'-OH n HOOC-R-COOH
HOOC-R-COOH + HO-R'-OH
HOOC-R-COOH HOOC-R-COO-R'-OH + HO-R'-OH
HOOC-R-COO-R'-OH + H2O 二聚体
HOOC-R-COO-R'-OOC-R-COOH + H2O 三聚体 HO-R'-OOC-R-COO-R'-OH + H2O
2 HOOC-R-COO-R'-OH
体形缩聚-高分子化学
2-3、2-4官能度体系
如:苯酐和甘油反应 苯酐和季戊四醇反应
a a a a b b b
O
体形缩 聚物
HOH2C
C O C O
CH2OH
C
HOH2C CH2OH
注意:双官能度体系的成环反应
在生成线形缩聚物的同时,常伴随有 成环反应 (副反应),环的稳定性与环大小关系如下: 5, 6 > 7 > 8 ~ 11 > 3, 4 环的稳定性越大,反应中越易成环, 五元环、 六元环最稳定,故易形成环状化合物。
二醇 二酸
结构单元数目 N0 Xn = = 大分子数 N
P=
N0-N N =1 - N0 N0
代入反应程度关系式
N0-N N P= =1 - N0 N0
300 250 200 150 Xn 100 50 0 0.0 0.2 0.4 0.6 0.8 1.0
1 P=1 - Xn 1 Xn = 1 -P
按生成聚合物的结构分类 线形缩聚 体型缩聚 按参加反应的单体种类 均缩聚:只有一种单体进行的缩聚反应,2 体系 混缩聚:两种分别带有相同官能团的单体进行 的缩聚反应,即 2-2体系,也称为杂缩聚
在均缩聚中加入第二种单体进行的缩聚反应
共缩聚 在混缩聚中加入第三或第四种单体进行的缩
聚反应
共缩聚在制备无规和嵌段共聚物方面获得应用: 无规共缩聚可适当降低聚合物的 Tg、Tm 可合成聚氨酯、聚酯型热塑弹性体
K值小, 如聚酯化反应,K 4, 副产物水对分子量影响很大 K值中等,如聚酰胺化反应,K 300~500 水对分子量有所影响 K值很大,在几千以上,如聚碳酸酯、聚砜 可看成不可逆缩聚
缩聚反应分类
按反应热力学的特征分类
指平衡常数小于 103 的缩聚反应 聚酯 K 4;聚酰胺 K 400 不平衡缩聚反应 平衡常数大于 103 采用高活性单体和相应措施 平衡缩聚反应
3. 反应程度
在缩聚反应中,常常选用多官能团单体,反应中一个单 体上的官能团可能不反应、部分反应或全部反应,不宜用 转化率表示反应进行的程度大小,故常用反应程度来描述 反应的深度。 反应程度:是参加反应的官能团数占起始官能团数的分 数,用P表示; 对于等物质量的二元酸和二元醇缩聚反应 (为例),设:
H HOOCR`CO H
OROH OH OH
结构单元:构成大分子 链并决定其结构,以单 体结构为基础的原子 (团)组合
降解反应使分子量降低,在聚合和加工中都可能发生
4.链交换反应
聚酯、聚酰胺、聚硫化物的两个分子可在任何地方 的酯键、酰胺键、硫键处进行链交换反应
H (OROCOR`CO )m ( OROCOR`CO)n OH H (OROCOR`CO )p ( OROCOR`CO)q OH
第二章要点:
1.本章的一些基本概念:如(平均)官能度、凝胶点 2.缩聚反应动力学特点: 逐步 可逆
3.线型缩聚反应平衡及相对分子质量控制方法
4.体型缩聚反应特点、基本条件及凝胶点的计算 5.缩聚实施方法及重要缩聚物如涤纶等的合成反应
2.1 缩聚反应基本概念
1. 缩聚反应ห้องสมุดไป่ตู้
是通过官能团相互作用并且伴有小分子生成而形成聚 合物的过程(多次缩合反应、最重要的逐步聚合) 单体常带有各种官能团: - COOH 、- OH 、- COOR 、- COCl 、- NH2 - NCO 等等, 以二元羧酸与二元醇的聚合反应为例
O O HO ( C R C
。 。 。 ) OR'O
n
H + (2n-1) H2O
(3)体系组成-反应体系始终由单体和分子量递增的一 系列中间产物组成,单体以及任何中间产物两分子间都 能发生反应; (4)分子量形成-聚合产物的分子量是逐步增大的。
