双官能团
双官能团
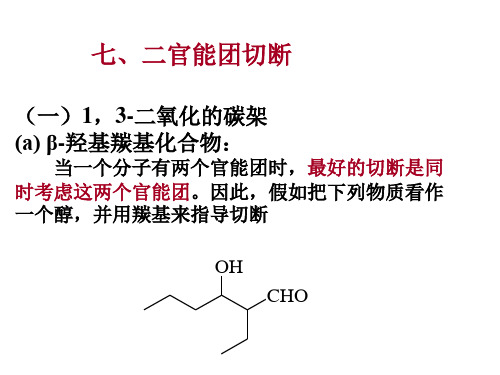
OH CHO TM84
二者的关系在1,3-位,而且分子的碳数是对称的,它正 好来自羟醛缩合:
H OH + B H
O
O H A
O
O H
合成:
O O H 碱 OH H TM84
两个官能团在1,3-位,还涉及到羰基活性的问题:
O H O TM85 H HCHO + OH O
H O A + HCHO 弱碱 TM85
O HO Ph O NMe2 TM110
• 分析如下:
O HO Ph O NMe2 FGI HO COOH + HO APh COOH + O C Ph D B NMe2
HO
COOH Ph
1,3-二氧
• 合成:缩合中需要控制,因为在烯醇化和亲电能 力两个方面,酮C都比酸D要活泼。Reformatsky反 应看来是一个好方法。
5.85
9 10. 21 11 11.2
环戊二烯
PhCOCH3 CH3COCH3 HC≡CH
16
16 20 ~25
CH3COOCH3 24. 5
CH2(CO2Et)2
(CH3SO2)2CH2 (CH3)2CHCHO EtOH
13.3
14 15.5 15.9
CH3CN
Ph3CH CH2=CH2 CH3CH3
O
5
COOEt 稳定的碳负离子
O -不饱和
CO2Et 1,5-二羰基化合物
两个组分:一般是一个活化了的碳负离子和一个αβ不饱和羰基化合物。
分析:对称,两侧切断相同, 试剂丙酮需要活化。
OMe O O 对称 O + O CHO OMe O + OMe
光催化1,3-二烯的双官能团化反应

光催化1,3-二烯的双官能团化反应1. 概述光催化反应是利用光能激发物质分子发生化学反应的一种方法,近年来备受科学家们的关注。
光催化反应不但能够在温和条件下实现许多传统化学反应所无法达到的选择性和高效性,还具有绿色环保的优势。
1,3-二烯是一类重要的有机分子,其双烯结构使其具有较高的反应活性,因此1,3-二烯的官能团化反应在有机合成领域具有重要意义。
2. 光催化1,3-二烯的双官能团化反应机理1,3-二烯的双官能团化反应是指1,3-二烯分子在光照条件下,通过光催化剂的作用,发生双官能团的加成反应。
光照能激发光敏剂从基态跃迁至激发态,激发态的光敏剂与1,3-二烯发生反应,形成中间体,最终生成双官能团化合物。
3. 光催化1,3-二烯的双官能团化反应的应用光催化1,3-二烯的双官能团化反应在有机合成领域具有广泛的应用前景,可以用于合成天然产物、药物、农药和功能材料等重要有机化合物。
该反应不但可以有效构建碳-碳、碳-氧、碳-氮等化学键,还能实现对官能团的精确选择性引入,为有机合成提供了新的工具和途径。
4. 影响光催化1,3-二烯的双官能团化反应的因素光催化1,3-二烯的双官能团化反应受到多种因素的影响,包括光催化剂的选择、反应条件的优化、1,3-二烯的结构特性等。
在实际应用中,科研人员需要综合考虑这些因素,合理设计反应体系,以提高反应的选择性和产率。
5. 光催化1,3-二烯的双官能团化反应的研究进展近年来,随着光催化领域的快速发展,越来越多的科学家们将目光投向了光催化1,3-二烯的双官能团化反应。
他们通过不断改进光催化剂的结构、优化反应条件和探索新的1,3-二烯官能团化反应类型,取得了一系列有意义的研究成果,为该领域的发展注入了新的活力。
6. 结语光催化1,3-二烯的双官能团化反应是一种具有重要意义的有机合成方法,其独特的反应特性和广泛的应用前景使其备受关注。
但与此该反应仍面临许多挑战,如光催化剂的设计、反应体系的稳定性等问题亟待解决。
廉价金属催化烯烃和炔烃自由基双官能团化反应

自由基双官能团化反应的机理和特点
• 自由基双官能团化反应的机理主要包括以下步骤:首先,一个分子中的自由基引发剂引发另一个分子的烯 烃或炔烃生成自由基;其次,生成的自由基与另一个分子中的烯烃或炔烃发生加成反应;最后,生成的新 的自由基与另一个分子中的烯烃或炔烃发生加成反应,生成最终的化合物。自由基双官能团化反应具有高 选择性、高效率和高原子经济性等特点。
烯烃和炔烃是常见的有机化合物,它 们具有丰富的化学反应性和生物活性 ,因此在有机合成、药物合成、材料 科学等领域具有广泛的应用。
传统的烯烃和炔烃官能团化反应主要 集中在氧化、还原、加成等反应,但 这些反应往往需要使用较为昂贵的催 化剂或条件较为苛刻,因此开发新的 、高效、环保的催化体系一直是化学 研究的重要方向。
03
官能团化试剂的研究
不同的官能团化试剂可以引入不同的 官能团,如羧基、羟基、氨基等,对 反应产物的结构和性质有重要影响。
廉金属催化的炔烃自由基双官能团化反应研究
炔烃自由基双官能团化反应的机理
在廉金属催化剂的作用下,炔烃分子中的π键被活化,生成自由基中间体,然后与不同的 官能团化试剂反应,实现双官能团化。
要点三
反应选择性和产物多 样性
目前对于烯烃和炔烃自由基双官能团 化反应的反应选择性和产物多样性仍 存在一定的限制,未来的研究将致力 于拓展反应的应用范围并提高产物多 样性。
06
参考文献
参考文献
01
参考文献1:作者1, 文章标题, 杂志名, 年份, 卷号(期号), 页码
• 引用内容1
02
参考文献2:作者2, 文章标题, 杂志名, 年份, 卷号(期号), 页码
温度对自由基双官能团化反应的速 率和产物分布有显著影响。在一定 范围内,提高温度可以促进反应速 率和产物纯度的提高。然而,过高 的温度可能导致副反应增多,降低 产物纯度。
烯烃双官能团化

烯烃双官能团化1. 简介烯烃是一类含有碳-碳双键的有机化合物,具有较高的反应活性和化学多样性。
双官能团化是指在烯烃分子中同时引入两个官能团,从而扩展其化学反应性和应用领域。
本文将介绍烯烃双官能团化的基本概念、常见反应类型及其应用。
2. 烯烃双官能团化的基本概念烯烃双官能团化是指在烯烃分子中引入两个不同的官能团,通常通过化学反应实现。
这种反应可以在烯烃分子的一个碳-碳双键上引入一个官能团,同时在另一个双键上引入另一个官能团。
通过这种方式,可以在烯烃分子中引入多种官能团,从而赋予其更多的化学反应性和应用价值。
3. 常见的烯烃双官能团化反应3.1 羟基化反应羟基化反应是将烯烃中的一个碳-碳双键转化为一个羟基官能团的反应。
常用的羟基化试剂有过氧化氢、水和苯酚等。
羟基化反应可以通过不同的催化剂和反应条件实现,例如过渡金属催化的氢氧化反应和非金属催化的水合反应。
羟基化反应在合成醇、酚和醚等化合物中具有广泛的应用。
3.2 卤素化反应卤素化反应是将烯烃中的一个碳-碳双键转化为一个卤素官能团的反应。
常用的卤素化试剂有氯、溴和碘等。
卤素化反应可以通过不同的催化剂和反应条件实现,例如卤化氢的加成反应和卤素化试剂的直接反应。
卤素化反应在合成卤代烃和卤代醇等化合物中具有广泛的应用。
3.3 羧基化反应羧基化反应是将烯烃中的一个碳-碳双键转化为一个羧基官能团的反应。
常用的羧基化试剂有酸酐、酸氯和酸酯等。
羧基化反应可以通过不同的催化剂和反应条件实现,例如过渡金属催化的氧化反应和非金属催化的酸酐反应。
羧基化反应在合成酸和酯等化合物中具有广泛的应用。
3.4 氨基化反应氨基化反应是将烯烃中的一个碳-碳双键转化为一个氨基官能团的反应。
常用的氨基化试剂有氨和胺等。
氨基化反应可以通过不同的催化剂和反应条件实现,例如金属催化的氨化反应和非金属催化的胺化反应。
氨基化反应在合成胺和氨基化合物中具有广泛的应用。
4. 烯烃双官能团化的应用烯烃双官能团化反应可以扩展烯烃的化学反应性和应用领域,为有机合成提供了重要的工具和方法。
第五章双官能团化合物的切断1

O
O Ph
NMe2
工业生产上,利用β-紫罗兰酮为原料制备维生素A的方法,就 是以Reformatzky反应为基础的
O B rC H 2 C O 2 C 2 H 5
Z n
1 )H + C O 2 C 2 H 5 2 )L iA lH 4
3 )C rO 3 ,P y
C H O C H 3 C O C H 3
C H 3 C O C H C O O C 2 H 5+H O C 2 H 5 N a
p K a = 1 6
2、酯的分子内的缩合(Dieckmann Condensation)
O CO2CH2CH3
O OCCHO22CCHH32CH3
CO2CH2CH3 CO2CH2CH3
O CO2CH2CH3
CO2CH2CH3 O
COOR
C2H 5ONa +CH 3COOC2H 5
CH COOC2H 5 +C2H 5OH CH O
COCH 2COOC2H 5 +ROH
C H 3 C H 2 C O 2 C 2 H 5 +(C O 2 C 2 H 5 )2 草 酸 二 乙 酯
1)C2H5ONaCH3CHCOCO2C2H5
2)H3+O, D
H
O
(2) CH3C OC2H5 +CH2COOC2H5
接受体
给予体
O-CH3C OC2H5 产生氧负离子
CH2COOC2H5
O--
(3) CH3C OC2H5
CH3COCH2COOC2H5 +C2H5O-- 生成产物
CH2COOC2H5
C H 3 C O C H 2 C O O C 2 H 5 + N a O C 2 H 5 p K a = 1 1
双官能团有机小分子电致发光材料的合成及性能(精)

双官能团有机小分子电致发光材料的合成及性能有机电致发光器件(OLED)具有低电压直流驱动、自发光、高亮度、宽视角、高分辨率、快响应、易于实现全彩色等突出优点,已逐渐成为一种很有前途的新型平板显示器,被誉为“21世纪平板显示技术”。
其广泛的应用前景和技术上的突飞猛进使得OLED成为当今国际上的研究热点之一。
有机电致发光材料是有机电致发光器件的最主要组成部分,因此设计、合成一系列的新型发光材料显得尤为重要。
本文从分子设计和材料设计的思想出发,合成了以三嗪基团作为吸电子单元,三苯胺基团作为给电子单元的七种化合物,并对其结构进行了表征。
对化合物P2和P6培养了单晶,解析其单晶结构,前者为单斜晶系,后者为三斜晶系。
测定了它们在二氯甲烷溶液中的紫外吸收光谱和荧光光谱。
结果表明:七种化合物的紫外吸收光谱基本相似,荧光发射光谱却有较大变化,分布在508nm~605nm之间。
并以硫酸奎宁为标准测定了它们的荧光量子产率。
用循环伏安法测试了这几种化合物的电化学性质,计算得出它们的电离势为5.88~6.01eV,电子亲和势为3.50~3.65eV。
结果表明所合成的化合物是一类具有载流子传输功能的发光材料。
此外,我们分别选取了化合物P1、P5、P6作为发光层制备了电致发光器件,研究了其电致发光性质,为绿光和黄光发射。
同主题文章[1].吴茂林. 薄膜式电致发光器件' [J]. 电子技术. 1985.(02)[2].郑永成. 类ZnS碱土硫化物的电致发光' [J]. 液晶与显示. 1991.(01)[3].李薇,苏媛,叶英植,唐明生,郭益群. 一种新型电致发光材料的合成研究' [J]. 郑州大学学报(自然科学版). 1999.(03)[4].高向鹏. 2008年我院共招收硕士研究生105名' [J]. 西安邮电学院学报. 2008.(05)[5].葛葆珪. 全国第一届商品化电致发光器件评审会在上海举行' [J]. 发光学报. 1989.(01)[6].周亚训. 多孔硅电致发光器件' [J]. 半导体杂志. 1996.(01)[7].马文婧. 如何更好地适应研究生阶段的学习' [J]. 计算机教育. 2005.(05)[8].王兰富. 冲击与希望——一个IT硕士研究生的“考研”、求职之路' [J]. 电脑爱好者. 2003.(22)[9].宁永强,全亿鑫. 多孔硅发光' [J]. 材料导报. 1993.(04)[10].章婷,徐征,滕枫,钱磊,王永生,徐叙瑢. 双掺杂聚合物电致发光中能量传递的光谱分析' [J]. 光谱学与光谱分析. 2006.(01)【关键词相关文档搜索】:物理化学; 三苯胺; 均三嗪; 齐聚苯撑乙烯; 合成; 电致发光器件【作者相关信息搜索】:延边大学;物理化学;周子彦;高选民;。
1、6双官能团化合物的合成

逆合成分析法是将合成目标经过多种逆合成操 作转变成结构简单的前体,再将前体按同样的 方法进行简化,反复进
目标分子
官能团转换
另外的目标分子
逆合成转变
前体
逆合成转变
前体的前体 ……
原料
• 遵循合理的反应机理是逆向切断时应该考虑 的基本原则。
• 一、切断应遵循的原则有:
切断。
6、逆推过程中适当的运用FGI(官能 团转换)策略。
• 二、1,6—二羰基化合物的拆开
• 1,6-二官能团化合物常由环己烯及其衍生物合成
• 而合成取代环己烯,经常用到Diels-Alder反应
COOH COOH
+
O
+
CHO
1、试设计以下化合物的合成路线
O
分析:
O
O
CH O
用羟醛缩合反应
O
格氏试剂
O O
分析:
O O O O O OH CN
羟醛或羟 酮缩合
O
O
O
CN
Br
OH
O
O
双键还原
COOC2 H5
脱羧
COOC2 H5
COOC2 H5 O
+
CH2(COOC2H5)2
合成路线:
O O
CH2(COOC2H5)2
EtONa
(1) 稀NaOH
COOC2 H5
(2) H+
COOC2 H5
O O O
(1) C2H5OH,H+
COOH
(2) 乙二醇,HCl(g)
COOC2 H5
O
O
(1)LAH
OTs
氰化钠
O
O CN
1,3—双官能团化合物的逆合成分析

合成:方法a:
C6H5CH2CO2C2H5 + (COOC2H5)2 C2H5Na C6H5CHCO2C2H5 O C COOC2H5
草酸二乙酯
C6H5CHCO2C2H5 COOC2H5
合成:方法b:
O C2H5Na C6H5CHCO2C2H5 COOC2H5
C6H5CH2CO2C2H5 + H5C2O C OC2H5
1,3—双官能团化合物的逆合成分析
三、1,3—二羰基化合物的合成
Claisen缩合:
• • • • 克莱森酯缩合是制备1,3—二羰基化合物的重要反应 Claisen缩合反应一般指酯之间的缩合、酮的烯醇负离子 (α -碳负离子)、腈的烯醇负离子与酯的缩合。 酯之间的缩合又分为相同酯间缩合,分子内酯缩合及不 同酯间缩合 这些缩合分别得到结构式略有差异的化合物,但最 终都能生成1,3-二羰基化合物,因此目标化合物可切断
1、相同酯间缩合
定义:具有-活泼氢的酯,在碱的作用下,两分子酯 相互作用,生成-羰基酯,同时失去一分子醇 的反应。
O H3C C OCH2CH3 O
+
H CH2 C
OCH2CH3
C2H5ONa
O H3C C CH2
O C
3
2
1
OCH2CH3
+ C2H5OH
β-羰基酸酯
• 产物:β -羰基酸酯(1,3—二羰基化合物) • 根据克莱森缩合的特点1,3-二羰基化合物可以如 下拆开:
5、酯与腈缩合
夺氢 Ph CO2C2H5 + C6H5CH2CN C2H5ONa C6H5CHCN Ph C O β 羰基腈
注意:
酯与睛的缩合也是睛与不含α -H的酯之间的
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(一)1,3-二氧化的碳架 (a) β-羟基羰基化合物:
当一个分子有两个官能团时,最好的切断是同 时考虑这两个官能团。因此,假如把下列物质看作 一个醇,并用羰基来指导切断
OH CHO TM84
二者的关系在1,3-位,而且分子的碳数是对称的,它正 好来自羟醛缩合:
H OH + B H
TM248
HN Michael O TM249 NC O
H2N
-不饱和
NC OHC
4 5
1
2 3
O
O
1
3 2
合成:
分子内的Michael加成
芳香族不饱和杂环的合成
Cl C-O Ph O Me TM256 Ph O O Me 1,4-DICO Ph O + O Me CO2Et
ቤተ መጻሕፍቲ ባይዱ
合成:
O Me CO2Et i. EtO ii. Ph O
常见有机化合物α-H的酸性 化合物 pKa 化合物 pKa
(CH3CO)3CH
(CH3CO)2CH2 CH3NO2 CH3COCH2CO2Et CH2(CN)2
5.85
9 10. 21 11 11.2
环戊二烯
PhCOCH3 CH3COCH3 HC≡CH
16
16 20 ~25
CH3COOCH3 24. 5
CH3CHO + H O
合理的切断是什么?
αβ-不饱和羰基化合物 切断时,可按如下的方式, 即直接将C=C切断即给出两部分原料:
O Ph OH PhCH=O + (CH3CO)2O Perkin 反应
(c) 1,3-二羰基化合物
这类化合物的合成一般是一个酯与一个酮 之间的缩合反应:
芳香族化合物合成总结
• 官能团的性质与定位
• 含氧基团的引入
• 卤素基团的引入
• 含氮基团的引入 • 烃基的引入
-
O
EtO
N N H
+
Ph
杂原子分离的例子---TM260的合成。
O HN O N H TM260 C-N O NH2 NH2 Michael加成 + EtO O O O EtO OEt + MeCHO
合成:杂原子部分就是尿素。
CH2(CO2H)2 MeCHO R2NH,H+ i. EtOH,H+ CO2H O ii. H2N NH2
FGI
O Ph
Friedel-Crafts
+
O Cl
合成:
O Cl AlCl3
O Ph
i. NH2OH/H+ ii. LiAlH4
H2N Ph
i. PhCOCl ii. LiAlH4
TM242
合成 分析:它比D-A产物差一个吸电子基和一个双键:
Ph FGI NH2 TM245 Ph + PhCHO + CH3NO2 Ph FGI NO2 Ph NO2 D-A
O
O H A
O
O H
合成:
O O H 碱 OH H TM84
两个官能团在1,3-位,还涉及到羰基活性的问题:
O H O TM85 H HCHO + OH O
H O A + HCHO 弱碱 TM85
A的自身缩合是不会发生的
CHO
(b) αβ-不饱和羰基化合物:
CHO CHO a H b OH O CH=O
-
CO2Et Cl Ph O O Me
水解 脱羧
Ph O O
H+ Me
不对称的五元杂环采用以上路线;对称的五元杂环则 采用以下简化的过程来合成1,4-二羰基化合物
1,4-二羰基化合物的合成:
O 2 OEt O I2 EtONa O CO2Et
CO2EtO O i. OHii. H+,(-CO2) O
产物与NH3、P2S2或P2O5作用就分别得到吡咯、噻吩或 呋喃。例如下题就是一个常见的考研合成题:
O Ph O Ph PhNH2 Ph N Ph Ph
与TM258相关的一个重要化合物是安替比林 (antipyrine,一种止痛药),它的合成是用 苯肼代替TM258中的肼:
O -H2O OEt HN Ph -EtOH O N Ph N Antipyrine O NH2 O OEt N HN Ph
合成:
HCHO CHO K2CO3 OHC OH CH2(COOH)2 NH3 TM108
• 试提出扩瞳剂(扩大眼睛的瞳孔)(cyclopentolate) 的合成方法。
O HO Ph O NMe2 TM110
• 分析如下:
O HO Ph O NMe2 FGI HO COOH + HO APh COOH + O C Ph D B NMe2
合成:
PhCHO base + CH3NO2
O2N
Ph O2N
Ph NO2
H2-Pd
Ph NH2
对称的胺合成。
MeO MeO H N OMe TM246 OMe
Ar
H N
FGI Ar Ar
H N O
Ar
C-N
Ar
NH2
+
Cl O
Ar
合成:
Cl MeO MeO HCHO HCl MeO MeO KCN MeO MeO CN
TM260
与尿素相关的合成中,较重要的是丙二酰脲 (也叫巴比土酸)类的合成:
O
O NH O
丙二酰脲 常见的一个合成题如下:以丙二酸二乙酯及其 他必要试剂合成5-苄基-5-乙基巴比土酸:
O C2H5 PhH2C O
O NH
合成:
O OEt OEt O O C2H5 PhH2C O OEt OEt H2N O NH2 i. EtONa ii. PhCH2Br PhH2C OEt O O C2H5 PhH2C O O OEt i. EtONa ii. C2H5Br
氯甲基化位置专一
这个合成的特点:两个反应中间体都来自同一个腈, 合成路线简化。
(二)杂环化合物
1,5-二羰基化合物
合成:
i. CH2(CO2H)2 etc PhCHO ii. EtOH/H+ Ph CO2Et CH (CO Et) 2 2 2 EtO-
CO2Et PhNH2 EtO2C CO2Et Ph
OMe O O 对称 O + O CHO OMe O + OMe
OMe
O 碱(只生成一种产物) O
OMe
CHO OMe O CO2Et 碱 O O CO2Et H+ H2O, TM119
八、杂原子和杂环化合物
(一)杂原子—醚和胺
合成
C-O PhO TM234 Br PhO- + FGI OH
Williamson醚合成
还原是胺制备的主要方法,如肟的还原:
R1 R2 OH LiAlH4 N 或溶剂金属 如Na,EtOH R1 R2 NH2
腈的还原:
LiAlH4 RCN or H2-Pd,etc RCH2NH2
硝基化合物的还原:
RNO2 LiAlH4 或溶剂金属 如Na,EtOH RNH2
设计合成。
Ph Ph H N Ph TM242 FGI Ph O H N Ph C-N O + H2N 胺 Ph Cl
FGI EtO2C EtO2C + CO2Et 控制 活泼的烯丙基溴 Br
合成:
多数情况下,胺的合成一般采用酰胺还原的方式,以 避免烷基化时的多烷基化。
NMe2 FGI TM240 NMe2 C-N O Cl + Me2NH O
合成:
Cl i. Mg,Et2O ii. CO2 iii. SOCl2 Cl O Me2NH Me2N O LiAlH4 TM240
HO
COOH Ph
1,3-二氧
• 合成:缩合中需要控制,因为在烯醇化和亲电能 力两个方面,酮C都比酸D要活泼。Reformatsky反 应看来是一个好方法。
i. P,Br2 PhCH2COOH ii. EtOH i. Zn,Et2O ii. O C O + Me2NH HO NMe2 Br Ph COOEt
O O O O+ O
(CH3COCl)
比如:
O Ph
O TM94 Ph
• 分析:
O Ph O Ph Ph O + OEt O Ph
• 合成:
O Ph
EtOPhCO2Et
TM94
Ph Ph O CO2Et TM95
两个切断都合理,但b 的切断使合成变得简单,因 为它注意到了分子的对称性:
a Ph b Ph O a CO2Et b Ph O Ph O OEt + O Ph + OEt CO2Et Ph OEt
HO
COOEt E Ph E 酯交换(碱) TM110
(二)1,5-二羰基化合物
1,5-二羰基化合物的合成主要为Michael加成:
O +
1
O
2 3 4
O
5
COOEt 稳定的碳负离子
O -不饱和
CO2Et 1,5-二羰基化合物
两个组分:一般是一个活化了的碳负离子和一个αβ不饱和羰基化合物。
分析:对称,两侧切断相同, 试剂丙酮需要活化。
O NH
杂环合成总结: 即只要核对好氧化度, 杂原子切断通常是比较好的:
X X Br
、
X
O 或
H2N CO2H (而后LiAlH4)
X
XO
;
X
O
X
