第7章习题解答
第7章气体动理论习题解答

第7章 气体动理论7.1基本要求1.理解平衡态、物态参量、温度等概念,掌握理想气体物态方程的物理意义及应用。
2.了解气体分子热运动的统计规律性,理解理想气体的压强公式和温度公式的统计意义及微观本质,并能熟练应用。
3.理解自由度和内能的概念,掌握能量按自由度均分定理。
掌握理想气体的内能公式并能熟练应用。
4.理解麦克斯韦气体分子速率分布律、速率分布函数及分子速率分布曲线的物理意义,掌握气体分子热运动的平均速率、方均根速率和最概然速率的求法和意义。
5.了解气体分子平均碰撞频率及平均自由程的物理意义和计算公式。
7.2基本概念1 平衡态系统在不受外界的影响下,宏观性质不随时间变化的状态。
2 物态参量描述一定质量的理想气体在平衡态时的宏观性质的物理量,包括压强p 、体积V 和温度T 3 温度宏观上反映物体的冷热程度,微观上反映气体分子无规则热运动的剧烈程度。
4 自由度确定一个物体在空间的位置所需要的独立坐标数目,用字母i 表示。
5 内能理想气体的内能就是气体内所有分子的动能之和,即2iE RT ν= 6 最概然速率速率分布函数取极大值时所对应的速率,用p υ表示,p υ==≈其物理意义为在一定温度下,分布在速率p υ附近的单位速率区间内的分子在总分子数中所占的百分比最大。
7 平均速率各个分子速率的统计平均值,用υ表示,υ==≈8 方均根速率各个分子速率的平方平均值的算术平方根,用rms υ表示,rms υ==≈ 9 平均碰撞频率和平均自由程平均碰撞频率Z 是指单位时间内一个分子和其他分子平均碰撞的次数;平均自由程λ是每两次碰撞之间一个分子自由运动的平均路程,两者的关系式为:Zυλ==或λ=7.3基本规律1 理想气体的物态方程pV RT ν=或'm pV RT M=pV NkT =或p nkT =2 理想气体的压强公式23k p n ε=3 理想气体的温度公式21322k m kT ευ==4 能量按自由度均分定理在温度为T 的平衡态下,气体分子任何一个自由度的平均动能都相等,均为12kT 5 麦克斯韦气体分子速率分布律 (1)速率分布函数()dNf Nd υυ=表示在速率υ附近单位速率区间内的分子数占总分子数的百分比或任一单个分子在速率υ附近单位速率区间内出现的概率,又称为概率密度。
第7章习题解答

z 2 = z 1 + 130
2 z z ) 2 + 100 z ( z ) = 0 1 - ( 1 + 130 1 + 82 1 + 130
2 - 260 z z ´ 130 = 0 1 - 130 + 182 1 + 82
78 z ´ 130 - 130 2 = -48 ´ 130 = -6240 1 = 82 z 1 = -80 z 2 = z 1 + 130 = 130 - 80 = 50 f = 40cm
p 3 . 14 - 8 2 l 2 ´ 6328 ´ 10 - 3 ④ q= = = 2 . 315 ´ 10 rad pw0 3 . 14 ´ 0 . 0174
(5)有一个平凹腔,凹面镜曲率半径 R=5m,腔长 L=1m,光波长l=0.5mm,求①两镜 面上的基模光斑半径②基模高斯光束的远场发散角 解:①
2、双凹腔两反射镜面曲率半径分别为 R1=100cm、R2=82cm,腔长 L=130cm,求等价共焦 腔的焦参数。 解:
z1 +
f 2 = - R 1 z 1
z 1 +
f 2 = -100 z 1
2 2 z 100 z 1 + 1 + f = 0
w 0 =
f l
p
=
0 . 4 R l
p
(2)对称双凹腔长为 L,反射镜曲率半径 R=2.5L,光波长为l,求镜面上的基模光斑半 径。 解:
L L 2 f 2 = ( 2 R - L ) = (2 ´ 2 . 5 L - L ) = L 4 4 f = L
2 z 2
f
2
大学电路习题解答第7章
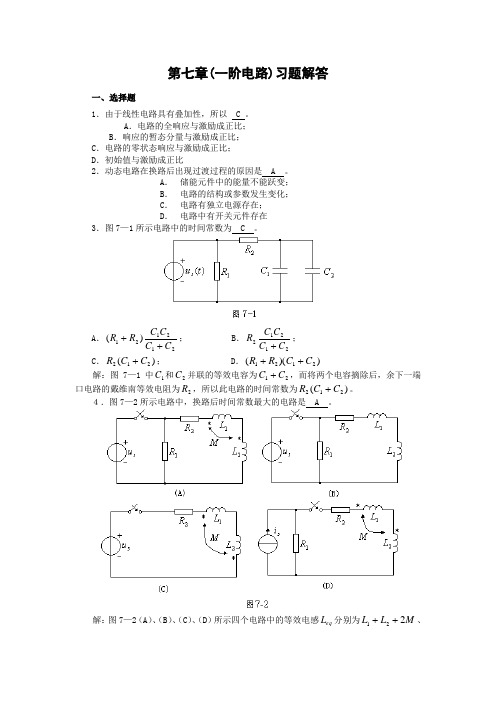
第七章(一阶电路)习题解答一、选择题1.由于线性电路具有叠加性,所以 C 。
A .电路的全响应与激励成正比;B .响应的暂态分量与激励成正比;C .电路的零状态响应与激励成正比;D .初始值与激励成正比2.动态电路在换路后出现过渡过程的原因是 A 。
A . 储能元件中的能量不能跃变;B . 电路的结构或参数发生变化;C . 电路有独立电源存在;D . 电路中有开关元件存在3.图7—1所示电路中的时间常数为 C 。
A .212121)(C C C C R R ++; B .21212C C C C R +;C .)(212C C R +;D .))((2121C C R R ++解:图7—1中1C 和2C 并联的等效电容为21C C +,而将两个电容摘除后,余下一端口电路的戴维南等效电阻为2R ,所以此电路的时间常数为)(212C C R +。
4.图7—2所示电路中,换路后时间常数最大的电路是 A 。
解:图7—2(A )、(B )、(C )、(D )所示四个电路中的等效电感eq L 分别为M L L 221++、21L L +、M L L 221-+和M L L 221++。
0>t 时,将图6—2(A )、(B )、(C )、(D )中的电感摘除后所得一端口电路的戴维南等效电阻eq R 分别为2R 、2R 、2R 和21R R +。
由于RL 电路的时间常数等于eqeq R L ,所以图7—2(A )所示电路的时间常数最大。
5.RC 一阶电路的全响应)e610(10tc u --=V ,若初始状态不变而输入增加一倍,则全响应c u 变为 D 。
A .t10e1220--; B .t10e620--;C .t10e1210--; D.t10e1620--解:由求解一阶电路的三要素法 τtc c c c u u u u -+∞-+∞=e)]()0([)( 可知在原电路中10)(=∞c u V ,4)0(=+c u V 。
教材第七章习题解答

第七章化学平衡习题解答1.回答下列问题(1)反应商和标准平衡常数的概念有何区别? (2)能否用r m G θ∆来判断反应的自发性?为什么? (3)计算化学反应的K θ有哪些方法?(4)影响平衡移动的因素有哪些?它们是如何影响移动方向的? (5)比较“温度与平衡常数的关系式”同“温度与反应速率常数的关系式”,有哪些相似之处?有哪些不同之处?举例说明。
(6)酸碱质子理论如何定义酸和碱?有何优越性?什么叫共轭酸碱对?(7)当往缓冲溶液中加入大量的酸和碱,或者用很大量的水稀释时,pH 是否仍保持不变?说明其原因。
(8)对于一个在标准状态下是吸热、熵减的化学反应,当温度升高时,根据勒夏特列原理判断,反应将向吸热的正方向移动;而根据公式∆r G m θ=∆r H m θ-T ∆r S m θ判断,∆r G m θ将变得更正(正值更大),即反应更不利于向正方向进行。
在这两种矛盾的判断中,哪一种是正确的?简要说明原因。
(9)对于制取水煤气的下列平衡系统:22C(s)+H O(g)CO(g)+H (g) ;r m H Θ∆。
问:① 欲使平衡向右移动,可采取哪些措施?② 欲使正反应进行得较快且较完全(平衡向右移动)的适宜条件如何?这些措施对K θ及k(正)、k(逆)的影响各如何?(10)平衡常数改变时,平衡是否必定移动?平衡移动时,平衡常数是否一定改变?【解答】(1)反应商是在一定温度下,任意给定态时,生成物的相对压力(或者相对浓度)以方程式中化学计量系数为幂的乘积除以反应物的相对压力(或相对浓度)以化学计量系数为幂的乘积。
在一定温度下,当反应达到平衡时,生成物的相对压力(或者相对浓度)以方程式中化学计量系数为幂的乘积除以反应物的相对压力(或相对浓度)以化学计量系数为幂的乘积是一个常数,称为标准平衡常数,是量纲为一的量。
标准平衡常数的数值只是温度的函数。
(2)只能用r m G θ∆判断在标准态下的反应的自发性。
任意给定态时,反应的自发进行的方向只能由r m G ∆来判断。
第7章习题解答

习 题7-1为什么一般矩形波导测量线的槽开在波导宽壁的中线上?答:因为矩形波导一般工作于10TE 模,由10TE 模的管壁电流知,在矩形波导宽壁中线处只有纵向电流,因此沿波导宽壁的中线开槽不会切断高频电流的通路,不会破坏波导内的场结构,也不会引起波导内的电磁波向外辐射能量。
7-2 推导矩形波导中mn TE 波的场量表达式。
7-3 已知空气填充的矩形波导截面尺寸为21023mm b a ⨯=⨯,求工作波长mm 20=λ时,波导中能传输哪些模式?mm 30=λ时呢? 解:矩形波导的截止波长22c 2⎪⎭⎫ ⎝⎛+⎪⎭⎫ ⎝⎛=b n a m πππλ当0,1==n m 时,mm a C 462==λ,1,0==n m 时,mm b C 202==λ, 0,2==n m 时,mm a C 23==λ, 1,1==n m 时,mm b a 34.181********222c =⎪⎭⎫⎝⎛+⎪⎭⎫ ⎝⎛=⎪⎭⎫ ⎝⎛+⎪⎭⎫ ⎝⎛=πππλ满足电磁波在波导中传播条件c λλ<的模式有10TE 、01TE ;当mm 30=λ时,只能传输10TE 模。
7-4 已知空气填充的矩形波导截面尺寸为248cm b a ⨯=⨯,当工作频率GHz 5=f 时,求波导中能传输哪些模式?若波导中填充介质,传输模式有无变化?为什么?解: cm f C 6105103910=⨯⨯==λ,矩形波导的截止波长22c 2⎪⎭⎫⎝⎛+⎪⎭⎫ ⎝⎛=b n a m πππλ,当0,1==n m 时,cm a C 162==λ,1,0==n m 时,cm b C 82==λ, 0,2==n m 时,cm a C 8==λ, 2,0==n m 时,cm b C 4==λ 1,1==n m 时,mm b a 15.74181222222c =⎪⎭⎫⎝⎛+⎪⎭⎫ ⎝⎛=⎪⎭⎫ ⎝⎛+⎪⎭⎫ ⎝⎛=πππλ满足电磁波在波导中传播条件c λλ<的模式有10TE 、01TE 、20TE 、11TE 、11TM ; 若波导中填充介质,工作波长变短,所以传输模式增多。
第七章 习题答案
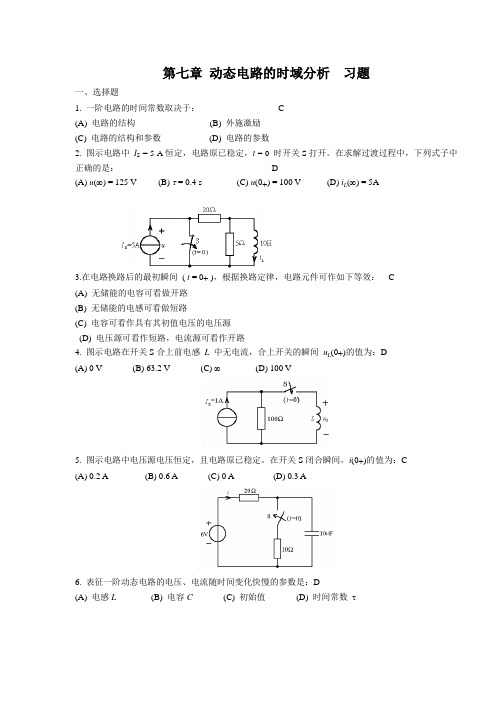
第七章动态电路的时域分析习题一、选择题1. 一阶电路的时间常数取决于: C(A) 电路的结构(B) 外施激励(C) 电路的结构和参数(D) 电路的参数2. 图示电路中I S = 5 A恒定,电路原已稳定,t = 0时开关S打开。
在求解过渡过程中,下列式子中正确的是: D(A) u(∞) = 125 V (B) τ = 0.4 s (C) u(0+) = 100 V (D) i(∞) = 5AL3.在电路换路后的最初瞬间( t = 0+ ),根据换路定律,电路元件可作如下等效: C(A) 无储能的电容可看做开路(B) 无储能的电感可看做短路(C) 电容可看作具有其初值电压的电压源(D) 电压源可看作短路,电流源可看作开路(0+)的值为:D4. 图示电路在开关S合上前电感L中无电流,合上开关的瞬间uL(A) 0 V (B) 63.2 V (C) ∞(D) 100 V5. 图示电路中电压源电压恒定,且电路原已稳定。
在开关S闭合瞬间,i(0+)的值为:C(A) 0.2 A (B) 0.6 A (C) 0 A (D) 0.3 A6. 表征一阶动态电路的电压、电流随时间变化快慢的参数是:D(A) 电感L(B) 电容C(C) 初始值(D) 时间常数τ7. 图示正弦脉冲信号的数学表达式为:B (A) sin ω t ⋅ ε (t ) + sin ω ( t - T ) ⋅ ε ( t - T ) (B) sin ω t ⋅ ε (t ) - sin ω t ⋅ ε ( t - T ) (C) sin ω t ⋅ ε (t ) - sin ω ( t - T ) ⋅ ε ( t - T ) (D) sin ω t ⋅ ε (t ) + sin ω t ⋅ ε ( t - T )8. 图示电路中,原已达稳态, t = 0开关 S 打开,电路的时间常数为:D (A)s 41 (B) s 61(C) s 4 (D)s 69. 示电路中,t = 0 时开关打开,则 u (0+)为:C(A) 0V (B) 3.75V (C) – 6V (D) 6V10.图示电路中,开关打开已久,在 t = 0 时开关闭合,i (0+) 为:D(A) 0A (B) 0.8A(C) 2A (D)1A11.R 、C 串联电路,已知全响应()()10C 83V,0t u t e t -=-≥,其零状态响应为:(A )(A) 1088V te-- (B) 1083V t e -- (C) 103V t e -- (D) 105V t e -12. .一阶电路的全响应()()10C 106V,0tu t et -=-≥若初始状态不变而输入增加一倍,则全响应u C (t)为 ( D ) (A) 20-12e -10t ; (B) 20-6e -10t ; (C) 10-12e -10t ; (D) 20-16 e -10t 。
第7章 信号处理电路 习题解答
7.3简述电荷放大器有什么特点,应用于何种场合。
解:电荷放大器应用于压电式加速度传感器、压力传感器等的后端放大。
上述两种传感器属于电容性传感器,这类传感器的阻抗非常高,呈容性,输出电压很微弱;他们工作时,将产生正比于被测物理量的电荷量,积分运算电路可以将电荷量转换成电压量,电路如下图所示。
解:1)LBF;2)BPF;3)HPF;4)BEF。
二、判断下列说法是否正确,用 “√”(正)和“ ”(误)填入括号内。
1)高通滤波器的通频带是指电压的放大倍数不变的频率范围。()
2)低通滤波器的截止频率就是电压放大倍数下降1/2的频率点。()
3)带通滤波器的频带宽度是指电压放大倍数大于或等于通带内放大倍数0.707的频率范围。()
其中 ;
该滤波器为二阶低通滤波电路,幅频特性如下图:
7.7试说明图P7-8所示各电路属于哪种类型的滤波电路,是几阶滤波电路。
(1)
(2)
图P7-7
解:
图(1)所示电路二阶带通滤波器或者二阶带阻滤波器。
前一个运放为高通滤波器(截止频率f1),后一个运放为低通滤波器(截止频率f2),如果 ,则f1<f2,该滤波器为二阶带通滤波器;如果 ,则f1>f2,该滤波器为二阶带阻滤波器。
电容性传感器可等效为因存储电荷而产生的电动势Ut与一个输出电容Ct串联,如图中虚线框内所示。根据集成运放的特点,可得到输出电压为: 。
7.4简述隔离放大器有什么特点,应用于何种场合。
解:隔离放大器通常应用于远距离信号传输。
在远距离信号传输的过程中,常因强干扰的引入使放大电路的输出有很强的干扰背景,甚至将有用信号淹没,造成系统无法正常工作。隔离放大器将电路的输入侧和输出侧在电气上完全隔离,它既可切断输入侧和输出侧电路间的直接联系,避免干扰混入输出信号,又可使有用信号畅通无阻。目前集成隔离放大器有变压器耦合式、光电耦合式和电容耦合式三种。
第七章习题解答
计算图示各系统的动能:(1)偏心圆盘的质量为,偏心距OC m e =,对质心的回转半径为C ρ,绕轴O 以角速度0ω转动(图a )。
(2)长为l ,质量为的匀质杆,其端部固结半径为,质量为的匀质圆盘。
杆绕轴O 以角速度m r m 0ω转动(图b )。
(3)滑块A 沿水平面以速度移动,重块B 沿滑块以相对速度下滑,已知滑块A 的质量为,重块B 的质量为(图c )。
1v 2v 1m 2m (4)汽车以速度沿平直道路行驶,已知汽车的总质量为0v M ,轮子的质量为m ,半径为R ,轮子可近似视为匀质圆盘(共有4个轮子)(图d )。
解:(1) 222200111()222C C C T mv J m e 2ωρω=+=+(2) 2222111(83)326O J ml mr ml m l r =++=+2220011(83)212O T J m l r 22ωω==+(3) 22121122A B T m v m v =+2221121212221212221211(2cos150)2211()m v m v v v v m m v m v m v v °=+++=++(4) ()2222000211111(4)422222v T M m v mv mR M m v R ⎛⎞=−+⋅+⋅⋅=+⎜⎟⎝⎠20一常力矩M 作用在绞车的鼓轮上,轮的半径为r ,质量为。
缠在鼓轮上绳索的末端A 系一质量为的重物,沿着与水平倾斜角为1m 2m α的斜面上升,如图所示。
重物与斜面间的滑动摩擦系数为μ。
绳索的质量不计,鼓轮可看成为匀质圆柱体,开始时系统静止。
求鼓轮转过ϕ角时的角速度。
解:为一自由度理想约束系统。
取鼓轮、重物及绳索组成的系统为研究对象,受力图如下图所示。
鼓轮转过ϕ角时系统的动能为2222212111222T m r m r 2ωω=⋅⋅+ 重力、摩擦力和力矩M 在此有限路程上所做的功为122sin W M Fr m gr ϕϕϕ→α=−−根据动能定理,有()222212211sincos 42m r m r M m gr ωωαμ+=−+αϕ⎡⎤⎣⎦ ω=绞车提升一质量为m 的重物,如图所示。
大学物理学(课后答案)第7章
⼤学物理学(课后答案)第7章第七章课后习题解答、选择题7-1处于平衡状态的⼀瓶氦⽓和⼀瓶氮⽓的分⼦数密度相同,分⼦的平均平动动能也相同,则它们[](A) 温度,压强均不相同(B)温度相同,但氦⽓压强⼤于氮⽓的压强(C)温度,压强都相同(D)温度相同,但氦⽓压强⼩于氮⽓的压强3分析:理想⽓体分⼦的平均平动动能τk= kT,仅与温度有关,因此当氦⽓和氮2⽓的平均平动动能相同时,温度也相同。
⼜由理想⽓体的压强公式p =nkT ,当两者分⼦数密度相同时,它们压强也相同。
故选( C)O7-2理想⽓体处于平衡状态,设温度为T,⽓体分⼦的⾃由度为i ,则每个⽓体分⼦所具有的[](A)动能为-kT (B)动能为丄RT2 2(C)平均动能为^kT (D)平均平动动能为^RT分析:由理想⽓体分⼦的的平均平动动能3 kT和理想⽓体分⼦的的平均动能2T⼆丄kT ,故选择(C)O27-3三个容器A、B、C中装有同种理想⽓体,其分⼦数密度n相同,⽽⽅均根1/2 1/2 1/2速率之⽐为V A : V B : V C 1:2:4 ,则其压强之⽐为P A : P B : P C[](A) 1:2:4 (B) 1:4:8 (C) 1 : 4 : 16 (D) 4:2:1分析:由分⼦⽅均根速率公式= J3RT,⼜由物态⽅程p = nkT ,所以当三容器中得分⼦数密度相同时,得p1: P2: P3 =T1 :T2 :T3 =1:4:16 O故选择(C)O7-4图7-4中两条曲线分别表⽰在相同温度下氧⽓和氢⽓分⼦的速率分布曲线。
如果(VP O和(V P 分别表⽰氧⽓和氢⽓的最概然速率,则[](A)图中a表⽰氧⽓分⼦的速率分布曲线且V P O z V P H= 4(B) 图中a表⽰氧⽓分⼦的速率分布曲线且V P O/ V P H? =1/4(C) 图中b表⽰氧⽓分⼦的速率分布曲线且V P O / V P H=1/4(D) 图中b表⽰氧⽓分⼦的速率分布曲线且V P O/ V P H2 =4分析:在温度相同的情况下,由最概然速率公式'..P=I j2RT及氢⽓与氧⽓的摩尔质量M H2£M o2,可知氢⽓的最概然速率⼤于氧⽓的最概然速率,故曲线a对应于氧分⼦的速率分布曲线。
第7章习题详细解答
第7章习题解答7—1判断题(对的打√,不对的打×)1。
数字电路分为门电路和时序逻辑电路两大类。
(× )2。
边沿触发器和基本RS触发器相比,解决了空翻的问题.(×)3. 边沿触发器的状态变化发生在CP上升沿或下降沿到来时刻,其他时间触发器状态均不变。
(√)4. 基本RS 触发器的输入端就是直接置0端和直接置1端。
(√)23 的计数器。
(×)5。
3位二进制计数器可以构成模为16。
十进制计数器最高位输出的周期是输入CP脉冲周期的10倍。
(√)7. 构成一个7进制计数器需要7个触发器。
(×)8.当时序电路存在无效循环时该电路不能自启动.( √)9。
寄存器要存放n位二进制数码时,需要n2个触发器。
(×)10.同步计数器的计数速度比异步计数器快。
(√)11。
在计数器电路中,同步置零与异步置零的区别在于置零信号有效时,同步置零还需要等到时钟信号到达时才能将触发器置零,而异步置零不受时钟的控制。
(√)12。
计数器的异步清零端或异步置数端在计数器正常计数时应置为无效状态。
(√)13。
自启动功能是任何一个时序电路都具有的。
(× )14。
无论是用置零法还是用置数法来构成任意N进制计数器时,只要置零或置数控制端是异步的,则在状态循环过程中一定包含一个过渡状态;只要是同步的,则不需要过渡状态。
(√)15。
用置零法或置位法可以设计任意进制的计数器.(×)7—2 由或非门组成的基本RS触发器如图7—38所示,已知R、S的电压波形,试画出与之对应的Q和Q的波形。
图7—38 题7-2图解:由或非门组成的基本RS触发器的特性表,可得该题的输出端波形如下图所示:或非门RS 触发器特性表 题7—2 波形图7—3由与非门组成的基本RS 触发器如图7-39所示,已知R 、S 的电压波形,试画出与之对应的Q 和Q 的波形。
图7-39 题7-3图解:由与非门组成的基本RS 触发器的特性表,可得该题的输出端波形如下图所示:与非门RS 触发器特性表 题7—3波形图7-4已知如图7-40所示的各触发器的初始状态均为0,试对应画出在时钟信号CP 的连续作用下各触发器输出端Q 的波形。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《无机化学》第7章习题参考答案一、填空题1.配位体,中心原子或中心离子,配位。
2.[Cu(NH3)4]2+,SO42+;离子键。
3.AgCl;[Ag(NH3)2]+,AgBr;[Ag(S2O3)2]3-,AgI;[Ag(CN)2]-。
二、选择题1.B2.A3.C4.C5.C6.A7.D8.D9.A 10.C三、是非题1.╳2.╳3. √4. ╳5.╳6. √7. ╳8. √四、问答题1. [Cr(H2O)4Cl2]Cl⋅2H2O ,[Cr(H2O)5Cl]Cl2⋅H2O ,[Cr(H2O)6]Cl32.试解释下列事实(1)[Ni(CN)4]2-配离子为平面正方形,[Zn(NH 3)4]2+配离子为正四面体。
Ni 2+3d4s4p在与CN -进行配位时,3d 轨道中的电子排列发生改变,8个电子挤入4个轨道中,空了一个3d 轨道,于是1个3d 轨道、1个4s 轨道和2个4p 轨道形成四个等价的dsp 2杂化轨道,每个dsp 2杂化轨道与配位体中的孤对电子所在的轨道重叠,形成4个配位键:dsp 2杂化dsp 2杂化轨道间夹角为90︒,因此,形成的4个配位键夹角也互成90︒,[Ni(CN)4]2-配离子的空间构型呈平面正方形。
Zn 2+的外层电子结构式为:Zn 2+3d4s4p在与NH 3进行配位时, 1个4s 轨道和3个4p 轨道形成四个等价的sp 3杂化轨道,每个sp 3杂化轨道与配位体中的孤对电子所在的轨道重叠,形成4个配位键:3dsp 杂化Sp 3杂化轨道呈四面体结构,因此,[Zn(NH 3)4]2+配离子为正四面体。
(2)单独用硝酸或盐酸不能溶解Au 或Pt 等不活泼金属,但用王水却能使其溶解。
因金或铂金属与其离子组成电对的电极电势很大,如V Au Au 50.1)/(3=+θϕ,金、铂单质很稳定。
尽管硝酸为强氧化性酸,但仍难氧化金、铂。
王水为浓硝酸与浓盐酸的混合酸,既有浓硝酸的强氧化性,又有高浓度的Cl -作配位剂,高浓度的Cl -可与Au 3+、Pt 4+形成配离子H[AuCl 4]、H 2[PtCl 6],从而降低了电对Au 3+/Au 、Pt 4+/Pt 的电势,使得金或铂可以与王水发生氧化还原反应而溶解。
反应式为:Au + HNO 3 +4HCl → H[AuCl 4] + NO + 2H 2O3Pt + 4HNO 3 + 18HCl → 3 H 2[PtCl 6] + 4NO + 8H 2O(3)Hg 2+能氧化Sn 2+,但在过量的I -存在下,Sn 2+却不能被Hg 2+氧化。
因θθϕϕ+++>242//Sn Sn Hg Hg ,所以Hg 2+能将Sn 2+氧化。
但如果加入过量的I -,则Hg 2+与I -形成[HgI 4]2-配离子,溶液中Hg 2+浓度变得很小,使得Hg Hg /2+ϕ下降,并且+++<242//Sn Sn Hg Hg ϕϕ,Hg 2+就不能氧化Sn 2+了。
(4)用NH 4SCN 溶液检验Co 2+时,如有少量Fe 3+存在,需加入NH 4F 。
Co 2+与SCN -形成蓝色配合物[Co(SCN)4]2-。
但Fe 3+与SCN -形成红色的配离子[Fe(SCN)n ]3-n ,会干扰检验。
当加入NH 4F 后,由于F-与Fe 3+形成更稳定的无色配离子[FeF 6]3-,避免了干扰。
3.用难溶电解质溶度积的大小和配离子的稳定常数的大小解释:在氨水中AgCl 能溶解,AgBr 微溶;而在Na 2S 2O 3溶液中AgCl 和AgBr 均能溶解。
难溶电解质在配位剂中的溶解度取决于难溶电解质的溶度积和形成的配合物的稳定常数大小,如果难溶电解质的溶度积不是很小而形成的配合物的稳定常数又比较大,则沉淀易溶解。
如果难溶电解质溶度积比较小,而配合物稳定常数又不大,则沉淀就比较难溶解。
这可以利用多重平衡规则计算沉淀转化为配合物的平衡常数来进行比较:AgCl + 2NH 3[Ag(NH 3)2]+ + Cl -371023101.3107.1108.1)])(([)(--+⨯=⨯⨯⨯=∙=NH Ag AgCl K K sp βθθAgBr + 2NH 3 [Ag(NH 3)2]+ +Br -671323105.8107.1100.5)])(([)(--+⨯=⨯⨯⨯=∙=NH Ag AgBr K K sp βθθAgBr 在NH 3水中转化为[Ag(NH 3)2]+反应平衡常数比AgCl 小,因此溶解度也小。
AgCl + 2S 2O 32- [Ag(S 2O 3)2]3- +Cl -313103232101.3107.1108.1)])(([)(⨯=⨯⨯⨯=∙=--O S Ag AgCl K K sp βθθAgBr + 2S 2O 32- [Ag(S 2O 3)2]3- + Br -5.8107.1100.5)])(([)(13133232=⨯⨯⨯=∙=--O S Ag AgBr K K sp βθθAgCl 和AgBr 在Na 2S 2O 3溶液中转化为[Ag(S 2O 3)2]3-的反应平衡常数都相对较大,所以均易溶。
五、计算题1.计算下列转化反应的K θ值,并判断转化反应能否进行。
(1)49132432432,243,2,243,105.1109.2103.4)])(([)])(([)()])(([)()])(([⨯=⨯⨯==⋅⋅=++++++NH Zn NH Cu Cu c NH Zn c Zn c NH Cu c K ββθ平衡常数较大,转化反应可以进行。
(2)12413024244,24,4,24,106.7105.2109.1)])(([)]([)]([)])(([)]([)]([-------⨯=⨯⨯==⋅⋅=CN Hg HgI I c CN Hg c CN c HgI c K ββθ平衡常数非常小,转化反应难以进行。
(3)67132332322232,23,23,3232,100.1107.1107.1)])(([)])(([)]([)])(([)]([)])(([⨯=⨯⨯==⋅⋅=+--+-NH Ag O S Ag O S c NH Ag c NH c O S Ag c K ββθ平衡常数较大,转化反应可以进行。
(4)413103232,3232,2232,103.3107.1108.11)])(([)(1)()])(([)]([------⨯=⨯⨯⨯=∙=⋅=O S Ag AgCl K Cl c O S Ag c O S c K sp βθθ平衡常数小,转化反应不易进行。
(5)72013224343,2,243,105.9102.2103.4)])([)])(([)]([)]([)])(([--+-+⨯=⨯⨯⨯=∙=⋅=OH Cu K NH Cu NH c OH c NH Cu c K sp θθβ 平衡常数很小,转化反应不易进行。
2.解:Ni 2+ + 4NH 3[Ni(NH 3)4]2+起始浓度(mol ⋅L -1) 0 0.80 0.05 平衡浓度(mol ⋅L -1) x 0.80+4x 0.05-x7443,2,243,101.9)480.0(05.0)]()[()])(([⨯=+-==++x x x NH c Ni c NH Ni c β 因x 很小,所以0.05-x ≈0.05 , 0.80+4x ≈0.8074101.980.005.0⨯=⨯x9103.1-⨯=x192,103.1)(--+⋅⨯=L mol Ni c19243,05.0103.105.0)])(([--+⋅=⨯-=L mol NH Ni c注:[Ni(NH 3)4]2+稳定常数是从其他教材查询得到,本教材未提供。
3.解:N i2+ + 2en [Ni(en)2]2+起始浓度(mol ⋅L -1) 0 0.90 0.05 平衡浓度(mol ⋅L -1) x 0.90+2x 0.05-x1322,2,22,109.6)290.0(05.0)]()[()])(([⨯=+-==++x x x en c Ni c en Ni c β 因x 很小,所以0.05-x ≈0.05 , 0.90+2x ≈0.90132109.690.005.0⨯=⨯x 16109.8-⨯=x1162,109.8)(--+⋅⨯=L mol Ni c11622,05.0109.805.0)])(([--+⋅=⨯-=L mol en Ni c与上题相比,由于Ni 2+与乙二胺形成的螯合物稳定常数更大,所以溶液中剩余的Ni 2+浓度更小。
注:[Ni(en)2]2+稳定常数是从其他教材查询得到,本教材未提供。
4.解:(1)Cu 2+ + 4NH3 [Cu(NH 3)4]2+ 起始浓度(mol ⋅L -1) 0 5.6 0.10 平衡浓度(mol ⋅L -1) x 5.6+4x 01-x13443,2,243,103.4)46.5(10.0)]()[()])(([⨯=+-==++x x x NH c Cu c NH Cu c β 因x 很小,所以0.10-x ≈0.10 ,5.6+4x ≈5.618104.2-⨯=x1182,104.2)(--+⋅⨯=L mol Cui c1183,6.5104.246.5)(--⋅=⨯⨯+=L mol NH c118243,10.0104.210.0)])(([--+⋅=⨯-=L mol NH Cu c(2)由于加入少量NaOH 固体,所以忽略溶液体积变化1,010.0)(--⋅=L mol OH c222182,2,104.2010.0104.2)]([)(---+⨯=⨯⨯=⋅=OH c Cu c Q202102.2])([-⨯=OH Cu K sp θ])([2OH Cu K Q sp θ<,无Cu(OH)2沉淀生成。
(3)20182,2,104.2010.0104.2)]([)(---+⨯=⨯⨯=⋅=S c Cuc Q36103.6)(-⨯=CuS K sp θ)(CuS K Q sp θ>,有CuS 沉淀生成。
5. 解:设NH 3⋅H 2O 起始浓度为cAgCl + 2NH 3 [Ag(NH 3)2] + Cl -平衡浓度(mol ⋅L -1) c-0.040 0.020 0.020)])(([)()]([)()])(([2323,,23,+-+∙=⋅=NH Ag AgCl K NH c Cl c NH Ag c K sp βθθ7102107.1108.1)040.0(020.0020.0⨯⨯⨯=-⨯-c 140.0-⋅=L mol c教材书后的计算题原答案部分有错误(计算过程见上),订正如下:第七章 五 1.(2)12106.7-⨯=θK2.192,103.1)(--+⋅⨯=L mol Ni c3.1162,109.8)(--+⋅⨯=L mol Ni c ,122,05.0)])(([-+⋅=L mol en Ni c 4.(3)20104.2)(-⨯=CuS Q。
