YBB30012012预灌封注射器用氯化丁基橡胶活塞
YBB30052012笔式注射器用溴化丁基橡胶活塞和垫片

288
不溶性微粒测定法 (YBB60022012)药用胶塞项下测定,每 1ml 中含 10µm 以上的微粒不得过 60 粒,含 25µm 以上的微粒不得过 6 粒。
【活塞滑动性试验】 取 10 个经硅油处理内表面的笔式注射器套筒,注水,装上试验用活 塞及垫片,加上铝帽,封口。将 1 个笔式注射器套筒安装于笔式注射器套筒夹持器(有平面和 活塞接触,夹持器必须确保能够穿刺安装在笔式注射器套筒上的垫片,注射针为一两端有刃口 的 皮 下 针 头 , 外 径 为 0.4mm, 当 活 塞 移 动 时 , 套 筒 内 的 水 应 能 通 过 该 针 排 出 ) 相 连 , 以 40mm/min±3mm/min 速度向下移动活塞,在笔式注射器套筒中移动一半距离时,暂停 5 秒钟, 然后将活塞完全压到底,其余笔式注射器套筒同法操作。记录每次试验中启动活塞的最大作用 力,取 10 个最大值的平均值作为“启动力”,应不得过 30N;记录每次试验中启动之后保持其移 动所需的力,取 10 个值的平均值作为“持续推动力”,应不得过 15N;记录每次试验中暂停 5 秒 钟后重新推动活塞的最大作用力,取 10 个最大值的平均值为“重新启动力”,应不得过 30N;并 检查在连续运动期间不得有“颤动”(指活塞的不规则运动)现象。
吸光度 取供试品液适量,用孔径 0.45μm 的滤膜过滤, 照紫外-可见分光光度法(中国药 典 2010 年版二部附录 IV A) 测定,在 220~360nm 波长范围内,最大吸光度不得大于 0.2。
预灌封注射器用氯化丁基橡胶活塞

YBB30012012预灌封注射器用氯化丁基橡胶活塞Yuguanfengzhusheqiyong Lühuadingjixiangjiao HuosaiChlorobutyl Rubber Plungers for Prefilled Syringes本标准适用于预灌封注射器用氯化丁基橡胶活塞。
活塞类型为扣合式(PSL)或螺纹式(PT)。
【外观】取本品数个,目视检测,表面色泽应均匀,不得有污点、杂质、气泡、裂纹、缺胶、粗糙、胶丝、胶屑、海绵状、毛边;不得有除边造成的残缺或锯齿现象;不得有模具造成的明显痕迹。
如果有浇道口,不应凸出于活塞的表面。
【鉴别】*(1)称取本品2.0g,剪成小颗粒,置坩锅中,加碳酸氢钠2.0g 均匀覆盖试样,置电炉上,缓缓加热至炭化,放冷,置马弗炉300℃加热至完全灰化,取出后,冷却至室温,加水10ml 使溶解,滤过,取续滤液1.5ml,置于试管中,加硝酸酸化,加入硝酸银试液1 滴,应产生白色沉淀。
(2)取本品适量,照包装材料红外光谱测定法(YBB60012012)第四法测定,应与对照图谱基本一致。
【活塞与推杆的配合性】、【活塞润滑性】、【活塞滑动性能】、【器身密合性】照预灌封注射器组合件(YBB40012012)项下的方法检查,应符合规定。
【灰分】取本品1.0g,照橡胶灰分测定法(YBB600212012)测定,不得过50%。
【挥发性硫化物】* 取本品,照挥发性硫化物测定法(YBB60052012)测定,应符合规定。
【不溶性微粒】取本品10 个,加微粒检查用水50ml,照包装材料不溶性微粒测定法(YBB60022012)药用胶塞项下测定,每1ml 中含10μm 以上的微粒不得过60 粒,含25μm 以上的微粒不得过6 粒。
【化学性能】供试品溶液的制备:取相当于表面积200cm2 的完整胶塞若干个,按样品外表面积(cm2)与水(ml)的比例1:2,加水浸没,煮沸5 分钟,放冷,再用同体积水冲洗5 次。
预灌封注射器在标准YBB001120042015中有哪些检测项目
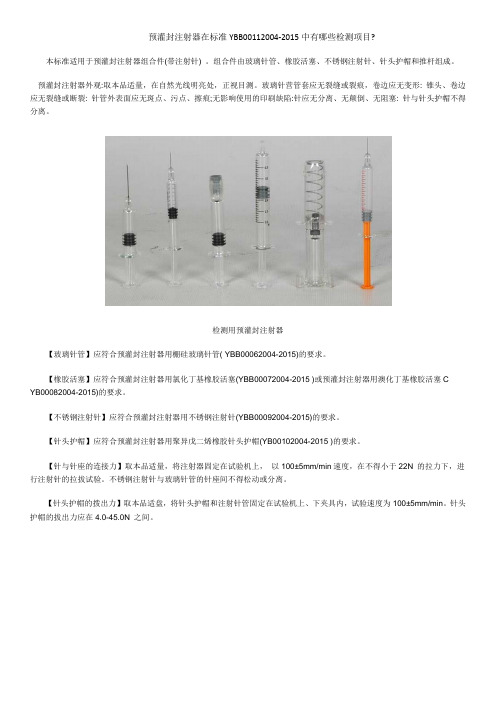
预灌封注射器在标准YBB00112004‐2015中有哪些检测项目?本标准适用于预灌封注射器组合件(带注射针) 。
组合件由玻璃针管、橡胶活塞、不锈钢注射针、针头护帽和推杆组成。
预灌封注射器外观:取本品适量,在自然光线明亮处,正视目测。
玻璃针营管套应无裂缝或裂痕,卷边应无变形: 锥头、卷边应无裂缝或断裂: 针管外表面应无斑点、污点、擦痕;无影响使用的印刷缺陷:针应无分离、无颠倒、无阻塞: 针与针头护帽不得分离。
检测用预灌封注射器【玻璃针管】应符合预灌封注射器用棚硅玻璃针管( YBB00062004-2015)的要求。
【橡胶活塞】应符合预灌封注射器用氯化丁基橡胶活塞(YBB00072004-2015 )或预灌封注射器用澳化丁基橡胶活塞CYB00082004-2015)的要求。
【不锈钢注射针】应符合预灌封注射器用不锈钢注射针(YBB00092004-2015)的要求。
【针头护帽】应符合预灌封注射器用聚异戊二烯橡胶针头护帽(YB00102004-2015 )的要求。
【针与针座的连接力】取本品适量,将注射器固定在试验机上,以100±5mm/min速度,在不得小于22N 的拉力下,进行注射针的拉拔试验。
不锈钢注射针与玻璃针管的针座间不得松动或分离。
【针头护帽的拨出力】取本品适盘,将针头护帽和注射针管固定在试验机上、下夹具内,试验速度为100±5mm/min。
针头护帽的拔出力应在4.0-45.0N 之间。
预灌封注射器测试仪器【活塞与推杆的配合性】(仅适用于带螺纹的活塞)取本品适量,将推杆和活塞相连接,把活塞完全插入经硅泊润滑过并装满一半水的预灌封注射器内,排除空气,在注射器上插上针头护帽,缓慢向后撤出约3 mm 的距离。
推杆应保持稳定,不应与活塞分离。
【活塞润滑性】取本品适量,将活塞插入硅泊润滑的注射器针管中,用推杆将活塞推入整个注射器针管中。
推杆活塞应平滑的移动,不应有突然的停顿。
【活塞滑动性能】取本品适量,将推杆活塞放入硅油润滑的针管中,以100±5mm/min的速度推动推杆。
注射液用氯化丁基橡胶塞及其制备方法

化胶 的性 能符合 要求
。
2, O 防老剂 MB 1 5 .,
一 表 5 优 化 配方 P M E D 硫化 胶 性 能
表 4 纳 米 高 岭 土 用 量 对 E D 硫 化 胶 性 能 的 影 响 PM
注: 同表 1 。
3 结 语
本 工作研 制 的打 印机送 纸胶 辊胶料 具有 良好
注 : ) 表 1注 3 。 基 本 配 方 为 E DM3 8 6 , P 1 同 ) P 00 0 E — D 3 6 4 , 氧 化 钛 M 02 O二 氧化锌 4 8 硬脂 酸 ., 3, O 白炭 黑 2 , 酸钙 2碳 1, 土 O陶 8 ,
的综 合 物理性 能 和耐臭 氧老化 性 能 。采 用优 化配 方试 制 的打 印机送 纸胶 辊 已经 在 多家打 印机制 造 厂试 用 , 能稳 定 , 映 良好 。 性 反
中 图分 类 号 : TQ3 3 6TQ3 6 4 3.; 3 . 文献标识码 : D
补强 填 充剂 3 , 色剂 ~5 着
1 ~ 10 硫 化 剂 0 0, O , 它 ~5 其
3 , ~5 活性 剂
1 5 ~。其 制备 步骤包
由江苏 博生 橡 塑有 限公 司 申请 的 专利 ( 利 专
号 C 0 4 7 8 , 开 日期 2 0 - 51 ) 注 N 1 129 0 公 0 90 - 3 “
括 配料 、 混炼 、 化 、 硫 冲切 、 洗和 包装 。该产 品性 清 能 指标 完 全 符 合 YB 0 4 2 0 B 0 0 - 0 5要 求 , 国外 与 同类 产 品技术 指标 相 当 。
收稿 日期 :0 91—5 2 0 —0 2
0 7硅 烷 偶 联 剂 KH一4 — 4 微 晶 石 蜡 ., 8 54 , 1 防 老 剂 MB 1 5 硫 化 剂 双 2 , ., 5
ybb预灌封注射器套筒标准

ybb预灌封注射器套筒标准
预灌封注射器的套筒,也称为针管,通常由高品质玻璃制成,以保证产品的安全性和可靠性。
YBB预灌封注射器套筒的标准主要遵循YBB00112004-2015的规定。
这些规定包括但不限于以下内容:
1.材质:套筒应采用符合医疗用途的优质玻璃材料制成,以确保其具有良好的化
学稳定性和生物相容性。
2.外观:套筒的外观应光滑、无气泡、无裂纹、无杂质,颜色均匀。
3.尺寸:套筒的尺寸应符合规定,包括长度、外径、内径等。
4.耐水性:套筒应具有良好的耐水性,能够在规定的条件下承受一定的水压而不
破裂。
5.内应力:套筒的内应力应符合规定,以确保其在使用过程中不会发生破裂或变
形。
此外,预灌封注射器的套筒还应符合其他相关标准,如YBB00062012(预灌封注射器用硼硅玻璃针管)等。
这些标准对套筒的材质、外观、尺寸、耐水性、内应力等方面都有详细的规定,以确保预灌封注射器的质量和安全性。
总之,YBB预灌封注射器套筒的标准旨在确保产品的质量和安全性,减少使用过程中的风险,保障患者的安全和健康。
注射液用氯化丁基橡胶塞
无变化
穿刺落屑
照注射剂用胶塞、垫片穿刺落屑测定(YBB00332004)第一法测定
照注射剂用胶塞、垫片穿刺落屑测定法(YBB60082012)第
一法测定
无变化
穿刺力
照注射剂用胶塞、垫片穿刺力测定(YBB00322004)第一法测定,
照注射剂用胶塞、垫片穿刺力测定法(YBB60072012)第一法测定,
包装材料不溶性微粒测定法
同“聚丙烯输液瓶”
2012药包材质量标准草案与2002标准汇编涉标准变更情况汇总表
品名
检验项目
2002标准汇编内容
2012标准草案修订内容增订来自况注射液用氯化丁基橡胶塞
/
本标准适用于……
本标准适用于……。
删去“的检验”
外观
照附表检查法检查
照表1依法检查
无变化
鉴别*(1)
/
/
无变化
(2)
照包装材料红外光谱测定法(YBB00262004)第四法测定
无变化
密封性与穿刺器保持性
用符合注射剂用胶塞、垫片穿刺力测(YBB00332004)
用符合注射剂用胶塞、垫片穿刺力测定法(YBB60072012)
无变化
灰分
800℃
修订为:“800±25℃”
挥发性硫化物*
易挥发性硫化物
删去“易”
不溶性微粒
表面积100cm2的“本品”若干个
修订为:表面积100cm2的“完整胶塞”若干个
无变化
注射液用氯化丁基橡胶塞
生物试验
热原*
急性全身毒性试验**
溶血**
附件一:注射液用氯化丁基橡胶塞检验项目中涉及的通用检验方法变化情况
YBB10032012笔式注射器用铝盖
YBB10032012笔式注射器用铝盖Bishizhusheqiyong LügaiCaps for Pen-injectors for Medical Use本标准适用于笔式注射器用铝盖。
本品是由橡胶垫片和铝帽两部分组成。
橡胶垫片应符合笔式注射器用氯化丁基橡胶活塞和垫片(YBB30042012)或笔式注射器用溴化丁基橡胶活塞和垫片(YBB30052012)的规定。
【外观】取本品适量,在自然光线明亮处目测,应清洁,无残留润滑剂、毛刺和损伤。
【配合性】取本品适量,盖在相适宜的装有标示容量水的笔式注射器用硼硅玻璃套筒(YBB00082012)上,用封盖装置封盖,应配合适宜。
【耐灭菌】取本品适量,封盖后置高压蒸汽灭菌器中,121℃±2℃30分钟,其中包含130℃±2℃5分钟。
铝帽表面应不出现断裂和异常变形。
【涂层牢固度】(适用于外表面有涂层的铝盖)取本品适量,经121℃±2℃30分钟,其中包含130℃±2℃5分钟高压蒸汽灭菌后,去除胶垫,用浸有80%乙醇溶液的脱脂棉擦拭表面30秒,再用浸有70%异丙醇溶液的脱脂棉拭表面30秒,涂层应无任何磨损。
【胶垫附着力】取本品适量,将本品顶端朝上放置于试验机上,通过一根直径略小于铝盖穿刺小孔的金属棒,以10mm/min±2mm/min的试验速度施加力至胶垫。
当胶垫在铝帽内发生移动时即刻读取试验机上的负载数值,胶垫从铝盖中分离力不得低于1.0N。
附件一:检验规则外观、配合性、耐灭菌、涂层牢固度、胶垫附着力的检验,按计数抽样检验程序第1部分:按接收质量限(AQL)检索的逐批检验抽样计划(GB/T2828.1-2003)的规定进行。
检验项目、检验水平及接收质量限,应符合表1的规定。
表1 检验项目、检验水平及接收质量限检验项目检验水平接收质量限(AQL)外观一般检验水平I 4.0配合性特殊检验水平S-2 4.0耐灭菌特殊检验水平S-2 4.0涂层牢固度特殊检验水平S-2 4.0胶垫附着力特殊检验水平S-2 4.0附件二:胶垫的规格尺寸(参考尺寸)类型A 类型B衬嵌密封模压胶垫图1 笔式注射器胶垫的构型表2 笔式注射器胶垫尺寸单位:mm公称容量ml 类型直径高度d1d2h11.5 A,B 7.1 min 7.8 max ±0.153 A,B 7.65±0.1 7.85 max1.54—6 B 9.85±0.15 10 max附件三:铝帽的规格尺寸应与笔式注射器用硼硅玻璃套筒(YBB00082012)相匹配。
预灌封注射器用溴化丁基橡胶活塞英文标准
预灌封注射器用溴化丁基橡胶活塞英文标准一、引言在医疗和药品生产领域,预灌封注射器是一种常用的药品输送设备。
为了确保注射器的安全性和可靠性,注射器活塞材料的选择是至关重要的。
溴化丁基橡胶被广泛应用于预灌封注射器活塞的制造中,其独特的性能使之成为首选材料之一。
本文将就预灌封注射器用溴化丁基橡胶活塞的英文标准进行探讨。
二、溴化丁基橡胶的特性溴化丁基橡胶具有良好的化学稳定性、耐油性和耐腐蚀性。
以下是溴化丁基橡胶的主要特性:1.耐药物溶液腐蚀:溴化丁基橡胶具有较好的耐药物溶液腐蚀性能,可以在各种化学环境下长时间稳定运行。
2.耐高温性能:溴化丁基橡胶可以在较高温度下保持材料的弹性和可靠性,适用于高温灭菌过程。
3.优异的封闭性能:溴化丁基橡胶活塞具有良好的封闭性能,能够有效防止药物泄漏和污染。
4.低溶胀率:溴化丁基橡胶活塞在接触药物后的溶胀率较低,有助于保持药物的稳定性和纯度。
三、预灌封注射器用溴化丁基橡胶活塞的英文标准为确保预灌封注射器用溴化丁基橡胶活塞的质量和可靠性,制定相应的英文标准是必要的。
以下是预灌封注射器用溴化丁基橡胶活塞的主要标准内容:3.1 材料要求预灌封注射器用溴化丁基橡胶活塞的材料要求如下:•橡胶材料应为纯度高、无异物和杂质的溴化丁基橡胶。
•材料应符合国际药典(例如USP、EP)或其他相关药典的相关要求。
3.2 尺寸要求预灌封注射器用溴化丁基橡胶活塞的尺寸要求如下:•活塞应具有符合设计要求的适当尺寸和形状。
•活塞底部应平整,无明显的瑕疵和缺陷。
•活塞与注射器筒体之间应有适当的配合间隙,以确保活塞在使用时的灵活性和流动性。
3.3 性能要求预灌封注射器用溴化丁基橡胶活塞的性能要求如下:•活塞应具有良好的可压缩性和回弹性能,以确保药液的准确注射和防止药物泄漏。
•活塞应具有良好的耐药物溶液腐蚀性能,在长时间的使用中不会发生物理或化学变化。
•活塞应具有合适的硬度,以确保使用时的灵活性和稳定性。
3.4 测试方法预灌封注射器用溴化丁基橡胶活塞的测试方法如下:1.外观检查:对活塞的外观进行检查,确保无明显的瑕疵和缺陷。
浅谈预灌封注射器的基本知识
浅谈预灌封注射器的基本知识发布时间:2021-09-22T07:04:07.939Z 来源:《医师在线》2021年5月10期作者:贾惠鹏[导读]贾惠鹏(扬子江药业集团江苏紫龙药业有限公司;江苏常州213000)摘要:预灌封注射器是一种新型的药用注射剂包装形式,在国内外被越来越多的厂家选择与应用。
预灌封注射器这种包装方式具有用药剂量更准确、保护使用者不受药液伤害、使用方便,无污染等优势,未来前景广阔。
预灌封注射器最早由美国BD公司研制成功,国内企业起步较晚,但发展势头良好,市场认可度与占有率逐年提升。
预灌封注射器最由针管、胶塞、推杆等部分组成,国内生产一般按YBB质量标准要求执行。
1.背景介绍随着国内仿制药一致性评价工作的逐步深入,越来越多的口服制剂的仿制药一致性评价工作被国内制剂企业纳入计划。
注射制剂产品相对于口服固体制剂来说,质量风险明显提高,国家食品药品监督管理总局药品审评中心发布的《化学药品注射剂仿制药质量和疗效一致性评价技术要求(征求意见稿)》中要求,“注射剂使用的包装材料和容器的质量和性能不得低于参比制剂,以保证药品质量与参比制剂一致”,这就对包装材料的安全性与稳定性提出了要求,而预灌封注射器是一种新型的注射剂包装形式,开始被越来越多的国内厂家选择与应用。
而之后国家药品监督管理局发布的《国家药监局关于开展化学药品注射剂仿制药质量和疗效一致性评价工作的公告》预灌封注射器发展提供了新的技术指导和法规依据。
2020年以来新冠疫情爆发,新冠疫苗的研发、生产在各主要国家蓬勃发展,作为包装材料的预灌封注射器需求量大增,带动了预灌封注射器产能全球供应不足,主要生产厂家纷纷制定扩产计划。
这一大趋势也刺激了中国预灌封注射器行业的发展,国内各大预灌封注射器生产企业也加大了资金投入力度,进行产能扩充。
2.产品优势预灌封注射器相比注射剂的其他包装形式,具有以下优点:(1)用药剂量更准确:对于粘度较大的注射液在使用过程中残留药液较多,预灌封式注射器可以最大限度的减少药液残留,用药剂量更加准确;(2)保护使用者不受药液伤害:对于一些特殊药物如果操作不当,易造成伤害。
笔式注射器用氯化丁基橡胶活塞质量控制及测试方法
摘要笔式注射器用氯化丁基橡胶活塞,本文将结合YBB30042012着重为您解读笔式注射器用氯化丁基橡胶活塞质量控制及标检测方法。
关键词笔式注射器活塞滑动性笔式注射器活塞泄漏性试验卡式瓶活塞滑动性试验橡胶活塞泄漏性试验卡式瓶质量检测胰岛素笔式注射器本文将结合国家食品药品监督管理局,国家药品包装容器(材料)标准之YBB30042012笔式注射器用氯化丁基橡胶活塞和垫片标准,着重为您解读笔式注射器用氯化丁基橡胶活塞质量控制及各项指标检测方法。
本检测方法适用于笔式注射器用氯化丁基橡胶活塞和垫片的检测。
笔式注射器用氯化丁基橡胶活塞,需对其穿刺落屑、泄漏试验、活塞滑动性试验进行分别测试,从而保证产品性能和质量。
1.【泄漏试验】取10 个经硅油处理内表面处理的笔式注射器套筒,注水,装上试验用活塞及垫片,加上铝帽,封口。
将1 个笔式注射器套筒安装于笔式注射器套筒夹持器(有平面和活塞接触),向活塞施加60N±3N 的作用力,保持1 分钟,试验结束后,检查活塞及垫片的泄漏情况。
其余笔式注射器套筒也同法操作,活塞及垫片部位不得有液体泄漏。
2.【活塞滑动性试验】取 10 个经硅油处理内表面的笔式注射器套筒,注水,装上试验用活塞及垫片,加上铝帽,封口。
将1 个笔式注射器套筒安装于笔式注射器套筒夹持器(有平面和活塞接触,夹持器必须确保能够穿刺安装在笔式注射器套筒上的垫片,注射针为一两端有刃口的皮下针头,外径为0.4mm,当活塞移动时,套筒内的水应能通过该针排出)相连,以40mm/min±3mm/min 速度向下移动活塞,在笔式注射器套筒中移动一半距离时,暂停5 秒钟,然后将活塞完全压到底,其余笔式注射器套筒同法操作。
记录每次试验中启动活塞的最大作用力,取10 个最大值的平均值作为“启动力”,应不得过30N;记录每次试验中启动之后保持其移动所需的力,取10 个值的平均值作为“持续推动力”,应不得过15N;记录每次试验中暂停5 秒钟后重新推动活塞的最大作用力,取10 个最大值的平均值为“重新启动力”,应不得过30N;并检查在连续运动期间不得有“颤动”(指活塞的不规则运动)现象。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
预灌封注射器用氯化丁基橡胶活塞
Yuguanfengzhusheqiyong Lühuadingjixiangjiao Huosai Chlorobutyl Rubber Plungers for Prefilled Syringes
本标准适用于预灌封注射器用氯化丁基橡胶活塞。 活塞类型为扣合式(PSL)或螺纹式(PT)。 【外观】 取本品数个,目视检测,表面色泽应均匀,不得有污点、杂质、气泡、裂纹、缺 胶、粗糙、胶丝、胶屑、海绵状、毛边;不得有除边造成的残缺或锯齿现象;不得有模具造成 的明显痕迹。如果有浇道口,不应凸出于活塞的表面。 【鉴别】*(1)称取本品 2.0g,剪成小颗粒,置坩锅中,加碳酸氢钠 2.0g 均匀覆盖试样, 置电炉上,缓缓加热至炭化,放冷,置马弗炉 300℃加热至完全灰化,取出后,冷却至室温,加 水 10ml 使溶解,滤过,取续滤液 1.5ml,置于试管中,加硝酸酸化,加入硝酸银试液 1 滴,应 产生白色沉淀。 (2)取本品适量,照包装材料红外光谱测定法 (YBB60012012)第四法测定,应与对照 图谱基本一致。 【活塞与推杆的配合性】、【活塞润滑性】、【活塞滑动性能】、【器身密合性】 照预灌封注 射器组合件(YBB40012012)项下的方法检查,应符合规定。 【灰分】 取本品 1.0g,照橡胶灰分测定法(YBB600212012)测定,不得过 50%。 【挥发性硫化物】* 取本品,照挥发性硫化物测定法 (YBB60052012)测定,应符合规 定。 【不溶性微粒】 取本品 10 个,加微粒检查用水 50ml,照包装材料不溶性微粒测定法 (YBB60022012)药用胶塞项下测定,每 1ml 中含 10µm 以上的微粒不得过 60 粒,含 25µm 以 上的微粒不得过 6 粒。 【化学性能】 供试品溶液的制备:取相当于表面积 200cm2 的完整胶塞若干个,按样品外 表面积(cm2)与水(ml)的比例 1:2,加水浸没,煮沸 5 分钟,放冷,再用同体积水冲洗 5 次。 移置于锥形瓶中,加同体积水,置高压蒸汽灭菌器中,升温至 121℃±2℃,保持 30 分钟,冷却 至室温,移出,即得供试品溶液,备用;并同时制备空白对照溶液。进行下列试验: 澄清度与颜色 取供试品溶液,依法检查(中国药典 2010 年版二部附录 IX B 和附录 IX A), 溶液应澄清无色。如显浑浊,与 2 号浊度标准液比较,不得更浓。如显色,与黄绿色 5 号标准 比色液比较,不得更深。 pH 变化值 取供试品溶液和空白对照溶液各 20 ml,分别加入氯化钾溶液(1→1000)1 ml, 照 pH 值测定法(中国药典 2010 年版二部附录Ⅵ H)测定,两者之差不得过 1.0。 吸光度 取供试品溶液适量,用孔径 0.45μm 的滤膜过滤,照紫外-可见分光光度法(中国 药典 2010 年版二部附录 IV A)测定,在 220~360nm 波长范围内,吸光度不得大于 0.2。 易氧化物 精密量取供试品溶液 20ml,精密加入 0.002mol/L 高锰酸钾滴定液 20ml 与稀硫酸 2ml,煮沸 3 分钟,迅速冷却,加碘化钾 0.1g,用硫代硫酸钠滴定液(0.01mol/L) 滴定至浅棕 色,再加入 5 滴淀粉指示液后滴定至无色。另取空白对照溶液同法操作,二者消耗硫代硫酸钠 滴定液(0.01mol/L)之差不得过 7.0 ml。 不挥发物 精密量取供试品溶液及空白对照溶液 100ml,分别置于已恒重的蒸发皿中,水浴
【生物试验】热原* 取本品,按不规则形状比例加入氯化钠注射液,置高压蒸汽灭菌器中 采用 115℃±2℃,保持 30 分钟,依法检查(YBB60232012),应符合规定。
急性全身毒性试验** 取本品,按不规则形状比例加入氯化钠注射液,置高压蒸汽灭菌器中 采用 115℃±2℃,保持 30 分钟,依法检查(YBB60252012),应符合规定。
如显色,与氯化铵溶液(取氯化铵 31.5mg 加无氯水适使溶解并稀释至 1000.0ml)2.0ml,加 空白提取液 8ml 与碱性碘化汞钾试液 2ml 制成的对照液比较,不得更深(0.0002%)。
锌离子 取供试品溶液,用孔径 0.45μm 的滤膜过滤,精密量取滤液 10ml,加 2 mol/L 盐酸 1ml 和亚铁氰化钾试液(称取 4.2g 亚铁氰化钾三水化合物,用水溶解并稀释至 100mL,摇匀,即 得,本品应临用新制)3 滴混合,不得显色;如显色,与标准锌溶液(称取 44.0mg 硫酸锌七水 化合物,用新煮沸并冷却的水溶解并稀释至 1000.0ml,本品应临用新配)3.0ml,加空白对照液 7ml 与 2 mol/L 盐酸 1ml 和亚铁氰化钾试液 3 滴对照液比较,不得更深(0.0003%)。
272
蒸干,在 105℃干燥至恒重,两者之差不得过 4.0mg。 重金属 精密量取供试品溶液 10ml,加醋酸盐缓冲液(pH3.5) 2ml,依法检查(中国药典
2010 版二部附录Ⅷ H 第一法)测定,不得过百万分之一。 铵离子 精密量取供试品溶液 10 ml,加碱性碘化汞钾试液 2ml,放置 15 分钟,不得显色;
电导率 在供试品溶液制备 5 小时内,用电导率仪测定:用水冲洗测定电极(光亮铂电极或 铂黑电极)数次,取空白对照溶液冲洗电极至少 2 次,测定空白对照溶液的电导率不得过 3.0µS/cm (20℃±1℃)。再用供试品溶液冲洗电极至少 2 次,测定供试品溶液的电导率,应不得过 40.0µS/cm。如果测定不是在 20℃±1℃下进行,则应对温度进行校正。
溶血** 取本品,依法检查(YBB60242012),溶血率应符合规定。
273
附件一:检验规则 1、产品检验分为全项检验和部分检验。 2、有下列情况之一时,应按标准的要求,进行全项检验。 (1)产品注册 (2)产品出现重大质量事故后,重新生产 3、有下列情况之一时,应按标准的要求,进行除 “**”外项目检验。 (1)监督抽验 (2)产品停产后,重新恢复生产 4、产品批准注册后,药包材生产、使用企业在原料产地、添加剂、生产工艺等没有变更的 情形下,可按标准的要求,进行除“*”、“**” 外项目检验。 5、外观的检验,按计数抽样检验程序 第 1 部分:按接收质量限(AQL)检索的逐批抽样 计划(GB/T2828.1—2003)规定进行,检验项目、检验水平及接收质量限见表 1。
