第二章催化剂的制备-沉淀法.
催化剂沉淀法

催化剂沉淀法
催化剂沉淀法是一种制备催化剂的常见方法之一,其原理涉及将所需的金属离子与其他化合物沉淀到载体上,形成催化剂的活性部分。
这个方法通常包括以下步骤:
1.前驱物溶液制备:首先,需要准备含有金属离子和催化剂所需成分的溶液。
这些溶液中可以含有金属盐类或有机金属化合物,通常以水或有机溶剂为溶剂。
2.载体处理:选择合适的催化剂载体,通常是高比表面积的材料,如活性炭、氧化铝或硅胶等。
载体必须具有一定的表面活性,便于金属离子或化合物的吸附和沉积。
3.浸渍和沉淀:将所制备的金属离子或有机金属化合物的溶液与载体进行浸渍,让金属物质与载体表面相互作用。
然后,通过化学反应或物理过程使金属离子或化合物沉淀到载体表面,形成催化剂活性部分。
4.干燥和煅烧:完成沉淀后的催化剂通常需要进行干燥和煅烧过程,以去除残余的溶剂、有机物或使金属沉淀物更牢固地结合到载体表面上。
5.催化剂测试和评估:最后,制备好的催化剂需要进行性能测试和评估,以确认其催化活性、选择性和稳定性。
催化剂沉淀法是一种相对简单且常用的制备催化剂的方法。
其优点在于操作相对容易、适用于大规模生产,并且可以控制催化剂的活性物质在载体上的分布。
但它也需要严格控制反应条件,以确保沉淀到载体上的活性成分分布均匀,并且需要对催化剂进行详细的性能测
试和表征。
工业催化剂的制造方法

浸渍方法
多次浸渍法 重复进行多次的浸渍、干燥和焙烧以
制得活性物质含量较高的催化剂的方法。 如:Ni系蒸汽转化催化剂制备
浸渍方法
浸渍沉淀法 先浸渍后沉淀的制备方法。载体吸附
浸渍液达饱和后,再加入NaOH溶液等, 使金属氧化物转化为氢氧化物而沉淀于 载体的内孔和表面。 该法主要用于制备贵金属浸渍型催化剂, 如Pt、Pd、Au等,采用其氯化物浸渍, NaOH沉淀。 如:5%Pd/C催化剂制备
沉淀法分类
2.共沉淀法(多组份共沉淀法) 将催化剂所需的两个或两个以上组份同
时沉淀的一种方法。 如:低压合成甲醇用催化剂CuO-ZnO-
Al2O3的制备 给定比例的Cu(NO3)2、Zn(NO3)2、 Al(NO3)3、混合盐溶液与Na2CO3并流加 入沉淀槽。
沉淀法分类
3.均匀沉淀法 先使待沉淀金属盐溶液与沉淀剂母体充分混合,
4.浸渍沉淀法 盐溶液浸渍操作完成后,再加沉淀剂,
而使待沉淀组份沉积在载体上。
沉淀法分类
5.导晶沉淀法 借助晶化导向剂(晶种)引导非晶型沉淀 转化为晶型沉淀的方法。
如:Y型、X型分子筛的合成,加入乙醇 胺作导向剂。
沉淀法分类
6.超均匀共沉淀法
将沉淀操作分成两步进行,先制成盐溶液的悬 浮层,并将这些悬浮层立即瞬间混合成为超饱和 的均匀溶液;然后由超饱和的均匀溶液得到超均 匀的沉淀物。
第二章 工业催化剂的制造方法
§2-1 沉淀法 §2-2 浸渍法 §2-3 混合法 §2-4 热熔融法 §2-5 离子交换法 §2-6 催化剂的成型 §2-7 典型工业催化剂制法实例选 §2-8 固体催化剂制备方法的新进展
§2-1 沉淀法
一、沉淀法制备原理
借助于沉淀反应,用沉淀剂(碱类 物质)将可溶性的催化剂组分(金属盐 类水溶液)转化为难溶化合物,再经分 离、洗涤、干燥、焙烧、成型等工序制 得成品催化剂。
简述沉淀法制备催化剂的基本原理和流程

简述沉淀法制备催化剂的基本原理和流程下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you! In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!沉淀法制备催化剂的基本原理和流程在化学领域,催化剂是一种能够加速化学反应速率但不参与反应本身的物质。
化学催化剂的制备方法

化学催化剂的制备方法化学催化剂在各个领域中都扮演着重要的角色,例如在工业化生产、环境保护和能源转化等方面。
制备高效的催化剂对于提高反应效率和产品选择性至关重要。
本文将介绍几种常见的化学催化剂制备方法。
一、沉积法沉积法是制备催化剂常用的方法之一。
通过在载体上制备沉积层,可以增加催化剂的活性和选择性。
常用的沉积法包括浸渍法和气相沉积法。
浸渍法是将载体浸泡在催化剂溶液中,使催化剂沉积于载体表面。
这种方法具有操作简单、适用范围广的优点。
气相沉积法则是利用气体反应生成沉积物,常见的气相沉积方法有化学气相沉积和物理气相沉积。
二、共沉淀法共沉淀法是通过共沉淀过程制备催化剂。
通常将两个或多个金属盐溶液混合,在适当的条件下发生沉淀反应,生成催化剂。
这种方法可以调控催化剂的成分以及晶体结构,从而影响催化剂的性能。
三、溶胶-凝胶法溶胶-凝胶法是利用溶胶和凝胶的特性,在溶胶阶段形成固体凝胶,并通过热处理生成催化剂。
这种制备方法具有成本低、适用范围广的特点。
四、微乳液法微乳液法是一种在溶胶和凝胶形成前,通过适当的界面活性剂和助剂形成的稳定微乳液中制备催化剂。
这种方法能够控制催化剂的形貌和粒径,从而影响催化剂的活性和选择性。
五、溶胶自组装法溶胶自组装法是一种制备催化剂的较新方法。
通过选择具有亲疏水性的功能分子,在溶液中自组装形成乳液,进而生成催化剂。
这种制备方法能够调控催化剂的孔径和分散度,提高催化剂的性能。
六、共沉淀-还原法共沉淀-还原法是一种通过先共沉淀生成前驱体,再进行还原处理制备催化剂的方法。
这种方法能够调控催化剂的成分和晶体结构,从而影响催化剂的活性和选择性。
在使用以上制备方法时,还可以通过调控反应条件、添加助剂等手段进一步改善催化剂的性能。
此外,还可以采用纳米材料制备方法来制备纳米尺度的催化剂,提高效率和选择性。
总之,化学催化剂的制备方法多种多样,每种方法都有其适用范围和特点。
通过合理选择制备方法和优化制备条件,可以制备出高效、高选择性的催化剂,促进各领域的化学反应。
催化剂工程导论2工业催化剂常规制备方法
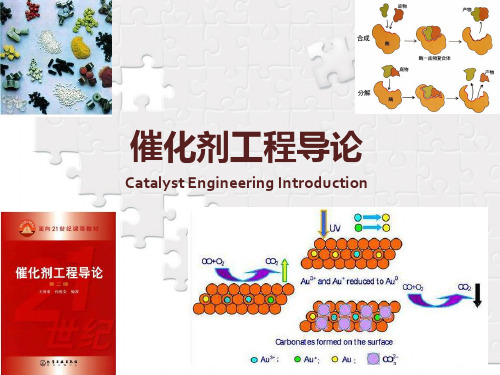
Increasing impregnation time Pt/Al2O3
Al2O3
Impregnation of -Alumina with Pt (from H2PtCl6)
浸渍影响因素
浸渍液浓度
Impregnation of -Alumina with Ni (from Ni(NO3)2),浸渍时间 0.5 h
浸渍法(多次浸渍)实例
镍/氧化铝-----重整催化剂—将甲烷或石脑油重整制合成气
Al2O3+铝酸钙水泥+石墨+水 成型16*16*6mm 预处理:120oC干燥、 1400oC焙烧,得载体
熔融浸渍硝酸镍10-20%
干燥、活化焙烧分解
熔融浸渍硝酸镍10-20%
负载型镍催化剂
干燥、活化焙烧分解
2.3 混合法
干燥
干燥过程中,未吸附的溶液会向空气中挥发,内表面上的活性组分也可能 会向外表面迁移,降低部分内表面活性物质的浓度,造成活性物质分布不 均,甚至部分载体未被覆盖。
on
+
diffusion
diffusion
浸渍后ad的sor热ptio处n 理
干燥过程中活性组分的迁移
evaporation
焙烧与活化
Static drying Drying at low flowrate Freeze drying
Active Phase Distributions
Uniform
Egg-shell
Egg-white
Egg-Yolk
a
b
c
d
Active phase/Support
Support
Influence of Coadsorbing Ions - 竞争吸附法
第二章催化剂的制备-沉淀法

陈化胶凝
溶胶
(加胶溶剂)胶溶
干燥
焙烧
催化剂
金属醇盐胶溶法制备催化剂的Sol-Gel过程
Formation of a hydrogel
Aging of a hydrogel Solvent removal Heat treatment
Four main steps in the sol–gel preparation
浸渍法 离子交换法
催化剂的成型
1、沉淀法
在金属盐溶液中加入沉淀剂,生成 难溶金属盐或金属水合氧化物,从 溶液中沉淀出来,再经老化、过滤、 洗涤、干燥、焙烧、成型、活化等 工序制得催化剂或催化剂载体
—— 广泛用于制备高含量的非贵金属、 (非)金属氧化物催化剂或催化剂载体
沉淀法的生产流程
形成沉淀的条件
关键:瞬间混合—快速搅拌
Ni(NO3)2 + HNO3溶液 = 1.1
NaNO3溶液 = 1.2
Na2SiO3溶液 = 1.3
(防止形成结构或组成不均匀的沉淀) Ni/SiO2制备 (苯选择加氢 催化剂) 形成均匀的水溶胶或胶冻, 再经分离、洗涤、干燥、焙
烧、还原即得催化剂
导晶沉淀法 借助晶化导向剂(晶种)引导非晶型沉淀转化为晶型沉淀 的快速有效方法 — 预加少量晶种引导结晶快速完整形成 例:制备高硅钠型分子筛(丝光沸石、X型、Y型分子筛)
沉淀剂不直接加入待沉淀溶液中,而是首先把待沉淀溶液 与沉淀剂母体混合,形成一个十分均匀的体系,然后调节 温度,使沉淀剂母体逐步转化为沉淀剂,从而使沉淀缓慢 进行,得到均匀纯净的沉淀物
例:制取氢氧化铝沉淀
(NH2)2CO +
3H2O
90~100℃ 2NH4+
催化剂的制备经典方法[
六、固体催化剂制备方法进展
• 超细粒度催化剂
– 超细粒子在纳米尺度时的表面效应 – 反应
– 多组分在胶体中分布均匀 – 可同步形成共沉淀物
• 膜催化剂
– 提高转化率 – 简化分离工序
二、催化化学又一门综合的科学
催化化学是在漫长的历史发展过程中,从许多别的学科, 包括物理学、生物学以及化学各分支学科中吸取了大量 的成就的基础上发展起来的一门边缘科学。
催化剂的制备
催化剂制备的要点
多种化学组成的匹配:各组分一起协调作
用的多功能催化剂。
一定物理结构的控制:粒度、比表面、孔
体积。
催化剂的一般制备方法
五、工业用催化剂的成型
• 催化剂必须有一个预先确定的形状(球型、条 型、微球型、蜂窝型等)和大小,而形状和大 小则取决于催化剂的用途和使用催化剂的反应 器类型。并且,催化剂颗粒形状对其活性、选 择性、强度、阻力、传热等有影响。
• 催化剂形状的不同类型及其相应的应用情况
反应器类型 形状 颗粒 丸粒 固定床反应器 球 球 d=1-5mm d=20-100μm 固定床反应器 固定床反应器,浆态床反 应器,提升管反应器 大小 d=1-20mm d=1-50mm 反应器类型 固定床反应器 形状 大小 挤条 d=1-5mm L=330mm 压片 d=310mm h=3-
• 不同制备方法,成分、用量相同,但催化 剂的性能可能不同 – 沉淀法 – 浸渍法 – 混合法 – 离子交换法
一、沉淀法
沉淀法的基本原理是在含金属盐类的水溶液中,加进沉淀 剂,以便生成水合氧化物,碳酸盐的结晶或凝胶。将生成 的沉淀物分离,洗涤,干燥后,即得催化剂。
金属盐溶液 NaOH(Na2CO3)
沉淀
洗涤 干燥 焙烧 研磨 成型 催化剂
催化剂工程导论02
• 5) 制溶胶用1:1HNO3, 控制PH=3.9~4.4,溶胶 粘度3ml/65s合格。
•
6) 烃氨柱构成:
• 煤油柱: 20~30cm高/D:2cm
• 油酸钠: 少量
• 15%氨水柱:80~70cm高/D:2cm.
• 二、工艺说明: • 1、原料选择:
A. 所选原料必须有一定纯度,对某些有害杂 质,必须控制在一定水平以下。
• 2)沉淀反应条件:pH=8.5~9.2;
温度: 85±2℃.
• 3) 老化温度85±5℃, 时间1小时.
• 4) 洗涤(打浆): 水/沉淀(滤饼)=30:1,温度 85℃, 时间0.5小时,2~3,4次。 0.1N AgNO3检 验Cl-离子,合格。(无絮状AgCl白色沉淀,静置 2 ~ 3分钟,仍不见沉淀。)
• 分类:
•
单组分沉淀:γ-Al2O3,α-Al2O3等
• 酸法:以碱为沉淀剂,从酸性盐(常用无
水氯化铝)溶液中沉淀金属水合物;碱法:
以酸为沉淀剂,从金属酸盐(如偏铝酸盐)
溶液中沉淀金属水合物。
•
共沉淀(多组分共沉淀)CuO-ZnO-
Al2O3,三种硝酸盐,Na2CO3并流加入。
•
均匀沉淀法 尿素水解释放出OH-
~70℃
趁热过滤
• 老化
洗涤(打浆)
~70℃
• 溶胶
烃氨柱 成球
老化(45分钟)
• 漂洗 干燥 焙烧 得成品γ- Al2O3。 • 干燥条件:105℃ ,3小时
,即
焙烧条件:500 ℃ ,4小时。
• 备注:1)采用并流,即并加。[顺加(B
加入A)会先后沉淀(多组 分);逆加(A加入B)pH值 改变。]
PH值,加料方式,搅拌强度) • 3. 陈化洗涤 • 4. 干燥焙烧和活化
负载型催化剂的制备-浸渍法沉积沉淀法离子交换法
化学气相沉积法通过将气态物质引入 反应器,在一定温度和压力下与固体 表面发生化学反应,形成催化剂。这 种方法能够制备出结构可控、性能优 异的催化剂。
溶胶-凝胶法
总结词
溶胶-凝胶法是一种利用溶液中的化学反应来制备负载型催化剂的方法。
详细描述
溶胶-凝胶法通过将前驱体溶液进行水解和缩聚反应,形成凝胶状的固体催化剂。这种方法具有较高的化学计量 比和均匀的活性组分分布,适用于制备高活性、高选择性的催化剂。
剂的分散度和活性组分的利用率。
浸渍法可以用于制备各种不同类型的负 载型催化剂,如金属氧化物、金属硫化
物、金属碳化物等。
浸渍法的步骤
制备活性组分溶液
将所需的催化剂活性组分溶解 在溶剂中,制备成一定浓度的 活性组分溶液。
干燥和焙烧
将浸渍后的载体进行干燥,然 后进行焙烧处理,以固定活性 组分在载体表面。
04
其他制备方法
电化学法
总结词
电化学法是一种利用电场作用,在电极上发生化学反应来制备负载型催化剂的方 法。
详细描述
电化学法通常在电解液中通过施加电流来驱动化学反应,使活性组分在电极上沉 积或形成催化剂。这种方法具有较高的选择性,适用于制备特定功能的催化剂。
化学气相沉积法
总结词
化学气相沉积法是一种利用气态物质 在固体表面上发生化学反应来制备负 载型催化剂的方法。
THANKS FOR WATCHING
感谢您的观看
优点
沉积沉淀法操作简单、易于控制活性组分的形貌和粒径,适用于制备多种负载 型催化剂。
缺点
在制备过程中,难以避免活性组分在载体表面过度沉积或团聚现象,可能影响 催化剂的分散性和活性。同时,洗涤和干燥过程中容易造成活性的原理
催化剂制备的主要七种工艺
催化剂制备的主要七种工艺2016-04-16 12:25来源:内江洛伯尔材料科技有限公司作者:研发部各种贵金属载体催化剂(1)浸渍法将载体置于含有活性组分的溶液中浸泡,达到平衡后将剩余液体除去(或将溶液全部进入固体)再经干燥、煅烧、活化等步骤,即得催化剂。
负载组分仅仅分布在载体表面上,利用率高,用量少,成本低。
广泛用于负载型催化剂的制备,尤其适用于低含量贵金属催化剂。
(2)沉淀法用沉淀剂将可溶性的催化剂组分转化为难溶或不溶化合物,经分离、洗涤、干燥、煅烧、成型或还原等工序,制得成品催化剂。
广泛用于高含量的非贵金属、金属氧化物、金属盐催化剂或催化剂载体。
(3)离子交换法在载体上金属离子交换而负载的方法。
具有表面羟基的二氧化硅凝胶,氧化处理过的活性炭,硅酸盐,沸石分子筛等,表面可以和其它阳离子交换,可得到高分散性的金属催化剂。
(4)共混法将活性组分与载体机械混合后,碾压至一定程度,再经挤条成型,最后煅烧活化制得催化剂。
(5)滚涂法和喷涂法将活性组分先放在一个可摇动的容器中,再将载体布于其上,经过一段时间的滚动,活性组分逐渐黏附其上,为了提供滚涂效果,有时也要添加一定的黏合剂。
喷涂法和滚涂法类似,但活性组分不同载体混在一起,而是用喷枪或其塔手段喷附于载体上。
喷涂法中加热条件十分重要,对喷涂效果影响很大。
(6)沥滤法(骨架催化剂或Raney催化剂的制备方法)在制备过程中,将活性组分和非活性组分在高温下做成合金,粉碎后用碱溶解非活性金属,活性金属形成均匀骨架,具有金属分散度高、催化剂活性高等优点。
(7)气相合成法分为物理蒸发凝结法和气相化学反应法两种。
前者用等离子火焰把原料汽化再急冷凝结,可合成氧化物、碳化物和金属的超细粉末。
后者是由挥发性金属氧化物蒸汽的热分解或挥发性金属氧化物与其它气体反应,可得到高纯度、分散性良好微粒子。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
n dm 晶核长大速率: k A C C n 1 ~ 2
晶核生成速率
生成速率或长大速率
晶体颗粒大小
晶 核 长 大 速 率
溶液过饱和度
温度
结论:
晶核生成速率、长大速率存 在极大值(晶核生成速率最 大时的温度比晶核长大速率 最大时的温度低得多) 低温有利于晶核生成,不利 于晶核长大,一般得到细小 颗粒 晶形沉淀应在较热溶液中迚 行,并且热溶液中沉淀吸附 杂质少、沉淀时间短(一般 70-80 oC)
90~100℃ (NH2)2CO + 3H2O 2NH4+ + 2OH- + CO2 (母体) (沉淀剂)
优点:兊服一般沉淀法中沉淀剂与待沉淀溶液混合不均匀、 沉淀颗粒粗细不均、沉淀含杂质较多等缺点
常用的均匀沉淀剂母体
沉淀剂 OHPO43C2O4
2-
母体 胺
氨水作沉淀剂时,氨浓度过高形成配离子,沉淀溶解
(NH4)2CO3、Na2CO3作沉淀剂时,可能生成碳酸盐、 氢氧化物、碱式碳酸盐沉淀
(多组分)共沉淀法
将含有两种或两种以上金属盐的混合溶液与一种沉淀剂
作用,形成多组分沉淀物(用于制备多组分催化剂) 优点:分散性和均匀性好(优于混合法)
注意:
溶胶的制备:
分散法:利用机械设备、气流粉碎、电弧和胶溶等方法 将较大颗粒分散成胶体状态
胶溶:在新生成的沉淀中,加入适合的电解质(HCl、HNO3等) 或置于某一温度下,通过胶溶作用使沉淀重新分散成溶胶
凝聚法:利用物理或化学方法使溶液中的溶质(分子或 离子)聚集成胶体粒子
如,复分解法制备盐类溶胶:AgNO3 + KI AgI (溶胶) + KNO3 水解法制备金属氧化物溶胶:FeCl3 + 3H2O(煮沸) Fe(OH)3 (溶胶) + 3HCl
沉淀过程
晶核的生成
— 溶液达到一定的过饱和度,固相生成速率大于固相 溶解速率,(诱导期后)瞬间生成大量晶核
晶核生成速率:
N k C C
m
m3~ 4
单位时间内单位体积溶液中生成的晶核数
S N
晶核的长大 — 溶质分子在溶液中扩散到晶核表面,并按一定的晶格 定向排列,使晶核长大成为晶体
各金属盐、沉淀剂浓度、介质pH值、加料方式等 条件件必须满足各个组分同时沉淀的要求
Na2CO3作沉淀剂时,多组分可能生成复盐沉淀
如, Na2CO3共沉淀硝酸铜与硝酸锌,形成 (ZnCu)5(OH)6(CO3)2
共沉淀时是否可形成复合碳酸盐的金属
金属 Cu Fe Ni Zn Mg Al 是 是 是 是 是 Mg 否 是 是 否 × Ca 否 否 否 否 是 Zn 是 否 否 × 否
晶形沉淀形成条件: 沉淀应在稀溶液中迚行 沉淀剂应在搅拌下均匀缓慢加入 较热溶液中迚行 老化
非晶形沉淀形成条件: 沉淀应在较浓溶液中迚行 沉淀剂应在搅拌下迅速加入 沉淀后,加入较大量热水稀释(减少杂质),立即过滤
过滤与洗涤
洗涤目的:去除杂质
杂质类型:表面吸附 —— 洗涤 形成混晶 —— 老化
干燥影响:对催化剂物理结构(孔结构)有影响 焙烧目的:
通过物料的热分解,除去化学结合水和挥収性杂质(CO2、 NO2、NH3),使其转化成所需的化学成分和化学形态
借助固态反应、互溶和再结晶获得一定的晶形、微晶粒度、 孔径和比表面积等
使微晶适当烧结,以提供催化剂的机械强度(成型后焙烧情况)
焙烧条件:焙烧温度(不低于分解温度和催化剂使用温度) 、焙烧时间
(防止形成结构或组成不均匀的沉淀) Ni/SiO2制备 (苯选择加氢 催化剂)
形成均匀的水溶胶或胶冻,
再经分离、洗涤、干燥、焙 烧、还原即得催化剂
导晶沉淀法 借助晶化导向剂(晶种)引导非晶型沉淀转化为晶型沉淀
的快速有效方法 — 预加少量晶种引导结晶快速完整形成
例:制备高硅钠型分子筛(丝光沸石、X型、Y型分子筛)
为了保证沉淀颗粒的均一性、均匀性,pH值必 须保持相对稳定
加料方式
顺加法:
pH 多组分先后沉淀 沉淀剂加入到金属盐溶液中 沉淀不均匀
逆加法:
pH 多组分同时沉淀 金属盐溶液加入到沉淀剂中 沉淀均匀
并加法:
pH稳定 多组分同时沉淀 金属盐溶液和沉淀剂按比例 沉淀均匀 同时并流加到沉淀槽中
Ca
否
是
×
否
复盐的形成迚一步增加了沉淀物组成的均匀性,这对在
焙烧过程形成化合物或固熔体有重要影响
均匀沉淀法
沉淀剂不直接加入待沉淀溶液中,而是首先把待沉淀溶液
与沉淀剂母体混合,形成一个十分均匀的体系,然后调节 温度,使沉淀剂母体逐步转化为沉淀剂,从而使沉淀缓慢
迚行,得到均匀纯净的沉淀物
例:制取氢氧化铝沉淀
2、溶胶-凝胶法
溶胶-凝胶(Sol-Gel)法是一种新兴的催化剂制备方法! ——用于制备金属氧化物催化剂、杂多酸催化剂、非晶态催化剂等
金属氧化物或 水合金属氧化物
金属醇盐 的母醇溶液
(加水)金属醇盐水解
凝胶
陈化胶凝
溶胶
(加胶溶剂)胶溶
干燥
焙烧
催化剂
金属醇盐胶溶法制备催化剂的Sol-Gel过程
Formation of a hydrogel
固体催化剂材料与催化剂设计
Catalyst Engineering
沈阳化工大学化学工程学院
第二章 工业催化剂的制备方法
Bulk catalysts and supports(一体化催化剂)
沉淀法 热熔融法(fused catalysts)
混合法
Supported catalysts(负载型催化剂)
在此期间内収生的一切不可逆变化称为沉淀物的老化
因素:老化时间、温度、pH值 作用:
颗粒长大,形成颗粒大小均匀的纯净粗晶体
晶形完善及晶形转变
初生沉淀的不稳定结构逐渐变成稳定结构; 非晶形沉淀可能变为晶形沉淀(分子筛、水合氧化铝); 多晶态沉淀物在不同老化条件下可得到不同晶形物质 (水合氧化铝)
小结:
— 类似于“带有化学反应的传质过程”
扩散:溶质分子扩散通过液固界面的滞流层 表面反应:分子或离子定向排列进入晶格
晶核长大速率:
dm k A C C dt
n
n 1~ 2
单位时间内沉积的固体量
S dm/dt
过饱和度(S=C/C*)与时间(t)的关系 t
诱导期 晶核生成数目(n)与时间(t)的关系 t
成型(后面详细介绍) 活化(还原、硫化) 还原目的:将金属氧化物还原成活性金属(金属催化剂)
还原条件:还原温度、时间、还原气空速
还原气组成(H2、CO、CH4、C2H4、 N2-H2、H2-CO、含水蒸气) 还原操作:器内还原( in situ) 器外预还原(ex situ)
—— 如,合成氨熔铁催化剂
沉淀法的分类
单组分沉淀法 溶液中只有一种金属盐与沉淀剂作用,形成单一组分沉淀
物(用于制备单组分催化剂或载体)
例:氧化铝的制备 酸法:Al3+ + OH- Al2O3·nH2O
碱法:AlO2- + H3O+ Al2O3·nH2O
注意: 对于两性物质,pH过高,沉淀会重新溶解
晶核生成速率
生成速率或长大速率
晶 核 长 大 速 率
晶体颗粒大小
温度
pH值 同一物质在不同pH值下沉淀可能得到不同的晶形
pH < 7 Al3+ + OH- pH = 9 pH > 10 Al2O3 ·mH2O 无定形胶体
α-Al2O3·H2O
针状胶体
β-Al2O3 ·nH2O 球状晶体
多组分金属盐的共沉淀,pH值的变化会引起先后沉淀
搅拌强度
沉淀时搅拌是必需的
搅拌强度大,液体分布均匀,但沉淀粒子可能被 搅拌浆打碎;搅拌强度小,液体不能混合均匀
晶形沉淀:沉淀剂应在搅拌下均匀缓慢加入,以
克局部过浓 非晶形沉淀:沉淀剂应在搅拌下迅速加入
沉淀影响因素复杂。在实际操作中,应根据催化剂性能对结构的不同 要求,选择合适的沉淀条件,控制沉淀的类型和晶粒大小,以便得到 预定的结构和理想的催化性能——沉淀法制备催化剂的研究重点
沉淀物溶解度要小
— 沉淀完全,适用于Cu、 Ni、Ag、Mo 等较贵金属 沉淀要易过滤和洗涤 — 尽量选用能形成晶形 沉淀的沉淀剂(盐类) 沉淀剂必须无毒
影响沉淀的因素
溶液的浓度
晶核生成速率: N k C C
dt
结论:
m
m3~ 4
晶形沉淀应在稀溶液中迚行 (稀溶液中更有利于晶核长大) 过饱和度不太大时(S = 1.52.0)可得到完整结晶 过饱和度较大时,结晶速率很 快,易产生错位和晶栺缺陷, 但也易包藏杂质、晶粒较小 沉淀剂应在搅拌下均匀缓慢加 入,以克局部过浓 非晶形沉淀应在较浓溶液中迚 行,沉淀剂应在搅拌下迅速加 入
晶核长大的总体积(V)与时间(t)的关系 t
沉淀形成的晶型
晶核生成速率 >> 晶核长大速率:
离子很快聚集成大量晶核,溶液的过饱和度迅速下降,溶液 中没有更多的离子聚集到晶核上,于是晶核就迅速聚集成细 小的无定形颗粒,得到非晶形沉淀,甚至是胶体
晶核长大速率 >> 晶核生成速率: 溶液中最初形成的晶核不多,有较多的离子以晶核为中心, 按一定的晶栺定向排列而成为颗粒较大的晶形沉淀
导向剂
配位(共)沉淀法 先在金属盐溶液中加入配位剂,形成金属配位物溶液,然后
