有效碰撞和活化分子
高中化学考点37 化学反应速率-备战2022年高考化学考点一遍过

考点37 化学反应速率一、化学反应速1.定义化学反应速率是用来衡量化学反应进行快慢的物理量。
2.表示方法通常用单位时间内反应物浓度的减少量或生成物浓度的增加量来表示。
数学表达式为v=ct∆∆,单位为mol/(L·min)、mol/(L·s)或mol/(L·h)。
3.化学反应速率与化学计量数的关系:对于已知反应m A(g)+n B(g)p C(g)+q D(g),其化学反应速率可用不同的物质来表示,当单位相同时,化学反应速率的数值之比等于方程式中各物质的化学计量数之比,即v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q。
例如:在一个2 L的容器中发生反应:3A(g)+B(g)2C(g),加入2 mol A,1 s后剩余1.4 mol,则v(A)=0.3 mol·L−1·s−1,v(B)=0.1 mol·L−1·s−1,v(C)=0.2 mol·L−1·s−1。
过关秘籍(1)在同一化学反应中,无论选用反应物还是生成物表示化学反应速率,其值均为正值。
(2)化学反应速率通常是指在某一段时间内的平均反应速率,而不是某一时刻的瞬时反应速率。
(3)同一化学反应中,在相同的反应时间内,不同的物质表示的反应速率的数值可能不同。
但表示的意义相同。
因此表示化学反应速率时,必须指明是用反应体系中的哪种物质作依据。
(4)固体或纯液体的浓度恒为常数,不能用固体或纯液体的浓度表示化学反应速率。
但是化学反应速率与固体和纯液体参与反应的表面积有关,因此,通常增大固体或纯液体参与反应的表面积(如将固体粉碎,将液体变成雾状,加速搅拌等)可加快化学反应速率。
(5)同一化学反应中,各物质表示的化学反应速率之比=化学方程式中各物质的化学计量数之比=各物质的浓度变化量之比。
4.化学反应速率的测定(1)测定原理测定不同反应时刻反应物或生成物的浓度,可通过观察和测量体系中的某一物质的相关性质,再进行适当的转换和计算达到测定目的。
《化学反应原理》知识点大全

《化学反应原理》知识点大全第一章、化学反应与能量考点1:吸热反应与放热反应1、吸热反应与放热反应的区别特别注意:反应是吸热还是放热与反应的条件没有必然的联系,而决定于反应物和生成物具有的总能量(或焓)的相对大小。
2、常见的放热反应①一切燃烧反应;②活泼金属与酸或水的反应;③酸碱中和反应;④铝热反应;⑤大多数化合反应(但有些化合反应是吸热反应,如:N2+O2=2NO,CO2+C=2CO等均为吸热反应)。
3、常见的吸热反应①Ba(OH)2·8H2O与NH4Cl反应;②大多数分解反应是吸热反应③等也是吸热反应;④水解反应考点2:反应热计算的依据1.根据热化学方程式计算反应热与反应物各物质的物质的量成正比。
2.根据反应物和生成物的总能量计算ΔH=E生成物-E反应物。
3.根据键能计算ΔH=反应物的键能总和-生成物的键能总和。
4.根据盖斯定律计算化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应的途径无关。
即如果一个反应可以分步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的。
温馨提示:①盖斯定律的主要用途是用已知反应的反应热来推知相关反应的反应热。
②热化学方程式之间的“+”“-”等数学运算,对应ΔH也进行“+”“-”等数学计算。
5.根据物质燃烧放热数值计算:Q(放)=n(可燃物)×|ΔH|。
第二章、化学反应速率与化学平衡考点1:化学反应速率1、化学反应速率的表示方法___________。
化学反应速率通常用单位时间内反应物浓度和生成物浓度的变化来表示。
表达式:___________ 。
其常用的单位是__________ 、或__________ 。
2、影响化学反应速率的因素1)内因(主要因素)反应物本身的性质。
2)外因(其他条件不变,只改变一个条件)3、理论解释——有效碰撞理论(1)活化分子、活化能、有效碰撞①活化分子:能够发生有效碰撞的分子。
②活化能:如图图中:E1为正反应的活化能,使用催化剂时的活化能为E3,反应热为E1-E2。
【知识解析】活化能

活化能1 基元反应与反应历程基元反应:一个化学反应往往经过多个反应步骤才能实现,每一步反应都称为基元反应。
反应历程:与某化学反应有关的一组基元反应反映了该反应的反应历程,反应历程又称反应机理。
自由基:像上述反应历程中的I·一样,带有单电子的原子或原子团叫自由基,如O·自由基。
2 有效碰撞与活化能(1)碰撞和有效碰撞碰撞特点①碰撞次数非常巨大;②不是每次碰撞都能发生化学反应有效碰撞概念能够发生化学反应的碰撞发生有效碰撞的条件①反应物分子必须具有一定的能量;②有合适的碰撞取向。
如反应2HI===H2+I2中分子碰撞示意图如图2-1-2所示:图2-1-2有效碰撞的实质有效碰撞能使化学键断裂,自由基可以重新组合形成新的化学键,从而发生化学反应(2)活化分子和活化能活化分子发生有效碰撞的分子必须具有足够的能量,这种能够发生有效碰撞的分子叫做活化分子活化能活化分子具有的平均能量与反应物分子具有的平均能量之差,叫做反应的活化能活化能与反应热E1——活化能E2——活化分子变成生成物分子放出的能量E1-E2——反应热(即ΔH)活化能与化学反应速率的关系在一定条件下,活化分子所占的百分数是固定不变的。
活化分子所占的百分数越大,单位体积内活化分子数越多,单位时间内有效碰撞的次数越多,化学反应速率越大。
可简略表示:活化能降低→普通分子变成活化分子→活化分子百分数增大→单位时间内有效碰撞的次数增多→化学反应速率增大3 运用有效碰撞理论解释外界条件对化学反应速率的影响(1)运用有效碰撞理论解释浓度对化学反应速率的影响其他条件不变时,对某一反应来说,活化分子在反应物分子中所占的百分数是一定的,增大反应物浓度→单位体积内活化分子的数目增多→单位时间内有效碰撞次数增多→化学反应速率增大。
(2)运用有效碰撞理论解释温度对化学反应速率的影响其他条件不变时,升高温度,反应物分子的能量增加,使一部分原来能量较低的分子变成活化分子(如图2-1-4所示)→活化分子百分数增加→单位时间内有效碰撞次数增多→反应速率增大。
《化学反应原理》复习知识清单1-4章
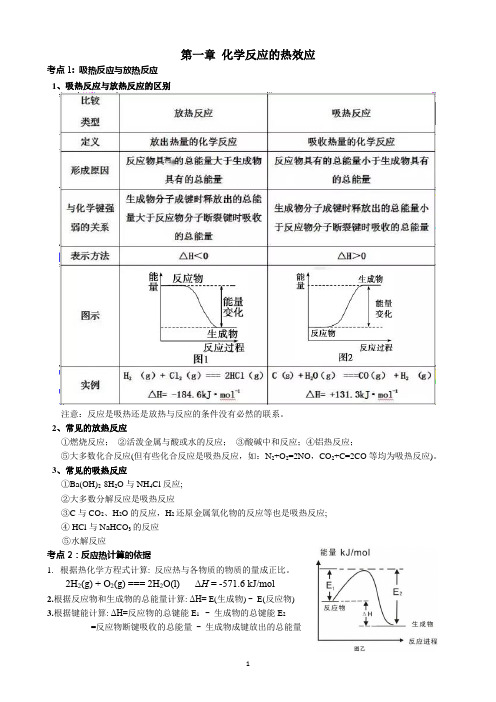
第一章化学反应的热效应考点1: 吸热反应与放热反应1、吸热反应与放热反应的区别注意:反应是吸热还是放热与反应的条件没有必然的联系。
2、常见的放热反应①燃烧反应;②活泼金属与酸或水的反应;③酸碱中和反应;④铝热反应;⑤大多数化合反应(但有些化合反应是吸热反应,如:N2+O2=2NO,CO2+C=2CO等均为吸热反应)。
3、常见的吸热反应①Ba(OH)2·8H2O与NH4Cl反应;②大多数分解反应是吸热反应③C与CO2、H2O的反应,H2还原金属氧化物的反应等也是吸热反应;④ HCl与NaHCO3的反应⑤水解反应考点2:反应热计算的依据1.根据热化学方程式计算: 反应热与各物质的物质的量成正比。
2H2(g) + O2(g) === 2H2O(l) ΔH = -571.6 kJ/mol2.根据反应物和生成物的总能量计算: ΔH= E(生成物) - E(反应物)3.根据键能计算:ΔH=反应物的总键能E1 - 生成物的总键能E2=反应物断键吸收的总能量- 生成物成键放出的总能量4.根据盖斯定律计算:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应的途径无关。
如图:ΔH 1=ΔH 2+ΔH 3盖斯定律的主要用途是用已知反应的反应热来推知相关反应的反应热。
5.根据物质燃烧热进行计算6.中和热测定实验原理:中和热ΔH =-第二章 化学反应速率与化学平衡考点1:化学反应速率 1、化学反应速率的表示方法其常用的单位是mol/(L·min) 或 mol/(L·s) 2、影响化学反应速率的因素1)内因(主要因素):反应物本身的性质。
2)外因(其他条件不变,只改变一个条件)3、理论解释——有效碰撞理论 (1)活化分子、活化能、有效碰撞①活化分子:具有足够能量、能引发有效碰撞的分子。
②活化能:E 1为正反应的活化能,E 2为逆反应的活化能 E 3为使用催化剂时的活化能反应热ΔH =E 1-E 2。
2021人教版高中化学选修4第二章同步课时(导)学案2.2 影响化学反应速率的因素
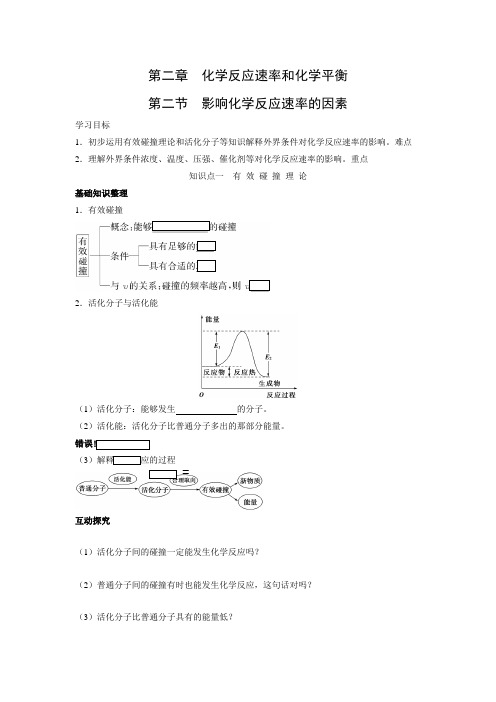
第二章化学反应速率和化学平衡第二节影响化学反应速率的因素学习目标1.初步运用有效碰撞理论和活化分子等知识解释外界条件对化学反应速率的影响。
难点2.理解外界条件浓度、温度、压强、催化剂等对化学反应速率的影响。
重点知识点一有效碰撞理论基础知识整理1.有效碰撞2.活化分子与活化能(1)活化分子:能够发生的分子。
(2)活化能:活化分子比普通分子多出的那部分能量。
错误!(3)解释化学反应的过程=互动探究(1)活化分子间的碰撞一定能发生化学反应吗?(2)普通分子间的碰撞有时也能发生化学反应,这句话对吗?(3)活化分子比普通分子具有的能量低?(4)化学反应的实质是分子的重新组合?归纳总结1.活化分子与有效碰撞的关系能够发生有效碰撞的一定是活化分子,但是活化分子不一定发生有效碰撞。
并不是反应物分子之间的任何一次直接碰撞都能发生反应,只有那些能量相当高的分子之间的直接碰撞才能发生反应。
2.单位体积内的活化分子数与活化分子百分数单位体积内的活化分子数就是指单位体积内能量达到一定要求的活化分子的总数;而活化分子百分数是活化分子数与总分子数的比值,总分子数包含:活化分子数以及普通分子的个数。
3.活化能与化学反应速率的关系活化能大小主要是由反应物自身的性质决定的改变外界条件也可以改变反应的活化能,如加入催化剂,即反应物自身的性质影响着化学反应所需的活化能,从而影响化学反应速率的大小。
例如:活化能小→普通分子容易变成活化分子→活化分子百分数大→单位体积内活化分子数多→单位时间、单位体积内有效碰撞次数多→化学反应速率大内因对化学反应速率的影响。
即时训练1.有效碰撞是指A.反应物分子间的碰撞B.反应物活化分子间的碰撞C.反应物分子发生合适取向的碰撞D.活化分子之间发生合适取向的碰撞2.下列说法正确的是①活化分子间的碰撞一定能发生化学反应;②普通分子间的碰撞有时也能发生化学反应;③反应物活化能越大,反应越快;④化学反应的实质是原子的重新组合;⑤化学反应的实质是旧化学键的断裂和新化学键的形成过程;⑥化学反应的实质是活化分子有合适取向时的有效碰撞。
单介绍关于活化能的定义`碰撞理论 `过渡状态理论,以图更好地

εi kBT
2
exp(−
εi kBT
ki
exp(−
εi kBT
)
)
−
i
εi kBT
2
exp(−
εi kBT
)
exp(− ε i )
=
Ea RT 2
=
Ea kB N AT 2
i
kBT
(18)
也就有
∑ ∑ kiε i ni
ε i ni
∑ ∑ Ea = N A ( i
−i ki ni
ni ) = N A (ε活化分子 − ε分子)= E活化分子 − E
exp RT
(10)
式中E0为绝对零度时势能面上活化络合体与反应物内能之差。
4
按式(1),得活化能
Ea = E0 + nRT
(11)
E0值并不能直接得到,因为位能面得到的位垒Eb是在位能面上沿最低能量途
径上鞍点与反应物分子势能底部的位能差值。关系为
∑ ∑ E0 = Eb +1/ 2(
hν
≠ 0
−
hν 0 )N A
浅谈活化能
徐立谦
(西北大学化学系 05 级材料化学专业 西安 710069)
摘 要:活化能是一个非常重要但其本质的解释却模糊不清的概念。本文通过简 单介绍关于活化能的定义、碰撞理论 、过渡状态理论,以图更好地理解活化能 这一概念。 关键字:反应速率 活化能 碰撞理论 过渡状态理论
一 引 言[1]
活化能是 1889 年前瑞典科学家阿仑尼乌斯(Arrhenius)最早提出的概念,它 在化学中具有重要的意义。但就其定义和本质,不同学者意见不同。例如,关于 对活化能概念的解释,至少有三类意见:
第2章第1节课时2影响化学反应速率的因素-导学案-2021-2022学年高二化学人教版选择性必修1

第二课时影响化学反应速率的因素学习目标:1.运用有效碰撞和活化分子模型描述和解释化学反应速率的影响因素。
(难点)2.理解浓度、温度、压强、催化剂等外因对化学反应速率的影响。
(重点)一、有效碰撞理论1.有效碰撞(1)概念:能够的碰撞。
(2)条件:具有足够的和合适的。
(3)与反应速率的关系:碰撞的频率越高,反应速率越。
2.活化分子与活化能(1)活化分子:能够发生碰撞的分子。
(2)活化能:活化分子比普通分子多出的那部分能量。
E1是E1—E2是关系:普通分子+ 成为活化分子(3)解释化学反应的过程二、影响化学反应速率的因素1.浓度影响规律。
其它条件不变时,增大反应物浓度,增大反应物浓度,单位体积内活化分子总数,有效碰撞几率,反应速率。
2.压强影响规律:对于有气体参加的化学反应,在相同温度下,缩小容器体积,气体压强增大,气体分子浓度,有效碰撞几率,反应速率。
相反减小气体压强,反应速率。
(2)理论解释。
压强增大→单位体积内活化分子总数→反应速率。
3.温度(1)影响规律。
其他条件不变时,反应速率,降低温度反应速率。
(2)理论解释。
温度升高,使普通分子吸收能量成为分子,因而活化分子百分数,有效碰撞的几率,反应速率。
4.催化剂(1)影响规律。
其他条件不变时,使用合适的催化剂,可化学反应速率。
(2)理论解释。
使用催化剂,改变反应途径,正催化剂降低反应的活化能,使活化分子百分数,有效碰撞的几率,反应速率。
5.其他因素对化学反应速率的影响如光辐照、放射线辐照、超声波、电弧、强磁场、高速研磨、增大反应物接触面积等,均会对化学反应速率产生影响。
例题1.判断正误(正确的打“√”,错误的打“×”)。
(1)随温度升高活化分子百分数增大,反应速率一般逐渐加快。
()(2)锌与稀H2SO4反应时,硫酸的浓度越大,产生H2的速率越快。
()(3)化学反应中,催化剂不参加化学反应,但可以改变反应速率。
()(4)密闭容器中反应A(g)+B(s)===C(g)+D(s),加入B物质后反应速率会加快。
新课程高考化学高中化学重难点复习教案化学反应速率及影响因素之活化能影响化学反应速率的因素

化学反应速率及影响因素之活化能影响化学反应速率的因素1.影响化学反应速率的因素:(1)内因(主要因素):反应物本身的__性质__。
(2)外因(其他条件不变,只改变一个条件)。
2.理论解释——有效碰撞理论:(1)活化分子、活化能、有效碰撞。
①活化分子:能够发生__有效碰撞__的分子。
②活化能(如下图):图中E1为__活化能__,使用催化剂时的活化能为__E3__,反应热为__E2-E1__。
③有效碰撞:活化分子之间能够引发__化学__反应的碰撞。
(2)活化分子、有效碰撞与反应速率的关系。
特别提醒:(1)分析外界因素对化学反应速率的影响时3注意:①催化剂在化学反应过程中参与了反应,降低了正、逆反应的活化能,同等程度改变正、逆反应速率,但不会改变反应的限度和反应热。
②升高温度正反应速率和逆反应速率都加快,但加快的程度不同;降低温度正反应速率和逆反应速率都减慢,但减慢的程度不同,吸热反应的反应速率总是受温度影响大。
③对于固体和纯液体反应物,其浓度可视为常数,改变用量速率不变。
但当固体颗粒变小时,其表面积增大将导致反应速率增大。
(2)压强对反应速率的影响情况:压强只对有气体参与的化学反应速率有影响。
①恒温时,压缩体积――→引起压强增大――→引起反应物浓度增大――→引起反应速率加快。
②恒温时,对于恒容密闭容器。
a .充入气体反应物――→引起气体反应物浓度增大(压强也增大)――→引起反应速率加快。
b .充入“惰性”气体――→引起总压强增大―→反应物浓度未改变―→反应速率不变。
③恒温恒压时。
充入“惰性”气体――→引起体积增大――→引起气体反应物浓度减小――→引起反应速率减小。
3.化学反应速率图象及应用 (1)全程速率—时间图象①如Zn 与足量盐酸的反应,反应速率随时间的变化出现如图情况原因解释:AB 段(v 渐大),因为该反应为__放热__反应,随着反应的进行,__温度__逐渐升高,导致反应速率__逐渐增大__;BC 段(v 渐小),则主要原因随着反应的进行,溶液中__c (H+)__逐渐减小,导致反应速率__逐渐减小__。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
具有较高能量,能够发生有效碰撞的分子
发生有效碰撞的分子一定是活化分子, 结论:
但活化分子的碰撞不一定是有效碰撞。
推论: 有效碰撞次数的多少与
单位体积内反应物中活化分子 的多少有关。
问题:
活化分子的多少又与什么有关?
2、活化能
活化分子高出反应物分子平均能量 的部分
其中E1为活化能
E2-E1是反应热
结论:
活化分子的多少与该反应的活化能的大小有关, 活化能的大小是由反应物分子的性质决定。
内因
推论:
活化能越小则一般分子成为活化分子越容易, 则活化分子越多, 则单位时间内有效碰撞越多, 发生反应, 而有的不能发生反应?与哪些因 素有关系?
一、有效碰撞理论
1、什么是有效碰撞?
引起分子间的化学反应的碰撞。
结论:
某一化学反应的速率大小与
单位时间内有效碰撞的次数有关
2、发生有效碰撞的条件
1)发生碰撞的分子具有较高的能量。 2)分子在一定的方向上发生碰撞。
二、活化分子和活化能理论
