《反应热的测量与计算》教案(苏教版选修4)
最新化学复习方略 选修4配套课件:1.1.2 反应热的测量与计算 能源的充分利用(苏教版)

)
【思路点拨】解答本题时要注意以下两点: (1)标准燃烧热所对应的可燃物的化学计量数为 1。
(2)稳定化合物:C→CO2(g)、H2→H2O(l)。
【解析】选D。A项、B项中标准燃烧热所对应的产物应是稳定的 化合物,分别是CO2(g)和H2O(l),故A、B错误;C项,标准燃烧
热所对应的可燃物的物质的量不是1 mol,故C错误。
测定反应前后溶液的温度 使反应充分进行、体系的温度均匀 保温作用 反应容器
2.反应热的计算——盖斯定律 (1)内容:
一个化学反应,无论是一步完成,还是分几步完成,其总的热 完全相同 。 效应_________
始态 和_____ 终态 有关,而与 (2)本质:化学反应的焓变只与反应的_____ 途径 无关。如图所示: 反应的_____
3.等量的氢气完全燃烧生成液态水比生成气态水状态不同,能量不同:气态 >液态>固态。 4.如果一个化学方程式通过其他几个化学方程式相加减而得到, 则该反应的焓变为相关化学反应的焓变的代数和。( )√
分析:由盖斯定律的内容可知,一步反应可以看做几步反应的 加和,其焓变也是如此。
5.在101 kPa时,1 mol C燃烧生成CO,所放出的热量就是碳的 标准燃烧热。 (× )
分析:C的标准燃烧热所对应的产物应为CO2(g)。
一、标准燃烧热和中和热的理解
1.标准燃烧热的含义
2.标准燃烧热与中和热的比较
【特别提醒】(1)书写表示某物质燃烧热的热化学方程式时,该 物质的化学计量数为1,故其他物质的化学计量数可能为整数, 也可能为分数。 (2)表示标准燃烧热和中和热时,文字表达时用“正值”,用 ΔH表达时,数值前一定带“-”号。如甲烷的标准燃烧热为
(3)意义:如25 ℃、101 kPa时,甲烷的标准燃烧热Δ H= 说明在101 kPa条件下1 mol甲烷完全燃烧 -890.3 kJ·mol-1,_____________________________________ 生成CO2(g)和H2O(l)时放出890.3 kJ的热量 。 ______________________________________
高中化学 1.1.2《反应热的测量与计算》学案 苏教版选修4

高中化学 1.1.2《反应热的测量与计算》学案 苏教版选修4第二课时 反应热的测量与计算[课标解读]1, 初步学习测定化学反应的反应热的实验方法,能正确分析误差产生的原因并能采用适当措施减小误差。
2,知道盖斯定律的内容,能运用盖斯定律计算化学反应的反应热。
[知识再现]知识点一:什么是燃烧热、中和热?如何正确书写燃烧热、中和热的热化学方程式?知识点二:什么是盖斯定律?如何利用盖斯定律计算反应热?知识点三:如何测定反应热?[典型解悟][例1] 已知反应:① 2C(s)+O 2(g)=2CO(g) ΔH =-221 kJ /mol② 稀溶液中,H +(aq)+OH -(aq)=H 2O(l) ΔH =-57.3 kJ /mol下列结论正确的是A .碳的燃烧热大于110.5 kJ /molB .①的反应热为221 kJ /molC .稀硫酸与稀NaOH 溶液反应的中和热为57.3 kJ /molD .稀醋酸与稀NaOH 溶液反应生成1 mol 水,放出57.3 kJ 热量[例2] 已知H 2(g)+Cl 2(g)=2HCl(g) △H =―184.6kJ·mol -1, 则反应HCl(g)=12H 2(g)+12Cl 2(g)的△H 为A .+184.6kJ·mol -1B .―92.3kJ·mol -1C .―369.2kJ·mol -1D . +92.3kJ·mol -1例3] 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。
通过测定反应过程中所放出的热量可计算中和热。
回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃用品是。
(2)烧杯间填满碎纸条的作用是。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会;(填“偏大”、“偏小”、“无影响”)。
2019最新苏教版化学选修4《反应热的测量与计算能源的充分利用》教案

2019最新苏教版化学选修4《反应热的测量与计算能源的充分利用》教案 第1单元 第2课时(本栏目内容,在学生用书中以活页形式分册装订!)一、选择题1.(2008年高考)植物及其废弃物可制成乙醇燃料,下列关于乙醇燃料的说法中错误的是( )A .它是一种再生能源B .乙醇易燃烧,污染小C .乙醇只能在实验室内作燃料D .粮食作物是制乙醇的重要原料【解析】 乙醇是一种常见燃料,是可再生能源;乙醇燃烧污染小,可用作汽车燃料;粮食发酵可生成乙醇,这也是酿酒的主要反应。
【答案】 C2.在25 ℃、101 kPa 下,1 g 甲醇燃烧生成CO 2和液态水时放热22.68 kJ,下列热化学方程式正确的是( )A .CH 3OH(l)+32O 2(g)===CO 2(g)+2H 2O(l) ΔH =+725.8 kJ/molB .2CH 3OH(l)+3O 2(g)===2CO 2(g)+4H 2O(l)ΔH =-1 452 kJ/molC .2CH 3OH(l)+3O 2(g)===2CO 2(g)+4H 2O(l)ΔH =-725.8 kJ/molD .2CH 3OH(l)+3O 2(g)===2CO 2(g)+4H 2O(l)ΔH =+1 452 kJ/mol【解析】 甲醇的摩尔质量为32 g/mol,1 g 甲醇相当于132mol 。
1 mol 甲醇燃烧生成CO 2和液态水时放出的热量为22.68 kJ/g ×32 g =725.8 kJ,表示为ΔH =-725.8 kJ/mol,A 、D 选项符号错,C 选项方程式中的甲醇为2 mol,与热量值不对应,只有B 选项符合题意。
【答案】 B3.(江苏高考)下列各组热化学方程式中,化学反应的ΔH 前者大于后者的是( ) ①C(s)+O 2(g)===CO 2(g) ΔH 1C(s)+12O 2(g)===CO(g) ΔH 2 ②S(s)+O 2(g)===SO 2(g) ΔH 3S(g)+O 2(g)===SO 2(g) ΔH 4③H 2(g)+12O 2(g)===H 2O(l) ΔH 5 2H 2(g)+O 2(g)===2H 2O(l) ΔH 6④CaCO 3(s)===CaO(s)+CO 2(g) ΔH 7CaO(s)+H 2O(l)===Ca(OH)2(s) ΔH 8A .①B .④C .②③④D .①②③【解析】 由所给热化学方程式及ΔH 的含义可以判断ΔH 1<ΔH 2、ΔH 3>ΔH 4、ΔH 5>ΔH 6、ΔH 7>ΔH 8,故选C 。
苏教版高中化学选修4《反应热的测量与计算》参考课件

1.如何设计实验得到以上所需数据?
⑴盐酸和氢氧化钠溶液的浓度和量取的体积要取定值。
⑵准确测量反应前后的温度值。
反应热的测量
第8 页
二、盐酸与NaOH溶液反应的反应热的测定 2.实验装置应该满足什么条件?
使用绝缘装置,避免热量散失到反应体系外 ——保温杯……
盐酸与氢氧化钠溶液混合后液面上方的空间尽可能小
A 思考:由起点A到终点B有多少条途径? 从不同途径由A点到B点的位移有什么关系?
反应热的计算
一、盖斯定律 1、盖斯定律内容 一个化学反应,不论是一步完成,还是分几 步完成,其总的热效应是完全相同的。
2、图解盖斯定律
ΔH
A
B
ΔH1
ΔH2
C
ΔH、ΔH1、ΔH2之间有何关系? ΔH=ΔH1+ΔH2
第 15 页
第 19 页
反应热的计算
二、由反应热书写热化学反应方程式,或比较焓变大小
第 20 页
3、沼气主要成分是 CH4 ,0.5 mol CH4 完全燃烧生成CO2和液态水时放出
445 kJ热量,则下列热化学方程式中正确的是 ( C )
A、2CH4(g)+4O2(g)===2CO2(g)+4H2O(l) ΔH=890 kJ·mol-1 B、CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=890 kJ·mol-1 C、CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1 D、1/2CH4(g)+O2(g)===1/2CO2(g)+H2O(l) ΔH=-890 kJ·mol-1
“偏小”或“无影响”)。 (4)实验中若改用60 mL 0.50 mol·L-1盐酸和50 mL 0.55 mol·L-1烧碱溶液进行
高中化学 1.1《反应热的测量与计算》教案 苏教版选修4
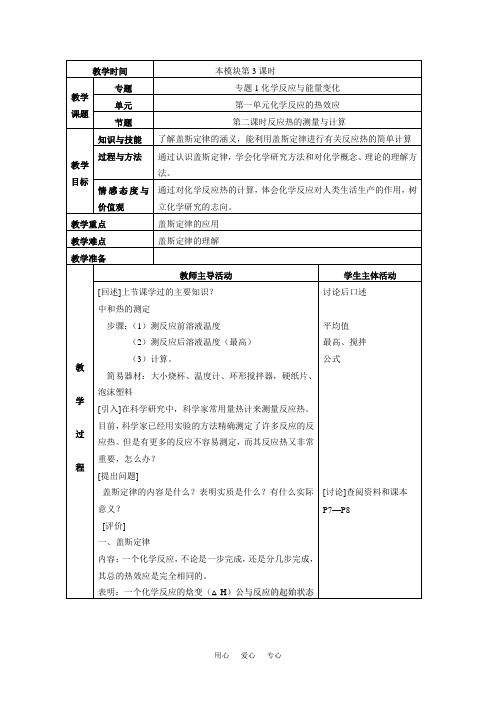
C(固、金刚石) + O2(气) == CO2(气) 回答有关问题: (1) 计算 C(石墨) +
1 O2(g) == CO(g) 的焓变 2
(2) 现有 18 克 C(石墨)粉在氧气燃烧后生成 CO2(气)、CO(g) ,其体积比 2:1, 求比完全燃烧损失的热量是多少? (3) 石墨转化为金刚石的热化学方程式是: (4)石墨和金刚石相比较,__________的稳定性更大。
教
教师主导活动
学生主体活动
用心
爱心
专心
学 过 程
[板书] (1) C(石墨) + O2(g) == CO2(g) CO(g)+ ΔH= -393.51 kJ/mol
整理,记笔记。
1 O2(g) == CO2(g) ΔH= -283.0 kJ/mol 2 1 O2(g) == CO(g) ΔH= -110.5 kJ/mol 2 1 O2(g) == CO2(g) ΔH= -283.0 kJ/mol 2
141.5kJ 有两种做法
两式相减得, C(石墨) +
(2)18 克 C(石墨)粉在氧气燃烧后生成 CO(g)为 0.5 mol CO(g)+ 0.5 mol (3) C(石墨) + O2(g) == CO2(g) C(金刚石) + O2(气) == CO2(气) 两式相减得 C(石墨) == C(金刚石) ΔH= +1.7 kJ/mol 从能量上看两种物质转化 较为容易, 但实际远不是这 样的, 所以化学反应还要考 虑其它方面。 [练习]: 1、某次发射火箭,用 N2H4(肼)在 NO2 中燃烧,生成 N2、 液态 H2O。已知: N2(g)+2O2(g)==2NO2(g) △ H=+67.2kJ/mol 2N2H4(g)+4NO2(g)==3N2(g) +4H2O(l) △ H=-399.6kJ/mol ΔH= -393.51 kJ/mol ΔH= -395.41 kJ/mol
苏教版化学选修4《反应热的测量与计算》ppt课件

1
24.5 25.0 24.75 26.5 1.75
2
3
22.0 22.4 22.2 25.4
25.0 25.4 25.2 28.2
3.2
3.0
ΔH = -
0.418 (t2-t1) 0.025
kJ/mol
理论上:强酸、强碱稀溶液反应: H+(aq)+OH-(aq)=H2O(l); △H= — 57.3kJ/moL [议一议]为何所测得的数据不是57.3 kJ/mol, 分析产生误差的原因。
ΔH1= -283.0 kJ/mol
ΔH2= -285.8 kJ/mol
③.C2H5OH(l) + 3 O2(g) ==== 2 CO2(g) + 3Байду номын сангаасH2O(l) ΔH3= -1370 kJ/mol
试计算④.2CO(g)+ 4 H2(g)==== H2O(l)+ C2H5OH(l) 的ΔH ①×2 + ②×4 - ③ = ④ 所以,ΔH=ΔH1×2 +ΔH2×4 -ΔH3 =-283.2×2 -285.8×4 +1370 =-339.2 kJ/mol
P(s、红磷)+5/4O2(g)=1/4P4O10(s) H2= -738.5 kJ/mol
试写出白磷转化为红磷的热化学方程式 P4(s、白磷)=4 P(s、红磷) H = -29.2 kJ/mol 。
练2、使18g焦炭发生不完全燃烧,所得气体中CO占 体积,CO2占
1 3
已知:C(S)+
CO(g)+ A、1/3Q1KJ C、1/3(Q1+Q2)KJ
练习课本P8 问题解决
你知道神七的火箭燃料是什么吗?
例2:发射火箭时,用N2H4(肼)在NO2中燃烧,生成 N2、液态H2O。已知: N2(g)+2O2(g)==2NO2(g)△H1=+67.2kJ/mol
【三维设计】高中化学 第一部分 专题1 第一单元 第二课时 反应热的测量与计算课件 苏教版选修4
[例2] (2011·海南高考)已知:2Zn(s)+ O2(g)===2ZnO(s) ΔH=-701.0 kJ·mol-1 2Hg(l)+ O2(g)===2HgO(s) ΔH=-181.6 kJ·mol-1
则反应Zn(s)+HgO(s)===ZnO(s)+Hg(l)的ΔH为
A.+519.4 kJ·mol-1 C.-259.7 kJ·mol-1
第二课时 反应热的测量与计算
1.一个公式(中和反应反应热的计算): ΔH=-cmnΔtH×2O10 -3 kJ·mol-1, 其中 c=4.18 J/(g·℃)
2.一个定律(盖斯定律): 一个化学反应,不论是一步完成,还是分几步完成, 其总的热效应是完全相同的。 3.两个概念: (1)标准燃烧热:101 kPa下,1 mol物质完全燃烧的反 应热。 (2)热值:101 kPa下,1 g物质完全燃烧放出的热量。
(√ )
(4)开发利用新能源有:太阳能、风能、氢能、潮汐
能、生物质能、电能。
(×)
2.标准燃烧热及热值 (1)标准燃烧热: ①定义:101 kPa下,1 mol 物质完全燃烧的反应热。 ②表示意义: CH4(g)+2O2(g)===CO2(g)+2H2O(l)
ΔH=-890.31 kJ·mol-1, 表示在101 kPa条件下, 1 mol CH4完全燃烧生 成 CO2(g)和 H2O(l) 时放出的热量是 890.31 kJ 。
[答案] (1)环形玻璃搅拌棒 (2)250 mL容量瓶 (3)3.4℃ (4)相等 偏小
改变酸、碱的用量,反应生成的 H2O 的量改变,反 应放出的热量也随之改变,但 ΔH=-nHQ2O kJ·mol-1 不变,即 ΔH 与酸、碱的用量无关。
提示:(1)不能,因 为铁能消耗H+而影 响实验结果。 (2)保温效果不好, 会有热量损失,使 中和反应反应热ΔH的绝对值偏小,ΔH偏大。
高中化学专题1第1单元第2课时反应热的测量与计算能源的充分利用教案苏教版选修4
第2课时 反应热的测量与计算 能源的充分利用目标与素养:1.了解定量测量反应热的基本原理和实验方法。
(科学探究与创新意识)2.从能量守恒角度理解并掌握盖斯定律。
(变化观念与平衡思想)3.理解标准燃烧热的概念,掌握有关燃烧热的计算。
(变化观念与平衡思想)4.了解化学在解决能源危机中的重要作用。
(科学态度与社会责任)一、反应热的测量1.实验中用到的仪器和药品 (1)实验仪器:简易量热计(2)实验药品:0.50 mol·L -1的盐酸,0.50 mol·L -1的NaOH 溶液等。
2.实验步骤(1)用量筒量取50 mL 0.50 mol·L -1盐酸,倒入简易量热计中,测量并记录盐酸的温度(t 1)。
(2)用另一量筒量取50 mL 0.50 mol·L -1氢氧化钠溶液,测量并记录氢氧化钠溶液的温度(t 2)。
(3)测量最高温度(t 3):将量筒中的氢氧化钠溶液迅速倒入盛有盐酸的简易量热计中,立即盖上盖板,用环形玻璃搅拌棒不断搅拌,观察温度计的温度变化,准确读出并记录反应体系的最高温度(t 3)。
3.实验数据处理与计算ΔH =-c ×m ×Δt ×10-3n (H 2O )kJ·mol -1二、盖斯定律1.内容:一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的。
2.本质:化学反应的焓变(ΔH)仅与反应的起始状态和反应的最终状态有关,而与反应的途径无关。
3.应用:对于进行得很慢的反应,不容易直接发生的反应,产品不纯(即有副反应发生)的反应,测定这些反应的反应热有困难,如果应用盖斯定律,就可以间接地把它们的反应热计算出来。
三、能源的充分利用1.能源(1)定义:能提供能量的自然资源。
(2)分类2.标准燃烧热和热值(1)标准燃烧热:在101_kPa的压强下,1_mol物质完全燃烧的反应热叫做该物质的标准燃烧热。
高二化学(苏教版)选修四学案:专题1 第1单元第2课时 反应热的测量和计算
《化学反应原理》专题一化学反应与能量变化专题一第一单元化学反应中的热效应反应热的测量和计算【学习目标】1.初步学习直接测定化学反应的反应热的实验方法2.能正确分析误差产生的原因并能采取适当措施减小误差3.知道盖斯定律的内容,能运用盖斯定律间接计算化学反应的反应热【学习过程】一、中和热的测定1.中和热的定义定义:在稀溶液中,酸和碱发生中和反应生成时所释放的热量为中和热。
注意: ①必须是酸和碱的稀溶液,因为浓酸溶液和浓碱溶液在相互稀释时会放热。
②强酸和强碱的稀溶液反应才能保证H+(aq)+OH-(aq)=H2O(l)中和热均为,而弱酸或弱碱在中和反应中由于电离吸收热量,其中和热kJ·mol-1;③以生成水为基准。
2.中和热的测定『活动与探究』反应热的测量(分三组测定盐酸与氢氧化钠溶液、盐酸与氢氧化钾、硝酸与氢氧化钠反应的反应热)。
『交流与讨论』1.大、小烧杯放置时,为何要使两杯口相平?填碎纸条的作用是什么?2.酸、碱混合时,为何要把量筒中的NaOH溶液一次倒入小烧杯而不能缓缓倒入?3.实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?为什么?4.有人建议用50mL0.55mol/LNaOH进行上述实验,测得的中和热数值会更准确。
为什么?二、反应热的计算1.盖斯定律(1)内容:化学反应的焓变只与反应体系的和有关,而与反应的无关。
如果一个反应可以分几步进行,则与各步反应的反应焓变之和与该反应一步完成的焓变是相同的,这就是盖斯定律。
如同登山,无论拾级而上,还是乘坐索道缆车,上升的高度是一样的。
如右图:由A 到B 可设计两个途径:途径一:A →B途径二:A →C→B 则焓变△H 、△H 1、△H 2的关系可以表示为:例:已知下述两个反应的反应热:C(石墨)+ O 2(g)= CO 2(g),△H 1 = -393.5 kJ·mol -1;CO(g)+ 1/2O 2(g)= CO 2(g),△H 2 = -283.0 kJ·mol -1试计算反应C(石墨)+ 1/2O 2(g)= CO(g)的反应热为: 。
苏教版高中化学选修四1.1《反应热的计算》参考教案
第一单元化学反应中的热效应第三课时反应热的计算一、教学目标1、深刻理解基本概念,如反应热、焓变、燃烧热、盖斯定律等。
2、根据热化学方程式进行有关的计算二、教学重点、难点1、盖斯定律在计算中的应用三、教学方法:讲授法四、教学过程【复习提问】1、什么是热化学方程式?书写热化学方程式要注意哪些要点?2、写出下列反应的热化学方程式(1)1molC2H5OH(l)与适量O2(g)反应,生成CO2(g)和H2O(l),放出1366.8kJ热量。
(2)18g葡萄糖与适量O2(g)反应,生成CO2(g)和H2O(l),放出280.4kJ热量。
【讲解】化学反应的反应热,有的能够测量,有的不能测量。
比如将一些生成不稳定物质的化学反应,例有C CO,CO或多或少的要转化为CO2,还有一些反应进行的比较慢,要几天,几个月,几年,甚至几十年,肯定不能测量。
对于这样的反应热,我们就要进行计算才能得到。
这节课我们就来讲讲反应焓变的计算。
【板书】一、反应焓变的计算【讲解】反应焓变之所以能够有计算得出,要归功于瑞士科学家盖斯提出的盖斯定律,我们来看看该定律的内容。
【板书】(一)盖斯定律:1、内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应焓变都是一样的。
【讲解】这就说明对于化学反应,只要其反应物和反应产物确定了,不管它中间经历了多少步,反应焓变总是一定的。
好比一个人登山,不管他选择什么途径,只要他从山脚到了山顶,他攀爬的高度总是一定的。
这也说明了反应焓变有点像物理学中的矢量。
究其原因是焓是一个状态函数。
【板书】2、理解要点:(1)反应焓变(反应热效应)只与始态(反应物)、终态(生成物)有关,与反应过程无关。
(2)焓变(反应热)总值一定。
【投影】△H = △H1+ △H2= △H3 + △H4 + △H5【讲解】下面就结合例题,利用盖斯定律来求反应焓变。
【板书】(二)焓变的计算方法1、利用已知焓变求未知焓变——热化学方程式相加减【例1】试利用298K时下述反应的实验数据,计算此温度下C(s,石墨)+12O2(g)=CO(g)的反应焓变。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一单元 化学反应中的热效应
第二课时 反应热的测量与计算
教学目标:1.学会测量反应热的方法,正确分析实验测量误差及原因,并采取适当的措施
减少误差。
2. 理解盖撕定律的内容,运用并能够计算。
教学重点、难点:测量反应热的方法,正确分析实验测量误差及原因
教学模式:边探讨边讲解
教学过程:
一、自学探究
1.中和反应的实质是 。
2.中和反应过程是吸热反应还是放热反应?
3. 是中和热。
4.怎样测定酸碱中和反应的中和热?
二、总结
1.中和热:
在稀溶液中,酸和碱发生中和反应而生成1mol 水时放出的热量。
研究条件:稀溶液
反应物:酸与碱
生成物及其物质的量:1mol
放出的热量:57.3kJ/mol
中和反应的实质是:H + + OH - = H 2O ,当强酸与强碱在稀溶液中发生中和反应时,都有:H +(aq) + OH - (aq) = H 2O(l);△H =-57.3kJ
注:强酸与弱碱反应,强碱与弱酸、弱酸和弱碱反应生成1molH 2
O 放出的热小于57.3KJ/mol 2.中和热的测定
(1)实验药品:
0.50 mol/L 和0.50 mol/L 的盐酸和0.50 mol/L 和0.50 mol/L 的氢氧化钠溶液
(2)实验仪器:简易量热计
(3)实验原理:
3
4.1810/0.025
m t H KJ mol -∆⨯∆=- (4)实验步骤:
1.组装量热器
在大烧杯底部垫泡沫塑料
(或纸条),使放入的小烧杯杯口与大烧杯杯口相
平。
然后再在大、小烧杯之间填满碎泡沫塑料
(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,如上图所示。
2.药品取用
用一个量筒最取50 mL 0.50 mol/L 盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,
记入下表。
然后把温度计上的酸用水冲洗干净。
用另一个量筒量取50 mL 0.55 mol/LNaOH溶液,并用温度计测量NaOH溶液的温度,记入下表。
3.酸碱混合
把量筒中的NaOH溶液迅速倒入量热计(注意不要洒到外面)。
立即盖上盖板,用环形玻璃搅拌棒轻轻搅动溶液,并准确读取混合溶液的最高温度,记为终止温度,记入下表。
4.数据处理
5.重复以上实验两次
你所测得的数据是否为57.4 kJ/mol,若不是,分析产生误差的原因
6 可能的原因有:
1>.量取溶液的体积有误差
2>药品的选用不当引起的误差
3>实验过程中有液体洒在外面。
4>.混合酸、碱溶液时,动作缓慢,导致实验误差
5>.隔热操作不到位,致使实验过程中热量损失而导致误差
6>.测了酸后的温度计未用水清洗而便立即去测碱的温度,致使热量损失而引起误差。
三、问题探究
1.大、小烧杯放置时,为何要使两杯口相平?填碎纸条的作用是什么?
减少热量损失
2.酸、碱混合时,为何要把量筒中的NaOH溶液一次倒入小烧杯而不能缓缓倒入?
减少热量损失
3.实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?为什么?
不能。
因为铜丝易导热,使热量损失较大
4.有人建议用50mL0.55mol/LNaOH进行上述实验,测得的中和热数值会更加准确。
为什么?
可以保证盐酸完全反应。
使测得的热量更加准确。
4.判断下列实验操作对中和热测定的数值有如何影响?填变大变小或者不变。
①大烧杯上没有盖硬纸板
变小
②用相同浓度和体积的氨水代替NaOH溶液进行实验
变小
③用相同浓度和体积的醋酸代替稀盐酸溶液进行实验
变小
④实验中改用60 mL 0.50 mol/L盐酸跟50 mL 0.55 mol/L NaOH溶液进行实验
不变
四、概念辨析
1.为了减小误差。
某同学在实验中两次测定中和热。
第一次是用50 mL 0.50 mol/L的盐酸和50 mL 0.50 mol/L氢氧化钠,第二次是用100 mL 0.50 mol/L的盐酸和100 mL
0.50mol/L的NaOH溶液。
请你预测该同学两次测得的中和热结果(相等
或者不相等)。
相等
2.若将1L1mol/LNaOH溶液中加入稀醋酸、浓硫酸、稀硝酸,恰好完全反应时的热效应分别为△H1、△H2、△H3;则三者的大小
关系为。
△H1>△H3>△H2
五、自学探究
讨论:是不是任一反应的反应热均能直接测出?
如何测出这个反应的反应热:
① C(s)+1/2 O2 (g)==CO(g) ;ΔH1=?
②CO(g)+1/2 O2 (g)= CO2(g);ΔH2=-283.0kJ/mol
③C(s)+ O2 (g)= CO2(g);ΔH3=-393.5kJ/mol
① + ② = ③
则ΔH1 + ΔH2 =ΔH3
ΔH1 =ΔH3- ΔH2
=-393.5kJ/mol+ 283.0kJ/mol
=-110.5kJ/mol
应用了什么规律?
六、总结
不管化学反应是一步完成或分几步完成,其反应热是相同的。
化学反应的焓变(ΔH)只与反应体系的始态和终态有关,而与反应的途径无关。
这就是盖斯定律。
如何理解盖斯定律?
ΔH、ΔH1、ΔH2之间有何关系?
ΔH=ΔH1+ΔH2
七、例题
1.某次发射火箭,用N2H4(肼)在NO2中燃烧,生成N2、液态H2O。
已知:N2 (g)+2O2(g)==2 NO2 (g)△H1=+67.2kJ/mol
N2H4 (g)+ O2 (g)== N2 (g)+2 H2O (l) △H2=-534kJ/mol
假如都在相同状态下,请写出发射火箭反应的热化学方程式。
答案:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l);△H=-1135.2kJ/mol
2.已知:H
(g)+1/2 O2 (g) =H2O (g) ; △H1 = -241.8kJ/mol
2
H
(g)+ 1/2 O2 (g) =H2O (l) ; △H2 = -285.8kJ/mol
2
H2O l) =H2O (g) ; △H3
则△H1、△H2、△H3的关系。
答案:△H1=△H2+△H3
3.已知:金刚石、石墨的热化学方程式:
C(s,金刚石)+ O2 (g) =CO2 (g);△H = -395.4 kJ/mol C(s,石墨)+ O2 (g) =CO2(g) ;△H = -393.5 kJ/mol
则石墨转化为金刚石的反应热△H= ,两物质中较为稳定。
答案:+1.9 kJ/mol 石墨。
