一次盐水操作规程
盐水精制岗位安全操作规程

盐水精制岗位安全操作规程岗位安全操作规程一、操作环境、前提要求及操作步骤1.操作环境要求:(1)操作场所应保持干燥、通风良好,无明火,无毒性气体泄漏等危险物质;(2)岗位周围应清洁整齐,无杂物堆积,保持通道畅通;(3)操作设备应保持良好的工作状态,无漏电、短路等隐患;(4)操作人员必须正确佩戴劳动防护用品,包括安全帽、防护眼镜、防护手套等。
2.前提要求:(1)操作人员必须熟悉岗位安全操作规程,了解操作设备的工作原理和操作方法;(2)操作人员必须经过专业培训,具备岗位操作技能;(3)操作人员必须身体健康,无饮酒、服用药物等影响工作安全的因素。
3.操作步骤:(1)准备工作:①检查操作设备的工作状态,确保设备正常工作;②佩戴劳动防护用品;③检查操作场所环境,确保安全无隐患。
(2)操作流程:①按照操作规程对设备进行操作,确保操作过程符合安全要求;②注意操作的时间和速度,避免操作过程中出现意外;③定期检查操作设备和工作环境,及时消除隐患。
(3)结束工作:①正常关闭操作设备;②清理操作场所,将杂物与废弃物放置到指定位置;③检查操作设备,确保设备处于关闭状态;④摘下劳动防护用品。
二、常见危险源及应对措施1.电气事故:(1)操作人员应了解岗位设备的电气安全知识,确保设备安全可靠;(2)操作人员在操作过程中应保持清醒,不得带电操作,避免发生触电事故;(3)发现设备出现电气故障时,应及时报修并尽量远离故障设备。
2.化学品泄漏:(1)操作人员应熟悉岗位设备所使用的化学品,了解其安全操作规程和应急处理方法;(2)操作人员在操作过程中应遵守安全操作规程,避免发生化学品泄漏;(3)发现化学品泄漏时,应立即采取应急措施,包括远离泄漏源、通知相关人员等。
3.火灾事故:(1)操作人员在操作过程中应严禁使用明火,避免引发火灾事故;(2)岗位设备周围应保持整洁,无易燃物和可燃物,确保火灾安全;(3)发现火灾时,应立即采取灭火措施,并及时报警。
一次盐水精制操作规程2

湖北宜化集团有限责任公司企业标准Q/YH.JS22040-2003 一次盐水岗位操作规程2003-10-1发布2003-12-25实施宜化集团有限责任公司发布前言1.本标准根据宜化集团二零零三年标准制修订2.本标准负责起草单位:宜化集团氯碱化工事业部3.本标准负责起草人:吕飞4.本标准负责审编人:舒晨宜化集团企业标准一次盐水精制岗位操作规程1.适用范围本规程规定了一次盐水精制工段的生产目的与任务,原盐、饱和食盐水的精制与特征,以及生产的基本原理,工艺流程,工艺控制指标,岗位操作法,事故处理等。
本规程适于宜化集团氯碱化工事业部一次盐水精制工段生产过程中的工艺管理和操作管理。
2.岗位范围本岗位的操作范围包括:溶盐桶、精制桶、澄清桶、一次盐水过滤器、盐泥压滤机、盐酸中和槽、精盐水槽、TXY、BaCl2、Na2CO3配制槽及各盐水泵等设备的生产。
3.岗位任务3.1 负责皮带运输机地下清盐和日常维护保养工作,保证皮带运输机的正常运行。
3.2 负责精制剂Na2CO3、BaCl2的正确配备与加入工作。
3.3 负责将粗盐水进行精制,保证Ca2+、Mg2+、SO42-等指标合乎工艺要求。
3.4 负责对盐水中不合格指标(NaCl浓度、SO42-含量)的协调与处理。
3.5 负责精制桶及澄清桶中盐泥的定期排放工作。
3.6 负责一次盐水过滤器的操作。
3.7 负责向二次精制输送合格的一次精制盐水。
3.8 负责各项参数的监控,按时巡检认真填写各种生产记录。
3.9 负责本岗位管道、阀门、泵等设备的维护保养工作。
3.10 负责生产用原辅材料、工具、器具(包括消防器材、公共劳保用品)等的保管与合理使用。
3.11 负责本岗位的环境工作,穿戴好劳保及其防护用品及协调汇报处理岗位上的各种不正常现象及事故隐患。
3.12 负责完成上级部门交办的其它工作任务。
5 . 生产原理原盐中除了NaCl还含有Ca2+、Mg2+、SO42-等化学杂质和机械杂质,这些杂质在化盐过程中,也被带进盐水中,用含有杂质的盐水进行电解,直接影响电流效率及离子膜的使用寿命,影响氯碱生产的经济效益。
氯碱一次盐水操作规程
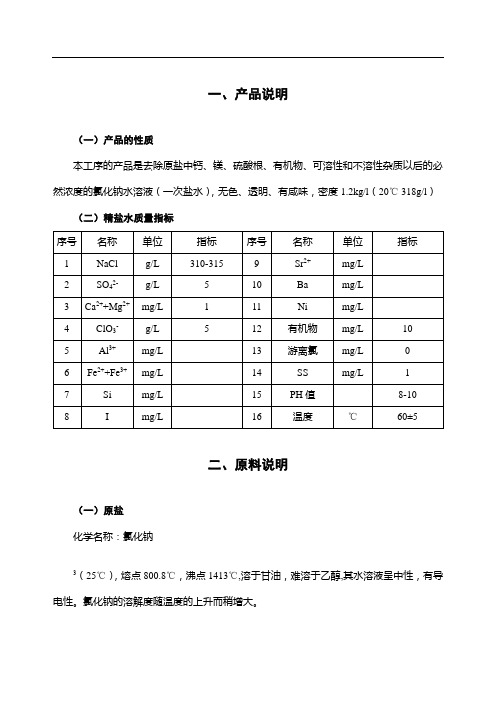
一、产品说明(一)产品的性质本工序的产品是去除原盐中钙、镁、硫酸根、有机物、可溶性和不溶性杂质以后的必然浓度的氯化钠水溶液(一次盐水),无色、透明、有咸味,密度1.2kg/l(20℃ 318g/l)(二)精盐水质量指标二、原料说明(一)原盐化学名称:氯化钠3(25℃),熔点800.8℃,沸点1413℃,溶于甘油,难溶于乙醇,其水溶液呈中性,有导电性。
氯化钠的溶解度随温度的上升而稍增大。
氯化钠溶解度与温度的关系化学性质:氯化钠熔融态电解可取得氯气和金属钠,而氯化钠的水溶液在直流电作用下,可取得烧碱、氯气、氢气。
NaCl(熔融)直流电Na + 1/2 Cl2↑2NaCl + 2H2O 直流电2NaOH + Cl2↑ + H2 ↑工业氯化钠化学指标见下表:(GB/T 5462-2003)氯碱工业对氯化钠的质量有严格的要求:一、氯化钠含量要高。
最低要求大于92%,最好能大于94%。
因为氯化钠含量高,其它有害杂质就相应少些,就能够有效地保证入槽盐水的质量。
二、水溶性杂质量要少。
要求小于1.6%,最好能小于1%。
水溶性杂质主若是指GaCl2、MgCl2、GaSO4、Na2SO4等,如含量高,将要增加精制剂用量,从而增加盐水精制费用,使烧碱本钱上升。
同时也阻碍盐水精制设备的能力发挥,专门是Ga2+、Mg2+含量比倒置时,一样澄清设备均很难知足工艺要求。
故要求原盐中Ga2+含量大于Mg2+含量,钙镁比为2最正确。
3、不溶于水的机械杂质要少。
一样要求小于0.4%,不然将加大澄清设备的排泥量,使烧碱的盐耗上升。
4、盐的颗粒要粗细适中,成立方体半透明结晶状。
盐粒太细太湿易结成硬块状,给运输和利用带来困难。
盐粒过细还会在化盐进程中被盐水溢流带出,给后道工序操作增加难度。
盐结成大块状,阻碍化盐速度。
劣质原盐一样外观盐粒偏细,湿度大,颜色暗及发灰或发黑。
优质原盐一样外观呈立方体晶体,干燥,颜色是半透明状微黄色或白色。
(二)纯碱化学名称:碳酸钠,俗名:碱面或苏打分子式:Na2CO3 分子量:106物理性质:白色粉末,密度/cm3(25℃),熔点851℃,易溶于水,在35.4℃达到最大溶解度,水溶液呈碱性,吸湿性强,能因吸湿而结成硬块。
一次盐水操作规程

无机膜法一次卤水精制过滤装置(建议稿)操作手册肥城光明岩盐有限公司二O一四年五月目录一、卤水过滤精制原理第2~4页二、岗位任务第4页三、工艺流程叙述及工艺流程图第2~5页四、原、辅材料标准与规格第5页五、工艺及操作指标第5~7页六、无机膜盐水过滤器开车操作第7~10页七、无机膜盐水过滤器停车操作第10~11页八、无机膜盐水过滤器清洗操作第11~13页九、主要故障处理第14页十、控制系统说明第15~16页十一、岗位操作要点第16~17页十二、中间产品质量标准第18页十三、设备一览表第18~22页十四、安全生产第22~23页十五、岗位责任制度第23页十六、关于试车第24~25页附表一:无机膜盐水过滤器阀门表第25页附表二:阀门状态表第26页附图一:工艺流程图附图二:阀门组示意图一、卤水过滤精制原理1. 卤水精制的原理1.1次氯酸钠除菌藻类及其它有机物次氯酸钠中的游离氯将原卤中带来的菌藻类及其它有机物氧化分解。
1.2碳酸钠除钙离子在卤水中加入碳酸钠溶液,使其和卤水中的Ca2+反应,生成不溶性的碳酸钙沉淀,其反应式如下:Ca2+ + CO32- → CaCO3↓为了将Ca2+除净,碳酸钠的加入量必须超过反应式的理论需要量,本工艺碳酸钠的过碱量300~500mg/l。
1.3氢氧化钠除镁离子在卤水中加入NaOH溶液,使其和卤水中的Mg2+反应,生成不溶性的Mg(OH)2沉淀,其反应式如下:Mg2+ + 2OH- → Mg(OH)2↓为了将Mg2+除净,NaOH的加入量必须超过反应理论需要量,本工艺氢氧化钠过碱量为100~300mg/l。
1.4卤水的过滤精制加入精制剂(Na2CO3、NaOH、NaClO)进行精制反应后的粗卤水,通过粗过滤器分离出粒径≥1mm的机械杂物,进入无机膜盐水过滤器,无机膜盐水过滤器采用无机膜管(无机膜元件的膜孔径规格为50nm,孔径分布在30~50nm之间,平均孔径为40nm)作为过滤元件、以“错流”过滤的方式,过滤去除精制反应之后生成的悬浮粒子,确保卤水中的SS含量小于0.5ppm,Ca2+、Mg2+的含量小于0.5ppm的工艺要求。
烧碱操作规程

2.1开车操作 51 2.2 正常停车 51 2.3 开停车程序表 52 第三节 紧急停车处理 54 3.1突然断电 54 3.2突然停蒸汽 54
第八章 应急预案 55
第一节 蒸发岗位断电停车应急预案 55
第二节 蒸发岗位泄漏应急预案 56 2.1 目的 56 2.2 汇报要求 56 2.3 处理办法(以V0304为例) 56
第二篇 蒸发操作规程
第一章 岗位任务 33
第一节 岗位任务 33 第二节 岗位概念 34 第三节 岗位职责 35
3.1主操职责 35 3.2 组员职责 35 第四节 巡检概念化 36
第二章 工作原理 37
第一节 反应原理 37 第二节 装置原理 38
2.1 设备简图 38 2.2 设计原理 41 2.3 控制点 41
第七章 开停车方案 87
第一节 液化冰机开停车方案 87 1.1组织机构 87 1.2正常开车步骤 87 1.3开车操作 87 1.4正常停车操作 87 1.5冰机紧急停车 88 1.6冰机系统不正常现象及处理 88 1.7液下泵操作 89 1.8注意事项: 89 1.9启泵 89 1.10停泵 90 1.11紧急氮气密封的使用 90 1.12液下泵不正常现象及处理 92
第车操作 94 2.3常规操作 94 2.4液化开车程序表 95 2.5正常停车操作 96 2.6紧急停车操作 96 2.7液化停车程序表 97 第八章 应急预案 98
第一节 液氯泄漏应急预案 98 1.1发现漏点 98
1.2预处理 98 1.3汇报 98 1.4现场指挥公告与联络 98 1.5现场控制 98 1.6处理完毕报告 99 第二节 液化岗位断电处理预案 100
氯碱一次盐水操作规程

、产品说明(一)产品的性质本工序的产品是去除了原盐中钙、镁、硫酸根、有机物、可溶性和不溶性杂质以后的定浓度的氯化钠水溶液(一次盐水),无色、透明、有咸味,密度1.2kg/l (20C 318g/l)(二)精盐水质量指标、原料说明(一)原盐化学名称:氯化钠分子式:NaCI 分子量:58.5物理性质:氯化钠为无色透明的正六面体结构,有咸味,密度 2.165g/cm3(25C),熔点8008C,沸点1413C,溶于甘油,难溶于乙醇,其水溶液呈中性,有导电性。
氯化钠的溶解度随温度的上升而稍增大氯化钠溶解度与温度的关系化学性质:氯化钠熔融态电解可得到氯气和金属钠,而氯化钠的水溶液在直流电作用下,可得到烧碱、氯气、氢气。
NaCI (熔融)直流电Na + 1/2 Cl2 T2NaCI + 2出0 直流电2NaOH + CI2 T + H2 T工业氯化钠化学指标见下表:(GB/T 5462-2003)1、氯化钠含量要高。
最低要求大于92%,最好能大于94%。
因为氯化钠含量高,其它有害杂质就相应少些,就能有效地保证入槽盐水的质量。
2、水溶性杂质量要少。
要求小于1.6%,最好能小于1%。
水溶性杂质主要是指GaCl2、MgCl2、GaSO4、Na2SO4等,如含量高,将要增加精制剂用量,从而增加盐水精制费用,使烧碱成本上升。
同时也影响盐水精制设备的能力发挥,特别是Ga2+、Mg2+含量比倒置时,一般澄清设备均很难满足工艺要求。
故要求原盐中0&2+含量大于Mg2+含量,钙镁比为2最佳。
3、不溶于水的机械杂质要少。
一般要求小于0.4%,否则将加大澄清设备的排泥量,使烧碱的盐耗上升。
4、盐的颗粒要粗细适中,成立方体半透明结晶状。
盐粒太细太湿易结成硬块状,给运输和使用带来困难。
盐粒过细还会在化盐过程中被盐水溢流带出,给后道工序操作增加难度。
盐结成大块状,影响化盐速度。
劣质原盐一般外观盐粒偏细,湿度大,颜色暗及发灰或发黑。
医院输血科交叉配血(盐水法)标准操作程序

输血科交叉配血(盐水法)标准操作程序
(原理)交叉配血主要是检查受血者血清中有无破坏供血者红细胞的抗体,故受血者血清加供血者红细胞相配的一管称为“主侧”,供血者血清加受血者红细胞相配的一管称为“次侧”,两者合称交叉配血。
交叉配血试验又称不配合性试验,是确保患者安全输血必不可少的试验,完整的操作规程应包括:①查阅受血者以前的血型检查记录,如与这次检查结果有所不同,应及时分析原因;②对收到的受血者血样应作ABO正反定型,RH(1)定型及血型抗体检测和鉴定;③选择预先进行血型检查的合格供血者作交叉配血试验。
交叉配血方法:
(一)盐水介质配血法
本法是目前最常用的配血方法,可以发现临床上最重要的ABO不配合性,当受血者和供血者细胞经混合并离心后,如有ABO不配合问题,就会很快显示出来,所以常称为“立即离心”配血试验。
[操作]
1、抽取受血者静脉血3-4ml,待凝固后分离血清,并配制2%-5%台红细胞盐水悬液。
2、将供血者血样以同样方法分离血清,并配制2%-5%红细胞悬液。
3、取洁净水试管2支,1支标明受血者血清(PS)+供血者细胞(DC)作“主侧”,另1支标明供血者血清(DS)+受血者细胞(PC)作“次侧”。
4、按标记“主侧”管如受血者血清2滴和供血者红细胞悬液1滴。
“次侧”管如供血者血清2滴和受血者红细胞悬液1滴混匀,以1000r/min离心1min,轻轻侧动试管,观察结果,冬季气温较低,应将试管保温,以防
冷凝集素引起的凝集反应影响结果判断。
ABO同型配血,“主侧”和“次侧”均无溶血及凝集表示无输血禁忌可以输血。
盐水测试操作规程

制定一个测试标准以评估产品于正常使用中、贮存及运输途中,抵抗带盐份环境的模拟环境试验标准。
2.范围
所有包含金属配件的玩具产ห้องสมุดไป่ตู้或配件。
3.仪器
电子称
4.试验样办
没有做过任何测试的含金属配件的玩具产品或配件。
5.程序
5.1用电子称量出一定的食盐和蒸馏水配成5%浓度的盐水。
5.2在测试进行之前,先对产品的外观及功能作出检查。
5.3将需测试的五金件放入盐水盒中,五金件一半放入盐水中,一半露在空气中(螺丝则全部浸泡于盐水中),然后将盐水盒放入57±3℃的焗炉中24个小时。
5.4试验结束后,需把样办置于室温环境下放置4小时。然后对照样办作外观、功能检查(主要留意金属配件表面有否产生生锈,氧化物等问题)。
6.评定
金属件有生锈和氧化为不合格
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
滨州海洋化工有限公司20万吨/年烧碱25万吨/pvc树脂项目电解车间化盐工序操作规程目录第一章物料说明 (2)第二章盐水精制的工艺目的及原理 (6)第三章工艺流程图及描述 (11)第四章岗位操作法 (15)第五章不正常情况处理 (21)第六章安全注意事项 (22)第七章三废处理 (25)第八章消耗定额 (25)第九章生产控制点一览表 (26)第十章主要设备一览表 (27)第一章物料说明1.1原料1.1.1.1 盐:化学名称氯化钠,白色四方结晶或结晶性粉末,因含杂质的不同,分别呈灰、褐等颜色,分子式NaCl,分子量58.44,熔点800.4℃,沸点1413℃,易溶于水,微有潮解性,由于工业盐中含有易吸收空气中水分的氯化钙、氯化镁杂质而潮解结块。
氯化钠易溶于水,其溶解度随着温度的升高稍有增大,不同温度下其溶解度(见表1):温度℃溶解度温度℃溶解度% g/h % g/h10 26.35 316.7 60 27.09 320.520 26.43 317.2 70 27.30 321.830 26.56 317.6 80 27.53 323.340 26.71 318.1 90 27.80 325.350 26.89 319.2 100 28.12 328.0表1 不同温度下氯化钠在水溶液中的溶解度1.1.1.2工业盐质量:NaCl:≥94.5%Ca2+:≤0.2% SO42-<0.6%Mg2+:≤0.2% 水不溶物:<0.01%要求:1、氯化钠含量高。
2、化学杂质如:氯化钙、氯化镁、硫酸钙、硫酸钠等含量要少,镁、钙比值要小。
3、不溶于水的机械杂质要少。
4、盐颗粒要粗。
5、天然有机物和菌、藻、腐殖酸等要低。
1.1.2 纯碱化学名称:碳酸钠,俗名:苏打,分子式:Na2CO3,分子量:106物理性质:白色粉末或结晶细粒,味涩,密度2.533g/cm3(25℃),熔点854℃,易溶于水呈强碱性,在35.4℃达到最大溶解度,吸湿性强,能因吸湿而结成硬块。
规格:纯度大于98%,本工序配成120-140g/l的水溶液。
1.1.3盐酸分子式:HCl,分子量:36.5物理性质:又名氯氢酸,纯盐酸为无色透明液体,工业盐酸因含有铁等杂质而呈黄色,有强烈的刺激性气味,能溶于水、乙醇和乙醚中,具有强腐蚀性。
本工序所需盐酸为无色透明液体。
1.1.4氯化钡分子式:BaCl2,分子量:208.4物理性质:固体BaCl2·2H2O含量大于97%,本工序配成20%的溶液。
1.1.5次氯酸钠分子式:NaClO,分子量74.5本工序采用有效氯5%的工业次氯酸钠溶液。
1.1.6三氯化铁分子式:FeCl3,分子量:163物理性质:黑色粉末,易溶于水,具有很强的氧化性,对铁、铜等金属腐蚀性特强,水溶液呈酸性。
规格:三氯化铁含量:≥40wt% 氯化亚铁:≤4% 水不溶物:≤3.5%1.1.7亚硫酸钠分子式:Na2SO3分子量:126 外观:白色粉末密度:2.633, 易溶于水,溶液呈碱性,具有还原性。
纯度:≥97wt%,重金属含量:≤10wtppm1.2产品1.2.1 精制盐水:不含或含有微量杂质的符合进离子交换树脂塔工艺要求的氯化钠水溶液。
规格:NaCl:305±5g/lCa2+、Mg2+含量:≤1mg/lSS:≤1mg/l水不溶物:<1mg/l游离氯:无1.3盐质量对盐水精制的影响1.3.1 影响精制剂的消耗及精制操作:如果盐水中钙、镁、硫酸根等离子及天然有机物含量高,则要增加精制剂、烧碱、纯碱、氯化钡、次氯酸钠、铁盐的用量,从而增加费用影响生产成本。
1.3.2 影响设备能力的发挥:如果盐水中杂质的含量高,特别是天然有机物、镁、钙、硫酸根等离子,将直接影响化盐、精制设备的效率。
1.4盐水中杂质对离子膜电解及其他工序的影响1.4.1 天然有机物及Ca2+ Mg2+的影响如果盐水中大量天然有机物、Ca2+、Mg2+不除去,超过了树脂的处理能力,发生过量天然有机物、Ca2+、Mg2+的泄漏,造成树脂使用周期缩短,能力下降,进电解槽的盐水质量不合格,在电解过程中Ca2+ Mg2+就会与从阴极室迁移到阳极室的OH-结合,生成氢氧化物,和天然有机物一起沉积在离子膜内或靠近阴极一侧的膜内导致电流效率下降,从而破坏电解的正常运行。
1.4.2 SO42-的影响如果盐水中SO42-含量高,则会生成Na2SO4沉积在离子膜内,造成电流效率下降,SO42-还会阻碍Cl-放电,促使OH-放电,产生O2,氯中含O2量增加,氯气纯度降低,O2还会腐蚀阳极。
1.4.3 菌藻类、腐殖酸及机械杂质的影响菌藻类、腐殖酸及不溶性泥沙等机械杂质随盐水进入本工序会造成过滤器处理能力降低及运行周期缩短,增加了盐泥的量和过滤器的运行负荷。
如进入树脂塔,会造成树脂塔树脂结块,交换能力下降,导致盐水的质量下降,离子膜效率降低,严重破坏电解槽的正常生产。
第二章盐水精制的工艺目的及生产原理2.1盐水精制的工艺目的由于工业盐中含有Ca2+、Mg2+、SO42-等无机杂质,细菌、藻类残体、腐殖酸等天然有机物和机械杂质,这些杂质在化盐时会被带入盐水中,如不彻底去除会造成树脂塔树脂结块,交换能力下降,导致离子膜效率下降,严重破坏电解槽的正常生产,因此必须除去大量杂质,满足树脂塔的要求。
2.2盐水精制的生产原理2.2.1 原盐的溶解原盐可在地下池式或地上桶式化盐桶中溶化,得到饱和的粗盐水。
本工艺采用地下化盐池化盐。
化盐时,盐水的浓度、原盐的溶解速度与化盐桶内盐层的厚度以及化盐水的温度成正比。
一般保持盐层的厚度为2.5-3.0m,控制化盐水的温度在60-70℃,盐水停留的时间不少于30分钟。
为了制得饱和盐水,生产中采用热法化盐,这是因为:a)氯化钠的溶解度随温度的升高而稍有增大。
b)能加速原盐的溶解速度,缩短盐水达到饱和的时间。
c)促进盐水中沉淀反应进行完全,加速沉淀物的沉降速度。
d)能加速碳酸钙沉淀(CaCO3)生成的速度,对除钙离子(Ca2+)有利。
e)能降低盐水及泥浆的粘度,降低盐水的过滤能力,提高盐水的过滤速度。
但化盐温度也不能太高,防止因环境温度太低,造成粗盐水中氯化钠溶解度降低而结晶析出,堵塞管道。
在本工艺中,要求控制化盐水温度60-70℃。
2.2.2 盐水精制原理原盐溶解后的粗饱和盐水中含有钙、镁、硫酸根等杂质,不能直接供电解工序使用,需要加以精制。
对一次盐水工序,过多的钙、镁等化学杂质将会加大二次精制螯合树脂塔的生产负荷,缩短再生周期,严重时会使螯合树脂塔出现穿透现象,因此要求钙、镁不超过某一值,一般采用化学精制方法,即加入精制剂,与杂质反应成为溶解度很小的沉淀而分离出去。
盐水中的有机物会附着在HVM膜及螯合树脂上面,影响HVM 膜的过滤作用及螯合树脂的吸附效果。
同时盐水中的游离氯会破坏HVM膜及螯合树脂的结构。
因此,既要去除盐水中的有机物杂质,又要严格控制盐水的游离氯含量为零。
盐水精制采用次氯酸钠---氯化钡---纯碱---烧碱---铁盐法。
2.2.2.1 SO42-的去除SO42-离子一部分由原盐带入,同时在化学除ClO-的过程又生成一部分SO42-,因而硫酸根在盐水系统中是一个积累的过程。
为控制盐水中SO42-离子的浓度在电解槽要求指标5g/l以下。
一般采用加BaCl2与SO42-反应生成BaSO4沉淀而去除,本工艺采用将返回的含SO42-离子较高(约7g/l)的淡盐水的一部分(约总量的1/3)送到澄清桶,同时补入氯化钡溶液,达到除去部分SO42-离子的目的,使SO42--离子控制在要求的范围(≤5g/l)。
Ba2++SO42-BaSO4加入精制剂氯化钡不应过量,否则将增加离子交换树脂的负荷。
若产生Ba2+泄露,则进电槽和OH-生成Ba(OH)2,堵塞离子膜。
2.2.2.2 Mg2+的去除Mg2+通常是以氯化物的形式存在于粗盐水中,加入精制剂氢氧化钠(NaOH)生成不溶性的氢氧化镁(Mg(OH)2)沉淀,其离子方程式为:Mg2++2OH-Mg(OH)2为了提高反应速度和反应程度,氢氧化钠的加入量需要超过理论用量,以保证适当的碱度。
Mg(OH)2在PH=8时,开始生成胶状沉淀,而在PH=10.5-11时,反应完全。
在本工艺中,控制粗盐水NaOH过碱量为0.1-0.3g/l。
通过加入NaOH,粗盐水中的铁离子、三价铬离子等生成氢氧化物沉淀与镁离子一同除去。
2.2.2.3 Ca2+的去除Ca2+一般以氯化钙、硫酸钙的形式存在于原盐中。
精制时向粗盐水中加入碳酸钠(Na2CO3),使其与盐水中的Ca2+离子反应,生成不溶性的碳酸钙(CaCO3)沉淀,其离子反应方程式为:Ca2++CO32-CaCO3加入碳酸钠的量为理论用量时,需搅拌数小时,才能使反应达到碳酸钙沉淀的终点。
但若加入超过理论用量0.8g/l时,会使反应在15分钟内完成90%,在不到1h之内就能实际完成并使溶解的钙离子浓度在1ppm以下。
为了把Ca2+除净,精制剂Na2CO3的加入量必须稍稍超过反应所需理论用量。
本工艺控制粗盐水中Na2CO3过碱量为0.3-0.6g/l。
2.2.2.4 菌藻类及其他有机物的去除盐水中的有机物会对HVM过滤膜及二次盐水工序中离子交换树脂造成损害,所以必须除去。
在本工艺中,通过加入氧化剂次氯酸钠(NaClO)溶液,把盐水中的菌藻类及其他有机物氧化成小分子有机物,最终通过絮凝剂三氯化铁(FeCl3)的吸附和共沉淀作用,在预处理器中除去。
2.2.2.5 过量游离氯的去除盐水中的游离氯,一般以ClO-的形式存在,会对过滤设备、二次盐水精制设备造成很大危害,必须全部除去。
本工艺采用加入还原剂亚硫酸钠(Na2SO3)溶液,使其与盐水中过量的游离氯发生氧化还原反应,以除去盐水中残留的游离氯。
ClO-+ Na2SO3Na2SO4+Cl-本工艺要求进HVM过滤器的游离氯含量为零。
2.2.2.6 浮上澄清精制过程中产生的大量Mg(OH)2为胶状絮片,极难沉降,同时不利于HVM膜过滤器正常操作,故采用浮上法经预处理器将Mg(OH)2先行除去。
首先,将粗盐水通过加压溶气罐,罐内保持0.2-0.35MPa压力,在压力的作用下,使粗盐水溶解一定量空气(一般5l/m3粗盐水),在粗盐水进入预处理器后压力突然下降,粗盐水中的空气析出,产生大量细微的气泡,细微的气泡在絮凝剂的作用下与盐水中的机械杂质形成假比重较低的颗粒一起上浮,在预处理器上面形成浮泥,通过上排泥口定时排放,部分较重颗粒下沉形成沉泥,通过下排泥口排放。
清液自清液出口流出。
浮上澄清法的优点是适合于含Mg2+较高的原盐,受温度变化的影响较小,清液分离速度快,生产能力大。
浮上澄清法的效果取决于(1)精制反应充分完成;(2)空气与粗盐水有足够的接触机会,并保持一定的压力;(3)溶于盐水中的空气在絮凝反应室内完全释放为细微的气泡;(4)粗盐水中加入适量的絮凝剂;(5)及时排出浮泥和沉泥。
