关于印发化妆品产品技术要求规范的通知
1.《化妆品安全技术规范》第一 二 三章拟修订内容.doc
附件1
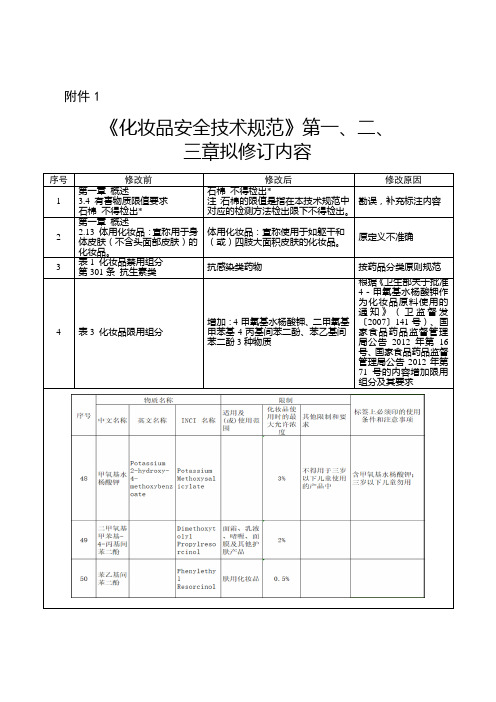
《化妆品安全技术规范》第一、二、
三章拟修订内容
序号修改前修改后修改原因
1
第一章概述
3.4 有害物质限值要求
石棉不得检出*
石棉不得检出*
注:石棉的限值是指在本技术规范中
对应的检测方法检出限下不得检出。
勘误,补充标注内容2
第一章概述
2.13 体用化妆品:宣称用于身
体皮肤(不含头面部皮肤)的
化妆品。
体用化妆品:宣称使用于如躯干和
(或)四肢大面积皮肤的化妆品。
原定义不准确
3
表1 化妆品禁用组分
第301条抗生素类抗感染类药物按药品分类原则规范4 表3 化妆品限用组分
增加:4-甲氧基水杨酸钾、二甲氧基
甲苯基-4-丙基间苯二酚、苯乙基间
苯二酚3种物质
根据《卫生部关于批准
4-甲氧基水杨酸钾作
为化妆品原料使用的
通知》(卫监督发
〔2007〕141号)、国
家食品药品监督管理
局公告2012年第16
号、国家食品药品监督
管理局公告2012年第
71号的内容增加限用
组分及其要求
—2 —
—4 —。
国食药监保化[2011]500号-关于印发化妆品用乙醇等3种原料要求的通知
![国食药监保化[2011]500号-关于印发化妆品用乙醇等3种原料要求的通知](https://img.taocdn.com/s3/m/1fc51ed776eeaeaad1f33038.png)
关于印发化妆品用乙醇等3种原料要求的通知-国食药监保化[2011]500号2011年12月23日发布各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为规范化妆品原料技术要求,进一步提高化妆品质量安全,化妆品用乙醇等3种原料要求已经国家食品药品监督管理局化妆品标准专家委员会审议通过,现予印发。
附件:1.化妆品用乙醇原料要求2.化妆品用滑石粉原料要求3.化妆品用甘油原料要求附件1:化妆品用乙醇原料要求为规范化妆品原料技术要求,提高化妆品卫生质量安全,根据我国化妆品监管相关规定,编写《化妆品用乙醇原料要求》,本要求针对性地规定了乙醇的安全性要求及检验方法,其他相关要求及检验方法按相应规定执行。
1. 基本信息1.1 名称乙醇1.1.1 INCI名称及其ID号ALCOHOLID:651.1.2 INCI标准中文译名乙醇1.1.3 化学名称乙醇(Ethanol)1.1.4 《中国药典》中名称2010年版《中国药典》(二部)中名称:乙醇1.1.5 常见别名酒精1.2 登记号1.2.1 CAS登记号64-17-51.2.2 EINECS登记号200-578-61.3 分子式、结构式及分子量分子式:C2H6O结构式:CH3CH2OH分子量:46.071.4 性状及理化常数无色澄清液体,具有特征性气味,味灼烈;易挥发,易燃烧,燃烧时显淡蓝色火焰。
与水、甘油、三氯甲烷或乙醚能任意混溶。
乙醇(95%)沸点:78.2℃,乙醇(95%)凝固点:-114.1℃,乙醇(95%)相对密度:0.8129(20℃)。
2. 技术要求2.1 原料使用目的乙醇在化妆品产品中可作为溶剂、消泡剂、粘度调节剂、收敛剂等使用。
2.2 原料适用范围乙醇广泛用于化妆品中。
2.3 限量要求2.3.1 乙醇含量要求乙醇(φ/%)≥95.0(20℃)。
2.3.2 乙醇中相关组分限量要求乙醇中甲醇体积分数(φ/%)≤0.2。
3. 检验方法3.1 乙醇鉴别试验方法参见2010年版《中国药典》(二部)所载乙醇的鉴别试验方法(见附1)。
国产非特殊用途化妆品备案检验工作规范介绍-20140227修改

检验申请表 • 检验要求
3、宣称祛痘、除螨、抗粉刺等用途,需测抗生素和甲硝唑。 4、宣称去屑用途,需测去屑剂。
5、pH≤3.5(用后冲洗类产品除外),加测pH。
• 检验要求 6、含滑石粉的产品,加测石棉。
检验申请表
7、指甲油卸除液,或是乙醇含量≥75%(W/W),不需要检微生物。
8、除防晒产品外,防晒剂(二氧化钛和氧化锌除外)含量≥0.5%(w/w)的其他产品也应当加测防晒剂项 目。
• 性状 颜色+物态
检验申请表
透明液体 淡黄色膏体 无色透明液体附着在白色无纺布上(面膜) 无色颗粒与褐色油双相结构
检验申请表
• 检验类别 非特殊产品分类: 发用品 护肤品:普通护肤品 易触及眼睛的护肤品 彩妆品:普通彩妆品 眼部彩妆 唇部彩妆 指(趾)甲用品 芳香化妆品
检验申请表
• 生产批号或生产日期、限期使用日期或保质期 • 《化妆品标识管理规定》
检验申请表
• 样品中文名称 禁止使用 虚假、夸大和绝对化的词语 庸俗或带有封建迷信色彩的词语 已经批准的药品名 外文字母、汉语拼音、数字、符号等(注册商标必须使用、约定俗成、习惯使用的除外,如 维生素C) 其他误导消费者的词语
检验申请表
• 样品中文名称 商标名+通用名+属性名 例:杰西卡辛普森奇妙的爱女士香水 核对样品包装,看是否写全 如果申报单位出错或者更改,可以走补充报告程序
备案检验受理工作要点 符合要求的,进行检验受理编号并出具检验受理通知书,在产品配方、中文说明书上加盖印章 不符合要求的,应当及时以书面或适当方式告知申请企业,并说明理由。
备案检验受理工作要点
国产非特殊用途化妆品备案检验受理通知书
XXX :
国家药监局综合司关于印发化妆品标准制修订工作程序规定(试行)的通知

国家药监局综合司关于印发化妆品标准制修订工作程序规定(试行)的通知文章属性•【制定机关】国家药品监督管理局•【公布日期】2024.08.13•【文号】药监综妆〔2024〕67号•【施行日期】2024.08.13•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】美容业、化妆品管理正文国家药监局综合司关于印发化妆品标准制修订工作程序规定(试行)的通知药监综妆〔2024〕67号国家药监局化妆品标准化技术委员会秘书处、各分技术委员会:《化妆品标准制修订工作程序规定(试行)》已由国家药监局化妆品标准化技术委员会全体委员审议通过。
现印发给你们,请遵照执行。
国家药监局综合司2024年8月13日化妆品标准制修订工作程序规定(试行)第一章总则第一条为了加强化妆品标准化管理,规范化妆品(含牙膏,下同)标准制修订工作,建立公开、透明、高效的化妆品标准制修订工作机制,根据《化妆品监督管理条例》和《国家药品监督管理局化妆品标准化技术委员会章程》等有关规定,制定本规定。
第二条本规定所称化妆品标准,是指由国家药监局依据职责组织制修订,按照法定程序发布,在化妆品生产、经营、监督管理等活动中遵循的统一的技术要求。
化妆品标准包括化妆品强制性国家标准、推荐性国家标准、行业标准、化妆品安全技术规范、化妆品补充检验项目和检验方法等。
第三条本规定适用于化妆品标准的制订、修订,包括立项、起草、验证、审查、批准和发布等,以及化妆品标准制修订快速立项审查程序等。
强制性国家标准、推荐性国家标准的制修订还应当符合国家标准化行政主管部门的规定。
第四条化妆品标准制修订工作应当遵循公平公正、科学规范、急用先行的原则。
第五条化妆品标准实行信息化管理。
中检院(标委会秘书处)负责化妆品标准制修订信息系统(以下简称信息系统)的建设和维护。
第二章标准立项第六条化妆品标准立项建议包括下列来源:(一)标委会秘书处公开征集立项建议;(二)标委会秘书处通过追踪国内外化妆品标准化管理动态等,提出立项建议;(三)分技委通过追踪国内外化妆品标准化管理动态等,提出本专业领域立项建议;(四)国家药监局化妆品相关直属技术支撑机构提出立项建议;(五)各省、自治区、直辖市药品监督管理部门提出立项建议。
国家食品药品监督管理局公告第71号――关于执行《关于实施化妆品

国家食品药品监督管理局公告第71号――关于执行《关于实施化妆品产品技术要求规范有关问题的通知》受理有关事宜
的公告
【法规类别】药品管理
【发文字号】国家食品药品监督管理局公告第71号
【发布部门】国家食品药品监督管理局(原国家药品监督管理局)(已撤销)
【发布日期】2011.03.24
【实施日期】2011.04.01
【时效性】现行有效
【效力级别】部门规范性文件
国家食品药品监督管理局公告
(第71号)
关于执行《关于实施化妆品产品技术要求规范有关问题的通知》受理有关事宜的公告依据《
1 / 1。
2013年第10号通告附件1 - 国产非特殊用途化妆品备案要求

2013年第10号通告附件1 - 国产非特殊用途化妆品备案要求附件1国产非特殊用途化妆品备案要求凡在中华人民共和国境内生产的非特殊用途化妆品~应当按以下要求进行产品备案:一、备案程序相关要求,一,生产企业应当在产品上市销售前整理、归档下列资料:1(产品配方(不包括含量~限用物质除外。
下同,,2(产品销售包装,含产品标签、产品说明书,,3(产品生产工艺简述,4(产品技术要求,5(产品检验报告,6(委托生产协议复印件,委托生产的产品,。
第1、2项资料应当按要求通过统一的网络平台报送至所在地行政区域内的省级食品药品监管部门~其他资料由企业存档备查。
,二,委托生产的产品~委托双方应当分别向所在地行政区域内的省级食品药品监管部门报送备案信息。
境外企业委托国内企业生产的产品及国内企业生产的仅供出口的产品~由实际生产企业向所在地行政区域内的省级食品药品监管部门报送备案信息。
,三,省级食品药品监管部门收到企业备案信息后~应当在5个工作日内组织完成对产品是否属于备案范围、备案信息是否完整、备案信息是否符合规定形式等方面的核查。
产品备案信息符合要求的~经省级食品药品监管部门确认后~在食品药品监管总局政务网站统一公布产品部分信息~供公众查询。
,四,对于不属于备案产品范围的、备案信息不齐全或不符合规定形式的~食品药品监管部门应当在5个工作日内告知企业并说明理由。
食品药品监管部门在备案信息确认过程中发现产品存在明显违法情形的~对尚未上市销售的产品~应当责令改正,对已经上市销售的产品~应当依法予以查处~并在产品备案信息相关栏目予以标注。
,五,省级食品药品监管部门应当在备案后3个月内组织开展对备案产品的检查~发现不符合要求的~责令改正,发现违法的~依法立案查处~并在产品备案信息相关栏目予以标注。
,六,已经备案的产品~拟变更原备案事项的~应当在变更前将相关变更信息通过网络平台重新报送备案,涉及备案管理部门改变的~应当主动注销原备案信息后重新申请备案。
国家食品药品监督管理局关于印发国家食品药品监督管理局国产特殊用途化妆品行政许可批件等式样的通知

国家食品药品监督管理局关于印发国家食品药品监督管理局国产特殊用途化妆品行政许可批件等式样的通知文章属性•【制定机关】国家食品药品监督管理局(已撤销)•【公布日期】2011.03.28•【文号】国食药监许[2011]134号•【施行日期】2011.04.01•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】卫生医药、计划生育综合规定正文国家食品药品监督管理局关于印发国家食品药品监督管理局国产特殊用途化妆品行政许可批件等式样的通知(国食药监许[2011]134号)各省、自治区、直辖市食品药品监督管理局(药品监督管理局),有关单位:为规范化妆品行政许可工作,根据《化妆品行政许可申报受理规定》、《化妆品产品技术要求规范》等有关要求,国家食品药品监督管理局制定了《国家食品药品监督管理局国产特殊用途化妆品行政许可批件》(式样)、《国家食品药品监督管理局进口特殊用途化妆品行政许可批件》(式样)和《国家食品药品监督管理局进口非特殊用途化妆品备案凭证》(式样),现予印发,请遵照执行。
自2011年4月1日起受理的化妆品行政许可(备案)申请,按照本通知执行。
附件:1.国家食品药品监督管理局国产特殊用途化妆品行政许可批件(式样)2.国家食品药品监督管理局进口特殊用途化妆品行政许可批件(式样)3.国家食品药品监督管理局进口非特殊用途化妆品备案凭证(式样)国家食品药品监督管理局二○一一年三月二十八日附件1:国家食品药品监督管理局产品名称产品类别生产企业地址说明:在地址后应注明生产企业卫生许可证号审批结论经审核,该产品符合《化妆品卫生监督条例》的有关规定,现予批准。
批准文号国妆特字G********批准日期年月日请于批件有效期满4个月前提出延续申请。
批准单位盖章国家食品药品监督管理局化妆品产品技术要求(式样)编号:HZGT******** 中文名称汉语拼音名【配方成分】【生产工艺】【感官指标】【卫生化学指标】【微生物指标】【检验方法】【使用方法】【贮存条件】【保质期】说明:本《化妆品产品技术要求》作为国产特殊用途化妆品行政许可批件的一部分,加盖批准单位印章后生效。
国家食品药品监督管理总局通告2013年第10号——关于调整化妆品注册备案管理有关事宜的通告

国家食品药品监督管理总局通告2013年第10号——关于调整化妆品注册备案管理有关事宜的通告文章属性•【制定机关】国家食品药品监督管理总局(已撤销)•【公布日期】2013.12.16•【文号】国家食品药品监督管理总局通告2013年第10号•【施行日期】2013.12.16•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】美容业、化妆品管理正文国家食品药品监督管理总局通告(2013年第10号)关于调整化妆品注册备案管理有关事宜的通告为进一步规范化妆品注册备案管理工作,保障消费者健康权益,依据《化妆品卫生监督条例》及《国务院办公厅关于印发国家食品药品监督管理总局主要职责内设机构和人员编制规定的通知》(国办发〔2013〕24号)的相关规定,现就调整化妆品注册备案管理有关事宜通告如下:一、国产非特殊用途化妆品实行告知性备案自2014年6月30日起,国产非特殊用途化妆品生产企业应当在产品上市前,按照《国产非特殊用途化妆品备案要求》(附件1),对产品信息进行网上备案。
备案的产品信息经省级食品药品监管部门确认后在食品药品监管总局政务网站统一公布,供公众查询,省级食品药品监管部门不再发放国产非特殊用途化妆品备案凭证。
省级食品药品监管部门应当在备案后3个月内组织开展对备案产品的检查,发现不符合要求的,责令改正;发现违法的,依法立案查处,并在产品备案信息相关栏目予以标注。
未按要求履行国产非特殊用途化妆品上市前产品信息报备义务的,依照《化妆品卫生监督条例实施细则》第四十五条第七项相关规定处理。
二、美白化妆品纳入祛斑类化妆品管理目前,市场上大部分宣称有助于皮肤美白增白的化妆品,与宣称用于减轻皮肤表皮色素沉着的化妆品作用机理一致。
为控制美白化妆品的安全风险,决定将其一并纳入祛斑类化妆品管理。
自本通告发布之日起,食品药品监管部门不再受理国产或进口美白产品的非特殊用途化妆品备案申请,生产企业应按照《美白化妆品管理要求》(附件2)进行产品注册申请。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
关于印发化妆品产品技术要求规范的通知
国食药监许[2010]454 号
2010 年11 月26 日发
布各省、自治区、直辖市食品药品监督管理局(药品监督管理局):
为进一步规范化妆品行政许可工作,提高化妆品卫生质量安全控制水平,加强化妆品生产经营卫生监督,指导化妆品
产品技术要求编制工作,国家食品药品监督管理局组织制定了《化妆品产品技术要求规范》,现予印发,请遵照执行。
附件:1.国家食品药品监督管理局化妆品产品技术要求(文本格式)
2.化妆品产品技术要求编制指南
国家食品药品监督管理局
二0一0年十一月二十六日
化妆品产品技术要求规范
一、根据《化妆品卫生监督条例》,为进一步规范化妆品行政许可工作,提高化妆品卫生质量安全控制水平,加强化妆品生产经营卫生监督,保障消费者使用安全,制定本规范。
二、国家食品药品监督管理局负责批准化妆品产品技术要求,并监督其执行。
三、化妆品产品技术要求应当符合国家有关法律法规、标准规范。
四、化妆品产品技术要求应符合其文本格式的规定。
文本格式应当包括产品名称、配方成分、生产工艺、感官指标、卫生化学指标、微生物指标、检验方法、使用说明、贮存条件、保质期等序列(见附件1),并按照《化妆品产品技术要
求编制指南》(见附件2 )编制。
五、化妆品产品技术要求是产品卫生质量安全的技术保障。
生产企业应当按照化妆品产品技术要求组织生产经营,食品药品监督管理部门应当将化妆品产品技术要求作为开展卫生监督执法的重要依据。
六、化妆品产品技术要求适用于化妆品新产品的许可和产品延续。
七、化妆品产品技术要求编号。
国产特殊用途化妆品按照HZ+GT+ 年份+0000 编制;进口特殊用途化妆品按照HZ+JT +年份+0000编制;进口非特殊用途化妆品按照HZ+JF+年份+0000编制。
"HZ"表示"化妆品”,"GT"表示"国产特殊用途”,
"JT"表示"进口特殊用途”,”JF"表示"进口非特殊用途”,"年份+0000"为化妆品批准文号(或备案号)的年份和顺序号。
八、本规范自2011 年4 月1 日起施行。
附件1
国家食品药品监督管理局
化妆品产品技术要求(文本格式)
产品技术要求编号)
中文名称
汉语拼音名
配方成分】
生产工艺】
感官指标】
卫生化学指标】
微生物指标】
检验方法】
使用方法】
贮存条件】
保质期】
附件2 :
化妆品产品技术要求编制指南
一、主要内容
化妆品产品技术要求应当能够准确反映和控制产品的卫生质量安全。
化妆品产品技术要求的每项内容应符合以下要求,并按照化妆品产品申报资料的具体要求进行编制。
(一)产品名称包括中文名称和汉语拼音名。
产品名称应当准确、清晰,能表明产品的真实属性,符合《化妆品命名规定》。
(二)配方成分配方成分应包括生产该产品所使用的全部原料。
所有原料应按含量递减顺序排列,并注明其使用目的。
化妆品使用的原料应符合《化妆品卫生规范》的相关要求。
配方成分中所用原料的中文名称应使用《国际化妆品原料标准中文名称目录》标准中文名称。
原料无国际化妆品原料名称(INCI 名称)或未列入《国际化妆品原料标准中文名称目录》的,应使用《中国药典》中的名称或化学名称或植物拉丁学名。
(三)生产工艺
应用文字简要描述完整的生产工艺。
(四)感官指标
分别对产品内容物应有的颜色、性状、气味等感官指标依次进行描述,并用分号分开。
(五)卫生化学指标
(六)微生物指标感官指标、卫生化学指标、微生物指标等相关内容应阐述根据《化妆品行政许可检验管理办法》等有关要求确定的检测项目、指标。
如果用表提供信息有利于检测项目的理解,则宜使用列表。
(七)检验方法
应将卫生化学指标、微生物指标的检验方法依次列出。
(八)使用方法
应阐述化妆品的使用方法及其注意事项。
(九)贮存条件应根据产品包装及产品自身稳定性等特点阐述产品贮存条件,如温度、避光保存等。
(十)保质期应根据相关实验结果确定产品保质期,保质期的格式应标注为:生产日期和保质期或生产批号和限用使用日期。
二、基本要求
(一)编制工作应符合国家法律、行政法规、部门规章、技术标准和规范性文件的相关规定。
(二)产品技术要求的设计、内容和数据应符合公认的科学原理,准确可靠。
(三)产品技术要求的文字、数字、公式、单位、符号、图表等应符合标准化要求,引用的标准准确、有效。
术语的定义应符合国家有关规定。
1. 应使用规范汉字。
使用的标点符号应符合GB/T15834 的规定。
2. 应使用GB3101 、GB3102 规定的法定计量单位。
表示量值时,应写出其单位。
3. 应准确列出引用标准或文件的目录。
4. 引用的标准或文件应包括出版本号或年号以及完整的标准(文件)名称。
5. 如果引用的标准(文件)可以互联网在线获得,应提供详细的获取和访问路径。
应给出被引用标准(文件)的完整的网址。
为了保证溯源性,应提供源网址。
(四)产品技术要求中所建立的检测方法准确、精密,并经过方法学验证。
(五)产品技术要求中有限量要求的,须使用明确的数值表示。
不应仅使用定性的表述,如"适量"或"合适的温度"等。
(六)产品技术要求研究的实验记录书写应真实、完整、清晰,保持原始性并具有可追溯性。
其研究方法和过程要如实记录,并在申报资料中予以充分体现。
(七)产品技术要求中使用的表均应在条文中明确提及。
1. 不准许表中有表,也不准许将表再分为次级表。
2. 每个表均应有编号。
表的编号由"表"和从1开始的阿拉伯数字组成,例如"表1"、"表2"等。
只有一个表时,仍应给出编号" 表1"。
3. 每个表应有表题。
4. 每个表应有表头。
表栏中使用的单位一般应置于相应栏的表头中量的名称之下,表头中不准许使用斜线。
5. 如果某个表需要转页接排,则随后接排该表的各页上应重复表的编号、表题和"(续)"。
续表均应重复表头和关于
单位的陈述。
(八)产品技术要求可能涉及知识产权的,国家食品药品监督管理部门不承担识别该知识产权的责任。
(九)应使用国家法定部门认可的标准物质(包括标准品和对照品)。
若使用的对照物质是自行研制的,应按相关的要求提交相应的鉴定研究资料和对照物质。
供研究用样品应是配方确定、生产工艺稳定、具有代表性的多批产品。
(十)开展产品技术要求的研究,应在能满足该产品技术要求研究条件的实验室进行,并由相应技术人员承担。
THANKS !!!
致力为企业和个人提供合同协议,策划案计划书,学习课件等等
打造全网一站式需求
欢迎您的下载,资料仅供参考。
