平流层化学
6第六章 平流层化学

UV-B: 280-315nm 臭氧吸收 绝大多数,危害大;
UV-C: <280nm 氧、臭氧完 全吸收,危害极大
6.1.2、平流层的化学特征
1. 臭氧层
对于臭氧的垂直分布,平流层占整个大气臭氧总量的 90%以上,在高度20-25km范围内,臭氧含量很高,因此 称之为“臭氧层”。
1985年在南极上空有一个“臭氧空洞”,其臭氧含量 下降了40%。
南
计极
算
机 的
臭
三
维 模
氧
拟
图浓
度
1、臭氧损耗最严重的区域基本上是 离地面15~25km的范围。
2、臭氧发生损耗最为严重的区域也 是气温最低的区域,这一高度范围 内10月左右的气温处于-80℃以下。
南极臭氧洞的损耗状况仍在恶化: ❖ 1、1997年至今,科学家进一步观测到臭氧洞发
造成臭氧洞的元凶。 ❖ 深入的科学研究发现,南极臭氧洞的形成机制是平
流层云表面的非均相过程。
1、为什么仅仅在南极、北极出现臭氧空洞?
2、为什么在热带地区的平流层中没有发现 臭氧层的破坏?
南极地区特殊的气候环境:
❖ 1、南极地区上空的温度极低 ❖ 2、在极低的温度下,天然过程中释放到平流层的含硫化
合物转化形成的硫酸,使得南极平流层地区生成颗粒物成 为可能。
含卤族化合物以极易光解的HOCl,Cl2气态的形式释放出来
❖ 6、春天,紫外线增多,Cl2和HOCl便开始大量地发生光解 ,产生大量的原子氯,以致造成严重的臭氧损耗。
❖ 7、随着更多的太阳光到达由极,南极地区的温度上升, 结果使南极涡旋逐渐消失。
南极臭氧损耗过程示意图:
平流层光化学

环科院 焦岩
平流层中几个主要物种族循环
?源分子:
?在对流层相对寿命较长,进入平流层后,发生解 离,产生自由基。( H2O,N2O,CH4/CFCs)
?活性基:
?由源分子产生的中间体,寿命短,引发反应。
?HOx (OH,HO2),NOx (NO,NO2),ClOX(Cl,ClO) ?储库分子:
?活性基与其它物种分子结合,生成稳定的长寿命 分子,使链反应中止。
?HNO3,HCl, ClONO 2,N2O5
第三章 平流层的光化学
环科院 焦岩
奇氢族的循环
?平流层奇原子氢 HOx主要产生机制:
O(1D)+H 2O ? 2OH
O(1D)+H 2 ? OH+H
O(3P)+H 2O ? 2OH (不能发生)
?平流层奇原子氢 HOx主要消耗机制:
HO 2 ? OH ? H 2O+O 2
3. O 3 ? h? ? O(3P) +O 2 (1? g ) 310< ? <350nm
O3 的弱选择吸收带- Huggins 带 4. O 3 ? h? ? O( 3P) +O 2 (3? g ) 450< ? <750nm
O第三章3的平流弱层的吸光化收学 带- Chappuis 带
环科院 焦岩
2. O 2 ? h? ? O( 3P) +O( 3P)
中间层中部
176< ? <195nm
3. O 2 ? h? ? O( 3P) +O( 3P) 185< ? <242nm
Herzberg 连续带 平流层
平流层奇原子氧的主要来源,对决定O平3浓流度层起主要作用
平流层化学
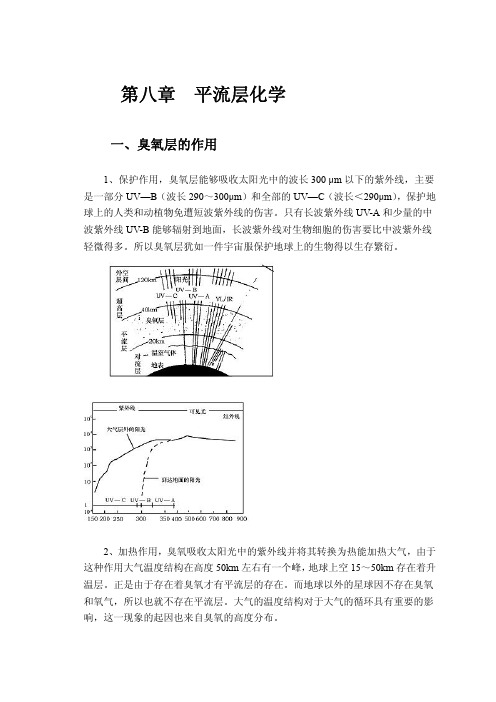
第八章平流层化学一、臭氧层的作用1、保护作用,臭氧层能够吸收太阳光中的波长300 μm以下的紫外线,主要是一部分UV—B(波长290~300μm)和全部的UV—C(波长<290μm),保护地球上的人类和动植物免遭短波紫外线的伤害。
只有长波紫外线UV-A和少量的中波紫外线UV-B能够辐射到地面,长波紫外线对生物细胞的伤害要比中波紫外线轻微得多。
所以臭氧层犹如一件宇宙服保护地球上的生物得以生存繁衍。
2、加热作用,臭氧吸收太阳光中的紫外线并将其转换为热能加热大气,由于这种作用大气温度结构在高度50km左右有一个峰,地球上空15~50km存在着升温层。
正是由于存在着臭氧才有平流层的存在。
而地球以外的星球因不存在臭氧和氧气,所以也就不存在平流层。
大气的温度结构对于大气的循环具有重要的影响,这一现象的起因也来自臭氧的高度分布。
3、温室气体的作用,在对流层上部和平流层底部,即在气温很低的这一高度,臭氧的作用同样非常重要。
如果这一高度的臭氧减少,则会产生使地面气温下降的动力。
因此,臭氧的高度分布及变化是极其重要的。
二、臭氧层破坏的危害臭氧层耗减对全球环境造成的影响,只能是从最近10多年的环境情况与10多年前或更早年代的情况相比,发现了某些特异的变化,就目前情况而言,还不能认为已经产生了明显的严重后果。
臭氧层的耗减产生的直接结果就是使太阳光中的紫外线UV-B达到地面的数量增加。
通常认为臭氧浓度降低1%,UV-B辐射量增加1 .5~2%。
紫外线UV-B能破坏蛋白质的化学键,杀死微生物,破坏动植物的个体细胞,损害其中的脱氧核糖核酸(DNA),引起传递遗传特性的因子变化,发生生物的变态反应。
下面就其对人类健康、生物和环境等产生的危害予以介绍。
1、对人类健康的影响适量的紫外线照射对人体的健康是有益的,它能增强交感肾上腺机能,提高免疫能力,促进磷钙代谢,增强人体对环境污染物的抵抗力。
但是长期反复照射过量紫外线将引起细胞内的 DNA改变,细胞的自身修复能力减弱,免疫机能减退,皮肤发生弹性组织变性、角质化以至皮肤癌变,诱发眼球晶体发生白内障等。
大气层的化学组成

大气层的化学组成大气层是地球重要的外部层,因为它对生命的存在和发展,以及地球环境的稳定性都有着不可替代的作用。
而大气层中有着各种各样的化学物质,这些物质又分别有着不同的来源和作用,这篇文章就来讲讲大气层的化学组成。
第一部分:概述大气层的化学组成大气层按照海拔高度分为五个层次:对流层、平流层、中间层、热层和外层。
不同层次的大气层中的化学组成也有所不同。
大气层主要由气体、杂质、和微粒组成。
其中气体是最主要的组成部分,约占到99%以上。
第二部分:大气层的气体成分大气层的气体成分主要包括氮、氧、氩、氦、甲烷、二氧化碳和水蒸气等。
氮是大气层中最主要的成分,占到了78%以上,因为它是地球上大气层的主要来源之一。
氧的结构与氮类似,但是占的比例只有21%左右。
氦是稀有气体,存在于平流层和外层之间,占大气层质量的0.0005%左右。
甲烷是温室气体,是人类活动的主要产物,它可以在大气层中吸收长波辐射从而导致温室效应。
二氧化碳是另一种温室气体,它也与人类活动有很大的关系,其浓度随着人类活动的增加而增加。
最后,水蒸气是大气层中的水分,它对天气和气候有着重要的影响。
第三部分:大气层的杂质成分大气层中的杂质成分主要包括氮氧化物、二氧化硫、臭氧、碳氢化合物和微粒等。
氮氧化物是立体烷基和直链分子异氰酸甲酯分解出的气体,是一种空气污染物。
二氧化硫存在于大气层中是由于火山喷发、工业生产中的燃煤和石油等化石燃料燃烧时散发出来的。
臭氧存在于平流层中,对于地球与人类健康有着重要的作用。
由于化学反应和人类活动的影响,臭氧的含量会有一定的变化。
碳氢化合物一般存在于低层大气层,与温室效应有关。
最后,具有相同材质和形状的颗粒物在大气层中漂浮着,并成为行星在空中的折射因素。
第四部分:大气层的微粒成分大气层中的微粒成分主要包括液态水、土壤颗粒、泥沙、沙尘等。
液态水是水蒸气凝结时形成的雾霾,它与人类和动物的健康有着重要的关系,会引起许多呼吸道疾病和过敏症。
环境化学复习

第二章大气环境化学1、大气层的结构 Layers of the Atmosphere(英文)A、对流层troposphere对流层是大气的最底层,其厚度在赤道附近为16—18km;在中纬度地区为10—12km,两极附近为8—9km。
最显著特点是气温随海拔高度的增加而降低,大约每上升100m,温度降低0.6度。
另一个特点是密度大,大气总质量的3/4以上集中在对流层。
B、平流层stratosphere从对流层顶到海拔高度约为50km的大气层。
特点:①空气没有对流运动,平流运动占显著优势。
②空气比对流层稀薄得多,水汽、尘埃的含量甚微,很少出现天气现象③在高15—60km内,有约20km的一层臭氧层The Ozone Layer。
O2→O•+O•、O•+O2→O3、O3→O•+O2、O3+O•→2O2是臭氧光解的过程。
平流层温度随海拔高度的增加而增加。
C、中间层mesosphere从平流层顶到80km高度的大气层。
空气较稀薄,由于臭氧层消失,温度随海拔高度的增加而迅速降低。
D、热层(电离层)thermosphere从80km到约500km的大气层。
大气温度随海拔高度的增加而迅速增加。
2.大气中的主要污染物含硫化合物;含氮化合物;含碳化合物;含卤素化合物2、辐射逆温层Radiation inversion对流层大气的重要热源是来自地面的长波辐射,故离地面越近气温越高;离地面越远气温越低。
随高度升高气温的降低率称为大气垂直递减率:Γ=-dT/dz T—热力学温度K, z—高度当Γ=0 时,称为等温气层;当Γ<0 时,称为逆温气层。
这时气层稳定性强,对大气的垂直运动的发展起着阻碍作用。
根据逆温形成的过程不同,可分为两种:近地面层的逆温:辐射逆温、平流逆温、融雪逆温、地形逆温;自由大气的逆温:乱流逆温、下沉逆温、锋面逆温气块在大气中的稳定度与大气垂直递减率(Γ)和干绝热垂直递减率(Γd)两者有关。
若Γ<Γd,表明大气是稳定的;若Γ>Γd,大气是不稳定;若Γ=Γd,大气处于平衡状态。
平流层臭氧生成途径解析

平流层臭氧生成途径解析平流层臭氧是指大气中位于地球表面上部的平流层中存在的臭氧。
它在平流层中起着重要的作用,既是大气层中的一种温室气体,也对地球上的生物圈发挥着保护作用。
然而,平流层臭氧的生成并非简单,它是通过复杂的化学反应途径才能形成的。
本文将解析平流层臭氧生成的途径,以便更深入地理解大气中臭氧的形成机制。
首先,平流层臭氧的生成主要是通过光解作用。
太阳辐射中的紫外线照射到平流层中的氧分子(O2)上,将其分解成两个单独的氧原子(O)。
这是一个光化学反应,需要能量来克服化学键的能量。
这些单独的氧原子与其他氧分子结合形成臭氧分子(O3)。
这个反应过程可以分为两个步骤:第一步是氧分子的光解,第二步是单独的氧原子与氧分子的反应生成臭氧。
其次,平流层臭氧的生成也与一氧化氮(NO)有关。
在平流层中,一氧化氮主要由人类活动排放的氮氧化合物和自然放电产生的雷电过程中产生。
一氧化氮经过光解或与臭氧反应生成一氧化氮和氧原子(NO2 + O → NO + O2),这些氧原子与臭氧反应形成一氧化氮和臭氧(O + O3 → 2O2)。
一氧化氮和臭氧之间的循环反应使得平流层中的臭氧浓度得以增加。
此外,甲烷以及其他碳氢化合物也参与了平流层臭氧的生成。
甲烷是一种大气中的主要温室气体,它主要来自于湿地、生物发酵和化石燃料燃烧等过程。
甲烷经过一系列的化学反应,最终与一氧化氮反应生成臭氧(CH4 + NO → CH3 + HNO2,CH3 + O2 → CH3O2,CH3O2 + NO → CH3O + NO2,CH3O + O2 → CH2O +HO2)。
这些反应过程中的自由基链式反应产生了大量的CH3O,它与氮原子一起参与到了臭氧的生成过程中。
另外,氯氟碳化物(CFCs)也是平流层臭氧生成的重要因素。
CFCs是一类人造化学物质,常用于制冷剂、驱动剂和泡沫剂等工业应用中。
然而,CFCs会通过大气层上升到平流层,并被紫外线辐射分解释放出氯原子。
环境化学期末复习资料
环境化学期末复习资料第⼆章⼤⽓环境化学1.⼤⽓主要成分N2(78.08%)、 O2(20.95%)、 Ar(0.943%)和CO2(0.0314%)。
⼏种惰性⽓体:He、Ne、Kr和Xe的含量相对⽐较⾼。
⽔蒸⽓的含量是⼀个可变化的数值,⼀般在1% ~3%.2.⼤⽓层的结构1. 对流层(Troposphere)⾼度: 0~(10~16) km ,随纬度和季节发⽣变化温度:⼤约每上升100 m,降低 0.6 ℃空⽓运动:低纬度较强,⾼纬度较弱,夏季较强,冬季较弱密度:密度⼤,占⼤⽓总质量的3/42.平流层(Stratosphere)⾼度: (10~16)~50 km温度:同温层 [对流层顶端~(30~35 km)]30~35 km以上开始下降空⽓运动:没有对流,平流为主空⽓稀薄,很少出现天⽓现象3. 中间层 (Mesosphere): 50~80 km4.热层(电离层)(Thermosphere):80~500 km吸收紫外线造成温度上升,空⽓⾼度电离,因此也称为电离层,占⼤⽓质量的0.5%5. 逃逸层,外⼤⽓层 (Exosphere)3.辐射逆温层对流层⼤⽓的重要热源是来⾃地⾯的长波辐射,故离地⾯越近⽓温越⾼;离地⾯越远⽓温越低。
随⾼度升⾼⽓温的降低率称为⼤⽓垂直递减率:Γ=-dT/dz式中:T——热⼒学温度,K;z——⾼度。
在对流层中,dT/dz<0,Γ = 0.6 K · (100m)-1,即每升⾼100 m ⽓温降低0.6 ℃。
⼀定条件下出现反常现象当Γ=0 时,称为等温层;当Γ<0 时,称为逆温层。
这时⽓层稳定性强,对⼤⽓的垂直运动的发展起着阻碍作⽤。
辐射逆温产⽣特点●是地⾯因强烈辐射⽽冷却降温所形成的。
●这种逆温层多发⽣在距地⾯ 100~150 m ⾼度内。
●最有利于辐射逆温发展的条件是平静⽽晴朗的夜晚。
●有云和有风都能减弱逆温。
●风速超过 2~3 m · s-1,逆温就不易形成4.主要⾃由基及其来源HO ?和HO2 ?来源1) HO ?来源清洁⼤⽓:O3 的光解是清洁⼤⽓中HO ?的重要来源O3 + h→ O ? + O2O ? + H2O → 2HO ?污染⼤⽓,如存在HNO2,H2O2 (HNO2 的光解是⼤⽓中HO ?的重要来源)HNO2 + h→ HO ? + NOH2O2 + h→ 2HO ?2)HO2 ?来源①主要来⾃醛类的光解,尤其是甲醛的光解H2CO + h→ H ? + HCO ?H ? + O2 + M → HO2 ? + MHCO ? + O2 → HO2 ? + CO②只要有 H ?和 HCO ?存在,均可与 O2 反应⽣成 HO2 ?③亚硝酸酯和 H2O2 光解CH3ONO + hv → CH3O ? + NOCH3O ? +O2 → HO2 ? + H2COH2O2 + hv → 2HO ?HO ? + H2O2 → H2O + HO2 ?④若有CO存在,则:HO ? + CO → CO2 + H ?H ? + O2 → HO2 ?R ?,RO ?,RO2 ?来源1) R ?烷基⾃由基来源:⼤⽓中存在最多的烷基是甲基,它的主要来源是⼄醛和丙酮的光解。
第六章平流层臭氧.
1 臭氧层形成与损耗的化学反应 2 臭氧层耗损物质 3 替代化合物 4 替代物对平流层臭氧的影响
5 替代物的臭氧损耗潜势
平流层臭氧
臭氧层存在于平流层中,主要分布在距地 面 15-35 km范围内,浓度峰值在20-25km处。 由于臭氧层能够吸收99%以上来自太阳的紫外 辐射(240~320nm),从而保护了地球上的生 物不受其伤害。
为什么?
臭氧层的形成与损耗的化学反应
1 、清洁大气中:O3 的形成 O2 + hv → 2O(200nm) O + O2 + M → O 3 + M 总反应 : 3O2 + hv → 2O3 2、O3 的猝灭 O3 + hv → O + O2(240-320nm) O3 + O → 2O2 两种反应动态平衡,维持臭氧层一定厚度。当大气被污 后,导致 O3 的猝灭,影响 O3 的厚度 。
要,主要是传输至对流层。 所以CF3Ox对O3的破坏不重要,而且永久性汇
机制更进一步降低了CF3Ox破坏。
(3)FC(O)Ox对臭氧层的破坏 含氟替代物的降解产物HC(O)F及C(O)F2能少 量地光解生成FC(O)自由基, FC(O)与O2迅速 结合生成FC(O)O2自由基。 FC(O)O2+O3→ FC(O)O+ 2O2 FC(O)O +O3→ FC(O)O2+O2 (K<6×10-14cm3· mol-1· s-1) 总反应:2O3 → 3O2 FC(O)O+NO →CO2+FNO(FC(O)O的永久性汇) (根据反应速率和平流层中NO和O3的浓度值,说明 FC(O)O对O3的破坏不重要。)
人们使用冰箱、空调时释放出的氟氯烃化 1、原因: 合物,通过光化学反应大量消耗臭氧。
对流层平流层主要化学成分
对流层平流层主要化学成分1.引言1.1 概述概述对流层平流层是大气层中最底部的两个层次,分别位于地球表面上方的对流层和平流层。
对流层主要是人类活动和大气循环的关键,而平流层则是大气层中更稳定和较少变化的区域。
对流层平流层中存在着许多化学成分,这些成分对于地球的气候、气象和生态系统有着重要的影响。
对流层主要化学成分主要包括氮气、氧气和水蒸气。
其中,氮气是最主要的成分,占据大约78的体积百分比。
氮气在大气循环中起着重要的作用,它不会直接参与化学反应,但是通过生物固定和氮氧化还原反应,氮气在大气中的含量可以发生变化。
氧气是大气中的第二大成分,占据大约21的体积百分比。
氧气对于维持生命起着关键作用,它是动物和植物进行呼吸和新陈代谢所必需的气体。
此外,氧气也参与了许多大气和地球化学过程,如臭氧形成和大气氧化作用。
水蒸气是大气中存在的重要化学成分之一。
它是地球上水循环的主要组成部分,也是大气变温和降水的关键因素。
水蒸气的含量随着温度和湿度的变化而变化,在大气中形成云、雨和雪等形式。
平流层主要化学成分相对稳定,主要由臭氧、氮氧化物和甲烷等组成。
臭氧是平流层中最重要的化学成分之一,它在平流层中形成臭氧层,起到了有效过滤和吸收紫外线辐射的作用。
氮氧化物和甲烷则参与了大气中的温室效应和大气化学反应。
探究对流层平流层主要化学成分对于了解大气层的组成和演化、气候变化和环境污染等方面具有重要意义。
在未来的研究中,我们需要进一步了解这些化学成分的来源、分布和相互作用,以及它们对人类活动和地球生态系统的影响。
通过深入研究对流层平流层主要化学成分,我们可以更加全面地认识和应对大气环境问题。
1.2 文章结构文章结构部分的内容可以包括以下方面:本文将按照以下结构来探讨对流层平流层的主要化学成分。
首先,在引言部分,我们将对本文要研究的问题进行概述,简要介绍对流层平流层的主要化学成分及其重要性,引发读者对该话题的兴趣。
接着,在正文部分,我们将分别讨论对流层和平流层的主要化学成分。
大气环境化学课件-平流层化学
三、平流層化學研究進展
1995年諾貝爾化學獎——人類活動影響平流層臭氧研究
左:Paul Crutzen(荷蘭) 中:Mario Molina(墨西哥) 右:F.SheRwood Rowland (美國)
1995年諾貝爾化學獎——人類活動影響平流 層臭氧研究
20多年前, Paul Crutzen“第一次把臭氧問題擺在人們的 面前”,他指出人類活動釋放的少量物質能夠損害全球範 圍的臭氧,把平流層的研究引導上正確的道路。
甲烷產生水蒸氣,對平流層 化學反應有重要影響。
3. ClOx和BrOx
源:
CH 3Cl hv Cl CH 3
CFCl3 hv(175nm 220nm) CFCl2 Cl
CFCl2 hv(175nm 220nm) CFCl Cl
O(1D) CFnCl4 n CFnCl3 n ClO
80年代,距地10-55km的南極出現臭氧洞,1987年,北 極也出現。
近幾年臭氧洞的深度和麵積仍在繼續擴展,1998 年臭氧洞的持續時間超過了100天,是南極臭氧 洞發現以來的最長記錄,而且臭氧洞的面積也在 擴大,相當於3個澳大利亞。
2000.9.3南極上空2830萬km2(中國面積2倍多、 美國3倍),今後20年,臭氧層處於最脆弱狀態。
陶普生單位(Du):1Du相當於10-3大氣釐米 其他品質單位:混合比和品質濃度
二、臭氧層的作用
太陽光組成:紅外光50%;可見光40%; 紫外光10%;其餘部分1%;
太陽光中的紫外線可劃分為: UV-A(315~400nm) UV-B(280~315nm) UV-C(280nm以下)
三個波段中UV-B輻射對生物有較大的傷害。而阻擋 UV-B輻射的就是臭氧。
O2+hv(λ<240nm)→O+O O2+O+M →O3+M O3+hv(λ<290nm)→O2+O O3+O →2O2 O+O+M →O2+M
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2.3.1 来源 天然:海洋生物产生卤代烷的光解 CH3Cl、CH3Br,大部
分在对流层反应去除,小部分输送至平流层光解。
CH3Cl + h(UV) CH3Br + h(UV)
Cl + CH3 (高层) Br + CH3 (低层)
2.3.2 催化机制 高层:
Cl + O3 ClO + O 总 O3 + O
NO2 + ClO + M
ClONO2 + M
ClONO2 + h 460nm
ClO + NO2
NO2 + HO2 + M
HO2NO2 + M HO2NO2 + Cl HO2NO2 + ClO HO2NO2 + HO
夜间
HO2NO2 + M
NO2 + HO2 + M
NO2 + HCl + O2 NO2 + HOCl + O2 NO2 + H2O + O2
低层:
Br + O3 BrO + O 总 O3 + O
协同效应:
BrO + ClO
ClO + O2 Cl + O2
2 O2
决速步
BrO + O2 Br + O2
2 O2
决速步
Br + Cl + O2
竞争:
Cl + CH4
CH3 + HCl
OH + HCl
Cl + H2O
Cl + HO2
1.1 Chapman机制
生成:
总: 去除:
(a)
(b)
总: (c)
O2 + h 242nm 2 O + O2 + M
O+O 2 O3 + M
3 O2 + h
3 O3
O3 + h 1140nm
O2 + O
O + O2 + M
O3 + M
O3 + h 1140nm
O2 + O
O3 + O 2 O3 + h
HO、HO2),含卤自由基Clx或ClOx(Cl、ClO)、Brx或
BrOx(Br、BrO)
<返回>
消耗比
Chapman(O3 + O2)
NOx HOx Clx(ClO)
20~30%
50~70% 10~20 <1%
2.1.1 来源 主:
N2O + h 315nm N2O + O(1D)
N+ O
N2 + O N2 + O2
2.2.1 来源
H2O + O(1D) CH4 + O(1D)
H2 + O(1D) H + O2
2.2 HOx
HO + HO HO + CH3 HO + O3 HO2 + O3
总 2 O3
O2 + HO2 O2 + HO + O2
总 2 O3 + h
O2 + NO3 O2 + NO
NO2 + O2
决速步
3 O2
竞争
NO2 + OH + M
HONO2 + h 345nm HONO2 + OH NO3 + h NO3 + h
HONO2 + M HO + NO2
H2O + NO3 NO + O2 NO2 + O
NOx的储库:可减弱NOx对O3耗损,HONO2、ClONO2、 HO2NO2
HOBr + h
NO2 + O3 NO3 + NO2
白天
O2 + NO3 N2O5
N2O5 + h 400nm
O + 2 NO2
2.1.3 分布和汇 分布:20~25km,NO、NO2,10ppb;<20km,HONO2
汇:平流层顶(弱作用)
NO + h 192nm N + NO N + NO2
H2O2 + h <300nm
HONO2 HO + NO2 HO2NO2 HO2 + NO2 + M H2O2 + O2
HO + HO
2.2.3 分布和汇 分布:<40km,HONO2、H2O2;>40km,HO、H 汇:可输入对流层被雨除
2.3 含氯和溴自由基Clx(ClOx)和Brx(BrOx)
O2 + HCl
HCl + h
Cl + H
ClO + NO2 + M
ClONO2 + M
ClONO2 + h 460nm
Cl + NO3
Br + HO2
O2 + HBr
HBr + h
Br + H
BrO + NO2 BrONO2 + h
HBr + OH
BrONO2 Br + NO3 H2O + Br
2 O2 3 O2
垂直向下输送到对流层
(1) (2) (3)
(4)
(a)过程并不清除O3,Ox = O + O3,只是吸收了UV转化为热能,是臭氧层基本功 能和平流层逆温原理。
1.2 催化机制
O3 + X XO + O
总 O3 + O
O2 + XO O2 + X
2 O2
X = 含氮氧化物NOx(NO、NO2),含氢自由基HOx(H、
次:
N2 + 宇宙射线 N + O2 N + O3
2.1 NOx
N2 + O(1D) NO + NO
N+ N NO + O NO + O2
2.1.2 催化机制
中平流层
O3 + NO NO2 + O
总 O3 + O
O2 + NO2 O2 + NO
2 O2
决速步
低平流层
NO2 + O3 O3 + h NO + O3
EUV UVC UVB
~290nm 290~320nm
被 O2、O 吸收 被 O3 吸收 90%被 O3 吸收
粒种: 源分子
活性基 储库分子
地表天然过程或人为活动排放,在对流层寿命较长而进入平流层发生光解,
包括 N2O、CH4、CFCs 等。 链反应中的活性基团,可在反应中再生。
活性基与其它分子形成的相对稳定的分子,可降低活性基作用,包括 HONO2、 ClONO2、HCl、H2O2、N2O5 等;可输入对流层发生化学反应再湿去除。
平流层化学
内容
1 平流层臭氧的基本光化学 2 各活性物种源、汇和储库 3 大气中源气体与其它气体的变化对平流层臭氧的影响 4 臭氧洞
10~55km 平流层,逆温特点,垂直对流弱
15~40km 臭氧层,占有90%臭氧,10ppm;O3可吸收 ≤300nm辐射,主要是紫外
<返回>
3 O2
决速步
高层
HO + O3 HO2 + O
总 O3 + O
O2 + HO2 O2 + HO
2 O2
决速步
H + O3 HO + O
O2 + HO O2 + H
决速步
总 O3 + O
2 O2
竞争
HO + NO2 HONO2 + h
HO2 + NO2 HO2NO2 + M
HO2 + HO2
