《化工原理II》计算试题
化工原理第二版习题答案

化工原理第二版习题答案化工原理第二版习题答案化工原理是化学工程专业的一门重要基础课程,它涉及到化学反应、质量平衡、能量平衡等方面的知识。
而习题是学习化工原理的重要方式之一,通过解答习题可以加深对知识的理解和掌握。
本文将为大家提供化工原理第二版习题的详细答案,希望能够对大家的学习有所帮助。
1. 题目:给出一个化学反应的平衡方程:2A + 3B → C + 4D。
已知在某一反应条件下,A的初始浓度为1mol/L,B的初始浓度为2mol/L,C和D的初始浓度均为0。
求在该反应条件下,C和D的最终浓度。
答案:根据平衡常数的定义,可以得到反应的平衡常数K为:K = [C][D]^4 / [A]^2[B]^3。
根据题目中给出的初始浓度,可以得到:[A] = 1mol/L,[B] =2mol/L,[C] = 0,[D] = 0。
代入平衡常数的定义式中,可以得到:K = 0 / (1^2 * 2^3) = 0。
由于K = 0,可以得知在该反应条件下,C和D的最终浓度均为0。
2. 题目:在一个封闭的容器中,有2mol的A和3mol的B。
经过一段时间后,A的浓度减少了1mol/L,B的浓度增加了2mol/L。
求该反应的平衡常数K。
答案:根据平衡常数的定义,可以得到反应的平衡常数K为:K = [C][D]^4 / [A]^2[B]^3。
根据题目中给出的初始浓度和最终浓度变化,可以得到:[A]初始= 2mol/L,[A]最终 = 1mol/L,[B]初始 = 3mol/L,[B]最终 = 5mol/L,[C] = 0,[D] = 0。
代入平衡常数的定义式中,可以得到:K = 0 / (1^2 * 5^3) = 0。
由于K = 0,可以得知该反应的平衡常数为0。
3. 题目:一个反应的平衡常数K为0.5,初始时反应物A的浓度为2mol/L,B的浓度为4mol/L,产物C的浓度为1mol/L,D的浓度为2mol/L。
求该反应的最终浓度。
化工原理第二章习题及答案

化工原理第二章习题及答案1. 有一气缸,内径为100mm,在一个压力器中充入25升压缩空气(压力为2.5MPa),用这个压缩空气推动空气缸推出500mm,求气缸推力和机械效率。
解答:气缸推力的计算公式为:F=P*A 其中,P为气缸内气压力,A为气缸有效面积。
首先,需要根据气缸内径计算出气缸有效面积。
气缸有效面积的计算公式为:A=π*(D^2 - d^2)/4 其中,D为气缸外径,d为气缸内径。
根据气缸内径100mm可得:D=100mm+(2×5mm)=110mm由此可得气缸有效面积:A=π*(1102-1002)/4=0.00813m^2因此,气缸推力为:F=2.5×0.00813=0.02033MN其次,需要根据机械原理计算气缸的机械效率。
气缸的机械效率为:η=F_load/F_in 其中,F_load为气缸的推力,F_in为压缩空气所做的功。
压缩空气所做的功为:W=P_1V_1ln(P_2/P_1) 其中,P_1为压缩前的气压,V_1为压缩前的容积,P_2为压缩后的气压。
压缩空气所做的功为:W=2.5×25×10^-3×ln(0.1/2.5)=-0.621J因此,气缸的机械效率为:η=0.02033/(-0.621)= -0.0327答案:气缸推力为0.02033MN,机械效率为-0.0327。
2. 在一艘船上,柴油机每小时消耗燃油1000升,每升燃油能释放38000J的热量,求柴油机的功率。
解答:柴油机的功率可以通过燃烧的热量和时间来计算。
柴油机的功率公式为:P=W/t=Q/t 其中,W为做功的量,t为做功的时间,Q为燃料燃烧所释放的热量。
柴油机燃料燃烧释放的热量为:Q=m_fuel * Q_fuel 其中,m_fuel为燃料质量,Q_fuel为燃料单位质量的燃烧热量。
每小时柴油机消耗的燃油量为:m_fuel = 1000kg/小时每升燃油能释放的热量为:Q_fuel = 38000J/升因此,柴油机燃料燃烧释放的热量为:Q = 1000 × 38000=3.8×10^7J/小时假设柴油机每小时工作3600秒,则计算柴油机的功率为:P = Q/t =3.8×10^7/3600 ≈ 10556W答案:柴油机的功率约为10556W。
化工原理II试题

一、填空题:1.( 2分)在常压下,20℃时氨在空气中的分压为114mmHg,此时氨在混合气中的摩尔分率y=________,比摩尔分率Y=_______.***答案***0.15 0.1762. ( 3分)对一定组成的二元体系,精馏压力越大,则相对挥发度______,塔操作温度____,对分离______。
***答案***越小越高越不利3. ( 2分)全回流时,达到一定的分离要求所需的理论板数________;最小回流比时,所需的理论板数_________。
***答案***最少;无限多4. ( 2分)某精馏塔的理论塔板数为17块(包塔釜)其全塔效率为0.5,则实际板数为()块。
***答案***325.( 2分) 干燥进行的必要条件是物料表面所产生的水汽(或其它蒸汽)压力__________________。
***答案***大于干燥介质中水汽(或其它蒸汽)的分压。
6.( 3分)吸收过程主要用于三个方面:__________,___________,_________.***答案***制备产品分离气体混合物除去气体中的有害组分7. ( 2分) 对于不饱和空气,表示该空气的三个温度,即:干球温度t,湿球温度t w和露点t d间的关系是______________。
***答案***t>t w>t d8.( 2分) 吸收中,温度不变,压力增大,可使相平衡常数_____(增大,减小,不变),传质推动力___(增大,减小,不变)。
***答案*** 减小增大9.( 2分) 溶解度很大的气体,吸收时属于____控制,强化吸收的手段是__________________。
***答案***气膜,增大气相侧的传质分系数。
10.( 2分)相对湿度φ值可以反映湿空气吸收水汽能力的大小,当φ值大时,表示该湿空气的吸收水汽的能力_________;当φ=0时,表示该空气为___________。
***答案***小;绝干空气11.( 8分) 某沸点进料的连续精馏塔, 已知其精馏段操作线方程为y=0.80x+0.172,提馏段操作线方程为y=1.2x-0.017,则回流比R=_______,馏出液组成x=__________,原料组成x=_________.釜液组成x=_________.***答案***4 0.86 0.5514 0.085二、选择题:1.( 3分)某塔的精馏段操作线方程为y=0.667X+0.32, 则馏出液组成为()。
化工原理(第二练习题及答案_上册.docx
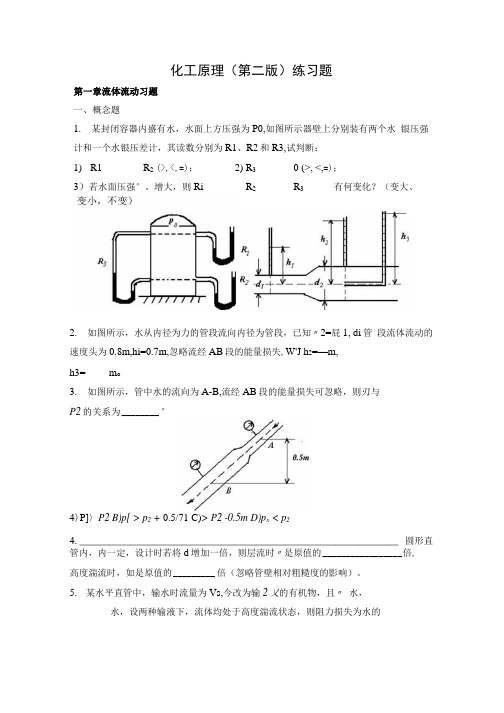
化工原理(第二版)练习题第一章流体流动习题一、概念题1.某封闭容器内盛有水,水面上方压强为P0,如图所示器壁上分别装有两个水银压强计和一个水银压差计,其读数分别为R1、R2和R3,试判断:1)R1 _______ R2(>,<,=);2) R3 ______ 0 (>, <,=);3)若水面压强°。
增大,则Ri________ R2 ______ R3_____ 有何变化?(变大、2.如图所示,水从内径为力的管段流向内径为管段,已知〃2=屁1, di管段流体流动的速度头为0.8m,hi=0.7m,忽略流经AB段的能量损失,W'J h2=—m,h3= ____ m o3.如图所示,管中水的流向为A-B,流经AB段的能量损失可忽略,则刃与P2的关系为________ °4)P]〉P2 B)p[ > p2 + 0.5/71 C)> P2 -0.5m D)p x < p24. ________________________________________________________ 圆形直管内,内一定,设计时若将d增加一倍,则层流时〃是原值的_________________ 倍,高度湍流时,如是原值的_________ 倍(忽略管壁相对粗糙度的影响)。
5.某水平直管中,输水时流量为Vs,今改为输2乂的有机物,且〃水,水,设两种输液下,流体均处于高度湍流状态,则阻力损失为水的倍;管路两端压差为水的_________ 倍。
6.已知图示均匀直管管路中输送水,在A、B两测压点间装一U形管压差计, 指示液为水银,读数为R (图示为正)。
则:1)R 0 (>,=, <)2)A、B两点的压差勺= ________ Pa。
QRg(Pi - P)B)RgS - p) + pgh C)pgh-RgS- p) D)Rg(Pi- p)- pgh3)流体流经A、B点间的阻力损失好为__________ J/kg。
化工原理第二版下册答案(题目已筛选)

气体吸收1. 在温度为40 ℃、压力为 kPa 的条件下,测得溶液上方氨的平衡分压为 kPa时,氨在水中的溶解度为 g (NH 3)/1 000 g(H 2O)。
试求在此温度和压力下的亨利系数E 、相平衡常数m 及溶解度系数H 。
解:水溶液中氨的摩尔分数为76.6170.07576.610001718x ==+由 *p Ex = 亨利系数为 *15.0kPa 200.00.075p E x ===kPa 相平衡常数为t 200.0 1.974101.3E m p === 由于氨水的浓度较低,溶液的密度可按纯水的密度计算。
40 ℃时水的密度为 992.2ρ=kg/m 3溶解度系数为kPa)kmol/(m 2760kPa)kmol/(m 180200299233S⋅=⋅⨯==...EM H ρ3. 在总压为 kPa 的条件下,采用填料塔用清水逆流吸收混于空气中的氨气。
测得在塔的某一截面上,氨的气、液相组成分别为0.032y =、31.06koml/m c =。
气膜吸收系数kG=×10-6 kmol/(m2·s ·kPa),液膜吸收系数kL=×10-4 m/s 。
假设操作条件下平衡关系服从亨利定律,溶解度系数H = kmol/(m3·kPa)。
(1)试计算以p ∆、c ∆表示的总推动力和相应的总吸收系数; (2)试分析该过程的控制因素。
解:(1) 以气相分压差表示的总推动力为t 1.06*(110.50.032)kPa 2.0740.725c p p p p y H ∆=-=-=⨯-=kPa其对应的总吸收系数为246G L G 11111()(m s kPa)/kmol 0.725 1.5510 5.210K Hk k --=+=+⋅⋅⨯⨯⨯35252(8.89910 1.92310)(m s Pa)/kmol 2.01210(m s Pa)/kmol =⨯+⨯⋅⋅=⨯⋅⋅6G 1097.4-⨯=K kmol/(m2·s ·kPa)以液相组成差表示的总推动力为33*(110.50.0320.725 1.06)kmol/m 1.504kmol/m c c c pH c ∆=-=-=⨯⨯-= 其对应的总吸收系数为m/s10855.6m/s 102.5725.01055.11111664G L L ---⨯=⨯+⨯=+=k H k K (2)吸收过程的控制因素 气膜阻力占总阻力的百分数为%58.95%100102.51097.4/1/166G G G G =⨯⨯⨯==--k K K k气膜阻力占总阻力的绝大部分,故该吸收过程为气膜控制。
《化工原理II》计算试题

石油大学(北京)化工学院化工原理(下册)题库二、计算题1、(15分)在一直径为1.2m 的Mellepak 250Y 规整填料吸收塔中,用清水吸收空气混合气中的SO 2。
吸收塔操作总压为101.3kpa, 温度为20 o C ,入塔混合气的流量为1000m 3/h, SO 2的摩尔分率为0.09,要求SO 2的回收率不低于98%,采用其汽相总体积传质系K Y a=0.0524 kmol/(m.s)。
该体系的相平衡方程为:y e =3.3x 。
试求:(1)推导传质单元数计算方程;(2)试证明:()ηm VL =m in 成立,其中η为溶质的吸收率,m 为相平衡常数; (3)最小溶剂用量,kgmol/h ;(4)若实际溶剂用量为最小溶剂量的1.2倍,计算出塔水中SO 2浓度(摩尔分率);(5)计算传质单元数,传质单元高度及完成该分离任务所需的填料高度。
2、(15分)一座油吸收煤气中苯的吸收塔,已知煤气流量为2240(NM 3/hr ),入塔气中含苯4%,出塔气中含苯0.8%(以上均为体积分率),进塔油不含苯,取L=1.4 Lmin,已知该体系相平衡关系为:Y*=0.126X ,试求:(1) 溶质吸收率η(2)Lmin 及L (kmol/h)(3)求出塔组成X b (kmol 苯/kmol 油)(4)求该吸收过程的对数平均推动力∆Y m(5)用解析法求N OG ;(6)为了增大该塔液体喷淋量。
采用部分循环流程,在保证原吸收率的情况下,最大循环量L ’为多少,并画出无部分循环和有部分循环时两种情况下的操作线。
3、(20分)在一座逆流操作的低浓度气体填料吸收塔中,用纯矿物油吸收混合气中的溶质,已知进口混合气中溶质的含量为0.015(摩尔分率),吸收率为85%,操作条件下的平衡关系Y*=0.5X 。
试求:(1)出口矿物油中溶质的最大浓度和最小液气比;(2)取吸收剂用量为最小溶剂用量的3倍时,用解析法求N OG ;(3)求该吸收过程的气相总对数平均传质推动力∆Ym ;(4)气体总传质单元高度为1m 时,求填料层高度;(5)为了增大该塔液体喷淋量,采用出塔液体部分循环流程。
化工原理第二版习题答案

化工原理第二版习题答案化工原理是一门研究化工生产过程中物质转化和能量转换规律的学科,它涉及到化学工程、物理化学、流体力学、热力学等多个领域。
第二版的习题答案在帮助学生巩固理论知识和提高解题技巧方面发挥着重要作用。
以下是一些习题答案的示例:习题1:流体力学基础问题:求在管道中流动的水的流速,已知管道直径为0.1米,流量为0.02立方米/秒。
答案:首先,我们使用连续性方程来计算流速。
连续性方程为 Q = A * v,其中 Q 是流量,A 是管道横截面积,v 是流速。
对于圆管,横截面积A = π * (d/2)^2,其中 d 是管道直径。
代入已知数值,我们得到:\[ A = π * (0.1 / 2)^2 = 0.00785 \, \text{平方米} \]\[ v = \frac{Q}{A} = \frac{0.02}{0.00785} \approx 2.547 \,\text{米/秒} \]所以,水的流速大约是2.547米/秒。
习题2:传热过程问题:一个长直管的外壁温度为100°C,内壁温度为50°C,热流密度为1000 W/m²。
求该管壁的热导率。
答案:使用傅里叶定律来解决这个问题,公式为 q = -k * (dT/dx),其中 q 是热流密度,k 是热导率,dT/dx 是温度梯度。
由于是长直管,我们可以假设温度梯度是线性的,并且只在一个方向上变化。
设管壁厚度为 L,内外壁温差为ΔT,那么温度梯度为ΔT/L。
代入公式得:\[ 1000 = -k * \frac{100 - 50}{L} \]\[ k = \frac{1000 * L}{50} \]如果知道管壁的厚度 L,就可以直接计算出热导率 k。
习题3:化学反应工程问题:在一个理想CSTR(连续搅拌槽反应器)中,A和B发生反应生成C,反应速率为 r = k * [A]^m * [B]^n。
已知初始浓度 [A]₀ = 1 mol/L,[B]₀ = 2 mol/L,反应速率常数k = 0.1 L/(mol·s),m = 1,n = 1。
化工原理试卷2答案.doc

1、 395mmHg>2105mmHg 3、A 4、C 5、B 8、C 9、C 10、C(1)整个管路的阻力损失,J/kg; 其中, £加=135.1 J /kg, Un~ Pi= Po=O (表压), HE, H 二20m 故 N e = W, x W, = 1381.5iv , 4=80%, N = = 1727w = 1.727bv 2、增加、降低3、降低、减小、降低、增加4、Ri >R 2> &、 Qi = Qz = Q 3 5、传导、 Qt 对流、辐射、、dQ = —Ads — dn 6、传质单元高度、 传质单元数7、双膜理论、溶质渗透理论、表面更新理论de 8、J A =-D AB —、增大、减小9、气膜控制,约100%、易10、增大、平衡线、增多 dz 〃、愈大、愈大、先减小后增大的过程一、选择题:(每题2分,共20分)1, A2、B 6, A 7、 A 三、计算题: (26 分)1、解:由题意知, =2.12m/s x0.052 x-) 4则 Z/) =/1・CU = O .O 3X 122_X 炎二= 135.1"耘 d 2 0.05 2(2)泵轴功率,kw ;在贮槽液面0-0'与高位槽液面IT'间列柏努利方程,以贮槽液面为基准水平面,有:代入方程得: = gH =9.81x20 + 135.1 = 331.3//危W =Vo = x 1000 = 4.11kg / s 3600(12分)2、解: 解:首先将此气液相组成换算为y 与x 。
NH3的摩尔质量为17kg/kmol,溶液的量为15kgNH3与1000kg 水之和。
故 n A n A15/17x =—=——-—= ------------------ =0.0156n n A +n R 15/17 +1000/18 A D * = 4 = 2.266 = o.O224 P 101.325化工原理试卷2答案二、填空题:(每空1分, 共30分)=4.713 左g/sm = 2: =些= 1.436x 0.0156由式(6-11) E=F • m=101.325XI.436=145.5kPa或者山式(6-1) E = £±= 2266 =145.3kPa x 0.0156溶剂水的密度P s =1000kg/m 3,摩尔质量M s =18kg/kmol,由式(6-10)计算H H a Ps = —_ = o 382kmol/ (m 3 • kPa) EM s 145.3x18H 值也可直接由式6-2算出,溶液中NH3的浓度为C =出="EM K =_15H7_ = 0 869kmol/m3V (m A +m s )/p s (15 + 1000)/1000所以 丑== °"69 = 0 383kmol/ (m 3 • kPa) p; 2.266 '(12分)3、解:(1)换热器每程提供的传热面积(外表面为基准),S,;由题意知,水以0.7m/s 的流速在管内流过,欲求S“需先知道每程的管子数,每程的管子数等于所需 冷却水的总流量与单管内水的流量之比。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《化工原理II》计算试题石油大学(北京)化工学院(第二部分)题库2,计算题1,(15分)在直径1.2m的Mellepak 250Y规整填料吸收塔中,空气混合物中的SO2用清水吸收吸收塔的总操作压力为101.3kpa,温度为20℃,混合气体进入塔内的流量为1000 m3/h,SO2的摩尔分数为0.09,SO2的回收率要求不低于98%,采用气相kya = 0.0524 kmol/(m·s)的总体积传质系统系统的相平衡方程为:ye=3.3x试着找出:(1)推导出计算传质单元数的公式;L?敏。
m?成立,哪一个?是溶质的吸收率,m是相平衡常数;(2)测试证书:V(3)最小溶剂剂量,千克摩尔/小时;(4)如果实际溶剂量是最小溶剂量的1.2倍,计算塔水中SO2浓度(摩尔分数);(5)计算完成分离任务所需的传质单元数量、传质单元高度和填料高度2,(15分)一种吸收煤气中苯的吸油塔。
已知煤气的流速为2240(NM3/hr),进入塔的气体中苯含量为4%,离开塔的气体中苯含量为0.8%(以上均为体积分数)。
进入塔内的油不含苯。
取L=1.4 Lmin。
已知体系的相平衡关系为Y * = 0.126 x。
试着找出:(1)溶质吸收率?(2)Lmin和L (kmol/h)(3)求柱组成Xb(kmol苯/kmol油)(4)求吸收过程的对数平均驱动力?Ym (5)解决非政府组织问题;用分析法;(6)以增加塔内的液体喷射量使用部分循环流量,在保证原始吸收率的条件下,最大循环量L’是多少,并画出无部分循环和部分循环两种情况下的操作线。
3,(20分)在一个逆流操作的低浓度气体填料吸收塔中,纯矿物油被用来吸收混合气体中的溶质。
已知在操作条件下,进口混合气体中的溶质含量为0.015(摩尔分数),吸收率为85%,平衡关系Y*=0.5X努力找出:出口矿物油中溶质的最大浓度为(1)最小液气比;(2)当吸收剂用量为最小溶剂用量的3倍时,NOG是用解析法计算的。
(3)找到吸收过程的总对数平均传质驱动力?Ym。
(4)当总气体传质单元的高度为1m时,计算填料层的高度;?1?(5)为了增加塔内液体的喷淋量,采用塔外液体部分循环流动。
在保证原吸收速率的条件下,假设气相流速为,最大循环量L’是多少,并画出无部分循环和部分循环两种情况下的操作线4。
在吸收塔中,某种气体混合物与清水逆流吸收。
塔中的气相组成为0.05(摩尔分数,下同)。
在该操作条件下,系统的平衡关系为y*=2x,操作液气比为1.25(L/V)min,塔内气相组成为0.01,吸收过程为气膜控制,Kya∝V0.7(V为气相摩尔分数)试算:(1)液相出口组成xb,NOG传质任务所需;(2)如果初始气液组成、流速和操作条件保持不变,当原始塔与另一个相同的塔串联和逆流操作时,离开塔的气体的最终组成是什么(3)如果初始汽液组成、流速和操作条件不变,原塔和另一个相同的塔平行逆流操作,汽液两相流分布相等,此时的气体出口组成是什么5,(20分)在逆流操作的填料吸收塔中,用清水吸收氨-空气混合物中的氨。
已知当混合气体进入塔时,氨浓度为y1=0.01(摩尔分数),吸收率为90%,气液平衡关系为y = 0.9x在这些条件下,试着找出:(1)溶液的最大出口浓度;(2)最小液气比;(3)当吸收剂的量是最小吸收剂量的两倍时,传质单元的数量是多少?(4)当传质单元高度为0.5m时,填料高度是多少米?6,(10分)试验证明吸收塔填料层高度计算中液相传质单元总数的解析公式为NOL???是吗?mxaln??1?a。
b?a。
1?a。
Yb?mxb?17,(20分)在逆流填料吸收塔中,用三乙醇胺水溶液吸收气相中的H2S。
塔气相中H2S含量为2.91%(体积%,下同)。
要求H2S回收率不低于99%,操作温度为27℃,压力为1个大气压。
进料溶剂新鲜,出料溶剂中H2S浓度为0.013 kmol(H2S)/kmol(溶剂),塔内惰性气体流速为0.015 kmol/(m2s),系统相平衡关系为:Y*=2X(1)尝试找到最小液气比和实际液气比(2)如果系统中鲍尔环的总体积传质系数为0.000395 kmol/(m3.s.kpa),请尝试找出满足生产要求所需的填料高度。
(3)如果使用浮阀塔板,总共需要25层以满足分离要求,并测试和计算系统中浮阀塔板的总塔效率。
?2?(4)尝试计算鲍尔环填料的等板高度HETP8,(20分钟)一个生产过程产生两种含盐酸的混合气体,一种流量yG1=0.1摩尔/秒,盐酸浓度yG1 = 0.1(摩尔分数),另一种流量yG2=0.04摩尔/秒,盐酸浓度yG2 = 0.04(摩尔分数)如今,有人建议用吸收塔从这两种气体中回收氯化氢,总回收率不低于85%。
所用吸收剂为20℃的纯水,亨利系数E = 2.786×105帕,工作压力为常压。
试着找出:(1)将两种材料混合后,从塔底进入塔内(图1中的A),吸收剂的最小量是多少?如果第二股气流在适当的高度单独加入塔中(图1中的b),最小吸收剂用量的变化是什么?(2)如果空塔气速为0.5m/s,在该气速下测量的Kya = 8×10-3mol/(s . m3),实际液气比是最小液气比的1.2倍,混合进料所需的填料层高度是多少?(3)塔径和实际液气比与(2)相同。
第二股气流在最佳位置输送。
要求的包装高度是多少?中间进料在哪里?9,(27分)填料吸收塔(见右图)用清水逆流吸收二元工业尾气中的有害成分A。
已知填料层为4m高,进入塔的气体浓度yb=0.02(摩尔分数,下同),溶剂对组分A的吸收率为80%,离开塔的液体组成xb=0.008,还已知操作条件下的气液平衡关系为Y * = 1.5x。
;(2)最小液气比是工作液气比的多少倍;(3)由于法定排放浓度ya必须≤0.002,因此建议增加填料层。
如果液气比和气液入口组成保持不变,填料层应提高多少?(4)如果气相和液相的数量以及入口的组成保持不变,并且同一塔与该塔串联,那么相因蒸汽而产生的出口浓度ya是多少?(5)如果吸收后塔内混合气体的浓度不能满足环保要求,可以采取什么措施来提高组分A的溶剂的回收率?10。
填料塔设计用于在常温常压下吸收空气-丙酮混合蒸汽中的丙酮和清水。
混合气体进入塔的流速为80千摩尔/小时,含有5%(体积分数)的丙酮,所需的吸收率为95%已知柱径为0.8m,操作条件下的相平衡关系可表示为y=2.0x,气相体积的总传质系数kya为150 kmol/m3?H、出口溶液中丙酮的浓度为饱和浓度的70%,试着找出: (1)完成分离任务需要多少水量[·m3/h];(2)所需填料层高度,m;(3)最低用水量是多少倍?3?(4)可以采取什么措施来提高气体回收率?11逆流操作常压填料吸收塔,用清水吸收混合气体中的溶质A。
进入塔的气体中的浓度为0.01(摩尔分数)。
吸收后,溶质A的回收率为80%。
此时,水消耗是最小溶剂消耗的1.5倍,相平衡线的斜率是1 L?试着找出:(1)最小液气比???;?v?(2)液体从塔中流出形成XB;(3)当气相总传质单元高度为1m时,所需填料层高度为12,(28分)连续蒸馏塔分离二元理想混合物。
已知进料速率F=10kmol/s,进料组成xF = 0.5(摩尔分数,下同),进料为饱和蒸汽,顶部产物的组成xd为0.95,底部产物的组成xw为0.1,系统的相对挥发度α为2塔底采用再沸器,塔顶采用全冷凝器,泡点回流,塔底蒸发量为最小蒸发量的2倍。
设法找出: (1)塔顶挥发性组分的回收率;(2)塔底汽化;(3)液相成分流出第二块板(从上到下)13,(27分)连续精馏塔分离二元理想混合物,已知进料速率F=100 kmol/h,进料组成为0.5(摩尔分数,下同),进料为气液混合物,气液摩尔比为1∶1;塔底使用重沸器,塔顶使用全冷凝器。
实际回流比r 是最小回流比Rmin的3倍。
塔顶产品组成xd为0.8,塔底产品组成xw为0.2,系统相对挥发度α为3试算:(1)原料气相和液相组成;(2)塔顶挥发性组分回收率;(3)塔釜的汽化量;(4)完成分离任务所需的理论塔板数14,(15分钟)用连续精馏塔分离苯-甲苯混合溶液。
原料液含0.40苯,塔顶馏出物含0.95苯(以上均为摩尔分数)。
原料液为蒸汽和液体的混合进料,其中蒸汽占1/3(摩尔分数),苯-甲苯的平均相对挥发度为2.5,回流比是最小回流比的2倍。
试着找出:(1)原料液中气相和液相的组成;(2)最小回流比;(3)如果塔顶采用全冷凝器,计算从塔顶下降的第二块理论塔板的液体组成。
?4?15,(10分)在连续精馏塔中,精馏段操作线方程y=0.75x+0.2075,q 线方程y=-0.5x+1.5xF,试找出:(1)回流比r,馏出液组成xD,进料液q值;(2)当进料组成xF=0.44时,精馏段操作线和汽提段操作线交点处的x值是多少,并判断进料的热状态16,(20分钟)组成为0.40的原料以气液混合状态进入精馏塔,原料气液摩尔比为1∶2,进料摩尔流量为f,塔顶产品组成为xD=0.95,塔顶挥发性组分回收率为95%(以上为摩尔分数),回流比R=2Rmin,组分相对挥发度为2.5,试(2)塔顶产品量,塔底产品量和组成;(3)列出整风断面作业线方程;(4)列出汽提段的操作线方程;(5)列出进料热状态线方程;17,(25分)如图所示,甲、乙混合液在常压连续精馏塔中分离。
两种进料为F1=100千克摩尔/小时,xF1=0.6(摩尔分数,下同),饱和液体进料,F2=100千克摩尔/小时,xF2=0.2,饱和液体进料。
要求是:分离后馏出液中组分a的含量不小于0.8,釜液中组分a的浓度不大于0.02,操作回流比R=2Rmin,系统的相对挥发度α为1.6试着找出:(1)塔顶和塔底的产品数量;(2)操作回流比;(3)精馏段操作线方程;(4)气液流速和汽提段操作线方程;(5)两个进料之间中间部分的气体和液体流速和操作线方程18。
用精馏塔分离二元水溶液时,水很难挥发成分。
进料中轻组分的组成为0.3(摩尔分数,下同),进料速率为100克分子/小时,进料的热态q=1.1。
二元混合物符合相平衡关系。
2x1?X、塔顶采用全冷凝器,泡点回流,回流比R=1.5Rmin,塔底直接用饱和蒸汽加热,蒸汽量为s,塔顶馏出物xD=0.9试着找出:(1)最小回流比;?5?。
