《药品生产许可证》编号方法及代码
国家药品编码本位码编制规则
国家药品编码本位码编制规则
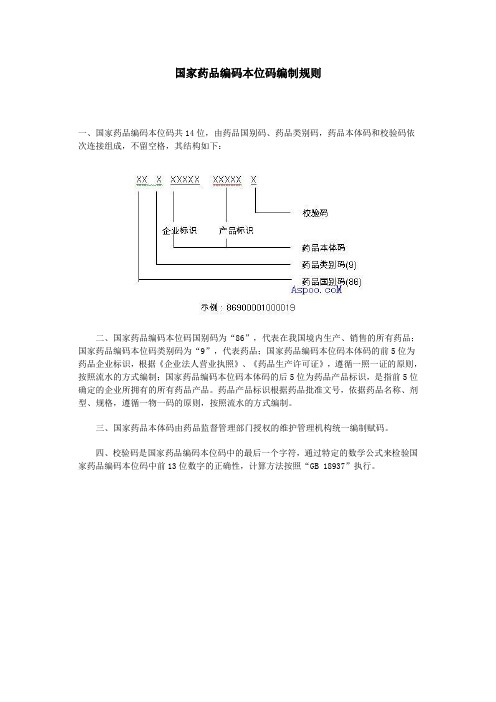
一、国家药品编码本位码共14位,由药品国别码、药品类别码,药品本体码和校验码依次连接组成,不留空格,其结构如下:
二、国家药品编码本位码国别码为“86”,代表在我国境内生产、销售的所有药品;国家药品编码本位码类别码为“9”,代表药品;国家药品编码本位码本体码的前5位为药品企业标识,根据《企业法人营业执照》、《药品生产许可证》,遵循一照一证的原则,按照流水的方式编制;国家药品编码本位码本体码的后5位为药品产品标识,是指前5位确定的企业所拥有的所有药品产品。
药品产品标识根据药品批准文号,依据药品名称、剂型、规格,遵循一物一码的原则,按照流水的方式编制。
三、国家药品本体码由药品监督管理部门授权的维护管理机构统一编制赋码。
四、校验码是国家药品编码本位码中的最后一个字符,通过特定的数学公式来检验国家药品编码本位码中前13位数字的正确性,计算方法按照“GB 18937”执行。
GMP-证书编号的意义

证书编号的意义一、GSP认证证书编号的意义:首位字母(大写)+“-”+地区拼音代码(大写)+年度码+“-”+年度该类型证书流水号;首位字母规定为:批发企业为字母“A”:零售连锁企业为字母“B”;零售企业为字母“C”。
如C-SD04-0435表示山东省,零售企业,2004年发证;A-HLJ04-116表示黑龙江省,批发企业,2004年发证;A-JS05-028表示江苏省,批发企业,2005年发证;A-GD04-0432表示广东省,批发企业,2004年发证。
二、药品GMP证书编号的意义:1、省、自治区、直辖市简称+字母+顺序号2、国家药品监督管理局颁发的证书编号为:字母+顺序号。
3、由负责认证的药品监督管理局按以下编号方法分别填写,“字母”项为英文大写字母,按顺序分别代表不同年份,“A”代表1999年,“B”代表2000年,“C”代表2001年,“D”代表2002年,依次类推;4、“顺序号”项为四位阿拉伯数字自然顺序,中间不得有空号,跨年度继续上年度的顺序编号。
三、《药品生产许可证》编号方法及代码一、编号方法省汉字简称十大写字母十小写字母十年号十四位数字顺序号。
大写字母为生产企业类别代码,按H、Z、S、T、Y、Q、F、J、C、X顺序填写;小写字母为原料药、制剂代码,按a、b顺序填写。
对每个生产企业,填写一个类别代码及相应原料药或制剂代码后,再填写另一个类别代码及相应原料药或制剂代码。
二、代码释义(一)大写字母代码H:化学药Z:中成药S:生物制品T: 体外诊断试剂Y:中药饮片Q:医用氧等F: 药用辅料J: 空心胶囊C: 特殊药品X: 其他(如中药提取物,中药配方颗粒等)(二)小写字母代码a: 原料药b:制剂例如:*HabZab20050001* HabZb20050002四、现行版药品经营许可证编号的含义目前的药品经营许可证证号由一个汉字、两个大写英文字母和7位阿拉伯数字组成。
汉字为省、自治区、直辖市的简称;第一个英文字母表示:A为批发企业,B为零售连锁企业,C为连锁门店,D为单体药店;第二个英文字母表示:批发企业、零售连锁企业、单体药店的A为具有独立法人资格的企业,B 为非独立法人资格的企业,连锁门店的A为加盟店,B为直营店;前两位数字为省辖市地区编号;批发企业的第3、4、5位数字为流水号,后两位数字为分支机构号码;零售连锁企业的第3、4位数字为总部专有流水号,后三位为分部流水号;连锁门店的第3、4位数字为总部专有流水号,后三位为门店流水号;单体药店的第3位为城乡代码,1为县城以上药店,2位乡镇药店,3位乡镇以下药店,后四位为流水号。
国家食品药品监督管理局关于开展换发《药品生产许可证》工作的通知

国家食品药品监督管理局关于开展换发《药品生产许可证》工作的通知文章属性•【制定机关】国家食品药品监督管理局(已撤销)•【公布日期】2005.01.08•【文号】国食药监安[2005]17号•【施行日期】2005.01.08•【效力等级】部门规范性文件•【时效性】失效•【主题分类】药政管理正文*注:本篇法规已被:国家食品药品监督管理局关于废止和宣布失效的规范性文件目录(第二批)的公告(发布日期:2011年6月28日,实施日期:2011年6月28日)宣布失效国家食品药品监督管理局关于开展换发《药品生产许可证》工作的通知(国食药监安[2005]17号)各省、自治区、直辖市食品药品监督管理局(药品监督管理局):为进一步加强药品生产的监督管理,巩固监督实施药品GMP成果,保证药品质量和人民用药安全有效,促进医药事业的健康发展,根据《药品管理法》、《药品管理法实施条例》、《药品生产监督管理办法》及有关规定,国家食品药品监督管理局决定2005年在全国范围内开展《药品生产许可证》的统一换发工作。
现将换证工作有关事项通知如下:一、各省、自治区、直辖市食品药品监督管理局(药品监督管理局)要高度重视,加强领导,精心组织本辖区换证工作,按照《药品管理法》及国家食品药品监督管理局的有关规定,制定具体换证工作方案,组织实施,并将换证工作方案抄送我局药品安全监管司。
二、换发《药品生产许可证》工作从2005年7月1日开始,至2005年12月31日结束。
凡依法持有《药品生产许可证》且有效期至2005年12月31日的药品生产企业,应按规定申请换发新版《药品生产许可证》;至2005年12月31日,依法持有《药品生产许可证》有效期尚未期满的药品生产企业,应申请更换新版《药品生产许可证》。
自2006年1月1日起,全部启用国家食品药品监督管理局统一印制的新版《药品生产许可证》,旧版《药品生产许可证》同时废止。
三、药品生产企业应在2005年6月30日前向所在地省(自治区、直辖市)食品药品监督管理局(药品监督管理局)提出换证申请,并报送以下资料:1.药品生产许可证登记表并附电子文档(见附件1,可从国家食品药品监督管理局网站直接下载后填写);2.原《药品生产许可证》正、副本复印件;3.《企业法人营业执照》或《营业执照》的正、副本复印件;4.《药品GMP证书》复印件;5.药品生产企业生产质量管理情况自查报告;6.药品生产企业接受监督检查(包括跟踪检查)及整改落实情况;7.不合格药品被质量公报通告情况及整改情况。
药品经营许可证号九位编码

药品经营许可证号九位编码摘要:1.药品经营许可证的概念与作用2.药品经营许可证号的编码规则3.九位编码的构成及含义4.药品经营许可证号的重要性5.结论正文:药品经营许可证是药品经营企业在我国开展药品经营活动的法定凭证。
企业在取得药品经营许可证后,方可进行药品的采购、销售、储存、运输等经营活动。
药品经营许可证号九位编码则是标识该许可证的唯一编码,对于药品经营企业而言具有重要意义。
一、药品经营许可证的概念与作用药品经营许可证是药品监督管理部门依据《药品管理法》和其他相关法规,对符合条件的药品经营企业颁发的证书。
持有药品经营许可证的企业可以在许可范围内开展药品经营活动。
药品经营许可证分为批发企业和零售企业两种类型,其有效期为5 年。
二、药品经营许可证号的编码规则药品经营许可证号由九位数字组成,按照一定的编码规则进行编制。
具体编码规则如下:1.前两位数字代表省份或直辖市,如“11”代表北京市,“31”代表上海市等;2.第三位数字代表药品经营许可证的类别,其中“1”代表批发企业,“2”代表零售企业;3.第四、五位数字代表药品经营许可证的年份,如“20”代表2020 年;4.第六、七位数字代表药品经营许可证的发证地市,如“01”代表北京市,“31”代表上海市等;5.最后两位数字为流水号,用于区分同一地区、同一年份、同一类型的药品经营许可证。
三、九位编码的构成及含义通过以上编码规则,我们可以分析一个药品经营许可证号,如“京药营批字[2020]01 号”。
其中,“京”代表北京市,“药”代表药品经营许可证类别为批发企业,“营批”代表发证地市为北京市,“字”代表年份为2020 年,“01”代表流水号。
四、药品经营许可证号的重要性药品经营许可证号九位编码具有唯一性,是药品经营企业开展经营活动的重要凭证。
药品经营企业应当将许可证号在相关经营场所显著位置公示,便于消费者和监管部门查询、核实。
同时,药品经营许可证号也是药品监管部门对药品市场进行监管的重要手段。
湖北省药品零售分级许可证编号方法

附件2:
湖北省药品零售分级许可证编号方法
发放《药品经营许可证》采用“鄂”+“2位固定数字”+ “2位英文字母”+“罗马数字” + “4位证书流水号”的证书编号方法。
一、“鄂”表示为湖北省。
二、“2位固定数字”表示地区编号,即:“武汉市01、宜昌市02、襄阳市03、黄石市04、鄂州市05、孝感市06、荆门市07、黄冈市08、十堰市09、随州市10、咸宁市11、恩施州12、荆州市13、天门市14、仙桃市15、潜江市16、神农架林区17”。
三、“2位英文字母”表示企业类型,即:Ca表示零售连锁门店(法人门店),Cb表示零售连锁门店(非法人门店)、Da表示单体零售企业(法人)Db表示单体零售企业(非法人)”。
四、“罗马数字”表示零售企业级别,即:“Ⅰ”表示一级零售企业,“Ⅱ”表示二级零售企业,“Ⅲ”表示三级零售企业。
五、“4位证书流水号”,用4个阿拉伯数字表示按不同类型企业排序形成的顺序号码。
国家药品编码本位码

国家药品编码本位码
国家药品编码本位码是由药品国别码、药品类别码、药品本体码和校验码依次连接组成的一串数字码。
其中,国家药品编码本位码的国别码为“86”,代表在我国境内生产、销售的所有药品;国家药品编码本位码类别码为“9”,代表药品;国家药品编码本位码本体码的前5位为药品企业标识,根据《企业法人营业执照》、《药品生产许可证》,遵循一照一证的原则,按照流水的方式编制;国家药品编码本位码本体码的后5位为药品产品三、国家药品本体码由药品监督管理部门授权的维护管理机构统一编制赋码。
校验码是国家药品编码本位码中的最后一个字符,通过特定的数学公式来检验国家药品编码本位码中前13位数字的正确性,计算方法按照“GB 18937”执行。
总的来说,国家药品编码本位码是用于国家药品注册信息管理,首次注册登记时赋予本位码,是国家批准注册药品唯一的身份标识。
如需更多信息,建议查阅国家食品药品监督管理总局官网或咨询相关工作人员。
医药商品碥码

李小翚 李小翚副教授中药学院中药营销教研室 办公电话:39358670 办公电话:39358670 Emil:546647632@ 2012,091一、药品编码的优点编码是医药商品分类体系和目录的一个重要 组成部分标准化的药品编码将加大与国际接轨的力 度,优化药品的生产流通质量与效率,有 利于药品信息查询。
2二、医药商品编码的原则(1)惟一性原则: (1)惟一性原则: 即一品一码,一码一品,每一个编码只 惟一性原则 能对应于一个编码对象。
(即一一对应 即一一对应) 即一一对应 (2)稳定性原则 稳定性原则: (2)稳定性原则:避免人力、物力和财力的浪费。
(3)可识别性原则 可识别性原则: (3)可识别性原则:编码时必须确定明显的识别标志 (4)可扩性原则 (4)可扩性原则 :编码结构应留有足够的后备码位 (5)简明性原则 (5)简明性原则 :应简单、易记、易校验。
(6)层次性原则 层次性原则: (6)层次性原则:应能清楚地反映出分类体系的层次结构。
(7)统一协调性原则 统一协调性原则: (7)统一协调性原则:与国家商品分类编码和国际通用商 品编码相协调,以利于实现商品信息的交流和信息共享。
(8)自检能力原则 自检能力原则: (8)自检能力原则:必须做到代码校验、校正的方便性, 而且做到计算机有自动检测差错的核对性能。
3三、医药商品编码的种类医药商品编码按其所用的符号类型可分为4种: : 医药商品编码按其所用的符号类型可分为 数字型编码 字母编码 数字和字母混合型编码 条形码4四、条形码的概念与发展P26条形码是由一组宽窄不同、黑白(彩色)相间的 条形码 平行线按照一定的规则排列组合,用以表示一定信 息的商品标识图形。
包含商品的原产国、制造商、产地、类别、名称等信息。
是专为计算机处理编制的特殊的商品代码,可由专用的光 电扫描设备迅速识别并读入计算机。
条形码:二十世纪50年代由美国首先提出的UPC条码,于 70年代在欧洲发展成为EAN条码,并于80年代开始EAN条形 码逐渐成为国际通用的商品代码。
药品经营企业编码规程

编码规程
1.供货单位:G+(A生产企业、B经营企业)+代码(3位流水号);
2.客户:K+(A生产企业、B经营企业、药品连锁企业、C、单体药
店、D、医疗机构)+代码(3位流水号);
3.药品品种:商品编码统一由5位数构成,前面2位为字母,后3
位为数字,字母第1位为大类别,第2位为明细类别,3位数字表示序号。
(1)字母第1位表示:、①药品R;②、中药Z;③、医疗器械Q;
④、非药品F;
(2)字母第2位表示:
Ⅰ. 药品项下:①、胶囊J;②、片剂P;③、颗粒剂K;
④、注射剂Z;⑤、丸剂W;⑥、口服溶液剂T;
⑦、外用制剂C;⑧、散剂S;⑨、其他Q;
Ⅱ. 中药项下:①、中药材Z;②、中药饮片Y;
Ⅲ. 医疗器械项下: ①、器械Q;②、医疗设备、仪器S;
③、敷料及卫生材料F;④、高分子材料及制品G;
⑤、综合类Z;
Ⅳ. 非药品项下:①、食品及保健品B;②、洗化类X;
③、其他类Q;。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附件2:《药品生产许可证》编号方法及代码
一、编号方法
省汉字简称+大写字母+小写字母+年号+四位数字顺序号。
大写字母为生产企业类别代码,按H、Z、S、T、Y、Q、F、J、C、X顺序填写;小写字母为原料药、制剂代码,按a、b顺序填写。
对每个生产企业,填写一个类别代码及相应原料药或制剂代码后,再填写另一个类别代码及相应原料药或制剂代码。
二、代码释义
(一)大写字母代码
H:化学药
Z:中成药
S:生物制品
T:体外诊断试剂
Y:中药饮片
Q:医用氧等
F:药用辅料
J:空心胶囊
C:特殊药品
X:其他(如中药提取物,中药配方颗粒等)
(二)小写字母代码
a:原料药
b:制剂
例如:*HabZab20050001
HabZb20050002
附件3:《药品生产许可证》中生产范围分类及填写规则
一、《药品生产许可证》的生产范围应按《中华人民共和国药典》制剂通则及国家药品标准填写,主要有以下剂型:
大容量注射剂、小容量注射剂、粉针剂、冻干粉针剂、片剂、硬胶囊剂、软胶囊剂、颗粒剂、散剂、丸剂(蜜丸、水蜜丸、水丸、浓缩丸、微丸、糊丸、蜡丸)、滴丸剂、干混悬剂、混悬剂、合剂、口服液、口服溶液剂、乳剂、糖浆剂、酒剂、酊剂、茶剂、露剂、搽剂、洗剂、栓剂、涂剂、软膏剂、乳膏剂、眼膏剂、凝胶剂、透皮贴剂、巴布膏剂、橡胶膏剂、膏药、锭剂、流浸膏剂、浸膏剂、煎膏剂(膏滋)、胶剂、膜剂、滴眼剂、滴耳剂、滴鼻剂、气雾剂、喷雾剂、鼻喷剂、甘油剂、海绵剂、进口药品分包装(注明剂型)。
其中青霉素类、头孢菌素类、激素类、抗肿瘤药、避孕药应同时在
括弧内注明。
一种剂型既有类别品种也有其它普通品种,应在类别前加“含”字;外用制剂应在制剂后加括弧注明外用,既有口服也有外用的制剂,应在制剂后括弧内注明含外用。
例如:片剂(头孢菌素类),片剂(头孢菌素类、抗肿瘤类),小容量注射剂(含激素类),颗粒剂,胶囊剂(含头孢菌素类),冻干粉针剂,片剂(含青霉素类、头孢菌素类),酊剂(外用),酊剂(含外用)。
二、原料药、无菌原料药、中药提取物的填写,正本上只注明类别,副本上在类别后括弧内注明其国家药品标准规定的产品通用名称。
例如:正本生产范围:原料药。
副本生产范围:原料药(***、***)。
三、生物制品应在正本上按疫苗、血液制品、血清抗毒素、生物工程产品、免疫制剂、体内诊断试剂、过敏原制剂、体细胞及基因治疗制剂等分类填写,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:疫苗。
副本生产范围:疫苗(****、****)。
四、体外诊断试剂的正本上只填写类别,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:体外诊断试剂。
副本生产范围:体外诊断试制(****、****)。
五、医疗用毒性药品、麻醉药品、精神药品、药品类易制毒化学品等特殊药品,应在正本上填写类别,副本上在类别后括弧内注明产品名称。
例如:正本生产范围:医疗用毒性药品。
副本生产范围:医疗用毒性药品(****、****)。
六、药用辅料在正本上只填写类别,副本上在括弧内注明产品名称。
中药饮片在正本上括弧内注明含毒性饮片,副本上应除括弧内注明含毒性饮片外,还应括弧内注明含直接服用饮片及相应的炮制范围,包括净制、切制、炒制、炙制、煅制、蒸制等。
医用氧等应在正本上填写类别,副本上在类别后括弧内注明产品名称。
空心胶囊直接填写。
以上类别之外的药品可直接填写通用名称。
