文件控制程序文件更改通知单表格格式
文件控制记录表格
呼建发[2011]61号
1
毕学军
2011-5-5
市住建委
关于印发《呼伦贝尔市推广使用塔式起重机安全监控系统实施细则》的通知
呼建发
[2011]62号
1
毕学军
工会
于万学
归档
5
2011-5-13
市住建委
关于印发《2011年呼伦贝尔市建筑安全生产工作安排》的通知
呼建发[2011]104号
有效文件
程序文件
1
91
材料供应部
毕宗江
2011-10-1
HFJA/A.00-01-23-2011
(2011)第07号
有效文件
程序文件
1
91
办公室
季艳辉
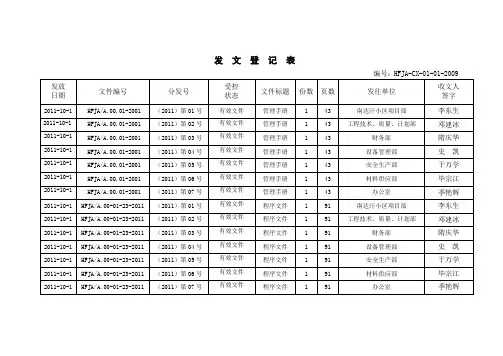
发文登记表
编号:HFJA-CX-01-01-2009
发放
日期
文件编号
分发号
受控
状态
文件标题
份
数
页
数
发往单位
收文人
签字
2011-10-1
HFJA-CX-01-03-2011
蛙式打夯机安全操作规程
管理文件
58
HFJA/GL-33-2011
磨石机安全操作规程
管理文件
59
HFJA/GL-34-2011
机修工安全作业要求
管理文件
60
HFJA/GL-35-2011
手拉葫芦安全操作规程
管理文件
61
HFJA/GL-36-2011
千斤顶安全操作规程
管理文件
62
HFJA/GL-37-2011
2011-10-1
HFJA/A.00-01-23-2011
文件控制程序(2015版ISO9001+2016版ISO13485医疗器械生产质量管理体系文件)

文件编号:YPIQEP-01文件名称:文件控制程序核准:杨x维核准日期:2016.12.13 制作部门:品质部审核:吕x豪审核日期:2016。
12.13 制作者:孙x妮制作日期:2011.11.15 变更日期:2016。
12.13 版本识别:第2版文件□建立■修改□废止履历表表单编号:YPIR-180-047 版本:2 生效日期:2016.12.13对质量、环境管理体系有关的文件进行控制,确保各部门及时得到并使用有效的版本。
2范围2.1本程序适用于公司质量、环境管理体系文件的控制和管理,包括公司内部形成的文件和适用的外来文件。
公司内部应形成的质量、环境管理体系文件:2.1.1一级文件:质量、环境手册(含质量、环境方针和质量、环境目标);2.1.2二级文件:程序文件;2.1.3三级文件:管理办法、图纸、BOM、操作规程、作业指导书、检验规范、变更通知单等;2.1.4四级文件:表单。
2.2适用的外来文件:2.2.1法律法规、标准;2.2.2顾客或供方提供的图样、技术文件等。
3定义3.1主文档(DMR):阐明器械将如何生产,包括试验和接收准则的以器械设计活动为基础的文件汇编。
包括: 3.1.1原材料、标识、包装材料、部件和医疗器械的规范;3.1.2零部件清单;3.1.3工程图纸;3.1.4软件程序;作业指导书、包括设备操作;3.1.5适用时,灭菌过程的描述;3.1.6质量计划;3.1.7制造/检验/试验程序和接收准则。
4职责4.1总经理:负责质量、环境手册的批准。
4.2管理者代表:负责质量、环境程序文件的批准。
4.3DCC:负责文件的登录、印发、回收、销毁及文件正本的保存。
4.4各部门:负责本部门文件的编制及使用保管。
5作业程序5.1文件编写、会签、批准5.1.1文件编制格式5.1.1.1品质部在共享“\\192。
168.0.218\loo\Systems\4 文件编制格式”文件夹,供各部门编写文件时使用。
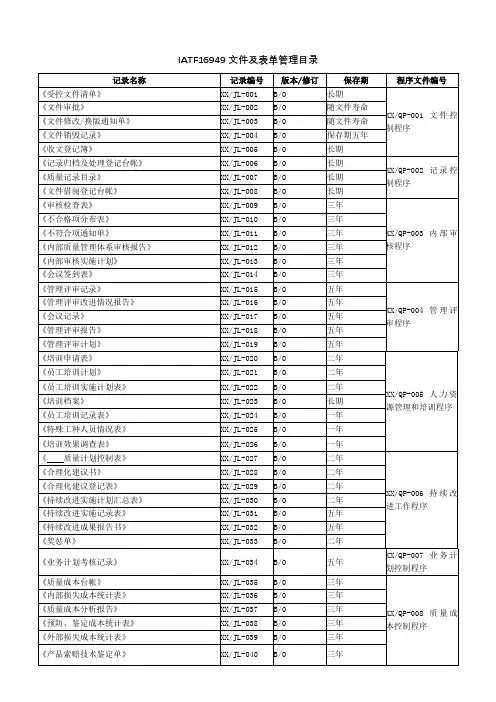
IATF16949文件及表单管理目录
三年
《不合格品汇总表》
XX/JL-130
B/0
三年
《8D报告》
XX/JL-131
B/0
三年
《质量状况月统计表》
XX/JL-132
B/0
一年
《让步接收申请单》
XX/JL-133
B/0
一年
《报废通知单》
XX/JL-134
B/0
一年
《返工/返修复检记录》
XX/JL-135
B/0
一年
《员工满意度调查表》
XX/JL-175
B/0
二年
XX/QP-035服务管理程序
《客户档案》
XX/JL-176
B/0
长期
《顾客投诉登记表》
XX/JL-177
B/0
二年
《服务工作总结报告》
XX/JL-178
B/0
二年
《工程更改申请单》
XX/JL-179
B/0
超过有效期
后一年
XX/QP-036工程变更控制程序
《计数型数据控制图》
B/0
三年
《产品索赔技术鉴定单》
XX/JL-040
B/0
三年
《产品立项报告》
XX/JL-041
B/0
长期
XX/QP-009产品质量先期策划控制程序
《产品设计可行性分析报告》
XX/JL-042
B/0
长期
《产品APQP进度计划》
XX/JL-043
B/0
长期
《材料清单(BOM)》
XX/JL-044
B/0
长期
B/0
长期
《供应商评定表》
XX/JL-124
文件及记录控制程序

1、目的对质量管理体系的所有文件进行有效控制,确保质量管理体系运行的各个场所使用有效文件,并处于受控状态,以及质量管理体系的持续有效进行,保证记录完整,实现质量追溯性。
2、范围适用于本集团公司及所属子公司质量管理体系所有文件和记录。
3、定义3.1受控文件:指最新有效文件,加盖“受控”印章的文件。
3.2非受控文件:未加盖“受控”或加盖“作废”的文件。
3.3质量体系文件:质量手册、程序文件、作业文件、质量记录、表格等。
3.4 记录:为完成的活动或达到的结果提供客观证据的文件。
3.5 外来文件:非本公司发布的,与质量体系有关的标准、规范、手册,与产品有关的法律法规,顾客提供的标准等文件。
3.6技术性文件:设计图样、工艺文件、作业指导书、检验规程等;“技术通知”3.7行政文件:除公司技术性文件、质量体系文件以外的行政管理性文件;4、职责4.1集团总经理:负责质量手册的批准。
4.2集团管理者代表:负责集团公司质量手册审核、程序文件的批准。
4.3集团质量管理部门:负责质量手册的编制、组织程序文件的编写、修改、校对与报批。
4.4各部门主任、子公司分管领导:负责本部门所需的三、四层次文件的批准。
4.5各部门、子公司各职能部门:负责本部门第三、四层次文件文件的编制、报批。
4.6集团质量部门:负责组织和主持质量管理体系文件编制、修改、评审、发布、更新、作废、处置的监督管理。
4.7集团技术部门:识别和编制所需的技术、工艺等文件,并负责该文件的归档管理,(含顾客图纸、样件等)。
4.8人力行政部门:编制公司行政管理文件并负责公司行政文件归档管理,(含人事任命、培训、基础建设等)。
4.9各部门:负责识别所需的各种内部管理性文件。
5、文件控制流程图6 过程要点描述。
实验室文件和资料控制程序(含表格)(参照模板)

文件和资料的控制程序1.目的:对与本实验室质量管理体系相关文件进行控制,确保各相关场所得到有效版本,并确保组织质量管理体系相关文件得到正确的使用。
2.范围:适用于与质量管理体系相关文件和资料的控制。
3.职责:3.1主任负责批准发布质量手册(含质量方针及质量目标);3.2技术负责审核质量手册(含质量方针及质量目标);3.3技术负责人审核质量管理室分程序文件,质量负责人负责审核管理部分程序文件;3.4各部门负责本部门相关文件的编制、使用和保管;3.5质量管理室总体负责组织质量体系相关文件的制订、编号、保管等管理工作和定期评审。
4.程序:4.1文件分类4.1.1第一级文件:质量手册(含质量方针、质量目标)。
4.1.2第二级文件:程序文件。
4.1.3第三级文件:作业指导书及各类检测标准、规范,与质量管理体系相关的外来文件,各种质量记录、技术记录文件。
4.2文件编号4.2.1质量手册编号:GYDS-QM-××(××表示版次,手册中各章以章节号区分),例如:GYDS-QM-01表示组织质量手册第一版。
4.2.2程序文件编号:GYDS-QP-××(××表示顺序号),例如:GYDS-QP-05表示组织编制的第5个程序文件。
4.2.3作业指导书、规范、制度编号:GYDS-QI类型-×××(×××为顺序号)。
4.2.4各程序文件后所附质量记录的编号:GYDS-QR-×××(×××为顺序号)。
其它质量记录可不编号,而以其名称作为标识.4.3 文件的制定与审批4.3.1质量负责组织编写《质量手册》,技术负责审核,实验室主任批准。
4.3.2质量负责组织编写和审核管理类程序文件,实验室主任批准。
4.3.3技术负责组织化学分析室编写和审核技术类程序文件,实验室主任批准。
程序文件-工程变更控制程序

4
物料功能、性
能升级或更正缺陷;工艺更
改
可控范围内最后接单日期前3个月,不可控范围内当即通知
生产商正式通知(电子或纸面) 直接提供相关的升级报告,版本说明文件,兼容性报告,勘误表;更改后型号的品质报告和足量样品
作为新物料重新验证检查产品设计、工艺,实施必要的修改,进行充分验证 刷新数据库中的物料资料及应用开发文档更改物料系统中数据
销售中心: 负责客户要求变更申请及变更后资料样品送客户承认,变更是否需发 PCN 给客户确认。
资源部:未进入量产阶段对变更后材料要求供应商重新打样。
物控部:依 ECN 信息发出,物控需确认变更后库存品、在制品处理方式,并及时切换未生产(包括已下订单未生产)的所有订单物料变更立即导入或 ECR 中有明确规定的切入时间点。 对进入量产阶段的变更后材料要求供应商重新打样,对量产后变更后图纸及时发送供应商更新,及主导因供应商改善品质变更所发生的新物料及 ECN 变更所需要试产的物料及工单试产安排。
工程变更:是指制程辅料、工艺、包材等发生更改。
客户变更:是指客户对产品性能(SPEC)、结构、材料及包装方式等要求的变更。
供应商变更:是指供应商 PCN 要求的变更和新供应商导入及替代物料引起的变更。
4. 职责与权限
开发中心:负责主导设计,材料及客户要求变更导入,及时将变更资讯知会到相关单位。
品保中心:依工程变更执行系统 BOM 修订,变更资料及原材料样品的回收、发行与记录,稽核变更执行,变更的验证并及时反馈变更后之品质状况及品质数据的统计,确保变更能够满足产品特性要求。供应商物料 PCN 窗口。
仓库
同意需修改,修 改意见于附页
文件名称: 工程变更管理控制程序
实验室常用记录表格
文件编号:GXZC-4000-00 记录表格编写:审核:批准:版本:受控状态:发放编号:发布日期:年月日实施日期:年月日1、文件和资料发放、回收记录表GXZC-4201-012、文件修改记录GXZC-4201-023、文件修改申请表GXZC-4201-034、文件修改通知单GXZC-4201-045、文件破损与丢失补发登记表GXZC-4201-056、文件和资料销毁登记表GXZC-4201-067、文件和资料借阅登记表GXZC-4201-078、备份文件记录GXZC-4201-089、文件和资料留用申请单GXZC-4201-0910、公正性声明措施执行情况检查表GXZC-4202-0111、外来人员参观审批表GXZC-4202-0212、查阅保密资料申请单GXZC-4202-0313、仪器设备(标准物质)申购单GXZC-4203-0114、仪器设备(标准物质)验收单GXZC-4203-0215、供应商评价表GXZC-4203-0316、合格供应商登记表GXZC-4203-0417、___年度服务和供应品采购计划GXZC-4203-0518、检测委托单GXZC-4204-0119、合同评审单GXZC-4204-0220、分包申请表GXZC-4205-0121、分包方能力调查表GXZC-4205-0222、合格分包方名单GXZC-4205-0323、申诉和投诉处理记录表GXZC-4206-0124、客户意见征求表GXZC-4206-0225、不符合工作控制处理表GXZC-4207-0126、内部管理体系审核检查表GXZC-4210-0127、不符合项报告GXZC-4210-0228、会议纪要GXZC-4211-0129、整改措施报告GXZC-4211-0230、会议签到表GXZC-4211-0331、检测人员上岗报批表GXZC-4212-0132、人员学习记录表GXZC-4212-0233、培训申请表GXZC-4212-0334、年度培训计划GXZC-4212-0435、个人技术档案表GXZC-4212-0536、年度人员培训记录表GXZC-4212-0637、公司办公及试验环境卫生情况检查表GXZC-4215-0138、仪器设备检定/校准报告GXZC-4217-0139、检测方法确认表GXZC-4218-0140、仪器设备(标准物质)期间核查记录表GXZC-4219-0141、更新标准实施审批表GXZC-4220-0142、新开展检测项目审批表GXZC-4220-0243、新开展检测项目验收表GXZC-4220-0344、仪器设备维修记录GXZC-4221-0145、计算机/自动化检测设备校核记录GXZC-4221-0246、计算机软件申购单GXZC-4221-0347、计算机软件验收单GXZC-4221-0448、仪器设备降级、停用、报废申请表GXZC-4222-0149、年度仪器设备周期检定/校准计划、实施记录表GXZC-4222-0250、仪器设备一览表GXZC-4222-0351、仪器设备周期检定/校准一览表GXZC-4222-0452、仪器设备档案资料借阅登记表GXZC-4222-0553、仪器设备租用/借出审批表GXZC-4222-0654、仪器设备租用/借出登记表GXZC-4222-0755、仪器设备(标准物质)送检通知书GXZC-4222-0856、年度仪器设备维护保养计划和实施记录GXZC-4222-0957、仪器设备(标准物质)使用记录GXZC-4222-1058、停用仪器设备启用申请单GXZC-4222-1159、检定/校准证书和测试报告确认表GXZC-4223-0160、允许偏离申请表GXZC-4224-0161、样品出入库登记表GXZC-4225-0162、日常质量监督抽查记录GXZC-4226-0163、检测报告更改申请表GXZC-4228-01文件和资料发放、回收记录表序号:编号:GXZC-4201-01文件修改记录序号:编号:GXZC-4201--02文件修改申请表序号:编号:GXZC-4201-03年月日文件修改通知单序号:编号:GXZC-4201-04文件破损与丢失补发登记表序号:编号:GXZC-4201-05文件和资料销毁登记表序号:编号:GXZC-4201-06文件和资料借阅登记表序号:备份文件记录序号:文件和资料留用申请单序号:公正性和行为准则执行情况审查表序号:外来人员参观审批表序号:查阅保密资料申请单序号:序号:序号:供应商评价表序号:合格供应商登记表序号:批准人: 编制人: 日期:______年度服务和供应品采购计划序号:批准: 审核: 编制:日期: 年月日检测委托单序号:合同评审单序号:分包申请表序号:分包方能力调查表序号;合格分包方名单序号:申诉和投诉处理记录表序号:客户意见征求表序号:不符合工作控制处理表序号:内部管理体系审核检查表序号:不符合项报告序号:会议纪要序号:整改措施报告序号:XZC-4211-02会议签到表序号:检测人员上岗报批表序号:人员学习记录表序号:序号:序号:制表:审核:批准:个人技术档案表序号:年度人员培训记录表序号:公司办公及试验环境卫生情况检查表序号:仪器设备检定/校准报告序号:编号:GXZC-4217-01检定单位:(章)检定员:审核:检测方法确认表序号:仪器设备(标准物质)期间核查记录表序号:负责人:设备管理员:更新标准实施审批表序号:序号:序号:仪器设备维修记录序号:编号:GXZC-4221-01计算机/自动化检测设备校核记录序号:编号:GXZC-4221-02校核人: 审核人:序号:序号:。
文件控制程序(版ISO9001+版ISO13485医疗器械生产质量管理体系文件).doc
文件编号:YPIQEP-01 文件名称:文件控制程序核准:杨x维核准日期:XXXX.12.13 制作部门:品质部审核:吕x豪审核日期:XXXX.12.13 制作者:孙x妮制作日期:XXXX.11.15 变更日期:XXXX.12.13 版本识别:第2版文件□建立■修改□废止履历表表单编号:YPIR-180-047 版本:2 生效日期:XXXX.12.13对质量、环境管理体系有关的文件进行控制,确保各部门及时得到并使用有效的版本。
2范围2.1本程序适用于公司质量、环境管理体系文件的控制和管理,包括公司内部形成的文件和适用的外来文件。
公司内部应形成的质量、环境管理体系文件:2.1.1一级文件:质量、环境手册(含质量、环境方针和质量、环境目标);2.1.2二级文件:程序文件;2.1.3三级文件:管理办法、图纸、BOM、操作规程、作业指导书、检验规范、变更通知单等;2.1.4四级文件:表单。
2.2适用的外来文件:2.2.1法律法规、标准;2.2.2顾客或供方提供的图样、技术文件等。
3定义3.1主文档(DMR):阐明器械将如何生产,包括试验和接收准则的以器械设计活动为基础的文件汇编。
包括:3.1.1原材料、标识、包装材料、部件和医疗器械的规范;3.1.2零部件清单;3.1.3工程图纸;3.1.4软件程序;作业指导书、包括设备操作;3.1.5适用时,灭菌过程的描述;3.1.6质量计划;3.1.7制造/检验/试验程序和接收准则。
4职责4.1总经理:负责质量、环境手册的批准。
4.2管理者代表:负责质量、环境程序文件的批准。
4.3DCC:负责文件的登录、印发、回收、销毁及文件正本的保存。
4.4各部门:负责本部门文件的编制及使用保管。
5作业程序5.1文件编写、会签、批准5.1.1文件编制格式5.1.1.1品质部在共享“\\192.168.0.218\loo\Systems\4 文件编制格式”文件夹,供各部门编写文件时使用。
工程变更控制程序文件
工程变更控制程序文件Engineering Change Control re文件编号/Doc No:XX-XX-XX文件版本/Doc Ed:XX生效日期/n:20XX-XX-XX文件名称:工程变更控制程序/ Engineering Change Control re更改史(REVISION HISTORY)版本/Doc Ed: XX更改日期/Change Date:原始版本/Originator: 研究资料整理更改原因/Reasons for Change: 首版目的:为了有效控制设计和生产等工程变更的风险,使公司各部门能在最短的时间内获得正确的变更信息,达到文件规范化管理,特制定本程序。
适用范围:本程序适用于XX公司生产、销售产品的设计、制造、检测、安装等过程及产品相关零件的设计、制造、检测等过程。
相关文件:定义:1.ECR: Engineering Change Request工程变更申请单;2.ECN: Engineering Change n工程变更通知单;3.工程变更:指涉及工艺技术、设备设施、工艺参数、生产地点等变更;4.同类替换:符合原设计规格的更换;5.微小变更:影响较小,不造成任何工艺参数、设计参数等的改变,但又不是同类替换的变更。
即“在现有设计范围内的改变”;6.紧急变更:在紧急情况下(例如:安装现场发生重大质量问题,工艺参数处于危险限值等情况,如不在短时间内处理可能导致重大安全事故、财产损失或客户丢失等情况的发生),正常的变更流程方式无法执行时。
职责:1.相关部门:负责ECR的申请与确认,并依工程部发布的ECN内容配合相关工作的实施与落实;2.工程部:负责工程变更的审查、执行、验证、ECN核发及相关技术文件的修订,并协助各部门工程变更后相关物料及产品处理方式的确定;3.销售部:负责接收客户变更信息和向客户传递变更信息。
6.3.5.在涉及产品材质、尺寸、外观、功能或可能影响客户使用的变更时,销售部必须提前通知客户,并征得客户同意,然后在ECR上进行会签。
最新GJB9001C:2017国军标一整套程序文件(含全套表单)
最新GJB9001C:2017国军标⼀整套程序⽂件(含全套表单)GJB9001C-2017程序⽂件汇编01⽂件控制程序.doc02图样和技术⽂件的审签程序.doc03⼯艺⽂件编制与管理程序.doc04图样及技术⽂件的归档及管理程序.doc 05记录控制程序.doc06质量职责制定与分配程序.doc07沟通与协调控制程序.doc08管理评审控制程序.doc09⼈员能⼒培训管理程序.doc10⽣产设备管理程序.doc11⼯作环境控制程序.doc12质量信息控制程序.doc13产品实现策划管理程序.doc14与产品有关要求的确定与评审程序.doc 15研制(设计和开发)策划程序.doc16产品研制总程序.doc17装备研制过程控制程序.doc18设计更改控制程序.doc19软件设计开发控制程序.doc20新产品试制控制程序.doc21合格供⽅选择和评定程序.doc22采购控制程序.doc23新设计开发产品的采购.doc24代⽤采购产品质量控制程序.doc25产品外包过程的管理办法.doc26产品制造过程的控制程序.doc27关键过程控制程序.doc28标识和可追溯性控制程序.doc29产品搬运、贮存、包装、防护和交付的控制程序.doc 30顾客财产控制程序.doc31产品交验控制程序.doc32交付后活动控制程序.doc33监视和测量设备的控制程序.doc34技术状态管理程序.doc35顾客沟通和顾客满意度评定控制程序.doc36内部审核控制程序.doc37过程监视和测量控制程序.doc38产品监视测量(试验)控制程序.doc39不合格品控制程序.doc40数据分析管理程序.doc41质量经济性分析程序.doc42质量成本统计核算与分析程序.doc43持续改进程序.doc44纠正措施控制程序.doc45预防措施控制程序.doc⽂件控制程序⼀、⽬的为确保质量管理体系⽂件的适宜性和充分性,以及在⽂件的使⽤现场能够得到有效版本,防⽌作废⽂件或不适⽤的⽂件⾮预期使⽤,制定本程序。
