4第四章 炔烃和二烯烃1解析
第四章炔烃和二烯烃

第四章炔烃和二烯烃4-1.(南京航空航天大学2008年硕士研究生入学考试试题)分子式为C4H6的三个异构体A、B、C能发生如下反应:(1)三个异构体都能与溴反应,对于等摩尔的样品而言,与B和C 反应的溴量是A的两倍;(2)三者都能与氯化氢反应,而B和C在Hg2+催化下和氯化氢作用得到的事同一种产物;(3)B和C能迅速地和含硫酸汞的硫酸溶液作用得到分子式为C4H8O的化合物;(4)B能和硝酸银氨溶液作用生成白色沉淀。
试推测化合物A、B、和C 的结构,并写出有关反应式。
解:由(1)条件可知A、B、C其均含有不饱和键且B和C的不饱和度是A的两倍;由(2)条件可知B和C为同分异构体,由(3)、(4)条件可知B和C含有三键,且确定出B中三键的位置。
所以,A为,B为CH3CH2C CH,C为CH3C CCH3。
相关的反应式如下:+BrCH3CH2C CH CH3CH2C(Br2)CHBr22Br2HClCH3CH2C CH2HCl3CH2C(Cl2)CH3CH3C CCH32HCl3CH2C(Cl2)CH3CH3C CCH3H2O CH3CH2CCH3OCH3CH2C CH H2O424CH3CH2CCH3OCH3CH2C CH AgNO3CH3CH2C4-2.(南京航空航天大学2006年硕士研究生入学考试试题)碳氢化合物A(C8H12)具有光学活性,在铂的存在下催化氢化成B(C8H18),B无光学活性;A用Lindor催化剂小心催化成C(C8H14),C有光学活性。
A在液氨中与金属钠作用得到D(C8H14),D与C互为同分异构体,但D无光学活性。
写出A、B、C、D的结构式。
解:根据题意A为炔烃,炔烃用Lindor催化剂催化成的C为烯烃,即D也为烯烃,所以A、B、C、D的结构式为:CCCC C C HHC(A)CCCC C HCCC(B)CC HC HC CHC CH CCH 3CD4-3.(中国科学院—中国科学技术大学2004年硕士研究生入学考试试题)用乙炔为原料选用适当的无机试剂合成CH 2BrCH 2BrBrBr解:要得到反应产物,需要根据狄尔斯—阿尔德反应得到环烯,然后与溴加成,而生成环烯又必须先得到共轭烯烃。
Ch.4 炔烃和二烯烃

第四章炔烃和二烯烃炔烃:定义、通式二烯烃:定义、通式烯炔:定义、通式第一节炔烃一、结构以乙炔为例根据已知事实,杂化轨道理论认为,每个处于激发态的C原子发生的是SP 杂化。
对-C≡C-必须认识到:①4个原子在一条直线上。
②C≡C是由1个σ键和2个π键组成的。
③C≡C及C-H键都比乙烯的短:原因: C C 间成键电子多,使两个核更靠近;SP杂化轨道比SP2轨道短。
④C≡C中的π键牢固,π电子云的流动性乙烯的小。
原因:C≡C较短,P轨道重迭较多,核对π电子的束缚力较大。
二、命名1.炔烃的系统命名法与烯烃的系统命名法相似,只须把烯字改为炔字即可。
2.炔烃的衍生物命名法以乙炔为母体,把其它炔烃看成是乙炔的H被取代后生成的衍生物。
3.烯炔的系统命名法在炔烃的系统命名法的基础上补充二点:①选择既含C≡C又含C=C的最长C链作主链(母体),称为烯炔,要分别标示C≡C和C=C的位次。
②编号使二个重键的位次符合最低(编码)系列原则,若C≡C和C=C的位置相当,应把最小位次给予C=C双键。
3-甲基-3-戊烯-1-炔 1-戊烯-4-炔三、物理性质(自习)物质状态:C2-C4(g)C5以上(l)更高级者(s)如1-十八碳炔m.p 22.5°Cb.p:随分子量的增加而升高。
比相应的烯烃高10-20°C,比相应的烷烃略高。
比重:比相应的烯烃大。
在水中的溶解度:比烷烃、烯烃都大些。
四、化学性质炔烃的化学性质与烯烃相似,也能发生加成、氧化、聚合等反应,但二者毕竟不完全相同,因此炔烃还有某些特有的性质。
1.加成反应⑴催化加氢如果使用的催化剂是Pt或Pd,反应难停留在第一步,主要产物是烷烃。
若使用经过降活处理的催化剂如林德拉催化剂(Lindlar cat.),可使炔烃只发生部分氢化,主要产物是顺式烯烃。
关于Lindlar cat.的成份问题:一种说法是P d-BaSO4 / 喹啉(题库);另一种说法是Pd(Pb)-CaCO3(教材与其它文献)。
炔烃和二烯烃

第四章炔烃和二烯烃(I )炔烃一、定义、通式和同分异构体定义:分子中含有碳碳叁键的不饱和烃。
通式:C n H 2n-2同分异构体:与烯烃相同。
二、结构在乙炔分子中,两个碳原子采用SP 杂化方式,即一个 2S 轨道与一个2P 轨道杂化, 组成两个等同的 SP 杂化轨道,SP 杂化轨道的形状与 SP 2、SP 3杂化轨道相似,两个SP 杂化 轨道的对称轴在一条直线上。
两个以SP 杂化的碳原子,各以一个杂化轨道相互结合形成碳碳6键,另一个杂化轨道各与一个氢原子结合,形成碳氢 6键,三个6键的键轴在一条直线上,即乙炔分子为直线型分子。
每个碳原子还有两个末参加杂化的P 轨道,它们的轴互相垂直。
当两个碳原子的两P轨道分别平行时,两两侧面重叠,形成两个相互垂直的 n 键。
三、命名炔烃的命名原则与烯烃相同,即选择包含叁键的最长碳链作主链,碳原子的编号从 距叁键最近的一端开始。
若分子中即含有双键又含有叁键时,则应选择含有双键和叁键的最长碳链为主链, 并将其命名为烯炔(烯在前、炔在后)。
编号时,应使烯、炔所在位次的和为最小。
例如:CfCfCHCHDHC 三 CH3-甲基-4-庚烯-1-炔CH 3但是,当双键和叁键处在相同的位次时,即烯、炔两碳原子编号之和相等时,则从 靠近双键一端开始编号。
如:Cf 二C 比三CH1-丁烯-3-炔四、 物理性质与烯烃相似,乙炔、丙炔和丁炔为气体,戊炔以上的低级炔烃为液体,高级炔烃为 固体。
简单炔烃的沸点、熔点和相对密度比相应的烯烃要高。
炔烃难溶于水而易溶于有机溶剂。
五、 化学性质 (一)加成反应1、催化加氢炔烃的催化加氢分两步进行,第一步加一个氢分子,生成烯烃;第二步再与一个氢分加成,生成烷烃。
催化剂HC 三 CH + H 2 —CH2、加卤素炔烃与卤素的加成也是分两步进行的。
先加一分子氯或溴,生成二卤代烯,在过量 的氯或溴的存在下,再进一步与一分子卤素加成,生成四卤代烷。
HC 三CH + Br2 -------- Br=CHBrCHB 广2CHB 2虽然炔烃比烯烃更不饱和,但炔烃进行亲电加成却比烯烃难。
4第四章 炔烃 二烯烃
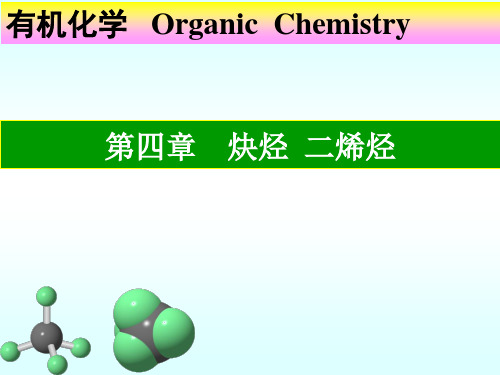
RCCR` KMnO4 RCOOH + R`COOH
H2O
(2) 缓慢氧化——二酮
OO
CH3(CH2)7CC(CH2)7COOH
KMnO4 H2O
CH3(CH2)7-C-C-(CH2)7COOH
pH=7.5
92%~96%
•利用炔烃的氧化反应,检验叁键的存在及位置
•这些反应产率较低,不宜制备羧酸或二酮.
有机化学 Organic Chemistry 第四章 炔烃 二烯烃
第四章 炔烃 二烯烃
(一) 炔烃
定义:分子中含有碳碳叁键的烃叫做炔烃,它的通式:
CnH2n-2 官能团为: -CC-
4.1 炔烃的异构和命名**
(1)异构体——从丁炔开始有异构体.
•同烯烃一样,由于碳链不同和叁键位置不同所引起的.由 于在碳链分支的地方不可能有叁键的存在,所以炔烃的 异构体比同碳原子数的烯烃要少. •由于叁键碳上只可能连有一个取代基,因此炔烃不存在 顺反异构现象.
炔烃和烯烃一样,也能和卤化氢、卤素等起亲电加成反
应,但炔的加成速度比烯慢
(A) 和卤素的加成
Br2
RC CR
Br
+
RC CR
Br-
反式加成
Br
R
CC
R
Br
卤素的活性F2>Cl2>Br2>I2
Br Br Br2 R C C R
这一反应可用于炔烃的鉴别。
Br Br
控制条件也可停止在一分子加成产物上.
❖加氯必须用FeCl3作催化剂。
•含有双键的炔烃在命名时,一般 先命名烯再命名炔 .
碳链编号以表示双键与叁键位置的两个数字之和最小
为原则。在同等的情况下,要使双键的位次最小。
第四章 炔烃和二烯烃

4.1 炔烃
二、炔烃的命名 1. 衍生物命名法
衍生物命名法只适用于简单的炔烃。以乙炔为母体,将其它的炔 烃看作乙炔的衍生物。
例如:
4.1 炔烃
2. 系统命名法
与烯烃的命名类似 ① 要选择含有 C≡C 的最长碳链为主链; ② 编号从最距离叁键最近的一端开始,并用阿位伯数字表示叁键的 位置。例:
837KJ/mol 0.120nm
611KJ/mol 0.134nm 0.108nm
( 3x347=1041)
347KJ/mol
0.154nm 0.110nm
H C C H H2C CH H
H3C C H2 H
原因: ① -C≡C-中有1个σ和2个π键; ② sp 杂化轨道中的 s 成份多。(s 电子的特点就是离核近,即 s 电子
CNa CNa + 2CH3I
CH3C CC2H5 + NaBr
CH3C CCH3 + 2NaI
炔化物作为亲核试剂,也可以与醛酮 发生亲核加成反应,得到 羟基炔化合物:
4.1 炔烃
(3) 过渡金属炔化物的生成及炔烃的鉴定
CH CH + 2Ag(NH3)2NO3 CH CH + 2Cu(NH3)2Cl
4.1 炔烃
③分子中同时含有双键和参键时,先叫烯后叫炔,编号要使双键和
参键的位次和最小。
1 2 3 45
CH C-CH=CHCH3
3-戊烯-1-炔
6 54 3 2 1
CH C-CH=C-CH=CH2
3-乙基-1,3-己二烯-5-炔
CH2CH3
④若双键、叁键处于相同的位次供选择时,优先给双键以最低编号。
4.1 炔烃
第4章 炔烃、二烯烃
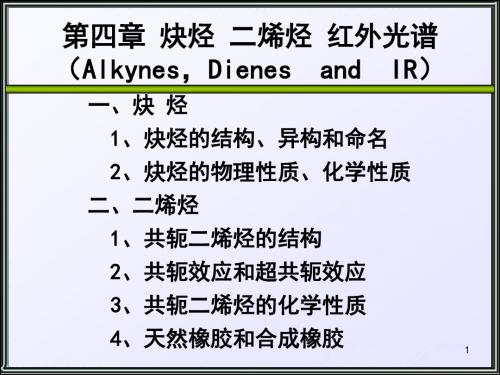
碳素酸的弱酸性
Na
+ 2 HC
+
HC
CH
CH
110℃
2 HC
CNa
+H
NH3
2
NaNH2
HC
CNa
+
13
R3C CH
Ka
R3C C
CH
+
44
H
+
物质名称
pKa
HOH
HC
H2 C
CH2
H3 C
CH3
15.7
25
50
端炔酸性的解释 端炔中的碳为sp杂化, 轨道中s成分较大, 核 对电子的束缚能力强, 电子云靠近碳原子, 使分子中的C-H键极性增加, 易断裂:
HC CH
+ 2 Ag(NH3)2NO3
+ 2 Cu(NH3)2Cl
AgC
CAg
+ 2 NH4NO3 + 2 NH3
乙炔银(白色)
HC CH
CuC
CCu
+ 2 NH4Cl + 2 NH3
乙炔亚铜(砖红色)
应用: 区别端炔与非端炔、端炔与烯烃。
RC CH
16
炔化物的生成
注意:炔化银或炔化亚铜在干燥状态下, 受热或震动容易爆炸。实验完毕后 加稀硝酸使其分解。
+
RC
CH2
> RCH
+
CH
22
炔烃的亲电加成
炔烃与烯烃反应活性比较: 炔烃的加成速度比烯烃慢。
加卤素
当化合物中同时含有双键和叁键时, 首先在双键上发生加成反应。
Br2 低温
Br Br
选择性加成
第4章炔烃

(Alkynes Diene IR )
分子中含有碳碳叁键“ C≡C ”的不饱和烃叫炔烃。 通式CnH2n-2,与同碳数二烯烃互为同分异构体。
第一节 炔 烃
4.1炔烃的命名
❖ 1.简单的炔,可用衍生物命名法命名。
以乙炔为母体,其它作为取代基。
❖ 如:
CH3CH2C≡CH CH3-C≡C-CH3 CH2=CH-C≡CH
❖ 二. 与Ag+、Cu+等重金属盐 反应——重金属炔化物的生 成
❖ 三. 炔氢弱酸性的解释
4.4.1 加成反应—催化加氢
❖ 炔烃催化加氢第一步生成烯,第二步继续加成为
饱和烃。常用催化剂有Pt、Pd、Ni等。
pKa 49
34
25
15.9
15.74
乙炔中的键电子云
H
H
❖ 每个键就不是孤立 的两块,它们形成分 布在C原子的上、下、 前、后的统一的筒状 电子云。
炔烃的异构
❖ 炔烃的异构可由碳链的结构及官能团位置变化引 起,但由于碳最高只有4价,叁键碳只能连有一个 烃基,所以炔烃不存在顺反异构体,炔烃的异构 体数因此较相应碳数烯烃的异构体要少。
两个碳链等长、不饱和键数目相同, 选含“双键”数最多的链为主碳链。
CH3C C CHCH2 CH CH2 CH CH2
4 _乙烯基 _ 1 _庚烯 _ 5 _ 炔 所含不饱和键数目相等,但碳链 不等长,选择较长的链为主碳链。
4.2 炔烃的结构
❖ 炔烃的结构特征是分子中含有“C≡C”,它与 “C=C”一样,是由键和键构成,下面以乙炔 为例说明叁键的形成及结构,乙炔为一直线型 分子,全部四个原子在同一直线上。
120.7pm
(Csp3-Csp3)
炔烃 二烯烃

第四章炔烃二烯烃学习要点:本章学习在了解炔烃和二烯烃结构的基础上,重点掌握这两类化合物的化学性质以及由共轭二烯烃的结构特征所引起的共轭效应及其对化学性质的影响。
第一节炔烃不饱和烃除了烯烃外还有炔烃。
例如气割气焊用的乙炔(HC≡CH),就是一个炔烃,凡含有碳碳叁键的不饱和烃均称为炔烃,碳碳叁键(-C≡C-)是它的官能团,它的通式为C n H2n-2,与碳原子数相同的二烯烃,环烯烃为同分异构体。
一、炔烃的结构以炔烃中结构最简单的乙炔为例,在乙炔中两个叁键碳原子都是只和两个原子相结合,因此它只需要用两个价电子来构成两个σ键,亦即炔碳原子中的s电子轨道只要和一个p电子轨道进行sp杂化就可以了,形成了两个相等的sp杂化轨道,如图4-1所示。
图4-1 碳原子轨道的sp杂化每个sp杂化轨道包含1/2s轨道成分和1/2p轨道成分,其形状与sp3,sp2杂化轨道相似,只是更“胖”些,两个sp杂化轨道对称地分布在碳的两侧,成为一条直线,两者之间的夹角为180º。
如图4-2所示。
所以在乙炔中每一个碳都以一个sp杂化电子轨道与氢的1s电子轨道相互重迭成为一个C-H键,两个碳又各以一个sp杂化轨道相重迭,形成C-C键,这些都是σ键。
图4-2 碳原子的sp杂化电子轨道两个C原子尚各余两个p电子轨道,它们的对称轴都与sp杂化轨道的对称轴互相垂直,这两个p轨道可以在各自侧面重迭形成两个π键,所以炔键叁键中一个是σ键,两个是π键。
实际上叁键中四个π电子的电子云是混合在一起,它们围绕着连接两个碳核的直线成圆筒形分布。
如图4-3所示。
图4-3 乙炔分子的圆筒形π电子云其他炔烃的碳碳叁键与乙炔相同,也是由一个σ键和两个π键组成。
二、炔烃的同分异构和命名炔烃中除了乙炔和丙炔没有异构体外,从丁炔开始有构造异构现象,但由于叁键碳上只有一个取代基,因此炔烃的构造异构体比烯烃少,也无顺反异构体。
例如丁烯有三个构造异构体,但丁炔只有两个构造异构体,如下:CH3CH2C CH CH3C CCH31-丁炔2-丁炔简单的炔烃可采用衍生物命名法,即以乙炔作母体,将其它基团看成取代基,而复杂的炔烃必须采用系统命名法,炔烃的命名与烯烃相似,只须将“烯”改为“炔”即可。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CH3CH2CCCH2CH3 + HCl
CH3CH2 H C
99%
Cl C CH2CH3
不同类型炔烃与HX加成反应的速度大小顺序为: RC≡CR’>RC≡CH>HC≡CH 碳正离子的稳定性顺序: R3C+>>R2CH+>RCH2+,RC+=CH2>RCH=CH+ 3 加 HBr
酸 性 逐 渐 增 强 其 共 轭 碱 的 碱 性 逐 渐 减 弱
2 鉴别方法
R-CCH
NaNH2 液氨 Ag (NH3)+2NO3 Cu (NH3)+2Cl
R-CC Na+NH3 R-CC Ag R-CC Cu
鉴 别 端 基 炔
R-CC Ag
-CN
HNO3 + H2 O HNO3
R-CCH + AgNO3 R-CCH + Ag(CN)-2 + HO-
CH2BrCHBr-CH2-CCH
碳sp杂化轨道的电负性大于碳 sp2杂化轨道的电负性,所以 炔中电子控制较牢。
2 加 HI 和 HCl
*1 与不对称炔烃加成时,符合马氏规则。
*2 与HCl加成,常用汞盐和铜盐做催化剂。
*3 由于卤素的吸电子作用,反应能控制在一元阶段。 *4 反式加成。
催化剂
CH3CH=CHC CH 3-戊烯-1-炔 3-penten-1-yne
1 8 H3C H 7 6 5 2 3 4
CHCCH2CH=CH2 1-戊烯-4-炔
1-penten-4-yne
CHCCH2CH=ຫໍສະໝຸດ HCH2CH2CH=CH2 4,8-壬二烯-1-炔 4,8-nonadien-1-yne
(S)-7-甲基环辛烯-3-炔 (S)-7-methylcycloocten-3-yne
本节作业
3 末端炔烃与醛、酮的反应
RCCH
H 2O KOH
RCC-
CH2= O
RCC-CH2O-
RCC-CH2OH + -OH
末端H被羟甲基取代
O n-C5H11CH
RCCH
n-C4H9Li, THF, -78oC
RCC-Li+
O-Li+ RCC-CHC5H11-n
H2O
OH RCC-CHC5H11-n
R-CCCu
R-CCH + Cu2(NO3)2 分解、纯化炔烃的方法
加浓盐酸也是分解炔化物的方法,方程式你知道吗?
问题4-4: 区别下列各组化合物
(1) CH≡CCH2CH3,CH3C≡CCH3 (2) CH ≡CCH2CH3, CH2=CH-CH=CH2 (3) CH ≡CCH2CH3, CH2=CHCH2CH3
二、 炔烃的物理性质
1.
简单炔烃的沸点(bp)、熔点(mp)以及密度(d)比碳原
子数相同的烷烃和烯烃高一些。见图4-6.
2. 炔烃分子极性比烯烃稍强。
3. 炔烃不易溶于水,而易溶于石油醚、乙醚、苯和四
氯化碳中。 CH3CH2C≡CH μ=0.80D CH3CH2CH=CH2 CH3C≡CCH3 0.30D 0 2-丁炔比1-丁炔稳定.
154pm (Csp3-Csp3)
134pm (Csp2-Csp2) 108.6pm (Csp2-Hs) 长 逐 渐 变 成 宽
120pm (Csp-Csp) 105.9pm (Csp-Hs) 圆
C-H:
110.2pm (Csp3-Hs)
轨道形状: 碳的电负性: pKa:
狭
随 S 成 份 的 增 大, 逐 渐 增 大。 ~50 ~40 ~25
答:炔烃没有顺反异构体。因为三键碳是SP杂化,为直线型构型,故无顺反异构现象。
2、 炔烃的异构
3、 命名
只有位置异构和碳架异构
衍生物命名法: 把乙炔作为母体, 其它炔烃作为乙炔的衍生物命名.
系统命名法: 1.选择含三键的最长碳链为主链,根据碳的数目称某炔. 2.从靠近三键一端编号,用号码最小的表示三键的位置. 3.在母体名称前加上取代基的位置和名称. 4.复杂的化合物也可以把炔基作为取代基.
三、 炔烃的化学性质
四、 炔烃的制备
一、
炔烃的结构、异构和命名
H C C H
SP杂化 线型分子 筒状电子云
1、炔烃的结构
H H H
s p3
s p2
C
H H C
sp
H C C
C
H
杂化方式: 键角: 键长不同 碳碳键长
SP3 109o28’
SP2 ~120o
问题4-1:炔 SP 烃有没有顺反 o 180 异构体,为什 么?
末端H被取代
的羟甲基取代
该反应主要用来制备炔醇、也可以用来接长碳链。
=
(二 ) 炔烃的亲电加成和自由基加成
1 加卤素
*1 HCCH
Cl2
H Cl C C Cl H
FeCl3
Cl2 FeCl3
CHCl2-CHCl2
为什么炔 烃的亲电 加成要比 烯烃难?
反应能控制在这一步。
*2 加氯必须用催化剂,加溴不用。 *3 CH2=CH-CH2-CCH + Br2 (1mol)
几个重要的炔基
HC C乙炔基 ethynyl CH3C C1-丙炔基 1-propynyl HC CCH22-丙炔基 2-propynyl
问题4-2:写出炔烃C6H10的异构体并命名。
问题4-2解答:
5. *若分子中同时含有双键和叁键,可用烯炔作词尾,给 双键和叁键以尽可能小的编号,如果位号有选择时,使双 键位号比叁键小。书写时先烯后炔. 实例
第四章
炔烃和共轭二烯烃
炔烃(alkyne)是含有碳碳三键的不饱和烃; 二烯烃(diene)是含有两个碳碳双键的不饱和烃; 它们的通式都是CnH2n-2.
本章内容
第一节 炔烃alkyne 第二节 二烯烃dienes 第三节 共轭效应
第四节 速率控制与平衡控制
第一节
炔烃的主要内容
一、 炔烃的结构异构和命名 二、 炔烃的物理性质
三 、 炔烃的化学性质
(一 ) 末端炔烃的酸性、鉴别
1 酸性
R3C-H
R3C- + H+
碳氢键的断裂也可以看作是一种酸性电离,所以将烃称为含碳酸
含碳酸的酸性强弱可用pka值判别, pka越小,酸性越强。
烷烃(乙烷)〈 烯烃(乙烯) 氨 〈 末端炔烃(乙炔)〈 乙醇 〈 水 pka ~50 ~40 35 25 16 15.7
实例
CH3C≡CCH3
二甲基乙炔
(CH3)2CHC≡CH
3-甲基-1-丁炔
CH3
dimethylacetylene (CH3)3CC≡CCH3
4,4-二甲基-2-戊炔
3-methyl-1-butyne
CH2C CH
4,4-dimethyl-2-pentyne
1-甲基-2-(2-丙炔基)-环己烯 1-methyl-2-(2-propynyl)-cyclohexen
