促甲状腺素化学发光免疫定量检测试剂盒的研制
促甲状腺激素(TSH)测定试剂盒(电化学发光免疫分析法)产品技术要求lianzhongtaike

促甲状腺激素(TSH)测定试剂盒(电化学发光免疫分析法)组成:适用范围:本试剂盒用于体外定量测定人体血清样本中促甲状腺激素(TSH)的含量。
2.1 外观2.1.1 试剂盒各组分应齐全、完整、液体无渗漏;2.1.2 磁分离试剂摇匀后应为棕色含固体微粒的均匀悬浊液,无明显凝集、无絮状物;2.1.3 其它液体组分应澄清,无异物,沉淀物或絮状物;2.1.4 包装标签应清晰、无磨损、易识别。
2.2 空白限应不大于0.01μIU/mL。
2.3 准确度用TSH国家标准品(150530)进行检测,其测量结果的相对偏差应在±10%范围内。
2.4 线性在[0.01,100.0]μIU/mL范围内,线性相关系数(r)应不小于0.9900。
2.5 精密度2.5.1 分析内精密度在试剂盒的线性范围内,浓度为(5.0±1.0μIU/mL)和(30.0±6.0μIU/mL)的样品检测结果的变异系数(CV)应不大于8%。
2.5.2 批间精密度在试剂盒的线性范围内,用3个批号试剂盒分别检测浓度为(5.0±1.0μIU/mL)和(30.0±6.0μIU/mL)的样品,检测结果的变异系数(CV)应不大于15%。
2.6 特异性2.6.1 与促卵泡生成激素(FSH)浓度不低于200mIU/mL促卵泡生成激素(FSH)样品,在本试剂盒测定结果应不大于0.01μIU/mL;2.6.2 与促黄体生成素(LH)浓度不低于200mIU/mL促黄体生成素(LH)样品,在本试剂盒测定结果应不大于0.01μIU/mL;2.6.3 与人绒毛促性腺激素(HCG)浓度不低于1000mIU/mL人绒毛膜促性腺激素(HCG)样品,在本试剂盒测定结果应不大于0.01μIU/mL。
2.7 效期末稳定性本产品效期为15个月,试剂盒在2~8℃下保存至有效期末进行检测,检测结果应符合2.1、2.2、2.3、2.4、2.5.1的要求。
促甲状腺激素测定试剂盒产品技术要求国赛

促甲状腺激素测定试剂盒产品技术要求国赛摘要:促甲状腺激素(TSH)测定试剂盒是一种通过化学发光免疫分析法来测定人体内促甲状腺激素水平的产品。
本文将从试剂盒的基本原理、技术指标、操作方法、结果判断等方面进行详细介绍,并提出了一些改进方案,以进一步提高其准确性和可靠性。
1.试剂盒的基本原理2.技术指标(1)测定范围:0.1-100mIU/L(2)灵敏度:0.1mIU/L(3)精密度:CV≤10%(4)准确度:与国家标准方法比较,差异不超过±10%3.操作方法(1)样品准备:采集血清样本,离心去除红细胞沉淀。
(2)试剂盒开封:将试剂盒从冰箱取出,放置室温下30分钟使其恢复平衡。
(3)标准曲线制备:用不同浓度的标准品配制标准曲线,按照试剂盒使用说明进行操作。
(4)样品测试:取适量血清样本,按照试剂盒使用说明进行操作,加入发光试剂后进行混匀,开始计时。
(5)数据处理:根据标准曲线上的吸光度值,计算出样品中促甲状腺激素的浓度。
4.结果判断(1)阳性结果:样品中促甲状腺激素浓度超过设定的参考范围上限。
(2)阴性结果:样品中促甲状腺激素浓度在参考范围内。
(3)结果异常:样品中促甲状腺激素浓度超过参考范围上下限,需要进一步检测。
5.改进方案(1)优化抗体:选择更具特异性的抗体,提高试剂盒的选择性。
(2)增加质控品:引入质控品,增加结果的稳定性和可靠性。
(3)提高灵敏度:通过改进试剂盒中的光学材料和化学试剂,提高试剂盒的灵敏度。
(4)缩短操作时间:优化操作流程,减少操作时间,提高实验效率。
(5)降低价格:通过技术改进和成本优化,降低试剂盒的价格,提高产品的竞争力。
总结:促甲状腺激素(TSH)测定试剂盒是一种重要的医学检验试剂,可以用于评估甲状腺功能的正常与否。
本文对其技术要求进行了详细介绍,并提出了一些改进方案,以进一步提高其准确性和可靠性。
希望上述内容能够为促甲状腺激素(TSH)测定试剂盒的开发和优化提供参考。
促甲状腺激素(TSH)测定试剂盒(化学发光免疫分析法)产品技术要求爱康试剂

促甲状腺激素(TSH)测定试剂盒(化学发光免疫分析法)1.性能指标1.1试剂条性能指标1.1.1外观试剂盒各组分应齐全、完整,液体无渗漏,包装标签应清晰、准确、牢固;试剂条中第7孔内组分应为棕色含固体微粒的液体或含棕色固体沉淀的透明液体;第12孔内化学发光底物应为无色或淡绿色液体;其余皆应为无色透明液体,无悬浮物、无沉淀、无絮状物。
1.1.2空白限应不大于0.005μIU/mL。
1.1.3准确度1.1.3.1在试剂盒规定的线性区间内,检测促甲状腺素国家标准品,测定结果的相对偏差应在±10%范围内。
1.1.3.2对具有溯源性的两个浓度水平的正确度控制品进行检测,检测结果与标定浓度的相对偏差应在±10%范围内。
1.1.4线性区间试剂盒在0.02μIU/mL~100μIU/mL区间内,其线性相关系数(r)应不小于0.9900。
1.1.5分析内精密度变异系数(CV)应不大于8.0%。
1.1.6批间精密度变异系数(CV)应不大于15.0%。
1.1.7特异性a)含浓度不低于200 mIU/mL的FSH的零浓度TSH样本,检测结果应不高于0.005μIU/mL;b)含浓度不低于200 mIU/mL的LH的零浓度TSH样本,检测结果应不高于0.005μIU/mL;c)含浓度不低于1000mIU/m L的HCG的零浓度TSH样本,检测结果应不高于0.005μIU/mL。
1.2校准品性能指标1.2.1外观校准品应为无色或浅黄色透明液体。
1.2.2装量装量偏差应在±10%之内。
1.2.3准确度Cal 1、Cal 2实测值与标示值的偏差应在±10%以内。
1.2.4均一性对同一瓶校准品1、校准品2分别重复10次检测,对同一批次10瓶校准品1、校准品2进行检测,检测校准品1、校准品2瓶内差CV应≤10%,批内瓶间差CV应≤10%。
1.3质控品性能指标1.3.1外观质控品应为无色或浅黄色透明液体。
促甲状腺激素(TSH)测定试剂盒(化学发光免疫分析法)产品技术要求taige

促甲状腺激素(TSH)测定试剂盒(化学发光免疫分析法)适用范围:本试剂盒主要用于体外定量测定人血清中的促甲状腺激素(TSH)含量。
1.1 包装规格48人份/盒,96人份/盒。
1.2 主要组成成分2.1 外观液体组分澄清,无沉淀或絮状物;其它组分无包装破损,标签外观完整、无脱落、标签标识清晰。
2.2 装量装量不少于标示值。
2.3 准确度试剂盒校准品与国家标准品(编号:150530)同时进行分析测定,用双对数数学模型拟合,要求两条剂量-反应曲线不显著偏离平行(t-检验);以TSH国家标准品(编号:150530)为对照品,试剂盒校准品的实测效价与标示效价之比应在0.900~1.100范围内。
2.4 剂量-反应曲线线性相关系数在[0.25,50]mIU/L范围内,用双对数数学模型拟合,剂量-反应曲线相关系数(r)的绝对值应不小于0.9900。
2.5 精密度2.5.1 重复性以同批次试剂盒,高低两种浓度的质控血清平行测定10次,求其平均值和标准差(SD),批内精密度(CV%)=SD/平均值×100%,重复性(CV%)应不高于15.0%;2.5.2 批间差三种不同批次试剂盒,对同一样品进行重复测定10次,计算各组测定结果的平均值和标准差(SD),批间精密度(CV%)=SD/平均值×100%,批间差(CV%)应不高于20.0%。
2.6 最低检出量应不高于0.1mIU/L。
2.7 质控血清测定值应在允许的范围之内。
2.8 特异性与浓度为80mIU/L 的促卵泡生成激素(FSH)反应,测定结果应小于0.1 mIU/L;与浓度为2000mIU/L 的人绒毛膜促性腺激素(HCG)反应,测定结果应小于0.1 mIU/L。
2.9 稳定性2.9.1 热稳定性37℃放置3天,测定结果应符合上述2.1~2.7项要求。
2.9.2 效期稳定性成品试剂盒2~8℃存放6个月后,测定结果应符合上述2.1~2.7项要求。
促甲状腺激素(TSH)测定试剂盒(磁微粒化学发光免疫分析法)产品技术要求beiaikang
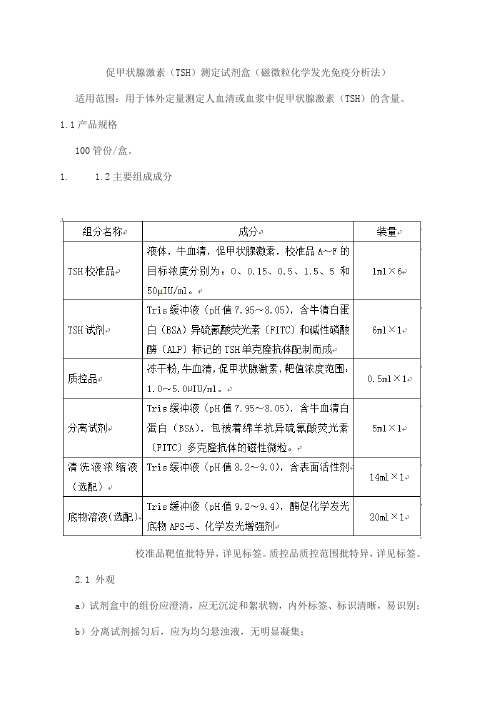
促甲状腺激素(TSH)测定试剂盒(磁微粒化学发光免疫分析法)适用范围:用于体外定量测定人血清或血浆中促甲状腺激素(TSH)的含量。
1.1产品规格100管份/盒。
1. 1.2主要组成成分校准品靶值批特异,详见标签。
质控品质控范围批特异,详见标签。
2.1 外观a)试剂盒中的组份应澄清,应无沉淀和絮状物,内外标签、标识清晰,易识别;b)分离试剂摇匀后,应为均匀悬浊液,无明显凝集;c)冻干组分呈白色或淡黄色疏松体,加水后应在20分钟内完全溶解,所得液体应无沉淀和不溶物质。
2.2 校准品溯源根据GB/T21415及有关规定提供校准品的来源、赋值过程及测量不确定度等内容,溯源至国家标准品(编号:150530)。
2.3 净含量试剂盒各液体组份的体积不得少于标称体积。
2.4 最低检出限试剂盒的最低检出限不高于0.1µIU/ml。
2.5 线性在(0.4,50µIU/ml)范围内剂量-反应曲线相关系数(r)的绝对值应≥0.9900。
2.6 精密度2.6.1分析内精密度:用高低两个浓度水平的样本,各重复检测10次其变异系数(CV)应不大于8%(全自动操作法)或不大于15%(手工操作法)。
2.6.2分析间精密度:在多次独立分析之间,质控品测定结果的变异系数CV应不大于20%(仅限手工操作法)。
2.6.3批间精密度:用三个批号试剂盒检测同一样本,则三个批号试剂盒试剂盒之间的变异系数(CV)应不大于20%。
2.7 冻干粉瓶间差质控品按照规定复溶后,瓶间浓度变异系数CV≤15%。
2.8 准确性试剂盒内校准品与相应浓度的国家标准品(编号:150530)同时进行分析测定,用双对数或其他适当的数学模型拟合,要求两条剂量-反应曲线不显著偏离平行;以TSH国家标准品为对照品,试剂盒内校准品的实测值与标示值的效价比应在0.900~1.100 之间。
2.9 质控品测定值质控品的测定结果应在质控范围内。
2.10 特异性试剂盒与表中有关潜在交叉反应物应无显著的交叉反应。
促甲状腺激素(TSH)测定试剂盒(化学发光免疫分析法)产品技术要求国赛

2.性能指标2.1试剂条性能指标2.1.1外观试剂盒应组分齐全,内外包装均应完整,标签清晰,液体试剂无渗漏。
试剂条中第7孔内组分为棕色含固体微粒的液体;其余皆为透明液体。
无悬浮物、无沉淀、无絮状物。
2.1.2装量溶液装量应不少于标示值。
其中试剂条第2孔为酶工作液孔,装量不少于80μL;第3、4、5孔为清洗液孔,装量均不少于380μL;第7孔为磁珠工作液孔,装量不少于45μL;第10孔为样本稀释液孔,装量不少于85μL;第12孔为底物孔,装量不少于130μL。
2.1.3空白限应不大于0.05mIU/L。
2.1.4准确性在试剂盒规定的测量范围内检测国家校准品,其实测值与理论值之比应在0.900-1.100之间。
2.1.5剂量-反应曲线的线性在0.1-100mIU/L区间内,其剂量-反应曲线线性相关系数(r)应不小于0.9900。
2.1.6精密度2.1.6.1分析内精密度变异系数(CV)应不大于8.0%。
2.1.6.2批间精密度变异系数(CV)应不大于15.0%。
2.1.7特异性浓度不低于200IU/L的FSH,在本试剂盒上的测定结果应不高于最低检出量水平0.05mIU/L。
浓度不低于200IU/L的LH,在本试剂盒上的测定结果应不高于最低检出量水平0.05mIU/L。
浓度不低于1000IU/L的hCG,在本试剂盒上的测定结果应不高于最低检出量水平0.05mIU/L。
2.2校准品性能指标2.2.1外观校准品CAL1、CAL2为冻干块。
加入纯水后在10min内溶解,无沉淀或絮状物。
2.2.2校准品准确性校准品CAL2,相对偏差应在±10%以内。
校准品CAL1为零浓度校准品除外。
2.2.3校准品均匀性校准品CAL2均匀性CV应≤10%。
校准品CAL1为零浓度校准品除外。
2.3质控品性能指标2.3.1外观质控品为冻干块。
加入纯水后在10min内溶解,无沉淀或絮状物。
2.3.2质控品准确性质控品测试结果应在靶值范围内。
促甲状腺素(TSH)测定试剂盒(化学发光免疫分析法)产品技术要求yuande

促甲状腺素(TSH)测定试剂盒(化学发光免疫分析法)适用范围:本产品用于体外定量测定人血清或血浆中的TSH的含量。
1.1 产品规格
试剂盒规格为48人份/盒、96人份/盒。
1.2主要组成成分
促甲状腺素(TSH)测定试剂盒(化学发光免疫分析法)主要组成成分
a) 酶结合物
以含牛血清白蛋白的缓冲液配制的连接HRP的TSH单克隆抗体,其中含
ProClin300做为防腐剂。
b) 校准品
校准品主要以小牛血清为稀释液,其中含ProClin300做为防腐剂,校准品A~F 中含TSH的目标浓度分别约为0、0.25 mIU/L、0.5 mIU/L、4.0 mIU/L、
10 mIU/L、50 mIU/L。
校准品具体浓度详见标签及试剂盒参数IC卡。
c) 发光液
发光液A主要成份为鲁米诺,发光液B主要成份为过氧化脲,两者均以pH8.6
的Tris-HCl缓冲液配制。
d) 包被微孔板
包被有TSH单克隆抗体白色聚苯乙烯微孔板,用铝箔袋真空包装。
e) 质控品(备选)
以正常人血清为基质制备的冻干品,其中含ProClin300做为防腐剂,其中值的靶值浓度范围QCⅠ为1.00 mIU/L~3.00 mIU/L,QCⅡ为5.00 mIU/L~8.50 mIU/L。
质控品具体浓度详见质控品参数表。
不同批号试剂盒中的相同组分不能互换。
促甲状腺素受体抗体测定试剂盒(化学发光免疫分析法)产品技术要求mairui

1 性能指标
2.1外观和性状
试剂盒各组分应齐全、完整、液体无渗漏;包装标签应清晰,准确、牢固;Ra 组分应为棕色含固体微粒的液体,无板结、无絮状物。
Rb、Rc 和Rd 组分应为清澈透明的液体,无沉淀、无悬浮物、无絮状物。
2.2装量
应不少于试剂瓶的标示装量值。
2.3准确度
对具有溯源性的两个浓度水平的正确度控制品进行检测,检测结果与标定浓度的相对偏差在±10%范围内。
2.4最低检测限
应不大于0.3 IU/L。
2.5线性
试剂盒在0.3 IU/L~40 IU/L 区间内,其相关系数(r)应不低于0.9900。
2.6重复性
变异系数CV 应≤ 5%。
2.7批间差
变异系数CV 应≤ 10%。
2.8稳定性
2~8℃避光保存,试剂盒有效期为365 天。
到有效期后90 天内的试剂盒应符合2.1、2.3、2.4、2.5、2.6 的要求。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
・论著・文章编号:1007-8738(2008)02-0192-02
促甲状腺素化学发光免疫定量检测试剂盒的研制
王 青1,王 缦23,魏东芝1,陈寒柏2,张黎明
2
(1华东理工大学生物化学与分子生物学系,上海200237;2上海科华生物工程股份有限公司,上海200233)收稿日期:2007-09-24; 接受日期:2007-10-26作者简介:王 青(1982-),女,河北保定人,硕士生
Tel:021*********;E 2mail:greenapp le_725@
3Corres ponding author,E 2mail:cshkh@online .sh .cn
[摘要] 目的:研制人血清中促甲状腺素(TS H )的化学发光
免疫检测试剂盒。
方法:采用辣根过氧化物酶标记的抗TSH β亚单位特异性单克隆抗体(mAb ),与固相包被的抗TSH α亚单位的另一mAb 配对,以鲁米诺作为底物,采用两步法建立了双位点夹心法人血清TSH 的化学发光免疫定量分析法。
结果:该方法灵敏度为010788m I U /L,批内CV 平均为
417%,批间CV 平均为814%,平均回收率为93105%。
该检
测与LH 、FSH 和HCG 无交叉反应。
部分实验样品的测试结果显示该试剂与国外同类试剂(雅培architect i2000)的测定结果明显相关(r =01984)。
结论:该方法具有较高的灵敏度、重复性和准确度,与其他同类产品相比简便、快捷、成本低,适于临床检测和科研应用。
[关键词]促甲状腺激素(TS H );化学发光免疫分析法;试剂盒[中图分类号]R392233 [文献标识码]B
促甲状腺激素(thyr oid sti m ulating hor mone,thyr otr op in,
TSH )是一种由垂体前叶分泌的糖蛋白激素,由α和β2个
亚基组成,相对分子质量(M r )为28000[1]。
TSH 本身受下丘脑分泌的TSH 释放激素T RH 的调控,TSH 的主要生理作用是调节甲状腺激素的合成与分泌,血液中甲状腺激素水平与腺垂体分泌TSH 的量之间有负反馈抑制关系
[2]。
甲状腺功能改
变时,TSH 的波动较甲状腺激素更迅速且明显,是反映下丘脑2垂体2甲状腺轴功能的敏感指标,因此采用灵敏度高的
TSH 免疫分析法具有重要的意义。
化学发光免疫分析(che m i 2lu m inescent i m munoassay,CL I A )是一种灵敏的免疫分析方法,
在免疫诊断试剂研制中已得到了广泛的应用
[3]。
本研究根据
化学发光免疫分析法的原理研制了血清TSH 的检测试剂盒,与国内外同类产品相比具有简便、快捷、成本低等优点。
1 材料和方法
1.1 材料 TSH 单克隆抗体(mAb )、TSH 标准品抗原和辣根
过氧化物酶(HRP )为Sig ma 公司产品,光免板为Ther mo Elec 2
tr on 公司产品,化学发光底物为B i oRad 公司产品。
1.2 方法
1.2.1 标准品的配制 将TS H 抗原标定后溶于小牛血清中,
配制成含011,1,5,20,100m I U /L 的标准溶液。
1.2.2 抗体包被板的制备 将100μL 含TS H mAb (015mg/L )
的pH916碳酸盐缓冲液加至包被板中,37℃包被2h,再用含
10mg/L BS A 的0101mol/L pH714磷酸盐缓冲液于37℃封闭2h 后晾干备用。
1.2.3 酶标记物的制备 TS H 的酶标记物采用过碘酸钠法
制备,然后经0101mol/L pH714磷酸盐缓冲液透析过夜后,加入等量的甘油于-20℃保存备用。
1.2.4 检测方法 将50μL 待测样品或标准品加入包被TSH
的光免板中,37℃温育30m in,弃反应液,用洗涤液(含015
mg/L T ween20的0101mol/L pH714磷酸盐缓冲液)洗5次,
加酶标记物50μL,37℃温育30m in 后同样用洗涤液洗5次,然后加入发光底物于5~10m in 内测定各孔的发光值RLU 。
样本中的TSH 浓度依据由标准品TSH 浓度和对应的RLU 建立的数学模型进行定量。
2 结果
2.1 动力学性质 在HRP 2鲁米诺2H 2O 2发光体系中,将不
同量的免疫复合物加入发光液中,发光强度(RLU )随反应时间而变化。
10m in 后RLU 接近峰值,在5~15m in 内RLU 较为稳定,随后开始缓慢下降。
2.2 反应条件优化
2.2.1 加样量对RLU 的影响 样本和酶标记物的加样量分
别为50μL 和100μL 考查标准品(0、011、1、5、20、100
m I U /L )RLU,发现加样量为100μL 与50μL RLU 相差不大,
说明50μL 的加样量反应能达到平衡(图1)。
图1 加样量对RLU 的影响
2.2.2 反应模式对RLU 的影响 采用二步法。
第一步:加
入标准品和待测样品后,将反应体系在37℃分别温育15、
30、45、60m in;第二步:加入酶标记抗体后,将反应体系在37℃分别温育15、30、45、60m in 。
结果表明温育时间为30m in 时反应皆能达到平衡(图2)。
图2 温育时间对RLU 的影响
A:第一步温育时间对RLU 的影响;B:第二步温育时间对RLU 的影响.
2.3 稳定性 将试剂盒放置于37℃6d 后,比较与放置前参
考标准品各点RLU 值,参考标准品各点RLU 值未见明显降低,且本底发光值无明显升高,表明试剂盒标准曲线无明显漂移,满足稳定性要求。
2.4 方法学评价
2.4.1 标准曲线与灵敏度 在设定的免疫反应和发光条件
下,以标准血清的浓度(0~100m I U /L )制作的标准曲线见图3。
同时测定20个零标准,用零标准均值加上2倍标准差,
计算出此方法的灵敏度为010788m I U /L 。
图3 TSH 标准曲线
2.4.2 精密度 取低(4144m I U /L )、中(19145m I U /L )和高(79123m I U /L )3种TSH 浓度各重复测定10次,测定批内CV
分别为612%、313%和416%,平均为417%。
隔日分别进行
5次独立试验,测批间CV 分别为813%、716%和913%,平
均为814%。
2.4.3 准确性 在已知TSH 浓度的血清中加入3种不同浓
度的标准血清,测定加入回收率为93105%。
将TS H 浓度为
44142m I U /L 的血清用标准零血清分别按1/2、1/4、1/8、1/16稀释,测量各稀释浓度的TSH 含量,测定稀释回收率为99186%。
2.4.4 特异性 在已知浓度的血清样品中加入不同浓度的LH 、FSH 和HCG 后,对TS H 的测定无干扰。
2.4.5 与进口试剂的比较 将研制的TSH C L I A 定量检测试
剂盒与Abbott architect i2000全自动化学发光系统共同对30例正常人、20例甲亢及80例甲低临床标本进行检测,
通过数据分析,得出两个检测系统所得数值具有明显相关性(图4)。
图4 与Abbott 全自动化学发光系统相关性曲线
3 讨论
血清促甲状腺素定量检测的方法主要有放射免疫法、酶联免疫法、时间分辨荧光免疫法和化学发光免疫法等几种
[4]。
考虑到目前化学发光和时间分辨
荧光分析仪器几乎全部为国外厂商生产,而绝大多数厂商采用仪器加试剂盒捆绑销售的垄断模式,并在仪器中人为设置排它性检测程序,从而抬高了配套试剂盒价格,增加了检测成本,所以本工作旨在开发国产低价、稳定、通用的人血TSH CL I A 试剂盒。
首先对读数时间进行了动力学研究,发现其在5~15m in 内RLU 处于平台期,反应时间选择10m in 。
其次
对反应条件进行了实验摸索,在不同的温育时间和加样量的条件下,各RLU 值相差不大,因此选择了50μL 的加样量与两步共1h 的反应时间。
我们研制的TSH 化学发光免疫测定试剂盒通过方法学鉴定表明无论是灵敏度、准确性、特异性等技
术指标均达到了临床诊断的要求[5]
;同时该方法具
有操作方便,反应时间短和成本低等优点,具有较广
阔的市场应用前景。
参考文献:
[1]Hay I D ,BayerMF,Kap lan MM ,et al .American thyr oid ass ociati on
assess ment of current free thyr oid hor mone and thyr otr op in measure 2ments and guidelines f or future clinical assays[J ].C lin Che m ,1991,37(11):2002-2008.
[2]尹东光,贺佑丰,刘一兵,等.促甲状腺激素化学发光免疫分析
的研究[J ].分析化学研究报告,2004,7(32):893-896.
[3]叶成果.促黄体生成素化学发光免疫定量检测试剂盒的研制[J ].
河南科技大学学报,2004,22(2):83-84.
[4]任均田.促甲状腺素实验检测进展[J ].国外医学・放射医学核
医学分册,2002,26(2):57-60.
[5]王永宁,李荣秀,李成武,等.微粒子化学发光免疫测定促甲状
腺素敏感性方法的建立和应用[J ].细胞与分子免疫学杂志,
2004,20(5):629-631.。
