氨基酸检测
17种氨基酸液相色谱法

17种氨基酸液相色谱法
液相色谱法是一种常用的分离和分析化学物质的技术。
在氨基
酸分析中,液相色谱法可以用于分离和检测氨基酸。
一般来说,液
相色谱法可以通过不同的色谱柱和检测方法来实现对氨基酸的分析。
针对17种氨基酸的液相色谱分析,首先需要准备样品,并进行
适当的前处理,如衍生化处理,以使得氨基酸能够更好地被分离和
检测。
接下来,选择合适的色谱柱和流动相,比如反相色谱柱和离
子交换色谱柱等,以实现氨基酸的分离。
此外,还需要选择合适的
检测方法,比如紫外检测器或荧光检测器等,来检测氨基酸的含量
和浓度。
在液相色谱分析过程中,需要严格控制实验条件,比如流速、
温度和pH 值等,以保证分离的准确性和重现性。
最后,通过比较
样品峰的保留时间和峰面积,可以定量分析出17种氨基酸的含量。
总的来说,液相色谱法对于17种氨基酸的分析需要精确的实验
操作和严格的条件控制,但可以实现对这些氨基酸的准确分离和定
量分析。
氨基酸检测标准方法

氨基酸检测标准方法
氨基酸检测标准方法有多种,包括分光光度法、毛细管电泳法、近红外光谱法、气相色谱法、高效液相色谱法等。
分光光度法主要利用氨基酸与衍生剂发生化学反应,产生蓝紫色化合物,该化合物在某一波长处有最大吸收峰,根据吸收值大小得到氨基酸含量。
毛细管电泳法根据分离原理的不同,可分为毛细管区带电泳、毛细管凝胶电泳、毛细管等电电泳、毛细管等速电泳以及胶束电动力学毛细管电泳。
近红外光谱法利用有机化合物的含氢基团在特定波长区域跃迁,产生光谱的变化,结合统计学方法间接地实现氨基酸的定量检测。
气相色谱法将氨基酸衍生化处理变为容易气化的物质,根据气态样品中各组分在流动相和固定相中的分配系数的不同,实现对氨基酸的定量分析。
高效液相色谱法是最常用的一种氨基酸检测方法。
由于大多数氨基酸本身没有紫外吸收和荧光反应,因此需要对样品进行衍生化处理将其转化为有紫外吸收和发射荧光的物质,衍生可分为柱前衍生和柱后衍生。
此外,还有氨基酸分析仪法,该方法是一种将色谱技术、电化学检测技术和计算机技术等有机结合在一起的氨基酸分析仪。
其原理是氨基酸与酸碱指示剂反应后,再利用光电转换器将透光度变化
为电信号,然后经过放大器输入到微处理机中,最后得到氨基酸含量。
该方法操作简便,快速准确,可以同时测定20种氨基酸。
总的来说,氨基酸检测标准方法有多种,具体选择哪种方法要根据实验要求和目标来决定。
氨基酸含量测定和标准曲线制作(茚三酮法)

茚三酮比色法测定游离氨基酸含量原理:茚三酮与氨基酸的反应分两步进行,首先是氨基酸被氧化,产生二氧化碳、氨和醛,而水合茚三酮被还原成还原性茚三酮;第二步是所生成的还原性茚三酮与另一个水合茚三酮分子和氨缩合生成成为蓝紫色化合物,该化合物颜色的深浅与氨基酸的含量成正比。磷酸缓冲液(pH.8.04):称磷酸二氢钾4.5350 g,定容500 ml。
称NAH2PO4·12H2O11.9380 g分别溶解定容500 ml。
取磷酸二氢钾10 ml与磷酸氢二钠190ml混合即为pH8.04的缓冲液2%茚三酮溶液:称取水合茚三酮 2 g,加水溶解后定容至 100 mL。
储成于棕色瓶中,避光保存。
0.25%抗坏血酸溶液:称取抗坏血酸 0.1 g,加水溶解后定容至 100 mL,现配现用,或者密封,冻存于-20 o C。
茚三酮反应液:取50 ml 2% 茚三酮,加入5 ml 0.25%的Vc,使用蒸馏水稀释到100 ml,密封储存在棕色瓶中。
亮氨酸标准液:称取 100 mg 亮氨酸(纯度不低于 99%)溶于 100 mL 水中,作为母液,此时亮氨酸的浓度为1 mg/mL。
茚三酮标准曲线制作溶液中氨基酸的浓度如果低于20 μg/ml,茚三酮显色反应将不能发生,故先配制不同浓度的氨基酸标准液,取十支试管,标号为1,2,3……10,按照下表配制1 2 3 4 5 6 7 8 9 10 11 120.4 0.5 0.6 0.7 0.8 0.9 1 1.1 1.2 1.3 1.4 1.5 1000 μg/ml亮氨酸超纯水 ml 9.6 9.5 9.4 9.3 9.2 9.1 9 8.9 8.8 8.7 8.6 8.5 亮氨酸 终浓度μg/ml 405060708090100110120130140150使用螺旋盖(内垫)试管分别取上述浓度的氨基酸标准液1ml,空白对照使用1ml 超纯水替代氨基酸标准液,然后向各个试管中加入0.5 ml 的茚三酮反应液和0.5 ml 的磷酸缓冲液,盖好盖子悬紧,置于沸水浴中煮沸15 min,分别加入3 ml 的超纯水,斡旋混匀,测定吸光度,绘制标准曲线取一支中等程度显色的试管进行紫外和可见波段的全波长扫描,结果如下图所示3004005006007008000.00.10.20.30.40.50.60.7吸光度波长(nm )403 nm565 nm选择565 nm 作为其最大吸收波长,测定各管的吸光度,弃去吸光度大于1的值 茚三酮终浓度(μg/mL) 565 nm 的吸光度 20 0.037 25 0.114 30 0.226 35 0.347 40 0.412 45 0.538 500.62155 0.692 60 0.754 65 0.834 700.968使用origin 8.5 绘制散点图并进行线性拟合,结果如下图所示0.00.20.40.60.81.0O D 565氨基酸浓度(μg/mL )注意事项:1. 茚三酮比色受测定环境中的pH 影响很大,故每次测定前需要将样品溶液的pH 值调整到中性(pH7左右),2. 茚三酮不光可以与氨基酸反应,与蛋白质同样可以反应,因此需要在测定前去除溶液中的蛋白质,因此正确做法是:向样品溶液中加入等体积等0.6 mol/L 三氯乙酸,斡旋震荡,静置10 min 后,3000 rpm 离心10 min,取上清调整pH 值至中性pH7左右,再进行测定,3. 稀释倍数的确定:因为标准曲线的测定范围为20-70 μg/mL,即20-70 mg/L,所以在不清楚你所要检测样品中氨基酸的浓度时,最好取部分样品稀释10倍和100倍,分别检测原液、十倍稀释液和100倍稀释液的OD565,发现哪个水平下OD565落在标准曲线的范围内,从而判断需要对样品稀释多少倍4. 标准曲线测定时最好选择密封性较好的试管(螺旋盖硅胶内垫),同时需要检查气密性,防止水浴蒸发导致计量误差或者使用10 mL 具塞比色管,以方便在水浴之后可以准确补水。
氨基酸测定方法
4。
1 光度分析法[5] [6]β-氨基丙酸和茚三酮溶液在弱酸的条件下可以生成蓝紫色物质[7],其颜色深浅主要与β-氨基丙酸的浓度有关。
因此可利用此显色反应采用比色法定量测量β—氨基丙酸。
我在实验中发现很多因素如浓度、pH 值、反应温度、以及反应时间等对此显色反应有很大的影响.如忽视这些因素会使实验产生很大的误差.就此显色反应的最佳条件我做了初步的探究.4.1。
1试剂的配制:缓冲液的配制:配制pH= 6。
00的NaAc -HAc 缓冲溶液β—氨基丙酸标准溶液的配制:用电子天平准确称取1。
020 g β-氨基丙酸(生化纯),溶于250ml pH=6.00缓冲溶液中,得到C = 4.080 g/L 标准溶液.茚三酮试剂的配制:称取0.5g 茚三酮溶于100ml 蒸馏水中,得到5g/L 的茚三酮水溶液。
4.1。
2标准曲线的确定分别准确移取0.30ml 、0。
40ml 、0。
50ml 、0.60ml 、0.70ml 、0。
80ml 、0.90ml 、1。
00ml 标准液于8个比色管中,用pH=6.00的缓冲溶液稀释到5.00ml 再加入1ml 茚三酮水溶液充分摇匀,将其放在沸水浴中加热10min 。
冷却到室温,用7230型分光光度计在569nm 下测其吸光度.以吸光度和浓度作一个标准曲线。
4。
1。
3样品的测定稀释待测液于0.24mg/ml-0.73mg/ml,调pH 值到6.00,以相同的反应条件,测其吸光值并与上面的标准曲线对照查出稀释液的浓度,再乘以稀释倍数即为β-氨基丙酸的浓度。
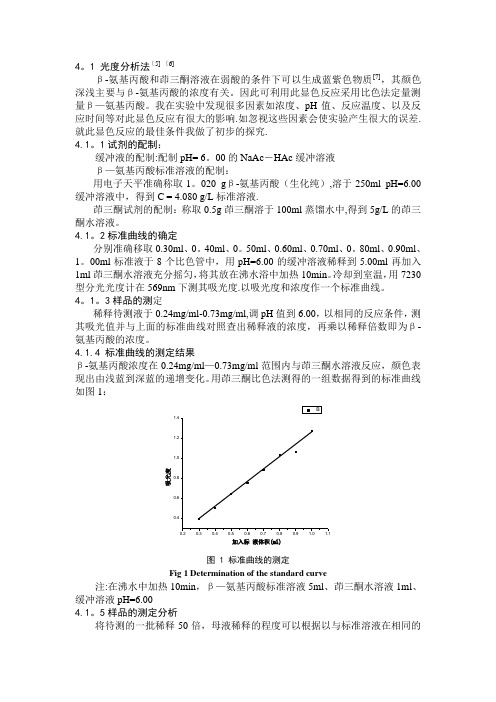
4.1.4 标准曲线的测定结果β-氨基丙酸浓度在0.24mg/ml —0.73mg/ml 范围内与茚三酮水溶液反应,颜色表现出由浅蓝到深蓝的递增变化。
用茚三酮比色法测得的一组数据得到的标准曲线如图1:吸光度加入标液体积(ml)图 1 标准曲线的测定Fig 1 Determination of the standard curve注:在沸水中加热10min ,β—氨基丙酸标准溶液5ml 、茚三酮水溶液1ml 、缓冲溶液pH=6.004.1。
氨基酸检测报告

氨基酸检测报告
委托单位:XXX医疗检测有限公司
受检单位:XXX先生
检测场所:XXX实验室
检测日期:20XX年X月X日
检测项目:氨基酸检测
检测结果:
按照标准检测方法,对受检单位的氨基酸进行检测,结果如下:氨基酸测试值参考值
苏氨酸X.XX μmol/L X.XX-XX.XX μmol/L
精氨酸X.XX μmol/L X.XX-XX.XX μmol/L
缬氨酸X.XX μmol/L X.XX-XX.XX μmol/L
谷氨酰胺X.XX μmol/L X.XX-XX.XX μmol/L
…… …… ……
分析与评价:
受检单位的氨基酸测试结果表明,其中苏氨酸、精氨酸、缬氨酸、谷氨酰胺等氨基酸指标均在正常范围之内,未发现异常情况。
检测完成后,报告交付给受检单位,由受检单位妥善保管。
本报告仅对本次氨基酸检测结果进行说明和评价,不涉及其他
医学问题。
如有疑问,请咨询医疗专业人员。
检测人员:XXX
报告编制人:XXX
报告审核人:XXX
报告编号:XXX
总体成果:
氨基酸检测结果正常,符合医学标准要求,本检测报告有效期为一年。
注:本报告不得作为法律依据。
食品中氨基酸总量的测定实验报告

食品中氨基酸总量的测定实验报告一、实验目的本实验旨在测定食品中氨基酸的总量,了解食品中蛋白质的组成和营养价值,为食品质量控制和营养评估提供依据。
二、实验原理氨基酸是含有氨基和羧基的有机化合物,它们在一定条件下与某些试剂反应可以产生特定的颜色或荧光,通过比色或荧光检测可以定量测定氨基酸的含量。
本实验采用茚三酮显色法测定食品中氨基酸的总量。
茚三酮在弱酸性溶液中与氨基酸反应,生成蓝紫色化合物,其颜色的深浅与氨基酸的含量成正比。
在一定波长下测定溶液的吸光度,通过与标准曲线对比,可以计算出样品中氨基酸的总量。
三、实验材料与设备1、实验材料标准氨基酸溶液(已知浓度)待测食品样品(如肉类、豆类、谷物等)茚三酮试剂缓冲溶液(pH 值 50)乙醇蒸馏水2、实验设备分光光度计分析天平容量瓶(100 mL、50 mL、25 mL 等)移液管(1 mL、2 mL、5 mL 等)具塞刻度试管(25 mL)水浴锅离心机四、实验步骤1、标准曲线的绘制分别吸取 000 mL、020 mL、040 mL、060 mL、080 mL、100 mL 标准氨基酸溶液于 25 mL 具塞刻度试管中,用蒸馏水补足至 100 mL。
向各试管中加入 100 mL 缓冲溶液(pH 值 50)和 100 mL 茚三酮试剂,摇匀。
将试管置于沸水浴中加热 15 min,取出后立即用冷水冷却至室温。
向各试管中加入 500 mL 60%乙醇,摇匀。
使用分光光度计,在 570 nm 波长下,以蒸馏水为空白,测定各溶液的吸光度。
以氨基酸的含量(μg)为横坐标,吸光度为纵坐标,绘制标准曲线。
2、样品处理称取适量待测食品样品,精确至 0001 g,放入研钵中研碎。
将研碎的样品转移至离心管中,加入适量蒸馏水,在沸水浴中加热30 min,以提取氨基酸。
冷却后,离心(3000 rpm,10 min),取上清液备用。
3、样品测定吸取 100 mL 样品上清液于 25 mL 具塞刻度试管中,按照标准曲线绘制的步骤进行操作,测定样品溶液的吸光度。
测定氨基酸的方法以及试剂
一采用氨基酸自动分析仪测定氨基酸1.氨基酸测定原理:食物蛋白质经盐酸水解成为游离氨基酸,经氨基酸分析仪的离子交换柱分离后,与茚三酮溶液产生颜色反应,再通过分光光度计比色测定氨基酸含量。
2.测定氨基酸所用仪器:真空泵;恒温干燥箱;水解管:耐压螺盖玻璃管或硬质玻璃管,体积20~30mL。
用去离子水冲洗干净并烘干;真空干燥器(温度可调节);氨基酸自动分析仪。
3.测定氨基酸所用试剂及其配制方法:3.1试剂:全部试剂除注明外均为分析纯,实验用水为去离子水。
浓盐酸(优级纯);苯酚(须重蒸馏); 混合氨基酸标准液(仪器制造公司出售):0.00250mol/L; 不同pH值柠檬酸钠缓冲液;氢氧化锂(LiOH·H2O);冰乙酸(优级纯);二甲基亚砜(C2H6OS);水合茚三酮(C9H4O3·H2O);还原茚三酮(C18H10O6·2H2O);NaOH;高纯氮气(纯度99.99%);冷冻剂:市售食盐与冰按1∶3混合。
3.2试剂配制方法:3.2.1. 6mol/L盐酸∶浓盐酸(3.1)与水1∶1混合而成。
3.2.2. pH2.2的柠檬酸钠缓冲液:称取19.6g柠檬酸钠(Na3C6H5O7·2H2O)和16.5mL浓盐酸加水稀释到1000mL,用浓盐酸或50%的氢氧化钠溶液调节pH至2.2。
pH3.3的柠檬酸钠缓冲液:称取19.6g柠檬酸钠和12mL浓盐酸加水稀释到1000mL,用浓盐酸或50%的氢氧化钠溶液调节pH至3.3。
pH4.0的柠檬酸钠缓冲液:称取19.6g柠檬酸钠和9mL浓盐酸加水稀释到1000mL,用浓盐酸或50%的氢氧化钠溶液调节pH至4.0。
pH6.4的柠檬酸钠缓冲液:称取19.6g柠檬酸钠和46.8g氯化钠(优级纯)加水稀释到1000mL,用浓盐酸或50%的氢氧化钠溶液调节pH至6.4。
3.2.3. 茚三酮溶液pH5.2的乙酸锂溶液:称取氢氧化锂(LiOH·H2O)168g,加入冰乙酸(优级纯)279mL,加水稀释到1000mL,用浓盐酸或50%的氢氧化钠溶液调节pH至5.2。
氨基酸的定量测定
6、三硝基苯磺酸法
原理: 三硝基苯磺酸(TNBS)是定量测定氨基酸的重要试剂之一。 TNBS 在偏碱性的条件下与氨基酸反应,先形成中间络合物。 中间络合物在光谱上有2个吸收值相近的高峰,分别位于355nm 和420nm 附近。然而溶液一旦酸化,中间络合物转化成三硝基苯 -氨 基酸(TNP-氨基酸),420nm 处的吸收值显著下降,而350nm 附近 的吸收峰则移至340nm 处。 利用 TNBS 与氨基酸反应的这一特性,可在420nm 处(偏碱性 溶液中)或在340nm(偏酸性溶液中)对氨基酸进行定量测定。在 340nm 处,各氨基酸的吸收度大致相近,而在420nm 处的吸光度因 2 氨基酸种类而异;在加入适量 SO3 时,吸收值升高。 本法允许的测定范围是 0.05~0.4μmol 氨基酸。
1、甲醛滴定法
计算结果:
氨基酸态氮含量=
(V2 V1 ) c 0.014 100 % m
式中:c——氢氧化钠标准溶液的浓度,mol/L V1——用中性红作指示剂滴定时消耗氢氧化钠标准溶液体积,mL V2——用百里酚酞作指示剂滴定时消耗氢氧化钠标准溶液体积, mL m——测定用样品溶液相当于样品的质量,g 1 0.014—— N2毫摩尔质量,g/mmol
100%
式中:VHClO ——所消耗的高氯酸标准溶液的体积 cHClO ——所消耗的高氯酸标准溶液的浓度 M——被测氨基酸的摩尔质量 m——被测氨基酸的质量
4
4、非水溶液滴定法
②回滴法(适用于不易溶解于冰醋酸而能溶解于高氯酸的氨基酸):精确称取氨 基酸样品30~40mg 左右,溶解于5mL高氯酸标准溶液中,加2滴甲基紫指示剂,剩 余的酸以醋酸钠溶液滴定,颜色变化由黄,经过绿、蓝至初次出现不褪的紫色为 终点。 氨基酸含量=
检测氨基酸的色谱柱
检测氨基酸的色谱柱
在色谱法中,可以使用各种类型的色谱柱来检测氨基酸。
以下是一些常用的色谱柱:
1.硅胶色谱柱:硅胶是一种无机化合物,具有高纯度、高活性和高比表面积等优点。
它是一种常用的色谱柱材料,可用于分离氨基酸和其他有机化合物。
2.氨基色谱柱:氨基色谱柱是一种特殊的色谱柱,可以用于分离氨基酸和蛋白质。
它的主要特点是具有极性基团,能够与氨基酸的极性基团相互作用,从而实现分离。
3.凝胶色谱柱:凝胶色谱柱是一种用于分离大分子物质的色谱柱。
它的主要特点是能够通过分子筛效应将大分子物质分离出来,对于氨基酸的分离效果也很好。
4.C18色谱柱:C18是一种特殊的烷基键合相,具有亲脂性和疏水性,可以用于分离极性和非极性化合物。
在氨基酸分离中,C18色谱柱可以用于分离具有不同疏水性的氨基酸。
需要注意的是,不同的色谱柱材料和固定相配方会影响氨基酸的分离效果和峰形。
因此,在选择色谱柱时,需要根据实验目的、样品性质和分离要求等因素进行综合考虑。
氨基酸常用的检测方法和原理
氨基酸常用的检测方法和原理氨基酸是构成蛋白质的基本组成单元,对于研究蛋白质结构和功能具有重要意义。
因此,准确、快速地检测氨基酸的方法和原理是科学研究和实际应用中的关键问题之一。
本文将介绍几种常用的氨基酸检测方法及其原理。
一、纸层析法纸层析法是一种简单、快速的氨基酸检测方法。
其原理是根据氨基酸在纸上的迁移速度差异来分离和检测氨基酸。
首先,将待测样品与色谱溶剂混合,然后将混合液滴在纸上,待溶剂上升至一定高度后,根据不同氨基酸的迁移距离和颜色变化,可以判断样品中是否含有特定的氨基酸。
二、高效液相色谱法(HPLC)高效液相色谱法是一种精确、灵敏的氨基酸检测方法。
其原理是利用氨基酸在液相中的分配系数差异来实现分离和检测。
首先,将待测样品通过色谱柱进行分离,然后通过检测器检测样品中各种氨基酸的浓度。
由于不同氨基酸的分配系数不同,它们在色谱柱中的停留时间也不同,从而实现了氨基酸的分离和检测。
三、毛细管电泳法毛细管电泳法是一种高效、快速的氨基酸检测方法。
其原理是利用氨基酸在电场作用下在毛细管中的迁移速度差异来实现分离和检测。
首先,将待测样品注入毛细管中,然后施加电场,通过检测器检测样品中各种氨基酸的浓度。
由于不同氨基酸的电荷性质和大小不同,它们在电场作用下的迁移速度也不同,从而实现了氨基酸的分离和检测。
四、质谱法质谱法是一种高精确度、高灵敏度的氨基酸检测方法。
其原理是利用氨基酸分子在质谱仪中的质量-电荷比差异来实现分离和检测。
首先,将待测样品通过质谱仪进行分离,然后通过检测器检测样品中各种氨基酸的质量-电荷比。
由于不同氨基酸的分子量不同,它们在质谱仪中的质量-电荷比也不同,从而实现了氨基酸的分离和检测。
纸层析法、高效液相色谱法、毛细管电泳法和质谱法是常用的氨基酸检测方法。
每种方法都有其独特的原理和优势,可以根据实际需要选择合适的方法进行氨基酸的检测。
这些方法的应用不仅在科学研究中具有重要意义,也在食品、医药等领域有着广泛的应用前景。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氨基酸检测
氨基酸是构成蛋白质的基本单位,在食品、医药、
饲料添加剂、化妆品及工农业等诸多方面有着广泛
的应用。
随着生物工程技术产业的发展逐渐成为21
世纪全球的主要产业之一,氨基酸的需求量越来越
大,品种变更越来越快,工艺改革越来越新。
科标检测中心在氨基酸检测方面具有资深经验,为
广大客户提供专业、全面的检测服务,并出具权威的检测报告。
1、脂肪族氨基酸:丙、缬、亮、异亮、蛋、天冬、谷、赖、精、甘、丝、苏、半胱、天冬酰胺、谷氨酰胺
2、芳香族氨基酸:苯丙氨酸、酪氨酸
3、杂环族氨基酸:组氨酸、色氨酸
4、杂环亚氨基酸:脯氨酸
检测对象
豆类谷物、药材、鱼类、肉类、饲料、食用菌类、保健品、化妆品等等。
检测项目
甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、苯丙氨酸、脯氨酸、丝氨酸、酪氨酸、蛋氨酸、苏氨酸、天冬氨酸、谷氨酸、赖氨酸、精氨酸和组氨酸、胱氨酸、色氨酸、谷氨酰胺、天冬酰胺。
相关标准
标准代号标准名称
GB/T14924.10-2008实验动物配合饲料氨基酸的测定
GB/T15399-1994饲料中含硫氨基酸测定方法--离子交换色谱法
GB/T15400-1994饲料中色氨酸测定方法--分光光度法
GB/T17419-1998含氨基酸叶面肥料
GB/T18246-2000饲料中氨基酸的测定
科标检测致力于推动检测行业的规范化、科学化发展,秉承“敢为人先、开拓创新、同心协力、勇承重载”
GB/T18654.11-2008
养殖鱼类种质检验第11部分:肌肉中主要氨基酸含量的测定
GB/T23296.12-2009
食品接触材料高分子材料食品模拟物中11-氨基十一酸的测定高效液相色谱法
GB/T28722-2012氨基酸中铁和铅的测定原子吸收光谱法GB/T5009.124-2003食品中氨基酸的测定
GB/T8314-2013茶游离氨基酸总量的测定
NY1429-2010含氨基酸水溶肥料
NY/T1618-2008鹿茸中氨基酸的测定氨基酸自动分析仪法NY39-1987饲料级L-赖氨酸盐酸盐
NY/T56-1987谷物籽粒氨基酸测定的前处理方法
QB/T2409-1998化妆品中氨基酸含量的测定
QB/T4356-2012黄酒中游离氨基酸的测定高效液相色谱法
SN/T0930-2000
进出口花粉中全氨基酸的测定方法氨基酸自动分析仪法
YC/T282-2009烟叶游离氨基酸的测定氨基酸分析仪法
YC/T448-2012
烟草及烟草制品游离氨基酸测定离子色谱-积分脉冲安培法
科标检测致力于推动检测行业的规范化、科学化发展,秉承“敢为人先、开拓创新、同心协力、勇承重载”。
