大学物理热学复习提纲
大学热学期末总复习资料.ppt
A
V2 pdV
V1
p(V2 V1)
Q
v
T2 T1
C
p,mdT
U
v
T2 T1
CV
,m
dT
Cp,m 绝热指数
CV ,m
3、等温过程
方程:T C(常量) 或:pV C(常量)
U 0
Q A vRT ln V2 V1
4、绝热过程
方程:
pV 常数 TV 1 常数
p 1 T
常数
Q0
• 理想气体温标:
注:在1000℃> T > 1K的范围适用。
T lim T ( p) 273.16K lim p (定容)
或:
ptr 0
p ptr 0 tr
T limT (V) 273.16K lim V (定压)
p0
V p0 tr
• 热力学温标T:不依赖测温物质及其测温属性。
单位:K (Kelvin),规定: T0=273.16K 在理想气体温标有效范围内二者一致。
3
3
代 入
1 3
v
cV
1 3
4km T 1 2
4km T 1 2
cV
n p kT
D 1 v 1 4k 3 T 3 2
3
3 m p
结论:1、T一定时,、 与p或n无关,D与p或n成反比。 2、p一定时,、、D 都随T的升高而加大;、 与
T1 2成正比,D与 T3 2 成正比。
四、低压下的热传导和粘滞现象
分子平动自由度 t ,转动自由度 r,振动自由度 s,平均总能 量:
(t r 2s) 1 kT
2
单原子分子 3 kT
2
刚性双原子分子 5 kT
热学 提纲
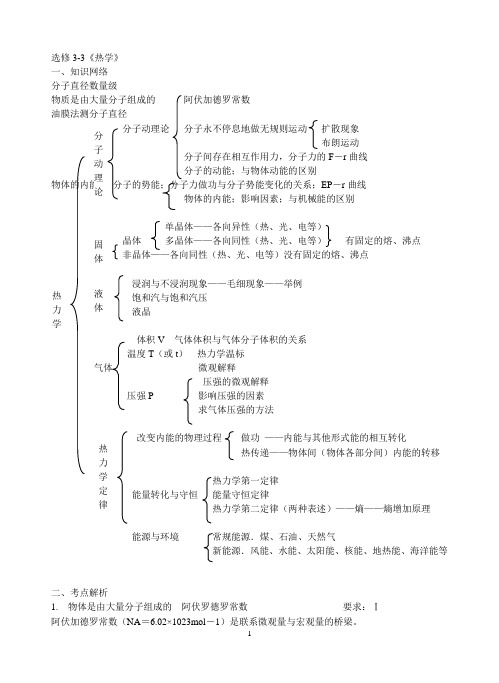
选修3-3《热学》一、知识网络分子直径数量级物质是由大量分子组成的 阿伏加德罗常数 油膜法测分子直径分子动理论 分子永不停息地做无规则运动 扩散现象 布朗运动 分子间存在相互作用力,分子力的F -r 曲线 分子的动能;与物体动能的区别 物体的内能 分子的势能;分子力做功与分子势能变化的关系;EP -r 曲线 物体的内能;影响因素;与机械能的区别单晶体——各向异性(热、光、电等)晶体 多晶体——各向同性(热、光、电等) 有固定的熔、沸点 非晶体——各向同性(热、光、电等)没有固定的熔、沸点浸润与不浸润现象——毛细现象——举例饱和汽与饱和汽压液晶 体积V 气体体积与气体分子体积的关系温度T (或t ) 热力学温标气体 微观解释压强的微观解释压强P 影响压强的因素求气体压强的方法改变内能的物理过程 做功 ——内能与其他形式能的相互转化热传递——物体间(物体各部分间)内能的转移热力学第一定律能量转化与守恒 能量守恒定律热力学第二定律(两种表述)——熵——熵增加原理能源与环境 常规能源.煤、石油、天然气新能源.风能、水能、太阳能、核能、地热能、海洋能等二、考点解析1. 物体是由大量分子组成的 阿伏罗德罗常数 要求:Ⅰ阿伏加德罗常数(NA =6.02×1023mol -1)是联系微观量与宏观量的桥梁。
分 子 动 理 论 热力 学固体 热力学定律 液体注意两个要求:①两个量中必须一个为宏观量,另一个为微观量②宏观量与微观量必须是同一物理量,如同为质量、同为体积(直径)等设分子体积V0、分子直径d 、分子质量m ;宏观量为.物质体积V 、摩尔体积V1、物质质量M 、摩尔质量μ、物质密度ρ。
(1)分子质量:A A ==N V N m ρμ(2)分子体积:A A 10PN N V V μ==(对气体,V0应为气体分子占据的空间大小)(3)分子直径:○1球体模型.V d N =)2(343A π303A 6=6=ππV N V d (固体、液体一般用此模型)○2立方体模型.30=V d (气体一般用此模型) (对气体,d 应理解为相邻分子间的平均距离)(4)分子的数量:A 1A 1A A ====N V V N V M N V N Mn ρμρμ固体、液体分子可估算分子质量、大小(认为分子一个挨一个紧密排列);气体分子不可估算大小,只能估算气体分子所占空间、分子质量。
大学物理热学复习提纲

期 末 复 习理想气体状态方程一、 理想气体:温度不太低,压强不太高的实际气体可视为理想气体。
宏观上,在任何情况下都符合玻-马、盖-吕、查理三定律的气体。
二、 三个实验定律:(1)玻—玛定律: pV = 常数 或 T = 常数(2)盖.吕萨克定律:VT = 常数 或 p = 常数 (3)查理定律: TP = 常数 或 V = 常数 三、 理想气体状态参量:体积(V ),压强(p ),温度(T ) ;内能(E ),焓(H ),熵(S ),摩尔数(ν )四、 理想气体分子模型:①全同质点;②弹性碰撞;③除碰撞瞬间外无相互作用,忽略重力五、普遍适用112212T T = :状态变化中质量不变阿佛伽德罗定律: p nkT = 六、 道尔顿分压定律:● 混合气体的压强等于组成混合气体的各成分的分压强之和● (几种温度相同的气体混于同一容器中,各气体的平均平动动能相等)● 12112212222()333t t t p n n n n p p =++=++=++εεε七、 关于p nkT =:1. 是状态方程的微观式,大学物理中常用此式2. 式中N N n V V ==d d :气体的分子数密度,即单位体积内的分子数3. R = 8.31 J/(mol ·K) :普适气体常数4.231238.31 1.3810J K 6.0210A R k N --===⨯⋅⨯:玻耳兹曼常量八、 关于压强p :● Γ:单位时间内碰在单位面积器壁上的平均分子数(气体分子碰壁数)●压强p :单位时间内气体(全部分子)① 压强的定义体现了统计平均。
② V x >0的分子占总分子的一半,或分子速度在某方向的分量平均值为0 ● (例如:在x 方向,有0x v =;在y 方向,有0y v =;在z 方向,有0z v =)这是机会均等的表现。
③ 2213x v v = 也是机会均等的表现。
④ 22i ixx i n v v n =∑∑是统计平均的表现。
大学物理1期末复习纲要

大学物理I 复习纲要本期考试比例:力学:28分;热学:25分;振波:22分;光学:25分。
大学物理I 包括:力学(运动学、牛顿力学、刚体的定轴转动);热学(气体动理论、热力学第一定律);振动波动(机械振动、机械波);光学(光的干涉、衍射和偏振)。
根据大纲对各知识点的要求以及总结历年考试的经验,现列出期末复习的纲要如下: 1. 计算题可能覆盖范围a. 刚体碰撞及转动定律;b. 热力学第一定律;c. 机械振动与机械波波动方程;d. 单缝衍射及光栅衍射 2. 大学物理I 重要规律与知识点(一)力学 质点运动学(速度、加速度、位移、路程概念分析、圆周运动);质点的相对运动,伽利略变换;质点运动的机械能与角动量;牛顿第二定律;质点动量定理;变力做功;刚体定轴转动定理;刚体定轴转动角动量定理及角动量守恒定律;刚体力矩(二)热学 理想气体的状态方程;理想气体的温度、压强、内能;能均分定理;麦克斯韦速率分布函数的统计意义和三种统计速率;热力学第一定律在理想气体等值过程中的应用;循环过程及效率、绝热过程。
(三)振动、波动 旋转矢量法的应用;同方向同频率简谐振动的合成;波速、周期(频率)与波长的关系(uT =λ);波程、波程差以及相位差;相干波及驻波;振动曲线和波动曲线,振动方程与波动方程的求解;波的能量。
(四)光学 光程差与相位差;杨氏双缝干涉;干涉与光程;半波损失;劈尖薄膜干涉、增透,增反;单缝衍射,光栅衍射;马吕斯定律。
1. 计算题21.(本题10分)一根放在水平光滑桌面上的匀质棒,可绕通过其一端的竖直固定光滑轴O 转动.棒的质量为m = 1.5 kg ,长度为l = 1.0 m ,对轴的转动惯量为J = 231ml .初始时棒静止.今有一水平运动的子弹垂直地射入棒的另一端,并留在棒中,如图所示.子m , lOvm '弹的质量为m '= 0.020 kg ,速率为v = 400 m ·s -1.试问: (1) 棒开始和子弹一起转动时角速度ω有多大?(2) 若棒转动时受到大小为M r = 4.0 N ·m 的恒定阻力矩作用,棒能转过多大的角度θ? 21. (本题10分) 解:(1) 角动量守恒:ω⎪⎭⎫⎝⎛'+='2231l m ml l m v 2分∴ l m m m ⎪⎭⎫ ⎝⎛'+'=31v ω=15.4 rad ·s -1 2分(2) -M r =(231ml +2l m ')β2分0-ω 2=2βθ2分∴ rM l m m 23122ωθ⎪⎭⎫ ⎝⎛'+==15.4 rad 2分22.(本题10分)一定量的单原子分子理想气体,从A 态出发经等压过程膨胀到B 态,又经绝热过程膨胀到C 态,如图所示.试求这全过程中气体对外所作的功,内能的增量以及吸收的热量. 22. (本题10分)解:由图可看出 p A V A = p C V C从状态方程 pV =νRT T A =T C ,因此全过程A →B →C∆E =0.3分B →C 过程是绝热过程,有Q BC = 0. A →B 过程是等压过程,有 )(25)( A A B B A B p AB V p V p T T C Q -=-=ν=14.9×105 J . 故全过程A →B →C 的 Q = Q BC +Q AB =14.9×105 J . 4分A BCV (m 3)p (Pa) 2 3.4981×1054×105O根据热一律Q =W +∆E ,得全过程A →B →C 的W = Q -∆E =14.9×105 J . 3分24.(本题10分)(3530)一衍射光栅,每厘米200条透光缝,每条透光缝宽为a=2×10-3 cm ,在光栅后放一焦距f=1 m 的凸透镜,现以λ=600 nm (1 nm =10-9 m)的单色平行光垂直照射光栅,求: (1) 透光缝a 的单缝衍射中央明条纹宽度为多少?(2) 在该宽度内,有几个光栅衍射主极大(亮纹)?24.解:(1) a sin ϕ = k λ tg ϕ = x / f 2分当x << f 时,ϕϕϕ≈≈sin tg , a x / f = k λ , 取k = 1有x = f l / a = 0.03 m 1分 ∴中央明纹宽度为 ∆x = 2x = 0.06 m 1分(2)( a + b ) sin ϕλk '=2分='k ( a +b ) x / (f λ)= 2.5 2分取k '= 2,有k '= 0,±1,±2 共5个主极大2分22.(本题10分)气缸内贮有36 g 水蒸汽(视为刚性分子理想气体),经abcda 循环过程如图所示.其中a -b 、c -d 为等体过程,b -c 为等温过程,d -a 为等压过程.试求:(1) d -a 过程中水蒸气作的功W da (2) a -b 过程中水蒸气内能的增量∆E ab (3) 循环过程水蒸汽作的净功W(4) 循环效率η(注:循环效率η=W /Q 1,W 为循环过程水蒸汽对外作的净功,Q 1为循环过程水蒸汽吸收的热量,1 atm=1.013×105 Pa) 22. (本题10分)解:水蒸汽的质量M =36×10-3 kg 水蒸汽的摩尔质量M mol =18×10-3 kg ,i = 6(1) W da = p a (V a -V d )=-5.065×103 J (2)ΔE ab =(M /M mol )(i /2)R (T b -T a )=(i /2)V a (p b - p a )=3.039×104 J(3) 914)/(==RM M V p T mol ab b KW bc = (M /M mol )RT b ln(V c /V b ) =1.05×104 J净功 W =W bc +W da =5.47×103 J(4) Q 1=Q ab +Q bc =ΔE ab +W bc =4.09×104 Jp (atm )V (L)Oabcd25 5026η=W / Q 1=13%23.(本题10分)图示一平面简谐波在t = 0 时刻的波形图,求 (1) 该波的波动表达式; (2) P 处质点的振动方程. 23. (本题10分)解:(1) O 处质点,t = 0 时0c o s 0==φA y , 0sin 0>-=φωA v 所以 π-=21φ 2分又 ==u T /λ (0.40/ 0.08) s= 5 s 2分故波动表达式为 ]2)4.05(2c o s [04.0π--π=x t y (SI) 4分(2) P 处质点的振动方程为]2)4.02.05(2c o s [04.0π--π=t y P )234.0c o s(04.0π-π=t (SI) 2分 补充题3-1用铁锤把质量很小的钉子敲入木板,设木板对钉子的阻力与钉子进入木板的深度成正比。
大学物理总复习——热学

3 R 2
气体定体摩尔热容 :____________________ , 气体定压摩尔热容 :________________
(3)
5 R 2
P128二、19. 用绝热材料制成的一个容器,体积为2V0, 被绝热板隔成A、B 两部分,A 内储有1 mol单原子分子 理想气体,B 内储有2 mol 刚性双原子分子理想气体,A、 B 两部分压强相等均为p0,两部分体积均为V0,则 3p0V0/2 ;EB= (1)两种气体各自的内能分别为EA=________ 5p0V0/2 ________; (2) 抽去绝热板,两种气体混合后处于平衡时的温度为T =______。 8p0V0/13R
式中A为常数.则该电子气电子的平均速率为
A 2 (A) v m 3
(B)
A 4 vm 4
(C) v
m
A 2 (D) v m 3
答:[ B ]
P127二、7. 质量为 6.2×10−14 g 的某种粒子悬浮于 27℃的气体中,观察到它们的方均根速率为 1.4cm/s, 则该种粒子的平均速率为_________________。(设 粒子遵守麦克斯韦速率分布律)
P56 6. 用公式 E CV、m T 式中CV为定体摩尔热容 、m
量,视为常量,ν 为气体摩尔数)计算理想气体内能 增量时,此式 (A) 只适用于准静态的等体过程. (B) 只适用于一切等体过程. (C) 只适用于一切准静态过程. (D) 适用于一切始末态为平衡态的过程. 答:[ D ]
200
(C)
10 R
(B)
400
10 R
答:[ c ]
10 R 10 R 200 + 2 (D) 400 10 R + 10 R 2
大学物理热学知识点和试题

热学知识点总结1.温度的概念与有关定义1)温度是表征系统热平衡时的宏观状态的物理量。
2)温标是温度的数值表示法。
常用的一种温标是摄氏温标,用t表示,其单位为摄氏度(℃)。
另一种是热力学温标,也叫开尔文温标,用T表示。
它的国际单位制中的名称为开尔文,简称K。
热力学温标与摄氏温标之间的换算关系为:T/K=273.15℃ + t温度没有上限,却有下限。
温度的下限是热力学温标的绝对零度。
温度可以无限接近于0 K,但永远不能到达0 K。
2.理想气体的微观模型与大量气体的统计模型。
速度分布的特征。
1)为了从气体动理论的观点出发,探讨理想气体的宏观现象,需要建立理想气体的微观结构模型。
可假设:a气体分子的大小与气体分子之间的平均距离相比要小得多,因此可以忽略不计。
可将理想气体分子看成质点。
b分子之间的相互作用力可以忽略。
c分子键的相互碰撞以及与器壁的碰撞可以看作完全弹性碰撞。
综上所述:理想气体分子可以被看作是自由的,无规则运动着的弹性质点群。
2)每个分子的运动遵从力学规律,而大量分子的热运动则遵从统计规律。
统计规律告诉我们,可以听过对围观物理量求平均值的方法得到宏观物理量。
气体的宏观参量(温度、压强等)是气体分子热运动的为管理的统计平均值。
3.理想气体状态方程与应用当质量一定的气体处于平衡态时,其三个状态参数P、V、T并不相互独立,二十存在一定的关系,其表达式称为气体的状态方程f(P,V,T)= 0最终得:T V p T pV '''=。
此式称为理想气体的状态方程。
标准状态:RT Mm pV =。
R=8.31J ·mol -1·K -1,称为摩尔气体常量。
设一定理想气体的分子质量为m 0,分子数为N ,并以N A 表示阿伏伽德罗常数,可得:T N R V N V RT m N Nm V RT M m p AA ===00 得:nkT p =,为分子数密度,可谓玻耳玆曼常量,值为1.38×10-23J ·K -1.这也是理想气体的状态方程,多用于计算气体的分子数密度,以及与它相关的其它物理量。
大学物理热学部分复习资料
W净= 曲线所围的面积 = Q1 + Q2 + ⋯ + Qn
20122012-1-3
20
热学习题课
1. 热机循环
p a O Q 1 A Q 2 V
W = Q1 − Q2
高温热源 T1 Q1 热机 W Q2 低温热源 T2 逆循环: 逆循环: 逆时针 热机效率
W = 1 − Q2 η= Q1 Q1
正循环: 正循环: 顺时针
dN :v − v + dv区间内的分子 N 数占 总分 子数 的百 分比 dN = f ( v ) dv N
四、麦克斯韦速率分布律
f (v)
dS
1.速率分布函数: 速率分布函数: 速率分布函数
dN f (v) = Ndv
o
d S = f ( v ) dv
内的分子数占总分子数
的百分比
v v + dv
∞
3.麦氏分布函数 麦氏分布函数
8kT 8RT v= = πM πm
平方平均速率
v = ∫ v2 f ( v) dv
2 0 ∞
m f ( v ) = 4π 2kT f (v) f max
3/ 2
e
mv 2 − 2 kT
v2
方均根速率
vrms 3kT 3RT = v = = m M
平均自由程
λ =
1 = 2 2πd n
kT 2 πd2p
20122012-1-3
15
热学习题课
热力学基础 一、热力学第一定律 系统对外做功 ∆V > 0,W > 0 外界对系统做功 ∆V < 0,W < 0 系统从外界吸收的热量 从外界吸收的热量, 系统从外界吸收的热量, 内能增量 i ∆E = ν ⋅ R∆T = ν CV ∆T 一部分使系统的内能增加, 一部分使系统的内能增加,另 2 i 一部分使系统对外界做功. 一部分使系统对外界做功. 定体摩尔热容 CV = R 2 其中 定压摩尔热容 C p = CV + R dW = pdV
大学物理(热学篇)
v1
v´1
x
A1 y °
z
1秒钟A1受到分子的总冲量
2mv x
vx 2x
mv
2 x
x
第三步 N个分子在1秒内对A1的碰撞
A1在1秒内受到的冲量——平均作用力F
F 2mv1x
v1 x 2x
2mv2x
v2x 2x
2mv Nx
vNx 2x
m x
(v12x
v22x
vN2 x )
m x
N
即在平衡态,一个自由度,代表一种独立的 运动和一份能量
如某种分子有t个平动自由度,r个转动自由度v振动 自由度,则分子具有:
平均平动动能 平均转动动能 平均振动动能
为什么均分到各自由度所对应的运动能量都 是二分之一KT呢? 主要是分子不断碰撞以达到平衡态的结果。
注意
1、 一般温度下(T <10 3 K)振
(1)每个分子作用于气壁的冲量I
解(1)每个分子作用于气壁的冲量等于气体 分子动量增量的负值
I 2mv 1.21024kgm/ s
(2)每秒钟碰在器壁单位面积上的分子数n0
解(2)器壁ΔA面积上在Δt时间内碰撞的分子数
N A vt n
z
6
n0
N At
nv 6
n0
1 6
nv
0.31028
/
m3
物体运动形式:平动、转动、振动
自由度数目 i t r v
平转振 动动动
例1 自由运动的质点 (三维空间) 3 个 平动自由度 记作 t = 3
若受到限制,自由度降低 平面上 : t=2 直线上 :t=1
例2 自由运动刚体 (如手榴弹)自由度。
大学物理(热学知识点总结)
2 kT
n n0e
m0 gz kT
p p0e
V2
m0 gz kT
dA pdV
A pdV
V1
dQ dE dA
Q E A
E CV ,m (T2 T1 )
7、 循环过程 卡诺循环 (1)热机效率与制冷系数
E 0
Q A E
A Q吸 Q放
1 1 b( P1 ,V1 ) c( P1 ,4V1 ) 4 4 P 1 4
P P1
a
c
b
Q A (3 / 4 ln4) p1V1
[2]. (8-4)0.02kg的氦气(视为理想气体),温度由170C升为270C, 若在升温过程中,(1)体积保持不变;(2)压强保持不变;(3) 不与外界交换热量,试分别求出气体内能的改变、吸收的热量、 外界对气体所作的功。
2
H2
(v p )O ( / vp) C)图中b表示氧气分子的速率分布曲线;
2
H2
/ v p ) H2 4 D)图中b表示氧气分子的速率分布曲线;(v p )O2 (
f (v )
a b
vp
v
2 RT M mol
O
2、两瓶不同种类的理想气体,它们的温度和压强都相同,但 体积不同,则单位体积内的气体分子数 n ,单位体积内气 体分子的总平动动能(EK / V ),单位体积内的气体质量 ρ ,分别有如下的关系:
大学物理 (热学) 知识点总结
一、基本物理概念:
1、理想气体的压强
1 2 2 p nm0 v nw 3 3
2、理想气体的温度和平均平动动能
3 w kT 2
2w T 3k
大学物理复习提纲
第一章 运动和力
一、质点运动学
1、
位置矢量
r
xi
yj
zk
运动方程:
r (t) x(t)i y(t) j z(t)k
x x(t)
分量式:
y y(t) z z(t) (消去t得轨道方程)
2、位移 r r2 r1
(x2 x1)i ( y2 y1) j (z2 z1 )k
m1v0l
(1 3
m2l
2
m1l
2
)
l m2
v0
摆动过程:机械能守恒
m1
1 2
(1 3
m2l 2
m1l 2 ) 2
m1gl(1
cos )
m2 g
l 2
(1 cos )
复习
第 4 章 流体力学
一、理想流体的稳定流动
(1)连续性方程: S1V1 S2V2
(2)伯努利方程:
p1
1 2
v12
gh1
p2
五、电势差
Ua
dq
4 π 0r
(电势叠加法)
b
Uab Ua Ub
E dl
a
六、电势力做的功 Aab q(Ua Ub ) q Uab
复习
第 9 章 恒定磁场
一、磁感应强度:
1、毕奥-萨伐尔定律:dB
0
Id
l
r
4r 3
(1) 一段载流直导线的磁场
B
0 I(c
4πa
os1
cos2)
复习
五、熵增加原理:
S 0
孤立系统中的可逆过程,其熵不变;孤立系统中的 不可逆过程,其熵要增加 .(孤立系统的熵永不减少)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大学物理热学复习提纲 Prepared on 22 November 2020期 末 复 习理想气体状态方程一、 理想气体:温度不太低,压强不太高的实际气体可视为理想气体。
宏观上,在任何情况下都符合玻-马、盖-吕、查理三定律的气体。
二、 三个实验定律:(1)玻—玛定律: pV = 常数 或 T = 常数(2)盖.吕萨克定律:VT= 常数 或 p =常数(3)查理定律: TP= 常数 或 V =常数三、 理想气体状态参量:体积(V ),压强(p ),温度(T ) ;内能(E ),焓(H ),熵(S ),摩尔数( )四、 理想气体分子模型:①全同质点;②弹性碰撞;③除碰撞瞬间外无相互作用,忽略重力五、普遍适用112212p V p V T T = :状态变化中质量不变阿佛伽德罗定律: p nkT = 六、 道尔顿分压定律:● 混合气体的压强等于组成混合气体的各成分的分压强之和 ● (几种温度相同的气体混于同一容器中,各气体的平均平动动能相等)七、 关于p nkT =:1. 是状态方程的微观式,大学物理中常用此式2. 式中N Nn V V==d d :气体的分子数密度,即单位体积内的分子数3. R = J/(mol·K) :普适气体常数4. 231238.31 1.3810J K 6.0210A R k N --===⨯⋅⨯:玻耳兹曼常量 八、 关于压强p : ●Γ:单位时间内碰在单位面积器壁上的平均分子数(气体分子碰壁数)● 压强p :单位时间内气体(全部分子)施于单位面积器壁的平均① 压强的定义体现了统计平均。
② V x >0的分子占总分子的一半,或分子速度在某方向的分量平均值为0● (例如:在x 方向,有0x v =;在y 方向,有0y v =;在z 方向,有0z v =)这是机会均等的表现。
③ 2213xv v = 也是机会均等的表现。
④ 22i ix x in v v n=∑∑ 是统计平均的表现。
九、1. 压强是相应的微观量:分子数密度和平动动能的统计平均。
● 压强与分子数密度n 有关,与气体种类无关。
2. 温度是相应的微观量:平均平动能的统计平均值。
● 温度是大量气体分子热运动的外在表现,实质就是反映了气体内部分子热运动的剧烈程度。
◆ 对不同气体,平衡态时,若T 相同,表示kt ε相同,但2v或不一定相同,因为还要考虑分子的质量m;同样,若同,也不一定T 相同。
3. 只有宏观量才能被测量,微观量不能。
4. 压强和温度都是大数量分子的微观量的统计平均,对于少数分子没有压强和温度可言。
十、 分子力:分子力是由静电力、电子轨道不同状态的结合力等组成的,并非来自万有引力麦克斯韦分布律一、 速率分布函数()Nf v N v=d d :分布在速率v 附近的单位速率间隔内的分子数占总分子数的比例,是速率v 的函数。
1. 涨落现象:偏离统计平均值的现象2. 统计规律永远伴随着涨落现象(粒子数越少,涨落现象越明显)。
3. 是统计规律,只适用于大量分子组成的集体。
也有涨落,非常小。
二、 三种速率(理想气体、温度为T 的平衡态)(1)讨论速率分布(概率)时用到● (是速率分布中的最大速率吗) (2)在讨论分子平均碰撞频率(平均自由程)时用到 (3)在计算分子的平均平动动能时用到● 同一气体:P rms v v v << ● 不同气体:它们都∝输运过程1、 气体分子碰撞● 使平衡态下分子速度有稳定分布; ● 实现能量均分;● 使气体由非平衡态平衡态。
(1) 描述的物理量有:碰撞截面σ;平均碰撞频率Z ;平均自由程λ(2) 刚球模型:把分子看作直径为d ,无引力作用的弹性刚球。
(3) 有效直径d :两分子在碰撞中其中心所能接近的最小距离,相当于完全弹性小球的直径d 。
它是统计平均值,可视为常数。
(4) 碰撞截面σ:以分子的有效直径d 为半径的球体的最大截面σ=πd 2.若两种不同的分子相碰,σ的半径为(d 1+d 2)/2(5) 平均碰撞频率z :一个分子在单位时间与其他分子的平均碰撞次数。
(∵v =,p nkT =)● z 一般109次/秒:即每秒碰几十亿次! ● 讨论:z 如何变化● 温度不变时,z 随压强的增大而增大:z P ∝ ● 压强不变时,z 随温度的增大而减小:1z ∝(6)平均自由程λ:分子在相邻两次碰撞之间自由走过的平均路程 (是统计平均值)●λ一般10-8~109 m(nm级),约为d 的200倍。
●讨论:λ如何变化●温度不变时,λ随压强的增大而减小:1p λ∝●压强不变时,λ随温度的增大而增大:Tλ∝●z和λ都反映了分子间碰撞的频繁程度:在v一定时,分子间的碰撞越频繁,z就越大,λ就越小。
2、三类输运过程:输运过程是指系统由非平衡态向平衡态的变化过程,其过程的快慢取决于分子间碰撞的频繁程度(即碰撞频率)。
输运过程中都有相应物理量的定向迁移。
(1)粘滞现象:因各气层定向流速不均匀而使相邻两气层互现切向内摩擦力的现象。
◆宏观表现为分子定向运动的动量迁移。
(2)热传导现象:因气体各层的温度不均匀而使相邻两气层有热量传递。
◆宏观表现为气体分子热运动能量迁移。
(3)扩散:当气体的密度不均匀时,气体的质量将从密度大的区域向密度小的区域移动的现象。
单纯由热运动产生的扩散叫纯扩散。
◆ 宏观表现为由于分子热运动所产生的气体宏观粒子迁移或质量迁移。
● 分子的热运动和分子间的碰撞是输运过程的内因,是出发点。
热力学第一定律一、 正确理解:准静态与非准静态过程;可逆与不可逆过程;自发与非自发过程;绝热与非绝热过程(1) 只有准静态过程才能用过程曲线表示(是否只能用p-V 图) (2) 自然界的一切自发过程都是不可逆过程 (3) 一切与热有关的过程都是不可逆过程 (4) 准静态过程是否一定是可逆过程密度不均匀温度不均匀流速不均匀 定向运动动量 运动平均动能质量 λρηv 31=13Vv C κρλ=13D v λ=扩散 热传导粘滞 现 象原 因传递量 系数公式 d d d d M D A t z ρ=-d d d d Q T A t zκ=-⋅d d d d K u A t z η=-动量沿流速减小的方向输运质量沿密度减小的方向输运 热量沿温度降低的方向输运输运定律 输运特征(5) 不可逆过程是否就是不能向相反方向进行 (6) 绝热过程是否一定是等熵过程例:但若系统做的是准静态绝热膨胀呢 1. 初态、末态、中间态都是平衡态2. 是一个非自发的、可逆的、绝热的、准静态的过程3. 全过程、全部状态(初态、末态、中间态)都可以在过程曲线中表示出来4. 过程曲线可以用p-V 图反映,也可以画成p-T 图,或画T-V 图(1) 系统对外作了功——不是迅速抽掉隔板,一定是气体缓缓地推动隔板(2) 系统的内能减少——∵Q=0,T 减小图示的系统(做绝热自由膨胀的气体)。
1. 初态、末态是平衡态2. 但中间态不是平衡态,所以经历的是非准静态的过程这是一个自发、不可逆、绝热、非准静态过程3. 该过程不能用过程曲线表示出来4. 但初态与末态可以在过程曲线中表示出来 (1) 系统对外没有作功—隔板抽掉,自由膨胀 (2) 系统的内能减少——∵Q=0,T 减小二、 能量均分定理和热容量1. 自由度i :决定一个物体的位置所需要的独立坐标数。
i = t (平动)+ r (转动)+ s (振动)。
当忽略振动自由度(经典热力学,常温):i = t+r自由度、比热容比、摩尔热容:2. 能量按自由度均分定理(能量均分定理) (1)在温度为T 的平衡态下,物质每个分子的每一个自由度具有相同的平均动能kT /2。
(2)一个分子的平均总1(2)2t r s kT =++•*,(3) 1mol 物质的总能量(内能)为单原子 32kT =ε,32m V m U RT C T == = C p ,m /C V ,mC p ,m =C V ,m +Ri=t+rC V ,m =iR /2 单原子 3(3+0) 5/3= 3R /2 5R /2 刚性双原子 5(3+2) 7/5= 5R /2 7R /2 刚性多原子6(3+3)4/3=3R4R常温双原子 52kT =ε 52m U RT =,V m C T = *高温双原子(考虑振动自由度s ) 72kT =ε 72m U RT =,V m C T =(4) M 千克物质的内能▲ 能量均分定理仅限于均分动能(含平动动能和转动动能)。
三、 热力学第一定律 21U U Q A -=+, d U = Q + A (微变式) 1. 21d V V A p V =-⎰:外界对系统作的功,是过程量。
● 外界对系统作功(体积压缩功)为正功;体积膨胀功为负功。
2. n 表示不同的过程,也是过程量 ● 系统吸热为正,放热为负。
3. ●理想气体的内能仅是温度的单值函数(态函数)4. 仅有体积功时:d U =Q ﹣p d V 四、 热力学第一定律的应用1. 等体过程:A V =0; ,2V V m M iQ U R T C T =∆=•∆=•∆νμ;p C T =2. 等压过程:A p =-p △V =-νR △T ; ,m p p Q C T =∆ν ;,V m U C T ∆=•∆ν; V C T=3. 等温过程:△U =0 ;1212ln ln T p V Q RT RT V p ==νν ;TT A Q =- ;pV C =4. 绝热过程:Q =0;,V m U C T ∆=•∆ν; A U =∆●绝热方程:1pV C γ= ; 12TV C γ-= ;13p T C γγ--= 或:1122pV p V γγ=; 111122TV T V γγ--= ;111122p T p T γγγγ----=●多方方程:——将绝热方程中的γ改做n 即可。
五、 热机:利用工作物质连续不断地把热转换为功的装置 1. 正循环:p-V 图中的顺时针闭合曲线 ▲ 系统经历一个循环之后,内能不改变 2.(1) Q 1: 热机从热源吸收的总热量;|Q 2|: 热机向热源放出的总热量(Q 2<0);A: 热机对外界所做的净功(2) 理想气体准静态过程的卡诺循环的效率只由高温热源和低温热源的温度决定,与工作物质无关。
(3)1(4) ηη≤不可逆可逆——卡诺定理2六、 制冷机:通过外界作功,从低温热源吸热的装置1. 逆循环:p-V 图中的逆时针闭合曲线2. 制冷系数:2212Q Q A Q Q ==-ε;卡诺制冷机制冷系数212C T T T =-ε(1) |Q 1| : 制冷机向高温热源放出的总热量 (Q 1<0) (2) Q 2: 制冷机从低温热源吸收的总热量 (3) A: 外界对制冷机所做的功热力学第二定律一、 开尔文表述:不可能从单一热源吸收热量,使之完全变为有用功而不产生其它影响。
