最经典--高中化学方程式的书写及意义检测
高中化学高考总复习--氧化还原反应方程式的书写和计算知识讲解及巩固练习题(含答案解析)

成
Fe2+,可以写出 Fe3++I-―→Fe2++I2,然后根据得失电子守恒、电荷守恒配平。FeCl3 与 KClO 反应时,根
据题目信息 Fe3+被氧化为 FeO42-,则 ClO-被还原成 Cl-,可以写出 Fe3++ClO-―→FeO42-+Cl-,然后根据氧
化还原反应中得失电子守恒可以得到:2Fe3++3ClO-―→2FeO42-+3Cl-,再结合溶液强碱性和电荷守恒,在 左边补上 OH-,然后配平即可。 【变式 4】向 Na2CO3 溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有 NaHCO3
__________ + __________ →
【答案】(1)FeSO4+HNO3→Fe(NO3)3+Fe2(SO4)3+N2O+H2O (2)FeSO4 N(3)得到 4(4)24FeSO4+30HNO3→ 类型二、 陌生氧化还原反应方程式的书写
【高清课堂:氧化还原反应的基本概念和规律 例 1】
【变式 3】(2015 衡水中学周练)FeCl3 与氢碘酸反应时可生成棕色物质,该反应的离子方程式为________
______________________;高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3
与 KClO 在强碱性条件下反应可制取 K2FeO4,其反应的离子方程式为
5SO2+2MnO4-+
=5SO42-+2Mn2++
,再用 H+离子调整电荷相等(右边加上 4 个 H+),最后在
左边补上 2 个水即可。
【总结升华】书写氧化还原反应的化学方程式重在分析化合价变化,强调一种元素化合价上升,必有
另一种元素的化合价降低。
举一反三:
2021-2022年高考化学 考点总动员系列 专题05 离子方程式和氧化还原反应方程式的书写(含解析
2021年高考化学考点总动员系列专题05 离子方程式和氧化还原反应方程式的书写(含解析)【母题再现】题型介绍:离子方程式和氧化还原方程式的书写为高考的必考题型,考查方式为填空题。
一些省市在工艺流程题或探究性实验题中考查,还有有些省的命题中考查基本概念和基本理论的答题中涉及方程式的书写。
这类题型涉及离子反应的基本原理,氧化还原反应的规律及产物的判断,氧化还原反应方程式配平的基本方法等相关知识。
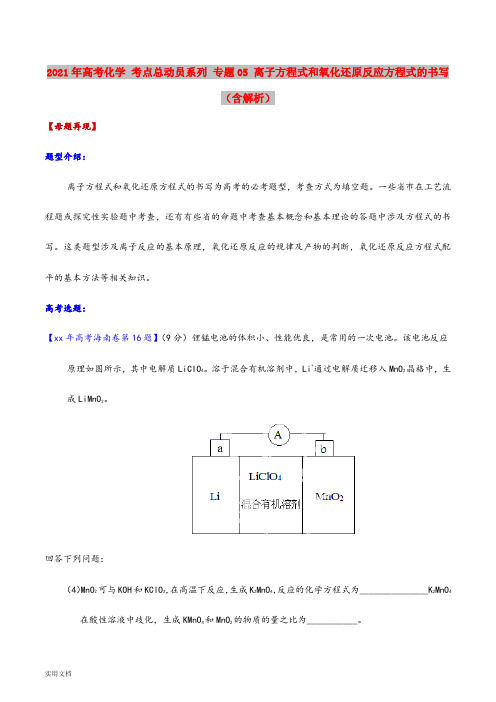
高考选题:【xx年高考海南卷第16题】(9分)锂锰电池的体积小、性能优良,是常用的一次电池。
该电池反应原理如图所示,其中电解质LiCIO4。
溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。
回答下列问题:(4)MnO2可与KOH和KClO3,在高温下反应,生成K2MnO4,反应的化学方程式为_______________K2MnO4在酸性溶液中歧化,生成KMnO4和MnO2的物质的量之比为___________。
解题技巧:对于反应方程式的书写在书写时注意一下几点:1、产物确定:对于一个未知的反应,产物的确定可能是方程式水的一大难点。
在实际书写过程中我们可以使用化学反应的基本原理以及元素及化合物性质来进行判断。
(1)运用类比的方法,可以确定相同反应原理的产物。
如CaC 2与H 2O 反应的原理为水解反应,水电离成H +和OH -,然后分别与Ca 2+和C 2-2结合,生成Ca(OH)2和C 2H 2,可以推知像CaC 2这样金属与非金属结合成的离子型化合物Al 4C 3、Mg 2C 3、Li 2C 2、Mg 3N 2、Na 2O 2等与水反应均类似,故可以顺利判断出生成物。
(2)根据量的关系及反应的先后顺序进行判断。
比如在NH 4Al(SO 4)2中加入少量、适量、过量的NaOH溶液,首先我们要确定反应的先后顺序为Al 3+、NH +4、Al(OH)3,如加入少量的NaOH ,发生反应为Al 3++3OH -=Al(OH)3↓;再加入发生的反应为NH +4+OH -=NH 3·H 2O ,两步还可以写出总反应;继续滴加发生的反应是氢氧化铝溶解,即如果加入过量的NaOH ,发生的反应为Al 3++ NH +4+5OH -= AlO -2+ NH 3·H 2O+2H 2O 。
高一化学离子方程式的书写及正误判断试题答案及解析

高一化学离子方程式的书写及正误判断试题答案及解析1.下列离子方程式书写错误的是()A.Na投入到水中:2Na+2H2O====2Na++2OH-+H2↑B.Al(OH)3溶于NaOH溶液中:Al(OH)3+OH-====Al+2H2OC.NaAlO2溶液中通入足量的CO2:2Al+CO2+3H2O====2Al(OH)3↓+CD.Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-====2Al+H2O【答案】C【解析】 NaAlO2溶液中通入足量的CO2应该生成碳酸氢钠。
【考点】铝的氧化物与氢氧化物从铝土矿中提取铝2.与离子方程式H++OH-====H2O相对应的化学方程式是()A.Ba(OH)2+2HCl====BaCl2+2H2OB.NaOH+NaHSO4====Na2SO4+H2OC.Ba(OH)2+H2SO4====BaSO4↓+2H2OD.NaOH+CH3COOH====CH3COONa+H2O【答案】A、B【解析】离子方程式H++OH-====H2O所表示的含义是可溶性强碱和强酸反应生成可溶性盐和水的反应。
NaHSO4是强酸的酸式盐,在水溶液中完全电离出H+,相当于强酸,A和B选项都正确;Ba(OH)2溶液和H2SO4溶液反应生成的BaSO4是难溶性物质,C选项错误;醋酸属于弱酸,不能拆成离子的形式,D选项错误。
【考点】离子反应3.仔细分析下列实验:实验1:实验2:A、B、C试管中的现象如下表所示:写出A、B、C试管中发生反应的离子方程式。
(1)A: ;(2)B: ;(3)C:。
【答案】(1)Ba2++====BaSO4↓ (2)Cu2++2OH-====Cu(OH)2↓(3)Ba2++Cu2++2OH-+====BaSO4↓+Cu(OH)2↓【解析】BaCl2溶液和CuSO4溶液混合Ba2+和结合成BaSO4白色沉淀,Cu2+和Cl-不反应,所以溶液仍然呈现蓝色;向A试管中得到的滤液中加入NaOH溶液,Cu2+和OH-反应结合成Cu(OH)2蓝色沉淀。
高中化学高考总复习--电极反应式的书写知识讲解及巩固练习题(含答案解析)

高中化学高考总复习--电极反应式的书写知识讲解及巩固练习题(含答案解析)【考纲要求】1.理解原电池的工作原理并正确书写各种化学电源的电极反应和总反应方程式;2.理解电解池的工作原理并正确书写电极反应和总反应方程式。
【考点梳理】【高清课堂:399199电极反应式的书写】考点一:正确书写原电池的电极反应式1.先确定原电池的正负极,列出正、负电极上的反应物质,在等式的两边分别写出反应物和生成物。
要点诠释:一般来说,较活泼的金属失去电子,为原电池的负极,但不是绝对的。
如镁片和铝片插入氢氧化钠溶液中组成的原电池虽然镁比铝活泼,但由于铝和氢氧化钠溶液反应失去电子被氧化,因而铝是负极,此时的电极反应为:负极:2Al-6e-===2Al3+正极:6H2O+6e-==6OH-+3H2↑或2Al3++2H2O+6e-+2OH-==2AlO2-+3H2↑再如,将铜片和铝片同时插入浓硝酸中组成原电池时,由于铝在浓硝酸中发生了钝化,铜则失去电子、作原电池的负极被氧化,此时的电极反应为:负极:Cu-2e-===Cu2+正极:2NO3-+4H++2e-===2NO2↑+2H2O2.要注意电解质溶液的酸碱性:要点诠释:在正负极上发生的电极反应不是孤立的,它往往与电解质溶液紧密联系。
如氢-氧燃料电池就分酸式和碱式两种, 如果是在碱性溶液中,则不可能有H+出现,同样在酸性溶液中,也不能出现OH-。
在酸性溶液中: 负极:2H2-4e-===4H+; 正极:O2+4H++4e-===2H2O 在碱性溶液中: 负极:2H2-4e-+4OH—===4H2O; 正极:O2+2H2O+4e-=4OH—。
3.要注意电子转移的数目要点诠释:在同一个原电池中,负极失去电子的总数一定等于正极得到电子的总数,所以在书写电极反应式时,要注意正负极得失电子相等。
这样可避免在由电极反应式写总反应方程式或由总方程式改写电极反应式时所带来的失误。
4.电极反应式的书写必须遵循离子方程式的书写要求:要点诠释:①电极反应式等式的两边原子数目及电荷必须守恒。
(整理)高中离子方程式经典练习题

(整理)高中离子方程式经典练习题离子反应问题及离子方程式的书写离子方程式的书写步骤:1、写:书写完全正确的化学方程式;2、拆:将能拆的化学式(完全电离的酸、碱、盐及融化态的金属氧化物)拆为离子符号;3、删:将未参加离子反应的离子从两边删掉(等个数),整理(系数应为最简整数比);4、查:⑴质量守恒、⑵电荷守恒、⑶注明“↑”“↓” ;⑷ 、为氧化还原反应时、氧化剂与还原剂得失电子数应相等。
? 书写相关知识1、完全电离的酸是指:HCl 、H 2SO 4、HNO 3、HI 、HBr 、HClO 4等强酸;中强酸(H 2SO 3、H 3PO 4),弱酸(H 2CO 3、H 2S 、HF 、HclO 、CH 3COOH 、H 2SiO 3)则不能拆。
2、完全电离的碱是指:NaOH 、KOH 、Ca(OH)2、Ba(OH)2等强碱、中强碱的溶液;而 NH 3?H 2O 及Cu(OH)2、Fe(OH)3等难溶性弱碱则不能拆。
3、完全电离的盐是指:所有易溶、可溶及微溶性的盐的溶液。
附:盐的溶解性规律:钾盐、钠盐、铵盐、硝酸盐,二元酸的酸式盐、磷酸的二氢盐均易溶。
碳酸盐、磷酸盐、硅酸盐的正盐中只有钾盐、钠盐、铵盐溶;氯化物中只有AgCl 不溶;硫酸盐中只有PbSO 4 、BaSO 4不溶,但CaSO 4、Ag 2SO 4为微溶。
4、特殊情况处理:微溶物:作反应物时,为溶液时拆,作产物时不拆。
浓硫酸作反应物时,不能拆,而浓盐酸、浓硝酸则必须拆。
酸式酸根离子只有HSO 4-必须拆,而HS -、HCO 3-、HSO 3-、HPO 42-、H 2PO 4-则不能拆。
5、凡单质、氧化物、气体、难溶固体、弱酸、弱碱、水等难电离的及非电解质均不能拆。
练习题一选择题1、下列电离方程式错误的是()A NaHCO 3 ====Na + +H ++CO 32―B NaHSO 4 ====Na + +H ++SO 42―C MgCl 2 ====Mg 2++2Cl ―D B a (O H )2 =====Ba 2++2OH ―2、离子方程式CO 32-+ 2H += H 2O + CO 2↑中的CO 32-代表的物质可以是() A 、CaCO 3 B 、NaHCO 3 C 、Na 2CO 3 D 、BaCO 33、下列化学方程式中,不能用离子方程式 Ba 2++SO 42―====BaSO 4 ↓A .Ba(NO 3)2+H 2SO 4==BaSO 4↓+2HNO 3B .BaCl 2+Na 2SO 4==BaSO 4↓+2NaClC .BaCO 3+H 2SO 4==BaSO 4↓+H 2O+CO 2↑D .BaCl 2+H 2SO 4==BaSO 4↓+2HCl4.下列各组离子反应可用H ++OH -H 2O 表示的是()A .氢氧化钡和硫酸B .氢氧化铁和盐酸C.硝酸和氢氧化钠D.硫酸氢钠和氢氧化钠5、下列离子方程式,书写正确的是()A、盐酸与碳酸钡反应 CO32-+2H+==CO2↑+H2OB、硫酸铜溶液中滴加氢氧化钡溶液Ba2++2OH-+Cu2++SO42-==BaSO4↓+Cu(OH)2↓C、硝酸银溶液中加入铜粉Ag++Cu==Cu2++Ag↓D、铁与稀盐酸反应2Fe+6H+==2Fe3++3H2↑6、下列离子方程式书写正确的是()A、氧化铜与盐酸反应O2― +2H+ ====H2OB、碳酸氢钠溶于盐酸:HCO3-+ H+ = H2O + CO2↑C、硫酸氢钠溶液与NaOH溶液混合:HSO4- + OH- = H2O + SO42-D、石灰石溶于硝酸:CO32-+ 2H+ = H2O + CO2↑7.下列反应的离子方程式中,正确的是()A.向硝酸银溶液中加盐酸Ag++C1-===AgCl↓B.碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+===Ca2++2H2O+2CO2↑C.盐酸跟氢氧化镁反应:H++OH-===H2OD.碳酸镁跟硫酸反应:MgCO3+2H+===Mg2++H2O+CO2↑8.下列离子方程式中,正确的是A.碳酸氢钙溶液与盐酸反应Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑B稀盐酸和碳酸钙反应 CO32- + 2H+ = CO2↑ + H2OC碳酸钠溶液与醋酸反应 CO32-+ 2H+ = CO2↑ + H2OD石溶于醋酸的反应CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O9.下列反应的离子方程式中,正确的是()A、氢氧化钡溶液和稀硫酸Ba2++OH-+H++SO42-=BaSO4↓+2H2OB、氯化铁溶液中加铁粉 2Fe3+ + Fe = 3Fe2+C、过量CO2通入NaOH溶液中CO2 + 2OH-= CO32-+ H2OD、少量CO2通入NaOH溶液中CO2 + OH-= HCO3-+ H2O10.下列离子方程式中,正确的是A、氨气通入醋酸CH3COOH + NH3 = CH3COO-+NH4+B.碳酸氢镁溶液中加过量石灰水Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓ C、澄清石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2OD、稀硫酸滴在铜片上:Cu+2H+==Cu2++H2↑11.下列各组中的离子,能在溶液量共存的是()A 、K+、H+、SO42-、OH-B、Na+、Ca2+、CO32-、NO3-C 、Na+、H+、CO32- Cl-D 、Na+、Cu2+、Cl、SO42-12、在无色透明强酸性溶液中,能大量共存的离子组是()A、K+、Cu2+、NO3-、SO42-B、K+、Na+、Cl-、CO32-C、Zn2+、NH4+、NO3-、Cl-D、K+、Na+、MnO4-、SO42-13、在PH=1无色透明溶液中能大量共存的离子组是()A.Al3+、Ag+、NO3-、Cl-B.Mg2+、NH4+、NO3-、Cl-C.Ba2+、K+、S2-、Cl-D.Cu2+、Na+、NO3-、SO42-14、在强酸性或强碱性溶液中都能大量共存的一组离子是()A.Ba2+,Fe3+,Br-,NO3-B.Na+,Ca2+,HCO3-,NO3-C.Al3+,NH4+,SO42-,Na+D.Na+,K+,NO3-,SO42-15、下列各组中的离子,能在溶液量共存的是()A.Mg2+、H+、C1-、OH-B.Na+、Ba2+、CO-23、NO-3C、Na+、H+、Cl-、CO-23 D.K+、Cu2+、NO-3、SO-24、16、在强酸性无色透明溶液中,下列各组离子能大量共存的是()A、Fe3+、K+、Cl-、MnO4-B、Ag+、Na+、NO3-、Cl-C、Zn2+、Al3+、SO42-、Cl-D、Ba2+、NH4+、Cl-、HCO3-17、巳知某溶液中存在较多的H+、SO42—、NO3—,则该溶液中还可能大量存在的离子组是A.Al3+、CH3C00—、Cl—B.Mg2+、Ba2+、Br—C.Mg2+、Cl—、I—D.Na+、NH4+、Cl—18、某工厂排放的工业废水中可能含有K+、Ag+、NH4+、Mg2+、SO42-、Cl-、NO3-、HCO3-等离子。
高中化学考试注意事项及电子式书写技巧

高中化学考试注意事项及电子式书写技巧1 、排列顺序时,分清是“由大到小”还是“由小到大”,类似的:“由强到弱”、“由高到低”等等。
2 、书写化学方程式时,分清是“=”还是“⇌”,如一种盐水解方程式一定用“⇌”不能用“=”,其产物也不能标“↓”或“↑”,弱酸、弱碱的电离一定要用“⇌”不能用“=”。
多元弱酸电离、多元弱酸根离子水解:不能一步写成和或漏写可逆符号;3 、别忽视题干中“混合物”、“化合物”、“单质”等限制条件。
4 、有单位的要写单位,没有单位的就不要写了。
如“溶解度”单位是“ g ”,却不写出,“相对分子质量”、“相对原子质量”无单位,却加上“g ”或“g ·mol -1”。
摩尔质量有单位(g ·mol -1) 却不写单位,阿伏加德罗常数单位是“ mol -1”而未写,失分。
5 、要求写“名称”却写分子式或其他化学式,要求写分子式或结构式却写名称。
电子式、原子或离子结构示意图、结构简式、结构式不看清,张冠李戴。
要求写离子方程式而错写成化学方程式。
书写电子式时,共价化合物忘了未成对电子,离子化合物中的阴离子与原子团离子忘了加中括号;元素符号和元素名称、结构简式和分子式、化学方程式和结构简式不要混淆。
6 、所有的稀有气体都是单原子分子而误认为双原子分子。
7 、273 ℃与273K 不注意区分,是“标况”还是“非标况”,是“气态”还是“液态”“固态”不分清楚。
22.4L.mol-1的适用条件。
注意三氧化硫、乙烷、己烷、水等物质的状态。
区分液态氯化氢和盐酸,液氨和氨水,液氯和氯水。
8 、计算题中往往出现“将样品分为两等份” ( 或“从 1000mL 溶液中取出50mL ”) ,最后求的是“原样品中的有关的量”,你却只求了每份中的有关量。
9 、请注意选择题“正确的是”,“错误的是”两种不同要求。
请注意,做的正确,填卡时却完全填反了,要十分警惕这种情况发生。
10 、求“物质的质量”与“物质的物质的量”、求气体的“体积分数”与“质量分数”不看清楚,失分。
小专题(九) 化学方程式的意义及书写-2024-2025学年九年级化学人教版上册

1
2
3
4
5
6
7
8
9 10 11 12 13 14
5. (2023·无锡)如图所示为“光催化固氮合成氨”反应前后分子种类 变化的示意图。下列叙述正确的是( B )
第5题 A. 乙和丙都是氧化物 B. 参加反应的甲和乙的分子个数比为1∶3 C. 反应后原子数目增加 D. 反应生成的丙和丁的质量比为32∶17
1
2
3
4
5
6
7
8
9 10 11 12 13 14
12. (2024·南阳方城期末)请写出下列化学方程式。 (1) 乙醇(C2H5OH)是一种可再生能源,请写出乙醇在空气中燃烧 生成水和二氧化碳的化学方程式:
C2H5OH+3O2 点燃 2CO2+ 3H2O 。
(2) 干粉灭火器中的干粉(主要成分为NaHCO3)受热时分解生成碳 酸钠、一种液态氧化物和一种常见的气态氧化物:
中,铝、氧气、氧化铝的质量比是( C )
A. 27∶32∶102
B. 27∶24∶43
C. 108∶96∶204
D. 4∶3∶2
3. (2023·天津)在反应C+2ZnO 高温 2Zn+CO2↑中,下列有关说 法正确的是( B ) A. 反应前后各元素的化合价均无变化 B. 反应前后锌元素的质量没有发生改变 C. 参加反应的碳与氧化锌的质量比为4∶27 D. 反应后固体总质量减小,不遵循质量守恒定律
体,该反应的化学方程式为
2Al2O3(熔融)
通电
4Al+3O2↑
。
(4) 《千里江山图》为运动员服装设计提供了灵感,其真迹的颜料含 有石绿。石绿[主要成分为Cu2(OH)2CO3]受热分解生成三种氧化物 (无化合价变化),反应的化学方程式为
高中化学 最基础考点系列 考点8 电离方程式的书写 新人教版选修4

考点8 电离方程式的书写【考点定位】本考点考查电解质的电离方程式的书写,提升对强、弱电解质的理解,进一步巩固离子反应与离子方程式的书写及正误推断的应用力量。
【精确解读】1.电离方程式的概念:用化学式和离子符号表示电离过程的式子,称为电离方程式;2.电离方程式书书写留意事项:(1)强电解质在水溶液中完全电离,在书写电离方程式时用符号“=”.例如NaCl=Na++Cl-,CH3COONH4=CH3COO-+NH4+(2)在书写难溶性和微溶性强电解质的电离方程式时用符号“=”,在书写其溶解平衡的化学方程式时用符号“⇌”.例如:BaSO4=Ba2++SO42-,Ca(OH)2=Ca2++2OH-,BaSO4(s)⇌Ba2+(aq)+SO42-(aq),Ca(OH)2(s)⇌Ca2+(aq)+2OH-(aq);(3)有些电解质因条件不同,其电离方程式的书写形式也不同.例如,熔融时,KHSO4=K++HSO4-;水溶液中:KHSO4=K++H++SO42-;(4)弱电解质在水溶液中发生部分电离,在书写电离方程式时用符号“⇌”.例如,CH3COOH⇌CH3COO-+H+,NH3•H2O⇌NH4++OH-;(5)多元弱酸在水溶液中的电离是分步进行的,要求分步写出电离方程式,几元酸就有几级电离方程式.例如,H2CO3⇌H++HCO3-,HCO3-⇌H++CO32-;多元弱碱在水溶液中的电离比较简单,因此多元弱碱的电离方程式的书写一般是一步到位,但仍用符号“⇌”.例如,Cu(OH)2⇌Cu2++2OH-(6)弱酸的酸式盐是强电解质,在水中第一步完全电离出阳离子和弱酸的酸式酸根离子,而弱酸的酸式酸根离子又可以进行电离,且为可逆过程.例如,NaHCO3在水溶液中的电离方程式为:NaHCO3=Na++HCO3-,HCO3-⇌H++CO32-;(7)检查电离方程式是否遵循质量守恒和电荷守恒。
【精细剖析】书写电离方程式易犯的错误:①含有原子团的物质电离时,原子团应作为一个整体,不能分开;②在书写难溶性和微溶性强电解质的电离方程式时错用符号“⇌”.例如,CaCO3⇌Ca2++CO32-,Mg(OH)2⇌Mg2++2OH-;③把熔融条件下KHSO4的电离方程式错写成:KHSO4=K++H++SO42-;④没有把多元弱酸的电离分步书写;⑤把多元弱碱写成了分步的形式;⑥未配平。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高中--化学方程式的书写及意义课堂学习效果检测1
班级姓名分数
1、定义:叫做化学方程式。
2、书写化学方程式的原则
(1)
(2)
3、化学方程式的书写步骤:(以双氧水分解制氧气的化学方程式的书写为例)
步骤(1) :、、,如有多种反应物生成物中间连接。
(2) :使化学反应两边的相等。
(3):标出生成物的状态如、等,注明化学反应条件如等。
(4):把短线改成等号。
4、化学方程式等号两边化学式前面的数叫,应取,且只能,不能是分数。
5、点燃、加热、高温、催化剂等写在,若
,则在生成的气体物质化学式后面标↑,若,,则在生成物中固体化学式后面标↓。
6、化学方程式的意义:以通电分解水为例,写出反应的化学方程式并说明其意义。
(1)化学方程式:
(2)意义:①
②
③
7、书写化学方程式常见的错误有哪些:8、为什么要把化学方程式配平?这样判断是否已经配平?
9、写出以下咱们以前学过的化学反应的化学方程式:
(1)点燃镁条:镁条和氧气反应生成氧化镁
(2)氢氧化钠溶液和硫酸铜溶液反应,生成氢氧化铜和硫酸钠
(3)金属锌和盐酸反应生成氯化锌和氢气
(4)水在直流电作用下分解成氢气和氧气
(5)氢气在空气中燃烧生成水
(6)测定空气中氧气的含量的实验:在加热的情况下,铜能跟空气中的氧气反应生成黑色的氧化铜。
(7)实验室分解双氧水制取氧气
(8)木炭在空气中燃烧生成二氧化碳
(9)铁丝在氧气中燃烧生成四氧化三铁
(10)盐酸和大理石(主要成分是碳酸钙)反应,生成二氧化碳、水和氯化钙。
(11)白磷在空气中燃烧,生成五氧化二磷。
