羟基酸的脱水反应
【有机】脱水反应您知多少?

【有机】脱水反应您知多少?在有机合成和药物合成中,从羟基化合物(包括伯醇、仲醇、叔醇)脱水形成烯烃的转化是一类非常重要的转化,脱水反应可以在酸或者Lewis酸性条件下发生,也可以将羟基衍生化成易离去基(如磺酸酯或卤素)再在碱性条件下消除,还可以在脱水剂的条件下脱水形成烯烃,其中最常见的反应是黄原酸酯消除和Grieco-Sharpless消除反应,最为常用的是两个脱水剂就是Martin Sulfurane 和Burgess脱水剂。
脱水反应的挑战在于在复杂体系中,存在区域选择性的问题,或者当体系中存在多个羟基的时候,存在化学选择性的问题。
如图1所示,羟基化合物4在三氟化硼-乙醚作Lewis酸的条件下,在DCM中-78 o C反应2 min,会得到动力学上favor的化合物5,如果延长时间,会得到6和7,如果升高温度,则会发生1,2-甲基迁移,得到四取代双键化合物8。
图1. 化合物4的脱水反应(图片来源:Nat. Prod. Rep.)黄原酸酯消除黄原酸酯消除也叫Chugaeve(楚加耶夫)消除反应,是基础有机化学中的经典人名反应。
如图2所示,羟基化合物在碱性条件下和二硫化碳以及碘甲烷反应形成黄原酸酯,然后加热条件下发生分子内消除,经历六元环过渡态,顺式消除,得到烯烃,放出硫氧化碳和硫醇,该反应的优点是不发生碳架的异构和双键的迁移。
图 2. 黄原酸酯消除反应及其机理(图片来源:Strategic Applications of Named Reactions in Organic Synthesis.)H.Hagiwara教授课题组在天然产物Solanapyrone E的首例不对称全合成中,就用到了黄原酸酯消除,由于黄原酸酯消除是顺式消除,所以该体系中可以良好的控制区域选择性,以两步89%的产率得到目标脱水产物。
图 3. 黄原酸酯消除反应应用举例(图片来源:Org. Lett.)Martin试剂Martin试剂,也叫Martin sulfurane, 双[a,a-双(三氟甲基)苯乙醇]-二苯基硫,结构如图4所示,也可以在温和条件下脱水,但对水敏感,最好保存在手套箱中。
羟基官能团的性质与有机物的脱水反应
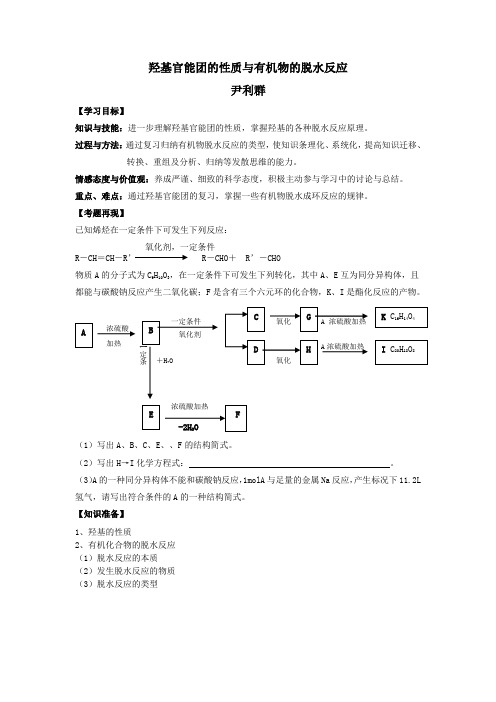
羟基官能团的性质与有机物的脱水反应尹利群【学习目标】知识与技能:进一步理解羟基官能团的性质,掌握羟基的各种脱水反应原理。
过程与方法:通过复习归纳有机物脱水反应的类型,使知识条理化、系统化,提高知识迁移、转换、重组及分析、归纳等发散思维的能力。
情感态度与价值观:养成严谨、细致的科学态度,积极主动参与学习中的讨论与总结。
重点、难点:通过羟基官能团的复习,掌握一些有机物脱水成环反应的规律。
【考题再现】已知烯烃在一定条件下可发生下列反应:氧化剂,一定条件R -CH =CH -R ’ R -CHO + R ’-CHO物质A 的分子式为C 9H 10O 3,在一定条件下可发生下列转化,其中A 、E 互为同分异构体,且都能与碳酸钠反应产生二氧化碳;F 是含有三个六元环的化合物,K 、I 是酯化反应的产物。
(1)写出A 、B 、C 、E 、、F 的结构简式。
(2)写出H →I 化学方程式: 。
(3)A 的一种同分异构体不能和碳酸钠反应,1molA 与足量的金属Na 反应,产生标况下11.2L 氢气,请写出符合条件的A 的一种结构简式。
【知识准备】1、羟基的性质2、有机化合物的脱水反应 (1)脱水反应的本质 (2)发生脱水反应的物质 (3)脱水反应的类型A浓硫酸 加热E3、已知某物质的结构简式为:1mol该物质分别与Na、NaOH、Na2CO3、NaHCO3、溴水充分反应,分别消耗多少mol?根据羟基的性质填写下表:以乳酸为例:乳酸(羟基酸)的结构简式为:【巩固练习】烯键碳原子上连接的羟基中的氢原子,容易自动迁移到烯键的另一个碳原子上,形成较为稳定的羰基化合物;有机分子内、有机分子间常可脱去水分子。
下列反应图式中,就有6步可以看作是脱水反应。
所有的反应条件和其它无机物都己略去。
请从图中推断化合物A、B、E、G的结构简式。
(1)A是;B是;E是;G(有6元环)是。
(2)写出B与乙二酸反应可能的化学方程式。
2、二元醇、酸的脱水方式:乳酸分子式为C3H6O3,在一定的条件下可发生许多化学反应,下图是采用化学方法对乳酸进行加工处理的过程,其中A、H、G为链状高分子化合物。
新课标高中化学人教版选择性必修123册知识解析〖酯化反应的类型〗

酯化反应的类型1.生成链状酯(1)一元羧酸与一元醇的反应CH3COOH+CH3CH2OH CH3COOC2H5+H2O (2)一元羧酸与二元醇或二元羧酸与一元醇的反应(3)无机含氧酸与醇形成无机酸酯2.生成环状酯(1)多元醇与多元羧酸进行分子间脱水形成环酯(2)羟基酸分子间脱水形成环酯(3)羟基酸分子内脱水形成环酯3.生成聚酯二元羧酸和二元醇通过酯化反应生成聚酯;分子内同时含醇羟基和羧基的有机物也可通过酯化反应生成聚酯(相关反应在后面学习)。
典例详析例1(郑州一中期中)吗啡与海洛因都是被严格查禁的毒品,已知吗啡的分子式是C17H19NO3,海洛因是吗啡的二乙酸酯,则海洛因的分子式是A.C21H23NO3B.C21H22NO5C.C21H23NO5D.C21H27NO7解析◆酯化反应中,1个羧基与1个羟基反应形成1个酯基的同时生成1分子水,则含有1个酯基的酯的分子中总原子数是羧酸和醇分子中原子总数减去3(2个氢原子和1个氧原子),以此类推。
根据题意:海洛因是吗啡的二乙酸酯,即1个吗啡分子与2个乙酸分子反应生成含有2个酯基的海洛因分子,其分子式是(C17H19NO3+2×C2H4O2-2H2O)=C21H23NO5。
答案◆C例2(福建福州模拟)如图3-3-5甲所示的有机物在一定条件下能发生水解反应生成两种有机物,乙中用①~⑥标出该有机物分子中不同的化学键,则该有机物在水解时,断裂的键是图3-3-5A.①④B.③⑤C.②⑥D.②解析◆该有机物中含有酯基,酯基的形成方式是酸脱羟基醇脱氢,所以酯水解则是从虚线处断裂,羰基结合羟基得羧酸、氧原子结合氢原子得醇,综上可知,该有机物水解时从③⑤处断裂化学键,B项符合题意。
答案◆B点评◆酯的水解反应是酯化反应的逆反应,酯化反应时结合的键即是酯水解时断开的键。
医本有机化学第8章羟基酸和酮酸

羟基酸的代表化合物
H2C HO C H2C COOH HC COOH COOH COOH H HO C 酶 +H2O HC H2C COOH COOH COOH COOH COOH 酶 C COOH -H2O H2C COOH O C 氧化酶 -2H HC H2C COOH COOH COOH
顺-乌头酸 脱羧 -CO2 O C H2C
H CH3 C C COOH O
O
+ CO2
O
CH3 C CH2
+ CO2
酮式-烯醇式互变异构现象
乙酰乙酸乙酯的制备:
O H3C C O C2H5 H CH2
NaOC2H5
O C O C2H5
O
O
H3C C CH 2 C O C2H5 + H5C2 OH
乙酰乙酸乙酯或β-丁酮酸乙酯
Claisen酯缩合反应 凡有α− H的酯,在醇钠作用下都可发生 Claisen酯缩合反应。
-COOH > -SO3H > (RCO)2O > -COOR > -COX > -CONH2 > -CN > -CHO > -CO- >-OH > ArOH > -NH2 > C-O-C > >C=C< > C C > -X
-R,-X,-NO2 不能作为母体基团,只能作为取代基命名
羟基酸的化学性质
受诱导效应、共轭效应和邻位效应的影响,
酚酸的化学性质
2.酚酸与三氯化铁显色反应 酚酸含有酚羟基,能与FeCl3水溶液发生颜色反 应。 COOH COOH
OH 浓 H 2SO 4 + (CH 3CO) 2O OCOCH 3 + CH 3COOH
第十四章 羟基酸
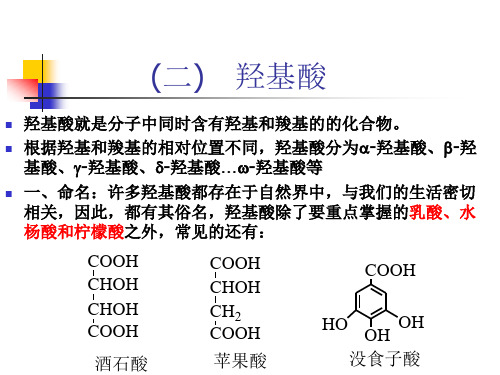
B rC H 2 C O O C 2 H 5 H 2O OH
R C H C H 2C O O C 2 H 5
2. -羟酸的制备
(3)类羟醛缩合反 具有-H的酯在二异丙氨基锂(LDA)作用下生成-碳负离子,然 后再与醛、酮缩合,水解后生成-羟基酯。
O LD A T H F ,-70℃ O C H 3C H C O C 2H 5 C 6H 5 C H O H3O OH O CH3 C 6 H 5 C H C H C O C 2H 5
(二) 羟基酸
羟基酸就是分子中同时含有羟基和羧基的的化合物。 根据羟基和羧基的相对位置不同,羟基酸分为-羟基酸、-羟 基酸、-羟基酸、-羟基酸…-羟基酸等 一、命名:许多羟基酸都存在于自然界中,与我们的生活密切 相关,因此,都有其俗名,羟基酸除了要重点掌握的乳酸、水 杨酸和柠檬酸之外,常见的还有:
COOH CHOH CHOH COOH 酒石酸 COOH CHOH CH2 COOH 苹果酸 HO OH OH 没食子酸 COOH
(二) 羟基酸的制备
二、制备: 1. -羟基酸的制备
Cl 2 P Cl HCN C CN OH (1 ) NaOH (2 ) H 3 O H 3O
(1 ) RCH 2 COOH
14.6 重要的羟基酸羧酸
COOH 1、乳酸 OH 2、酒石酸 3、水杨酸 具有酚羟基,能与FeCl3溶液显色,与乙酐反应生成乙酰水杨酸, 俗称“阿司匹林”。
COOH O H + (C H 3 C O ) 2 O COOH OCOCH3 + CH COOH 3
具有羧基,有酸性,能与Na2CO3反应放出CO2气体,能与甲醇 反应生成水杨酸甲酯,是“冬青油”的主要成份。
有机化学中的醇的酸催化脱水反应

有机化学中的醇的酸催化脱水反应在有机化学中,醇的酸催化脱水反应是一种常见而重要的转化反应。
它具有广泛的应用领域,包括有机合成、新药研发、材料科学等。
本文将详细介绍醇的酸催化脱水反应的原理、机制以及其在实际应用中的重要性。
一、醇的酸催化脱水反应的原理和机制酸催化脱水反应是通过引入强酸作为催化剂来促进醇分子中的羟基(—OH)与氢原子(—H)发生反应,去除一个水分子,形成一个双键(C=C)。
这个过程类似于酸催化下的酯化反应,但不同之处在于酯化反应中酸催化的是羧酸与醇的反应。
在醇的酸催化脱水反应中,强酸如硫酸(H2SO4)、磷酸(H3PO4)或盐酸(HCl)等通常被用作催化剂。
这些强酸具有很高的酸性,能够快速捕获醇分子中的羟基,并与之形成稳定的酸醇中间体。
酸醇中间体经过质子迁移和分子内重排等步骤,最终释放出水分子,生成烯烃。
二、醇的酸催化脱水反应的实际应用1. 有机合成中的应用醇的酸催化脱水反应在有机合成中具有广泛的应用。
它可以用于合成烯烃化合物,如烯烃烷化、烯烃的位点选择性烷基化等。
通过酸催化脱水反应,很多具有重要生物活性和药理活性的化合物得以合成,为新药研发提供了重要的合成路径。
2. 新药研发中的应用醇的酸催化脱水反应在新药研发中起着重要的作用。
通过有机合成中的酸催化脱水反应,可以合成出一系列的活性药物分子,如抗癌药物、抗生素、激素类药物等。
这些药物分子的合成通常需要进行复杂的化学转化,而醇的酸催化脱水反应常常是其中关键的步骤之一。
3. 材料科学中的应用醇的酸催化脱水反应还在材料科学中得到了广泛的应用。
通过该反应,可以合成出具有特定功能和结构的材料,如聚合物材料、功能性有机小分子等。
这些材料在能源领域、光电子领域、生物医学领域等都有着重要的应用潜力。
三、醇的酸催化脱水反应的优缺点1. 优点醇的酸催化脱水反应具有操作简便、反应条件温和、反应速率较快等优点。
由于醇在常温下较为稳定,酸催化反应通常在中性或几乎中性的条件下进行,避免了一些副反应的产生,提高了反应选择性。
12.1羟基酸的脱水反应
中性化合物
α-羟基酸的特征反应
12-01 羟基酸的脱水反应
R CH(CH2)nCOOH OH
二、 n = 1时,β-羟基酸,受热时分子内脱水生成α,β-不饱和酸。
RCH2 CHCH2COOH OH -H2O RCH2 CH=CHCOOH
不符合 saylzeff 规则,共轭体系,能量低。如:
R2CHCHCH2COOH OH
-01 羟基酸的脱水反应
R CH(CH2)nCOOH OH
三、 n = 2或3时,- 或 -羟基酸,受热时均发生分子内酯化脱水, 生成内酯和内酯。
CH2CH2CH2COH OH O
-H2O
O
O
12-01 羟基酸的脱水反应
R CH(CH2)nCOOH OH
12-01 羟基酸的脱水反应
主讲人:王刚
12-01 羟基酸的脱水反应
羟基酸对热敏感,遇热即发生脱水反应,但是随着分子中 羟基和羧基相对位置的不同,其脱水方式也各不相同
R CH(CH2)nCOOH OH
一、 n = 0时,α-羟基酸,受热分子间相互酯化,脱水成交酯
O R-CH-C-OH O H + H O HO-C-CH-R O H -2H2O O R O O R O
四、 n 4时,受热时发生分子间脱水,生成链状酯。
O mHO(CH2)nCOOH (m-1)H2O H O(CH2)nC OH m
羟基性质及脱水反应
羟基官能团的性质与有机物的脱水反应倪小重2012.09.04教学目标:使学生进一步理解羟基官能团的结构和主要反应,掌握羟基的各种脱水反应原理。
能力培养:通过复习归纳,使知识在头脑中有序贮存,提高迁移、转换、重组及分析、归纳的能力。
科学方法:讨论、归纳发散思维。
重点、难点通过羟基官能团的复习,掌握一些有机物脱水反应的原理。
教学过程设计教师活动【引言】我们学习各类重要的有机化合物,必须紧紧抓住物质的结构特征,特别是官能团的结构。
从官能团着手,理解物质的性质。
今天,我们复习羟基的性质及有机物的脱水反应。
【板书】一、羟基的性质:学生活动明确复习的内容。
领悟、思考。
【设问】我们知道醇、酚、羧酸分子结构中都有共同的官能团--羟基。
想一想:O-H键属哪一种类型的键?这三类物质中氢原子的活泼性有什么不同?而不同的原因又是怎样造成的?请举例分析说明。
思考回答:羟基中O-H键是一个强极性键,其中氢原子都具有一定的活泼性。
例如:都可以与金属钠等活泼金属反应,但它们的剧烈程度不同,反应最剧烈的是酸,其次是酚、醇。
造成氢原子的活泼性不同的原因是由于与羟基相连的基因吸引电子能力不同,由于吸引电子的能力是羰基>苯环>烷烃基。
因此,羧酸的羟基中氢的活泼性最大,具有弱酸性;与苯环相连的羟基中的氢活泼性次之,酚具更弱的酸性;醇的羟基中氢的活泼性最小,醇不显酸性。
【评价】对学生的回答给予肯定。
【投影】下列反应能否发生,能反应的请完成反应的化学方程式。
乙醇与金属钠苯酚与金属钠乙醇与氢氧化钠苯酚与氢氧化钠醋酸与碳酸钠苯酚与碳酸钠同学回答并到黑板上书写。
2C2H5OH+2Na→2C2H5ONa+H22C6H5OH+2Na→2C6H5ONa+H2C2H5OH+NaOH→不反应C6H5OH+NaOH→C6H5ONa+H2O2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2OC6H5OH+Na2CO3→C6H5ONa+NaHCO3【小结】(1)键断裂,可提供H+,使之与Na或NaOH反应,但由于与羟基相连的基团吸引电子的能力不同,其提供H+的能力有很大区别。
羟基性质及脱水反应
羟基官能团的性质与有机物的脱水反应倪小重2012.09.04教学目标:使学生进一步理解羟基官能团的结构和主要反应,掌握羟基的各种脱水反应原理。
能力培养:通过复习归纳,使知识在头脑中有序贮存,提高迁移、转换、重组及分析、归纳的能力。
科学方法:讨论、归纳发散思维。
重点、难点通过羟基官能团的复习,掌握一些有机物脱水反应的原理。
教学过程设计教师活动【引言】我们学习各类重要的有机化合物,必须紧紧抓住物质的结构特征,特别是官能团的结构。
从官能团着手,理解物质的性质。
今天,我们复习羟基的性质及有机物的脱水反应。
【板书】一、羟基的性质:学生活动明确复习的内容。
领悟、思考。
【设问】我们知道醇、酚、羧酸分子结构中都有共同的官能团--羟基。
想一想:O-H键属哪一种类型的键?这三类物质中氢原子的活泼性有什么不同?而不同的原因又是怎样造成的?请举例分析说明。
思考回答:羟基中O-H键是一个强极性键,其中氢原子都具有一定的活泼性。
例如:都可以与金属钠等活泼金属反应,但它们的剧烈程度不同,反应最剧烈的是酸,其次是酚、醇。
造成氢原子的活泼性不同的原因是由于与羟基相连的基因吸引电子能力不同,由于吸引电子的能力是羰基>苯环>烷烃基。
因此,羧酸的羟基中氢的活泼性最大,具有弱酸性;与苯环相连的羟基中的氢活泼性次之,酚具更弱的酸性;醇的羟基中氢的活泼性最小,醇不显酸性。
【评价】对学生的回答给予肯定。
【投影】下列反应能否发生,能反应的请完成反应的化学方程式。
乙醇与金属钠苯酚与金属钠乙醇与氢氧化钠苯酚与氢氧化钠醋酸与碳酸钠苯酚与碳酸钠同学回答并到黑板上书写。
2C2H5OH+2Na→2C2H5ONa+H22C6H5OH+2Na→2C6H5ONa+H2C2H5OH+NaOH→不反应C6H5OH+NaOH→C6H5ONa+H2O2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2OC6H5OH+Na2CO3→C6H5ONa+NaHCO3【小结】(1)键断裂,可提供H+,使之与Na或NaOH反应,但由于与羟基相连的基团吸引电子的能力不同,其提供H+的能力有很大区别。
羟基羧基脱水缩合
羟基羧基脱水缩合羟基羧基脱水缩合是一种重要的有机合成反应,它可以通过将羟基和羧基在合适的条件下进行脱水缩合来形成酯键。
这种反应在有机合成中具有广泛的应用,可以用于合成酯类化合物、脂肪酸等多种有机化合物。
羟基羧基脱水缩合反应是通过引入脱水剂来实现的,常用的脱水剂有DCC(二氯代膦酰胺)和EDC(1-(3-二甲基氨基丙基)-3-乙基碳二亚胺)等。
这些脱水剂可以与羟基和羧基发生反应,形成活化的酰胺中间体,然后再发生脱水缩合反应,生成酯键。
羟基羧基脱水缩合反应的反应条件通常包括适当的温度、pH值和反应时间等。
一般而言,较低的温度有助于控制反应速度和产物选择性,而较高的温度可能会导致副反应的发生。
pH值的选择也非常重要,过高或过低的pH值都可能影响反应的进行。
此外,反应时间的选择应根据具体反应体系的特点来确定。
羟基羧基脱水缩合反应在有机合成中具有广泛的应用。
首先,它可以用于合成酯类化合物。
酯类化合物在化学和生物学领域中具有重要的应用,例如作为溶剂、催化剂和药物等。
其次,羟基羧基脱水缩合反应还可以用于合成脂肪酸。
脂肪酸是生物体内的重要组成部分,对于维持生物体正常功能具有重要作用。
此外,羟基羧基脱水缩合反应还可以用于合成其他有机化合物,如酮类、醚类等。
羟基羧基脱水缩合反应的优点在于反应条件温和,反应选择性高,产物纯度较高。
同时,该反应的反应物易于获取,反应过程相对简单,操作方便。
因此,羟基羧基脱水缩合反应在有机合成中被广泛应用,并且已经发展出多种改进和变种反应。
羟基羧基脱水缩合是一种重要的有机合成反应,它可以通过脱水缩合反应形成酯键。
该反应具有广泛的应用领域,可以用于合成酯类化合物、脂肪酸等多种有机化合物。
在有机合成中,我们可以根据具体需要选择合适的脱水剂和反应条件,以实现高效、高选择性的反应。
通过对羟基羧基脱水缩合反应的研究和应用,可以为有机合成提供更多的方法和策略。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
羟基酸对热敏感,遇热即发生脱水反应,但是随着分子中 羟基和羧基相对位置的不同,其脱水方式也各不相同
R CH(CH2)nCOOH OH
一、 n = 0时,α-羟基酸,受热分子间相互酯化,脱水成交酯
O R-CH-C-OH O H + H O HO-C-CH-R O H -2H2O O R O O R O
四、 n 4时,受热时发生分子间脱水,生成链状酯。
O mHO(CH2)nCOOH (m-1)H2O H O(CH2)nC OH m
中性化合物
α-羟基酸的特征反应
12-01 羟基酸的脱水反应
R CH(CH2)nCOOH OH
二、 n = 1时,β-羟基酸,受热时分子内脱水生成α,β-不饱和酸。
RCH2 CHCH2COOH OH -H2O RCH2 CH=CHCOOH
不符合 saylzeff 规则,共轭体系,能量低。如:
R2CHCHCH2COOH OH
-H2 O
RCH=CHCH2COOH
x
12-01 羟基酸的脱水时,- 或 -羟基酸,受热时均发生分子内酯化脱水, 生成内酯和内酯。
CH2CH2CH2COH OH O
-H2O
O
O
12-01 羟基酸的脱水反应
R CH(CH2)nCOOH OH
