乙酰水杨酸的制备
乙酰水杨酸(阿司匹林)的制备 111

实验:乙酰水杨酸(阿司匹林)的制备教学方案教学目的:1、通过乙酰水杨酸的合成,初步了解有机合成中的乙酰化学反应原理及方法。
2、巩固减压过滤的操作。
3、进一步掌握用重结晶的方法来提纯固体有机化合物。
基本原理:水杨酸是一个双官能团的化合物(具有酚羟基和羧基)。
因此,有两种不同的酯化反应。
为了合成乙酰水杨酸,采用在强酸存在下,水杨酸和过量乙酸酐反应,水杨酸的酚羟基发生酯化。
反应结果可以看成是在水杨酸分子中引入个乙酰基。
这种在有机分子中引入酰基的反应称为酰基化反应。
若引入乙酰基就称为乙酰化反应。
提供酰基的试剂称为酰化剂,本实验中乙酸酐就是乙酰化试剂。
由于水杨酸是双官能团化合物,分子中的酚羟基和羧基彼此之间亦能起反应,生成少量的聚合物。
乙酰水杨酸能与碳酸氢钠反应生成水溶性钠盐,而副产物聚合物不能溶于碳酸氢钠,这种性质上的差别可用于阿司匹林的纯化。
可能存在于最终产物中的杂质是水杨酸本身,这是由于乙酰化反应不完全或由于产物在分离步骤中发生水解造成的。
它可以在各步纯化过程和产物的重结晶过程中被除去。
与大多数酚类化合物一样,水杨酸可以与三氯化铁形成深色络合物;阿司匹林因酚羟基已被酰化,不再与三氯化铁发生颜色反应,因此杂质很容易被检出。
本实验除采用三氯化铁鉴定纯度外,还可用测定熔点法来判断纯度。
实验药品:COOHOH COOHO +(CH 3CO)2OH+C CH 3O+CH 3COOH水杨酸,乙酸酐,浓硫酸,浓盐酸,饱和碳酸氢钠溶液,1%FeCl3 溶液主要试剂及产物的物理常数:名称分子量性状折光率比重熔点沸点溶解度:克/100mL 溶剂水醇醚水杨酸138.12 白色结晶粉末1.443156℃‐159℃易溶溶溶乙酸酐102.09 无色透明液体1.45 1.08 ﹣73.1℃138.6℃微溶易溶易溶乙酰水杨酸108.16白色结晶粉末135℃微溶易溶微溶浓硫酸无色油状液体1.84 ﹣90.8℃338℃易溶实验步骤(一)酰化反应1、称取2.0g(约0.014mol)固体水杨酸,放入125ml锥形瓶中,加入5.4g(5ml,0.05mol)乙酐,用滴管加入5滴浓H2SO4,摇匀。
乙酰水杨酸的制备原理方程式

乙酰水杨酸的制备原理方程式1. 引言乙酰水杨酸,听起来高大上吧?其实就是我们日常生活中常见的阿司匹林。
没错,就是那个能让你头痛不再的“救星”。
今天咱们就来聊聊它的制备原理和方程式,让大家对这位“药界明星”有个更深入的了解。
2. 乙酰水杨酸的制备过程2.1 原材料的准备首先,咱们得有两样主角:水杨酸和乙酸酐。
水杨酸就像那种清新脱俗的文艺青年,而乙酸酐呢,就像个充满活力的舞者,二者一结合,火花四射!你可能会想,这两个材料可真是绝配。
2.2 反应过程那么,这个反应到底是怎么发生的呢?简单来说,水杨酸的羟基(OH)和乙酸酐中的乙酰基发生了亲核取代反应。
在这个过程中,水杨酸的羟基被取代成乙酰基,最终形成了乙酰水杨酸。
简直就像一场精妙的化学舞蹈,每个分子都在跳着自己的舞步。
3. 反应方程式3.1 化学方程式好了,话不多说,直接进入重头戏!反应的化学方程式可以写成:C7H6O3 + C4H6O3 → C9H8O4 + C2H4O 。
看,这一长串化学式是不是让你眼花缭乱?别担心,咱们来慢慢拆解。
左边是水杨酸和乙酸酐,右边则是乙酰水杨酸和水。
你瞧,这一转眼,水就“悄无声息”地跑了出去,剩下的就是咱们心心念念的乙酰水杨酸了。
3.2 反应条件为了让这场“舞会”顺利进行,还需要一些特定的条件。
比如,加热一下,温度要合适,最好在60到70摄氏度之间。
而且,搅拌也很重要,就像要让一锅汤煮得匀称,不能让某一部分太热,而另一部分还冷冰冰的。
4. 乙酰水杨酸的性质4.1 药理作用你知道乙酰水杨酸为什么这么受欢迎吗?它的抗炎、镇痛、解热的效果可是杠杠的!就像是你工作一天后,喝上一杯冰镇饮料,清爽无比,让人顿时神清气爽。
尤其是当你头疼时,它简直是“救世主”。
4.2 使用注意不过,话说回来,药虽然好,但也得适度使用。
小心别像小孩一样,见了糖就直冲,乱吃乱喝可不行!过量服用可是会有副作用的,比如胃肠不适等。
像这样,大家在用药时可得三思而后行哦!5. 总结总之,乙酰水杨酸的制备过程就像一出精心编排的舞蹈,分子们在化学反应中翩翩起舞,最终合成了这种神奇的药物。
乙酰水杨酸的制备实验报告

胡雨露
一:实验步骤及现象:
实验步骤
实验现象
在100ml圆底烧瓶中;加入干燥的水杨酸2.0g和新蒸的乙酸酐5ml;再逐滴滴加5滴浓硫酸;充分摇动..
水杨酸溶解;溶液无色
水浴加热;保持瓶内温度在85-90℃之间;并缓慢摇动;维持5-10min..
溶液逐渐出现微弱的褐色
取出圆底烧瓶;室温冷却;加50ml水;搅拌;之后在冰水浴中冷却;并用玻璃棒摩擦瓶壁..
室温冷却无晶体析出;冰水浴冷却出现大量白色晶体..
抽滤;冷水洗涤几次;抽干
粗产品置于100ml烧杯中;缓慢加分溶解;并产生大量气体;溶液上漂浮有白色不溶物质..
用无颈漏斗过滤;将滤液转移至100ml烧杯中;缓慢加入15ml 4mol/L的盐酸;边加边搅拌;然后置于冷水浴中..
加盐酸有大量气泡产生;在冷水浴中有白色晶体析出..
抽滤;并用冷水洗涤2-3次;抽干..将晶体转移到表面皿上;干燥25min;称量..
取少量的乙酰水杨酸晶体;加入盛有5ml水的试管中;加入1-2滴FeCl3;观察颜色有无变化..
颜色无变化..
熔点测定:用毛细管开口一端填装样品;大约填装2-3mm左右;酒精灯封口;放入熔点仪中测定熔点
熔点没有测出;可能仪器的原因..
二.实验数据记录与处理
记录
计算
理论质量/g
实际质量/g
产率/%
乙酰水杨酸
2.6
1.5
58%
说明:本实验中乙酸酐过量;计算产率以水杨酸为基准
理论质量=2/138.12×180.15=2.6g
产率=1.5÷2.6×100%=58%
三.实验思考
乙酰水杨酸微溶于水;用水洗涤过多;少量产物溶解;影响产率..其次;反应不完全以及副产物的生成也降低了产率..在熔点测定中;没有测出熔点;可能因为装样过少或者熔点仪有问题..
乙酰水杨酸的制备实验报告

乙酰水杨酸的制备实验报告实验目的,通过乙酰化反应制备乙酰水杨酸,并对其纯度进行分析。
一、实验原理。
乙酰水杨酸是一种重要的有机合成中间体,可以用于制备阿司匹林等药物。
其制备原理是将水杨酸与乙酸酐在酸催化下发生酯化反应,生成乙酰水杨酸和醋酸。
二、实验步骤。
1. 将水杨酸和乙酸酐按摩尔比1:1加入反应瓶中;
2. 加入少量硫酸作为催化剂;
3. 在冰浴中搅拌反应混合物,控制温度在5-10摄氏度;
4. 反应结束后,用冰水淘洗得到的沉淀;
5. 用乙酸乙酯洗涤沉淀,得到乙酰水杨酸;
6. 对产物进行结晶、干燥,得到纯净的乙酰水杨酸。
三、实验结果。
通过红外光谱分析和熔点测定,得到的乙酰水杨酸样品与标准品的纯度相近,符合要求。
四、实验总结。
本实验成功制备了乙酰水杨酸,并对其纯度进行了分析。
通过实验,掌握了乙酰化反应的操作技巧,提高了对有机合成反应的理解和掌握。
五、实验注意事项。
1. 反应过程中要控制温度,避免产生副反应;
2. 实验操作要细致,避免产物受到杂质污染;
3. 实验后要及时清洗实验器皿,保持实验环境整洁。
六、参考文献。
1. 《有机化学实验》,XXX,XXX出版社,XXXX年。
2. 《有机合成实验指导》,XXX,XXX出版社,XXXX年。
以上为乙酰水杨酸的制备实验报告。
乙酰水杨酸的制备
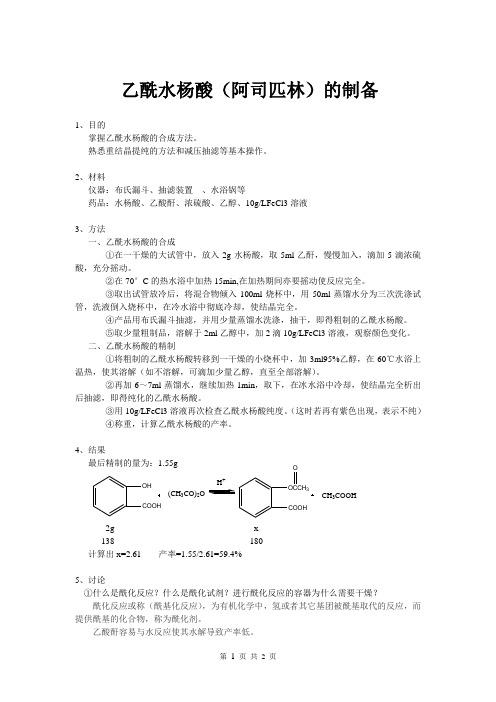
乙酰水杨酸(阿司匹林)的制备1、目的掌握乙酰水杨酸的合成方法。
熟悉重结晶提纯的方法和减压抽滤等基本操作。
2、材料仪器:布氏漏斗、抽滤装置 、水浴锅等药品:水杨酸、乙酸酐、浓硫酸、乙醇、10g/LFeCl3溶液3、方法一、乙酰水杨酸的合成①在一干燥的大试管中,放入2g 水杨酸,取5ml 乙酐,慢慢加入,滴加5滴浓硫酸,充分摇动。
②在70°C 的热水浴中加热15min,在加热期间亦要摇动使反应完全。
③取出试管放冷后,将混合物倾入100ml 烧杯中,用50ml 蒸馏水分为三次洗涤试管,洗液倒入烧杯中,在冷水浴中彻底冷却,使结晶完全。
④产品用布氏漏斗抽滤,并用少量蒸馏水洗涤,抽干,即得粗制的乙酰水杨酸。
⑤取少量粗制品,溶解于2ml 乙醇中,加2滴10g/LFeCl3溶液,观察颜色变化。
二、乙酰水杨酸的精制①将粗制的乙酰水杨酸转移到一干燥的小烧杯中,加3ml95%乙醇,在60℃水浴上温热,使其溶解(如不溶解,可滴加少量乙醇,直至全部溶解)。
②再加6~7ml 蒸馏水,继续加热1min ,取下,在冰水浴中冷却,使结晶完全析出后抽滤,即得纯化的乙酰水杨酸。
③用10g/LFeCl3溶液再次检查乙酰水杨酸纯度。
(这时若再有紫色出现,表示不纯) ④称重,计算乙酰水杨酸的产率。
4、结果最后精制的量为:1.55g2g x138 180计算出x=2.61 产率=1.55/2.61=59.4%5、讨论①什么是酰化反应?什么是酰化试剂?进行酰化反应的容器为什么需要干燥? 酰化反应或称(酰基化反应),为有机化学中,氢或者其它基团被酰基取代的反应,而提供酰基的化合物,称为酰化剂。
乙酸酐容易与水反应使其水解导致产率低。
OH COOH (CH 3CO)2O H +OCCH 3COOH OCH 3COOH②前后两次用FeCl3检测,其原理是什么?FeCl3与酚羟基反应显色。
6、结论第一步中没有用冰水浴而产生的结晶不彻底,导致实验结果偏小。
乙酰水杨酸的制备的实验报告

乙酰水杨酸的制备的实验报告乙酰水杨酸的制备实验报告
一、实验目的
本实验旨在通过将水杨酸与乙酸酐反应制备乙酰水杨酸,从而了解在实验条件下化合物的制备方法及其反应机理。
二、实验原理
本实验原理基于羧酸类化合物与酸酐类化合物的酰化反应。
水杨酸的羟基与乙酸酐的酰基发生酰化反应,生成乙酰水杨酸和乙酸。
三、实验步骤
1、选取一随意量的水杨酸,加入适量的乙酸酐中,搅拌均匀。
2、加入几滴浓硫酸,加入适量蒸馏水,搅拌均匀。
3、将其加热煮沸,使这种混合物在常压下失去酸酐的气体,制备乙酰水杨酸。
4、过滤固体,重结晶,获得纯净的乙酰水杨酸。
四、实验结果
在实验过程中,我们观察到混合物开始发生沉淀,并最终生成了纯净的白色乙酰水杨酸固体。
在对纯化过程中,我们可以通过将乙酰
水杨酸溶解在乙酸中,然后使其慢慢结晶到纯净的结晶物。
最终,我
们得到了高度纯化且非常纯净的乙酰水杨酸固体。
五、实验结论
通过实验结果,我们成功地制备出了纯净的乙酰水杨酸固体。
这
个过程不仅可以向我们展示出在一定条件下羧酸和酸酐的反应机制,
同时也表明了在实验条件下化合物的制备必须非常小心和谨慎。
最后还要提醒一点,乙酰水杨酸是一种有毒的物质,请谨慎使用,并在实验后立即将实验器材清洗干净,防止实验污染对其它活动产生
影响。
乙酰水杨酸的制备
合成过程中注意加样顺序!
8滴浓硫酸 滴浓硫酸
70~80℃水浴 ℃ 振摇,加热 振摇,加热10min
边加边摇
冷却至室温
(可用自来水降温) 可用自来水降温)
30mL水 水
减压过滤 冰浴结晶 蒸馏水洗涤2 蒸馏水洗涤2~3次 粗品
(检查纯度 检查纯度) 检查纯度
9
2. 乙酰水杨酸粗品的纯化(重结晶) 乙酰水杨酸粗品的纯化(重结晶)
重结晶溶剂:乙醇 水 重结晶溶剂:乙醇----水
6
3. 纯度检查
酚羟基 + FeCl3 颜色反应
最可能存在于最终产物中的杂质是水杨酸本身, 最可能存在于最终产物中的杂质是水杨酸本身,它的存 水杨酸本身 在是由于乙酰化反应不完全,或者由于产物在分离步骤 在是由于乙酰化反应不完全, 中发生水解造成的。 中发生水解造成的。 水杨酸像大多数酚一样, 离子形成深色络合物。 水杨酸像大多数酚一样,与Fe3+离子形成深色络合物。
OH O H
3
O
注意: 注意: 1. 反应温度不宜过高,否则将增加副产物的生成: 反应温度不宜过高,否则将增加副产物的生成:
O
OH
OCCH3
C O
O COOH
C O
O COOH
水杨酸水杨酸酯
乙酰水杨酰水杨酸酯
4
2. 在生成乙酰水杨酸的同时,水杨酸分子间可 在生成乙酰水杨酸的同时, 发生缩合反应,生成少量的聚合物。 发生缩合反应,生成少量的聚合物。
15
2
二、基本原理: 基本原理:
1.乙酰水杨酸的制备 乙酰水杨酸的制备
OHΒιβλιοθήκη +COOH
H3C
O C
O
O C
乙酰水杨酸的制备
乙酰水杨酸的制备一、实验目的1.能运用已学知识查阅相关资料及工具书,熟悉实验原理。
2.能独立设计实验方案(包括实验方法、主要仪器及试剂、主要实验步骤及实验装置图等)。
3.了解乙酰水杨酸制备的反应原理和实验方法。
4.通过乙酰水杨酸制备实验,初步熟悉有机化合物的分离、提纯等方法。
5.巩固称量、溶解、加热、结晶、洗涤、重结晶等基本操作。
二、实验原理将水杨酸与乙酐作用,通过乙酰化反应,使水杨酸分子中酚羟基上的氢原子被乙酰基取代生成乙酰水杨酸。
加入少量浓硫酸作催化剂,其作用是破坏水杨酸分子中羧基与酚羟基间形成的氢键,从而使酰化反应容易完成。
水杨酸分子中含羟基(—OH)、羧基(—COOH),具有双官能团。
本实验采用以强酸为硫酸为催化剂,以乙酐为乙酰化试剂,与水杨酸的酚羟基发生酰化作用形成酯。
反应如下:M=138.12 M=102.09 M=180.15 M=60.05反应原理:副反应:OOHOH2OHC OOOOH +OH 2OOHOC OCH3OOHOH+OC OCH3C OOO OH乙酰水杨酸能溶于碳酸氢钠水溶液,而副产物不能溶于碳酸氢钠水溶液,这种性质上的差别可用于阿司匹林的纯化。
可能存在于最终产物中的杂质可能是水杨酸本身,这是由于乙酰化反应不完全或由于产物在分离步骤中发上水解造成的。
它可以在各步纯化过程中和产物的重结晶过程中被除去。
与大多数酚类化合物一样,水杨酸可与三氯化铁形成配合物;阿司匹林因酚羟基已被酰化,不再与三氯化铁发生颜色反应,因此杂质很容易被检出。
本实验用FeCl3检查产品的纯度,此外还可采用测定熔点的方法检测纯度。
杂质中有未反应完酚羟基,遇FeCl3呈紫蓝色。
如果在产品中加入一定量的FeCl3,无颜色变化,则认为纯度基本达到要求。
三、实验药品与仪器药品:水杨酸5.00g(0.036mol),乙酸酐8.64g (8mL ,0.08mol),饱和NaHCO3(aq),4mol/L盐酸,浓流酸,冰块,蒸馏水,1%FeCl3 。
乙酰水杨酸的制备ppt课件 22页PPT文档
反应时间为30min
乙酰水杨酸的制取
1
在100mL锥形瓶 中加入7.5mL乙 酸酐,一定量的 硫酸铝钾,恒温 搅拌使硫酸铝钾 溶解
2
再加入5.4g干燥 的水杨酸充分振 荡使水杨酸溶解 70℃水浴加热30 分钟,不断搅拌
3
冷却,加20mL 冷蒸馏水,不断 搅拌数分钟,置 于冷水浴中冷却 出现白色晶体
乙酰水杨酸的制备
汇报人 陈彬清 樊威
目 录
CONTENTS
01 实验目的 02 实验原理 03 实验仪器与试剂 04 实验步骤
01
PART 01
第一部分
实验目的
1
掌握乙酰化反应 的原理
实验目的
2
学习乙酰水杨酸 的制备方法
3
巩固溶解、加热、 结晶、洗涤、重
结晶等操作
02
PART 02
第二部分
实验原理
实验原理
12345
乙酰水杨酸又称为阿司匹林,是一种历史悠久的解热镇痛药, 乙酰水杨酸治疗范围极广,包括发烧、疼痛、偏头痛、急性风 湿、心包炎等疾病,甚至有研究表明每天服用低剂量(75至300 毫克)乙酰水杨酸能在三年内减少癌症发病率四分之一,并且 在五年之内把癌症引起的死亡率降低15%。
实验原理
对设备的腐蚀性 大 易•输, 产入污 生文染 副字环反内境应容 ,使 产•输品入泛文淡字红内而容 不 利于提纯
因•输此入对文催字化内剂容的 使•输用入进文行字改内进容
实验原理
对传统方法进行改进
查询文献对比各催化剂的利弊,以及考 虑到实验条件的限制,最终选择以硫酸 铝钾为催化剂在传统方法的基础上制备 乙酰水杨酸。
实验原理
1
硫酸铝钾分子体积较
阿司匹林乙酰水杨酸的制备
产率计算:理论产量:2.6 g 实际产量:? 产率:产率 = ?/2.6×100 % = ?
五、注意事项
1.仪器要全部干燥,ห้องสมุดไป่ตู้品也要实现经干燥处理,醋酐要使用新蒸馏的,收集139~140℃的馏分。 2.本实验中要注意控制好温度(水温<90℃),否则将增加副产物的生成,如水杨酰水杨酸、乙酰水杨酰水杨酸、乙酰水杨酸酐等。
六、思考题
反应容器为什么要干燥无水? 何谓酰化反应?常用的酰化剂有哪些? 通过什么样的简便方法可以鉴定出阿斯匹林是否变质? 本实验中可产生什么副产物?
反应式:
由于水杨酸是一个双官能团化合物,一个官能团为酚羟基,另一个是羧基,因此可以形成少量的高聚物。在酰化过程中生成一种乙酰水杨酸酐副产物,这些微量杂质是引起 哮喘、等麻疹等的过敏源物质。为了除去这部分杂质,可先将乙酰水杨酸变为钠盐,再利用高聚物不溶于水的性质将它们分开。
相关知识介绍:
易
139.35(l)
102.09
醋酐
易
易
微
158(s)
138
水杨酸
醚
醇
水
m.p.或b.p. /℃
M
Name
四、实验步骤
2g水杨酸+5g乙酸酐+5滴浓硫酸,振摇溶解→70~80 ℃水浴加热5~10min,冷却→加水50ml析出晶体,洗涤得粗品。 粗品→加25ml饱和碳酸钠,搅拌至无CO2放出→布氏漏斗过滤,用水冲洗→3~5ml浓HCl+10mlH2O+滤液,冰水浴,析出晶体→吸滤,冷水洗2次,干燥,得精品。 干燥、称量,计算产率。
实 验 六 阿司匹林 (乙酰水杨酸) 的制备
一、实验目的 1.学习用乙酸酐作酰基化试剂酰化 水杨酸制乙酰水杨酸的酯化方法。 2.巩固重结晶,熔点测定,抽滤等基 本操作。 3.了解乙酰水杨酸的应用价值。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
反应,是水杨酸分子中酚羟基上的氢原子被乙酰基取代生成乙酰水
杨酸。加入少量浓硫酸作催化剂,其作用是破坏水杨酸分子中羧基 和酚羟基形成的氢键,从而使酰化反应容易完成。 反应方程式如下:
实验原理
传统方法存在的缺陷
对设备的腐蚀性 大,污染环境, •输入文字内容 易产生副反应使 •输入文字内容 产品泛淡红而不 利于提纯
浓盐酸 95%乙醇
1%三氯化铁溶 液
实验仪器
01
锥形瓶
02
抽滤瓶
03
布氏漏斗
04
水浴锅
04
PART 04
实验步骤
第四部分
制备的最佳条件
反应时间为30min
恒温70℃ n(水杨酸) :n(乙 酸酐)=1.0 :2.0 催化剂的用量为0.6g
乙酰水杨酸的制取
1
在100mL锥形瓶 中加入7.5mL乙 酸酐,一定量的 硫酸铝钾,恒温 搅拌使硫酸铝钾 溶解
•阿司匹林的制备研究(侯德顺 钟红梅)
•乙酰水杨酸合成方法改进(李 远军 陈丽)
乙酰水杨酸制备实验的改进(
肖佳薇 朱团 潘亮)
•乙酰水杨酸的制备(耿涛 蔡红 蔡艳飞) 阿司匹林合成催化剂研究进 展(周卫国 莫清 吴颖等)
•乙酰水杨酸的制备探索(冉旗 王凯 林成等) 乙酰水杨酸(阿司匹林)的制备 (王嘉林 周迎春 张鸿)
传统上用浓硫酸 作催化剂的缺陷
•输入文字内容 因此对催化剂的 使用进行改进 •输入文字内容
实验原理
对传统方法进行改进
查询文献对比各催化剂的利弊,以及考
虑到实验条件的限制,最终选择以硫酸
铝钾为催化剂在传统方法的基础上制备
乙酰水杨酸。
实验原理
1 硫酸铝钾分子体积较 大,分子中的质子极 易电离,是优良的质 子给予体 2 在均相反应中,质子 的酸性越强,越有利 于形成鎓盐 4
2
再加入5.4g干燥 的水杨酸充分振 荡使水杨酸溶解 70℃水浴加热30 分钟,不断搅拌
3
冷却,加20mL 冷蒸馏水,不断 搅拌数分钟,置 于冷水浴中冷却 出现白色晶体
4
抽滤,(虑液弃 去),所得的滤 渣为粗制的乙酰 水杨酸
乙酰水杨酸的纯化
01
将乙酰水杨酸粗产品加 入到饱和碳酸氢钠溶液 中 ,搅拌至无气泡,抽 滤 ,滤去聚合物
乙酰水杨酸的制备
汇报人 陈彬清 樊威
01
实验目的 实验原理 实验仪器与试剂 实验步骤
目 录
02 03 04
CONTENTS
01
PART 01
实验目的
第一部分
实验目的
1
掌握乙酰化反应 的原理
2
学习乙酰水杨酸 的制备方法
3
巩固溶解、加热、 结晶、洗涤、重 结晶等操作
02
PART 02
实验原理
第二部分
反
机
应
理
3
从而为其他亲核基 团的进攻提供了有 利条件
进而加快反应速度
反应原理
01
催化活性高
02
选择性好
使用硫酸铝钾 代替浓硫酸的 好处
04
03
原料价廉易得 对设备无腐蚀性 对环境无污染 催化效率比浓硫酸 强
05
03
PART 03
实验仪器与试剂
第三部分
实验试剂
水杨酸 乙酸酐 饱和碳酸氢钠 硫酸铝钾
感谢您的耐心观看
THANKS
02
滤液缓慢倒入盛有浓盐 酸的烧杯中 ,并不断搅 拌 ,有固体析出
03
将烧杯置于冰水浴中充 分冷却 ,使固体析出完 全
04
抽滤 ,干燥得到乙酰水 杨酸产品
合成产品的定性检验
将产品溶于 95% 乙醇中, 加入 2滴 1% 三氯化铁溶液
1
2
呈阴性反应 ,说明水杨酸在反应 中羟基已被酰化。
参考文献
•有机化学实验(陈红艳 丁来欣)
实验原理
1
2
3
Байду номын сангаас
4
5
乙酰水杨酸又称为阿司匹林,是一种历史悠久的解热镇痛药, 乙酰水杨酸治疗范围极广,包括发烧、疼痛、偏头痛、急性风 湿、心包炎等疾病,甚至有研究表明每天服用低剂量(75至300
毫克)乙酰水杨酸能在三年内减少癌症发病率四分之一,并且
在五年之内把癌症引起的死亡率降低15%。
实验原理
传统方法
