ALK基因突变和对应靶向药物
肺癌的基因突变与药物敏感性

肺癌的基因突变与药物敏感性肺癌是一种常见的恶性肿瘤,世界范围内每年有数百万人被诊断出患有这种疾病。
虽然早期诊断和治疗技术的进步,在肺癌治疗中取得了一定的成功,然而,由于复杂的病因和个体间的遗传变异,肺癌的治疗仍然面临很大的挑战。
近年来,研究人员发现,肺癌的发生和发展与基因突变密切相关。
基因突变是指基因序列发生异常改变,导致相关基因的功能异常或丧失。
肺癌中常见的基因突变包括EGFR、ALK、ROS1、KRAS等。
这些基因突变一方面参与了肺癌细胞的生长、分化和转移过程,另一方面也会导致肺癌对药物的敏感性发生改变。
EGFR基因突变被认为是最常见的肺癌驱动基因突变之一。
患有EGFR突变的肺癌患者通常对EGFR抑制剂具有显著的敏感性。
EGFR 抑制剂可以通过靶向抑制异常活跃的EGFR信号通路,从而阻断肿瘤细胞的生长和增殖,有效抑制肿瘤的发展。
相比之下,KRAS基因突变与对EGFR抑制剂的耐药性有关。
KRAS突变会导致EGFR抑制剂的治疗效果大大降低。
研究人员在探索KRAS突变与耐药性之间的关系时,发现了一些潜在的治疗策略,如KRAS信号通路的抑制和KRAS突变细胞的免疫治疗等。
此外,ALK和ROS1基因突变也经常在肺癌中被检测到。
这些突变导致了具有ALK突变或ROS1突变的肺癌患者对相应的靶向治疗药物(如ALK抑制剂和ROS1抑制剂)具有较好的反应。
这些抑制剂可以选择性地靶向抑制肿瘤细胞中异常活跃的ALK或ROS1信号通路,从而抑制肿瘤的生长和扩散。
基因突变与药物敏感性之间的关系也不仅仅局限于上述几个基因。
其他一些与肺癌发生相关的基因,如BRAF、HER2、MET等,也被发现与特定药物敏感性之间存在关联。
这些发现为肺癌的个体化治疗提供了新的思路和方法。
随着肺癌基因突变与药物敏感性之间关系的逐渐明确,精准医学在肺癌治疗中的应用也越来越广泛。
个体化治疗的核心是通过对患者的基因组学信息进行分析,为患者量身定制最合适的治疗方案。
alk融合靶向药原理

靶向药物和ALK融合靶向药物的基本原理1. 引言癌症是一类以细胞异常增殖和分化为特征的疾病。
传统的癌症治疗方法包括手术切除、放射治疗和化学治疗,这些方法对于一些癌症患者有效,但也存在一些局限性,如治疗效果不佳、毒副作用大等。
因此,研究人员开始寻找新的治疗方法,其中靶向药物是近年来获得广泛关注的一种新型治疗方法。
靶向药物是指通过特异性地作用于癌症细胞中的特定分子靶点,从而阻断肿瘤细胞的生长和增殖,并最终达到治疗癌症的目的。
在癌症治疗中,靶向药物已经取得了一些重要的进展,其中ALK融合靶向药物是一类针对ALK(Anaplastic Lymphoma Kinase)融合基因的靶向药物。
2. 癌症中的ALK融合基因ALK是一种酪氨酸激酶受体,正常情况下,在胚胎发育过程中起着重要的调控作用。
然而,一些癌症患者中的ALK基因发生融合,导致其产生异常的活性蛋白质。
这种ALK融合基因的产生与某些癌症的发生和发展密切相关。
ALK融合基因的产生通常是由于染色体异常,如染色体重排、染色体断裂等造成的。
这些染色体异常导致ALK基因与其他基因融合,形成一个新的融合基因。
这些融合基因产生的蛋白质具有异常的活性,可以促进癌细胞的生长和增殖。
3. 靶向ALK融合基因的靶向药物靶向ALK融合基因的靶向药物主要是通过与融合蛋白质相互作用来发挥药效。
这些靶向药物通常是小分子化合物或抗体,可以特异性地结合到融合蛋白质上,从而阻断其异常的活性,抑制癌细胞的增殖。
靶向ALK融合基因的靶向药物的研发通常经历以下几个步骤:3.1 靶点发现首先,研究人员需要确定可以针对ALK融合基因的靶点。
他们通常会通过基因测序等技术来鉴定癌症患者中的ALK融合基因类型,进而确定可以作为靶点的特定融合蛋白质。
3.2 药物筛选一旦确定了靶点,研究人员就可以开始进行药物筛选。
他们通常会利用高通量筛选技术,通过对大量化合物进行测试,筛选出能够特异性地结合到融合蛋白质上的化合物。
alk基因突变类型

alk基因突变类型
ALK基因是一种与多种癌症相关的基因,尤其是非小细胞肺癌(NSCLC)。
ALK基因突变是指该基因发生异常变异,导致蛋白质的结构或功能发生改变。
在癌症研究中,ALK基因突变主要涉及融合基因,即ALK基因与其他基因发生融合,产生异常的融合蛋白。
以下是一些与ALK基因相关的突变类型:
1.ALK融合基因:最常见的突变类型是ALK基因与其他基因的融合,形成融合蛋白。
例如,EML4-ALK是非小细胞肺癌中常见的一种ALK融合。
2.ALK基因点突变:除了融合外,ALK基因也可能发生点突变,即某些特定位置的碱基发生改变,导致蛋白质结构或功能的改变。
3.ALK基因扩增:在某些情况下,ALK基因可能会发生基因扩增,即复制多个拷贝,导致基因过度表达。
ALK基因突变的存在通常对肿瘤的治疗和预后产生影响。
针对ALK基因突变的药物,如ALK抑制剂,已经成为一些癌症治疗的重要手段,尤其是在非小细胞肺癌患者中。
alk靶点药物一二三代分类原则

ALK(酪氨酸激酶)是一种蛋白质,可以参与肿瘤的生长和转移。
针对ALK突变的肿瘤,已经开发出了多种靶向药物。
根据药物的开发历史和临床应用情况,ALK靶点药物一般分为一、二、三代三个代别。
一代ALK靶点药物:一代ALK抑制剂是最早出现的药物,如克唑替尼(Crizotinib)。
这类药物的作用机制是抑制ALK的酪氨酸激酶活性,从而阻断肿瘤细胞的生长和扩散。
但是,这些药物存在一定的耐药性,并且不能有效地穿过血脑屏障,因此对于存在脑转移的肿瘤治疗效果不佳。
二代ALK靶点药物:二代ALK抑制剂是在一代药物基础上进行改良的药物。
例如,里拉替尼(Lorlatinib)、布里加丙胺(Brigatinib)等。
这些药物可以抑制ALK的酪氨酸激酶活性,并且具有更强的候选性和更好的耐药性。
此外,这些药物可以穿过血脑屏障,并对存在脑转移的肿瘤具有更好的治疗效果。
三代ALK靶点药物:三代ALK抑制剂是最新开发的一类药物,例如沙可维替尼(Selpercatinib)。
这些药物不仅可以抑制ALK的酪氨酸激酶活性,还可以针对其他突变,如RET、ROS1等进行干预。
这些药物具有更高的选择性和更好的安全性,同时能够有效地穿过血脑屏障,对于存在脑转移的肿瘤具有较好的治疗效果。
总的来说,ALK靶点药物的一、二、三代分类主要根据药物的开发历史、作用机制、耐药性和临床应用效果等因素进行划分。
每一代药物都有其特点和优缺点,医生可以根据患者的具体情况进行选择和应用。
临床分析研究肺癌的基因突变与靶向治疗

临床分析研究肺癌的基因突变与靶向治疗肺癌是全球范围内的常见恶性肿瘤,其高发率和高致死率给人类健康带来了巨大的威胁。
随着分子生物学和基因组学的快速发展,科学家们逐渐揭示出肺癌发生和发展过程中的基因突变的重要作用。
基于理解基因突变的机制,靶向治疗成为了肺癌治疗领域的重要突破口。
本文将从临床分析的角度,探讨肺癌的基因突变与靶向治疗之间的关系。
一、基因突变与肺癌的关联肺癌中的基因突变常常与细胞增殖、凋亡和转移等关键生物学过程紧密相关。
通过临床研究,科学家们发现了一些与肺癌发生和发展密切相关的常见基因突变,比如EGFR、ALK、ROS1等。
这些基因突变可通过不同的途径引发肿瘤细胞的不控制增殖和抗凋亡能力,最终导致肺癌的恶变。
通过对这些基因突变的研究,科学家们为肺癌的靶向治疗提供了重要的方向和目标。
二、基因突变与靶向治疗1. EGFR突变与EGFR-TKI治疗EGFR基因突变在肺癌中具有重要的地位,其中最为典型的是EGFR激活突变。
近年来,EGFR酪氨酸激酶抑制剂(EGFR-TKI)作为一种靶向药物被广泛应用于临床。
通过与EGFR结合,EGFR-TKI可以有效抑制激活突变引起的肿瘤细胞的增殖,从而达到治疗肺癌的效果。
一些临床研究表明,EGFR-TKI在EGFR激活突变阳性的肺癌患者中显示出卓越的疗效,成为了一线治疗的首选药物。
2. ALK突变与ALK抑制剂治疗ALK基因突变是肺癌中的另一个重要靶点。
常见的ALK基因突变包括ALK融合基因和ALK点突变。
针对ALK突变的抑制剂可以通过抑制突变基因的活性,阻断肿瘤细胞的增殖和存活信号通路。
临床研究显示,ALK抑制剂对于ALK突变阳性的肺癌患者具有显著的治疗效果,并且副作用相对较小,因此在临床实践中得到了广泛应用。
3. ROS1突变与ROS1抑制剂治疗ROS1基因突变是肺癌中的另一个研究热点。
ROS1抑制剂可以抑制ROS1突变基因的活性,从而抑制肿瘤细胞的增殖和存活能力。
肺癌八大基因靶向药汇总
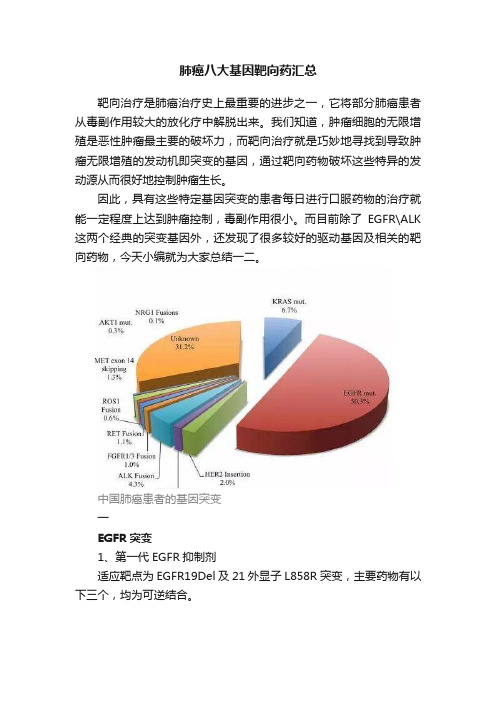
肺癌八大基因靶向药汇总靶向治疗是肺癌治疗史上最重要的进步之一,它将部分肺癌患者从毒副作用较大的放化疗中解脱出来。
我们知道,肿瘤细胞的无限增殖是恶性肿瘤最主要的破坏力,而靶向治疗就是巧妙地寻找到导致肿瘤无限增殖的发动机即突变的基因,通过靶向药物破坏这些特异的发动源从而很好地控制肿瘤生长。
因此,具有这些特定基因突变的患者每日进行口服药物的治疗就能一定程度上达到肿瘤控制,毒副作用很小。
而目前除了EGFR\ALK 这两个经典的突变基因外,还发现了很多较好的驱动基因及相关的靶向药物,今天小编就为大家总结一二。
中国肺癌患者的基因突变一EGFR突变1、第一代EGFR抑制剂适应靶点为EGFR19Del及21外显子L858R突变,主要药物有以下三个,均为可逆结合。
IPASS研究是一项比较吉非替尼和含铂化疗的临床试验,此研究首次证明EGFR突变状态是对吉非替尼疗效的强预测因子,奠定了肺癌靶向治疗的基石。
随后的First-SIGNAL、WJT0G3405、NEJSG002、OPTIMAL和EURTAC相继证实,存在EGFR突变的肺癌患者接受EGFR-TKIs疗效显著优于传统化疗,一线治疗的中位PFS达9-13个月,ORR为60%-85%,且不良反应及生活质量要显著优于化疗。
ICOGEN研究中,国产TKI凯美纳与吉非替尼头对头比较中,两者疗效相当。
入脑效果而言,CTONG0803研究结果证实厄洛替尼治疗NSCLC 脑转移的PFS为10.1个月,总体ORR为56.3%,治疗脑转移的效果在三者中首屈一指。
2、第二代EGFR抑制剂靶点为EGFR(包括19Del、L858R常见突变及罕见突变)、HER2及HER4,为不可逆结合。
基于LUX-LING 系列试验,阿法替尼获批以下适应症,具体见下表。
在Archer 1050研究中,达克替尼vs吉非替尼一线治疗EGFR+的NSCLC患者,两者PFS为14.7m vs 9.2m,OS为达克替尼34.1m vs 吉非替尼26.8m。
肺癌常见突变基因EGFR与ALK的认知

肺癌常见突变基因EGFR与ALK的认知肺癌是我国发病率最高,也是我国死亡率最高的癌症,而幸运的是在我国大约有40-50%的肺癌具有敏感基因突变,最常见的是EGFR突变及ALK融合突变(欧美10%),可以应用靶向药物治疗,EGFR/ALK靶点的突变应用靶向药物有效率高达70%,明显提高患者生存质量,提高生存期。
有效率虽然很高但总有一个跨不过去的坎那就是耐药。
一、EGFR(表皮生长因子受体)突变EGFR大家已经非常熟悉了,是非小细胞肺癌最常见的致癌基因,是目前肺癌靶向药物对应的主要驱动基因,常见的突变位点发生在18、19、20和21号外显子上。
最常见的有两种,一种是19号外显子的缺失(45%),另外一种是21号外显子L858R(40-45%)的突变。
针对EGFR突变的肺癌患者,比如19外显子缺失和L858突变,常用的药物一代EGFR抑制剂厄洛替尼、吉非替尼、埃克替尼和二代EGFR抑制剂阿法替尼,三代奥西替尼(9291),这些药物对EGFR 突变的非小细胞肺癌患者不错的药物。
但多数病人在使用第一代靶向药物1-2年时间内,就会出现耐药,肿瘤进展。
其中原因有四:1,60%的患者是由于出现继发耐药突变——T790M突变,一旦T790M突变,可以使用三代靶向药物奧希替尼(9291);2,20%的患者耐药是因为旁路激活,比如c-MET扩增,也就是说肿瘤细胞的增殖绕开了EGFR,走了另外一条路。
如果基因检测显示MET扩增或突变,可以应用克唑替尼;3,表型改变也是一代靶向药物产生耐药的一种情况,比如腺癌会向小细胞肺癌转化;4,EGFR驱动基因的下游信号通路激活,也会导致的原发耐药或者获得性耐药。
这种情况就要考虑化疗。
奧希替尼作为一代靶向药耐药后的选择,仍然会产生耐药。
比如继发C797S的共生突变,其他旁路激活等。
在EGFR突变的患者中,除了常见的19/21基因突变外,还有3种罕见突变:G719X(18外显子)、S768I(20外显子)和L861Q (21外显子)。
肺癌常见靶点及治疗方案

摘要:肺癌是全球范围内最常见的恶性肿瘤之一,严重威胁人类健康。
近年来,随着分子生物学研究的深入,肺癌的靶向治疗逐渐成为研究热点。
本文将介绍肺癌的常见靶点及相应的治疗方案,以期为肺癌患者提供更有效的治疗选择。
一、引言肺癌是一种高度异质性的恶性肿瘤,其发病机制复杂,涉及多个基因和信号通路。
近年来,随着分子生物学技术的不断发展,靶向治疗逐渐成为肺癌治疗的重要手段。
靶向治疗是指针对肿瘤细胞特异性分子靶点,通过抑制其功能或表达,从而抑制肿瘤生长和扩散的治疗方法。
本文将介绍肺癌的常见靶点及相应的治疗方案。
二、肺癌常见靶点1. EGFR(表皮生长因子受体)EGFR是一种跨膜受体酪氨酸激酶,其在肺癌的发生发展中起着重要作用。
约50%的非小细胞肺癌(NSCLC)患者存在EGFR基因突变。
针对EGFR的靶向药物主要有吉非替尼、厄洛替尼、奥希替尼等。
2. ALK(间变性淋巴瘤激酶)ALK是一种原癌基因,其异常表达与肺癌的发生发展密切相关。
约5%的NSCLC患者存在ALK融合基因。
针对ALK的靶向药物有克唑替尼、阿来替尼、布格替尼等。
3. ROS1(ROS原癌基因家族成员1)ROS1是一种原癌基因,其融合基因在肺癌中约占1%。
针对ROS1的靶向药物有克唑替尼、恩沙替尼等。
4. KRAS(鼠类肉瘤病毒癌基因家族成员RAS)KRAS基因突变是肺癌中最常见的突变之一,约30%的NSCLC患者存在KRAS突变。
针对KRAS的靶向药物有安罗替尼、索拉非尼等。
5. BRAF(B-raf原癌基因)BRAF基因突变在肺癌中约占2%。
针对BRAF的靶向药物有达拉非尼、曲美替尼等。
6. MET(肝细胞生长因子受体)MET基因扩增或突变在肺癌中较为常见。
针对MET的靶向药物有克唑替尼、卡博替尼等。
三、肺癌治疗方案1. 靶向治疗(1)EGFR靶向治疗:适用于EGFR突变阳性的NSCLC患者。
一线治疗药物有吉非替尼、厄洛替尼、奥希替尼等。
二线治疗药物有奥希替尼、阿法替尼等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
间变性淋巴瘤激酶(ALK)突变的形式有过量表达、与其他基因形成融合基因,发生点突变等等。
ALK基因融合突变是非小细胞肺癌(NSCLC)常见的一种驱动基因,中国非小细胞肺腺癌中ALK融合突变阳性的比例为5.3%,在非小细胞肺腺癌、年轻患者(小于60岁)以及不吸烟的人群中发生率较高,ALK阳性的非小细胞肺癌被认为是一种分子亚型,相对应的靶向药物与EGFR分子亚型完全不同。
ALK融合基因突变主要在肺腺癌里常见,一般肺鳞癌患者ALK融合基因突变概率很低,有报道说1400个肺鳞癌患者里ALK融合基因的发生率为1.3%。
考虑到ALK总体突变频率仅有5%,所以对于鳞癌患者也是可以做一下ALK检测的。
由于非小细胞肺癌里的驱动基因突变一般是互相排斥的,或者说一山不容二虎,癌细胞也没有必要搞两个驱动突变。
有研究说亚裔的EGFR、KRAS野生型的腺癌患者,ALK阳性比例高达30%-42%,因此如果发现EGFR 和KRAS是野生型,是更有必要测下ALK基因的。
一、ALK融合突变的检测图1:非小细胞肺癌中ALK的重排形式据报道,目前已发现21种EML4-ALK的融合形式,另外ALK还可能与TFG、KIF5B、KLC1、PTPN3、STRN等基因发生融合,因此ALK融合突变的诊断是存在一定难度的。
下表是关于ALK融合突变的诊断方法,及其相应的特点。
表1:ALK基因检测的方法需要注意,临床常用的三种方法是FISH、Ventana IHC及RT-PCR,三种方法FISH的灵敏度最低。
因此,如果是胸腔积液、细针穿刺取到的细胞学样本做成的蜡块,不建议使用FISH,避免假阴性。
另外通过抽血检测循环肿瘤DNA(ctDNA),循环肿瘤细胞(CTC)也正在发展起来。
总之在面对ALK检测结果模棱两可的时候,一定要换一个检测方法去验证,也没有哪一种方法灵敏度和特异性都是100%。
二、ALK的靶向药物ALK融合突变阳性的患者使用克唑替尼可以获益,克唑替尼具有ALK、c-MET、ROS1三个靶点。
克唑替尼治疗ALK阳性的非小细胞肺癌客观缓解率达60%,无进展生存期为8-10个月,显著改善并延长的总生存期。
需要注意的是,克唑替尼的赠药政策与其他靶向药物不同,第一年买四个月赠八个月,第二年仍需要买四个月,才能终身获赠,合计下来得几十万,价格相对较高,所以使用之前一定明确是ALK突变才行。
图2:相比多西他赛、陪美曲塞,ALK阳性的肺癌患者使用克唑替尼获益明显。
不管如何,靶向药物都有一个短板就是耐药,使用克唑替尼的患者往往在1-2年内出现对克唑替尼的耐药,以中枢神经系统的复发进展较为常见。
表2:ALK耐药的原因和应对策略克唑替尼耐药后,后续还有二代,三代的ALK抑制剂,最近的发现三代ALK抑制剂劳拉替尼(3922)耐药后,患者如果是存在L1198F导致的耐药,可以可以重新用回克唑替尼。
几种二代、三代ALK靶向药物的简介如下。
1、艾乐替尼(Alectinib,代号CH5424802),效率比克唑替尼强10倍,可对抗大多数的ALK激酶区突变,且对脑病灶控制较好。
日本的一项临床研究使用的计量为每次300mg、每日两次,46名患者的43名获得客观缓解(客观缓解率达93.5%),日本已经批准了该药使用,美国FDA也已经批准该药用于克唑替尼治疗后耐药的患者。
2016年ASCO会议上报道了一项研究,艾乐替尼一线治疗ALK阳性非小细胞肺癌中的无进展(PFS)显著优于克唑替尼。
克唑替尼的中位PFS为10.2个月,而艾乐替尼的中位PFS要大于20.3个月。
相比克唑替尼,艾乐替尼使得疾病恶化或死亡风险显著降低66%。
2、色瑞替尼(Ceritinib,LDK378),对C1156Y具有良好的活性,该药的最大耐受计量为每天750mg,亚裔人的耐受计量可能到不了那么高,又说600mg的。
79例克唑替尼耐药的ALK阳性非小细胞肺癌使用该药后,ORR为57%。
一项涵盖114名患者的临床表明色瑞替尼的中位PFS为8.6个月。
最常见的副作用是恶心、腹泻、呕吐和乏力。
有患者反映色瑞替尼的副作用非常大,很少有人耐受,但是如果撑过去了则可能获益期较长。
3、Brigatinib(AP26113),一种新型的ALK和EGFR双重抑制剂,可强效抑制ALK的L1196M突变和EGFR的T790M突变。
2016年ASCO会议上公布的一项研究结果,即将患者1:1随机分为两组,A组患者每天口服Brigatinib药物90mg,B组患者前7天每天口服Brigatinib药物90mg,后面加量到180mg,两组人群的ORR分别为46%/54%,A组有一例证实的完全缓解,B组有五例证实的完全缓解,中位PFS分别为8.8个月/11.1个月。
证明了该药良好获益。
4、劳拉替尼(Lorlatinib,PF06463922),该药应该算是第三代ALK抑制剂,可抑制克唑替尼耐药的9种突变,具有较强的血脑屏障透过能力,入脑效果较强,特别适合对其他ALK耐药的晚期NSCLC患者。
2016年6月5日,辉瑞在ASCO会议上公布了该药的I/II期临床研究数据,入组的54例患者有41例为ALK阳性,12例为ROS阳性,其中39例有脑转移。
该临床实验最终确定的给药方案为每日1次100mg,患者的总应答率为46%,3例实现完全应答,16例实现部分应答,中位PFS为11.4个月,另外还显示出缩小转移性的脑部肿瘤体积的效果。
另外还有几个药物如X-396,ASP3026等,其相应的靶点和相关数据见下图,如有兴趣的可以追溯相关参考文献进行延伸阅读。
图3:ALK新一代抑制剂的特点,最后两列为可以克服的克唑替尼耐药位点,以及无能为力的位点。
三、HSP90抑制剂与ALK耐药联合热休克蛋白(HSP90)是一类称为“分子伴侣”的蛋白质,可帮助新合成的蛋白质形成发挥他们特定生物学功能的正确形状。
体外细胞系研究发现HSP90抑制剂Ganetespib对ALK阳性的细胞系有活性,且不管是否经过克唑替尼处理都是如此(见下图)。
我们可以看到突变的EML4-ALK和HSP90是需要相互结合的。
目前有关HSP90抑制剂Ganetespib的临床实验正在进行中。
另一种HSP90抑制剂是AUY922,目前正在进行ALK阳性的NSCLC的II期临床实验,每周计量70mg/平M。
疾病控制率为59%(未经克唑替尼治疗的控制率为100%,克唑替尼耐药组的为36%)。
图4:ALK阳性NSCLC的靶向治疗机制四、EGFR和ALK双突变患者普遍认为,ALK和EGFR基因是互斥的,因为肿瘤其实没有必要制造两个驱动基因。
但是对于后期经过多种治疗后,反复耐药的患者。
EGFR和ALK共存的概率也不容忽视。
对于这一部分患者,联合使用EGFR和ALK的抑制剂较好,比单独使用一种起到更好的控制作用,但是联合治疗副作用会较大,也需要看患者的耐受情况。
目前关于两类靶向药物联用效果、副作用等还缺乏数据。
当然这部分患者可以考虑下Brigatinib(AP26113),该药是ALK和EGFR双靶点的抑制剂,可以考虑参加入组实验等。
但问题是该药可以抑制EGFR和ALK 守门员突变(T790M,L1196M),如最开始就使用Brigatinib,这可能是把最后一张牌给打了。
笔者曾见过一个原发性双突变的患者,同时具有EGFR和ALK阳性,该患者的治疗情况也将及时追踪,后续再和大家呈报。
五、什么时候停药即便是出现局部进展,也不是立刻停止克唑替尼等靶向药物的理由,因为可能还有很多癌细胞被药物所抑制。
立即停止靶向药物,会导致肿瘤的爆发性进展。
一项关于使用克唑替尼抑制ALK阳性非小细胞肺癌的研究发现,克唑替尼治疗进展后,继续使用克唑替尼相比停止克唑替尼的患者获益更好。
6个月总生存率为76.3% vs 31.2%,1年总生存率为64.7% vs 32.9%,OS为16.4个月vs 3.9个月。
也有部分患者使用克唑替尼后,肿瘤病灶快速消失掉了,于是患者把药给停止了,后来导致报复性的复发,有些患者再用克唑替尼也控制不了,即是一种脱靶效应,虽然这其中的机理不知道,但是确实是存在的。
这些现象是某些患者的血泪教训,虽然没有临床数据,但值得警惕。
因为CT看不到肿瘤了,不代表肿瘤细胞完全被杀灭干净了。
停药是一个非常谨慎的事情,望广大患者和家属慎之再慎。
六、完美的闭环?劳拉替尼(Lorlatinib,PF06463922)被作为ALK靶点的最后一张王牌,因为克唑替尼耐药的所有位点该药似乎都能克服。
直到出现了L1198F。
新英格兰医学杂志报道了一名患者治疗经过(见下图)。
该患者首先使用克唑替尼,耐药后检测发现了C1156Y,但是这个患者对二代ALK抑制剂没有应答,不得已使用劳拉替尼,但是后面新出现的L1198F导致对劳拉替尼耐药,看似山穷水尽,却不曾想L1198F突变导致了与克唑替尼结合更好,逆转了C1156Y的作用,患者对克唑替尼重新复敏。
图5:L1198F导致的劳拉替尼耐药对克唑替尼重新复敏这是一个非常有意思的发现,即劳拉替尼这个药物也不是最后的一张牌,这个药物耐药了,也许之前被放弃的药物仍可以有效。
所以也有说法ALK是一种钻石突变。
但需要谨慎的是不是每一个劳拉替尼耐药的患者都这样。
我们从图示看出患者同时存在C1156Y和L1198F突变,才造成了这种逆转。
也许其他的突变位点如L1196M等和L1198F就没有这种协同效果。
或者还有可能劳拉替尼耐药的原因是其他的旁路激活,如KRAS或EGFR等,具体的还是可以根据基因检测结果来谨慎分析和对待,不过现在的测序技术抽血测ctDNA 检测ALK的这些激酶突变总可能会有阴性,ArmsPCR等检测方法也还没有相应的产品,暂时只能尽量地取耐药后的新发组织样本,进行二代测序检测。
本文为“癌度”原创文章,转载需授权并注明作者和来源。
关注我们:搜索微信公众号“癌度”,不但能给你最规范的信息,还能帮你寻找同疾病友,在这里,大家交流第一手的资料,互相鼓励,与癌共舞!参考文献:1、冯勤杨欣林冬梅,ALK阳性非小细胞肺癌的诊断,中国肺癌杂志2 0 1 5年2月第1 8卷第2期。
2、蒋涛周彩存,中国肺癌杂志2015年2月第1 8卷第2期3、Alice T, J ClinOncol. 2013 Mar 10。
31(8): 1105–11114、Clin Cancer Res. 2014 March 1。
20(5): 1204–12115、Ou SH , et al. Ann Oncol, 2014, 25(2): 415-422.6、Zhang I,Lancet Oncol.2015 Oct。
16(13): e510-217、Ther Adv Med Oncol. 2016 Jan。
